徐氏腎炎靈膠囊抗大鼠腎炎的研究
徐 海 朱向軍 鄭 群 朱愛平 王傳斌 雷鈞濤
(1江蘇鹽城市第一人民醫院財務科,鹽城 224006;2江蘇鹽城市第一人民醫院腎內科,鹽城 224006;3江蘇鹽城市第一人民醫院科教科,鹽城 224006;4吉林醫藥學院藥學系,吉林 132013)
徐氏腎炎靈膠囊系傳統方劑,含益母草、牡丹皮、山萸肉、當歸、紫草、半邊蓮、淮山藥、玉米須、青蒿、牛膝、紅花等藥材,臨床與實驗均表明對急、慢性腎炎、腎病綜合征有良好的治療作用。筆者研制徐氏腎炎靈膠囊進行藥效學研究,為新藥報批及其臨床應用提供試驗依據。
1 材料與方法
1.1動物Wi s t a r大鼠90只 (吉林醫藥學院實驗動物中心提供), 體重180~220g。
1.2藥品 徐氏腎炎靈膠囊內容藥粉。由鹽城市第一人民醫院徐海提供,臨用前以蒸餾水配制所需濃度。
1.3試劑 Freund完全佐劑 (美國西格瑪公司)。肌酐、尿素氮、NO、SOD、MDA檢測試劑盒 (南京建成公司)。
1.4 Wi s t a r大鼠腎炎模型復制方法 取wistar大鼠,雌雄各半,腹腔注射10%水合氯醛麻醉,在無菌條件下剖開腹腔,結扎腎動脈,自結扎處向腎臟插管,剪斷腎靜脈,經插管用生理鹽水反復沖洗腎臟,使之成灰白色,取下腎臟,取腎皮質用電動勻漿器磨成勻漿,每次取皮質勻漿10g,加弗氏完全佐劑20mL,緩緩加入生理鹽水40mL置乳缽研勻,使乳化均勻完全。每只實驗大鼠腹腔注射上述同種大鼠腎皮質加弗氏完全佐劑液,每次2mL/只,每周注射1次,歷時6周。第五周注射結束開始給藥。
1.5給藥方案 模型成功大鼠隨機分為:Wistar腎炎模型組、空白對照組、徐氏腎炎靈膠囊大、中、小劑量組分別相當于含生藥2.7g/mL·100g, 1.35g/mL·100g,0.68g/mL·100g, 地塞米松組 (0.55g/mL·100g), 每組各10只。正常對照組和模型組給予同體積蒸餾水,連續5d, 10d, 15d, 20d。
1.6一般觀察指標 分別于給藥不同時間測量各組大鼠的尿蛋白、體重、血清及尿中的肌酐和尿素氮,以及血及組織中的SOD和MDA水平,并檢測毒性相關生化指標,同時在給藥結束后對大鼠腎進行切片做病理分析。1.7數據處理 測量數據以均數或均數±標準差表示,組間比較采用t檢驗或χ2檢驗,以P<0.0 5為有統計學意義。
2 結果
2.12 4 h尿蛋白定量 分別在給藥處理后5d,10d,15d,20d測定1次。
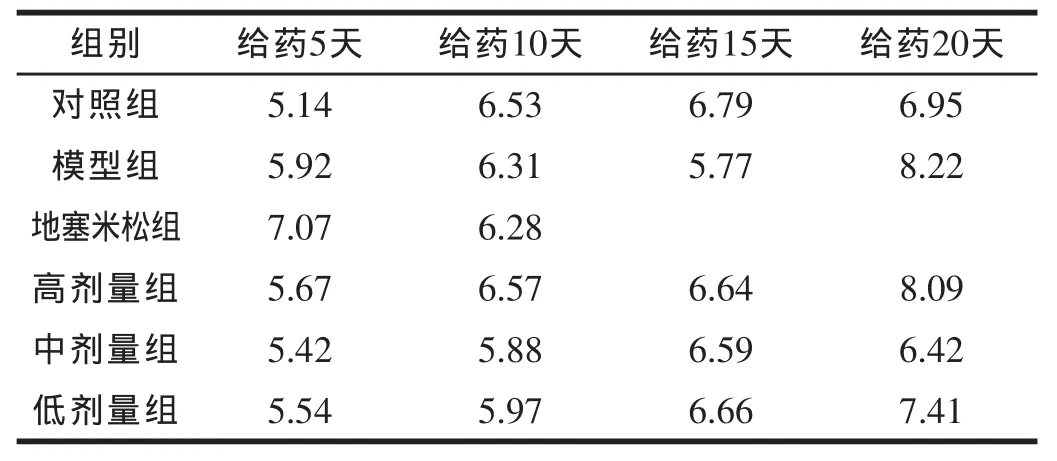
表1 24h尿蛋白定量 (×10-2mg)
第34天注射第五針,35天開始給藥,給藥10天、15天時變化不明顯,20天時模型組、高劑量組與中低劑量組、對照組差異明顯。
2.2體重 每隔三天稱體重一次,具體結果見下表。
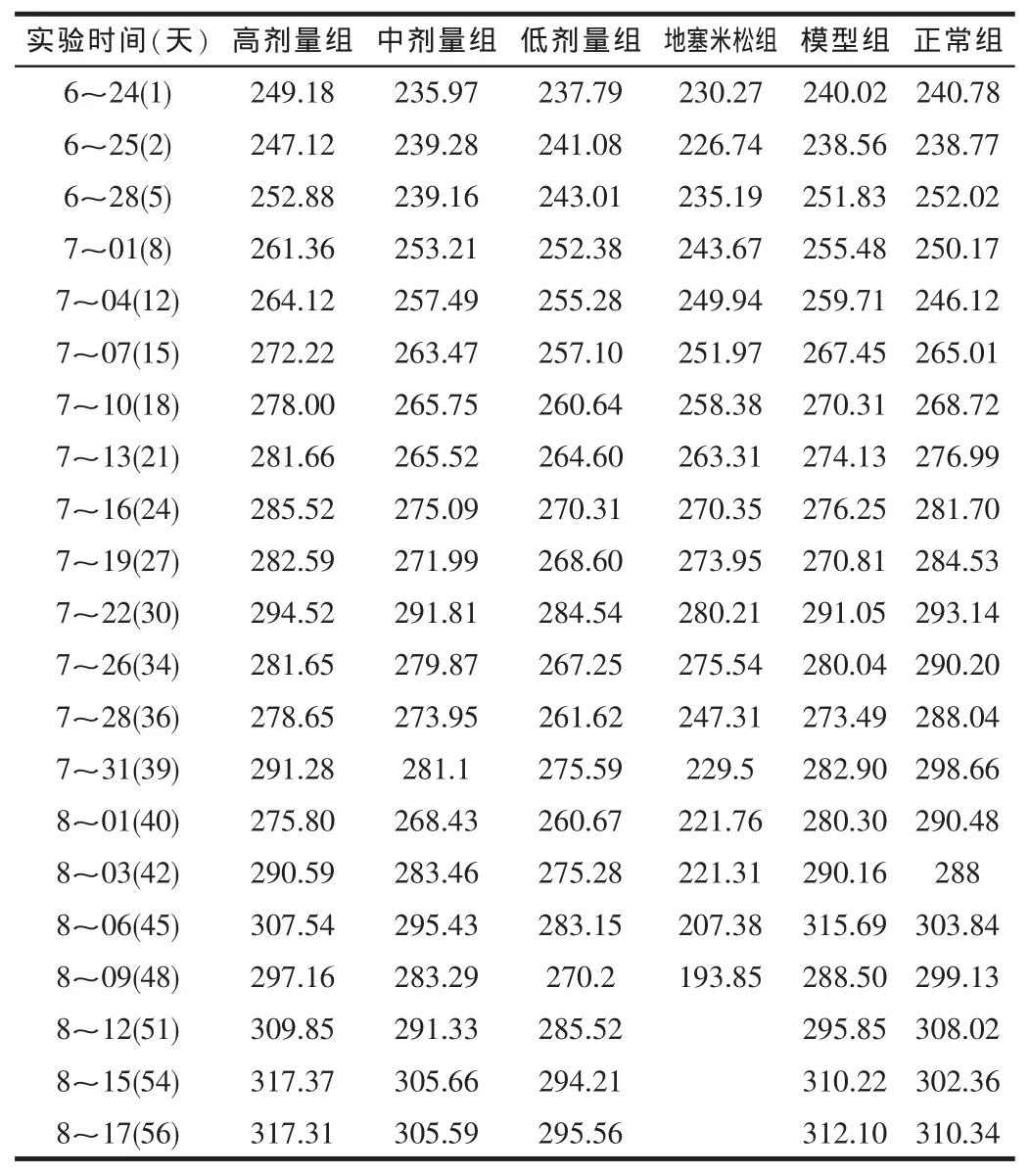
表2 各組體重變化比較 (g)
從表中數據看出第4天注射第一針,第11天注射第二針,第19天注射第三針,第25天注射第四針,第34天注射第五針,35天開始給藥,40天時注射佐劑的各組體重下降較明顯而模型組不明顯 (給藥組l5g,模型組2g),41天注射第六針,48天時注射佐劑的各組體重下降較明顯 (給藥組10g,模型組27g)。之后各組均持續增長到54天,到57天給藥組均停止增長,模型組增2g,對照組增10g。地米組體重明顯下降,動物狀態也不好,說明激素類藥物對本模型動物影響很大,第50天死一半,第51天全部處死,經解剖發現內臟全部病變。說明佐劑對動物體重有一定影響。
2.3肌酐
發布會上,昆明供電局黨委發布的《“三個導向”助推責任落實,黨的建設督導構建“昆供模式”》,解決責任“層層衰減”的案例,是推動黨的建設工作責任制有效落實落地,進一步構建完善大監督體系的有力體現。該項目有效地實現黨的建設工作重在日常、抓在時常、嚴在經常,書記項目、黨員突擊隊等載體成為了黨的建設融入中心、重點項目攻堅、推動生產經營的有力抓手,不僅帶動了一批黨的建設業務能手,還起到了助推企業發展的效果。
表3 各組血清及尿中肌酐水平比較 )
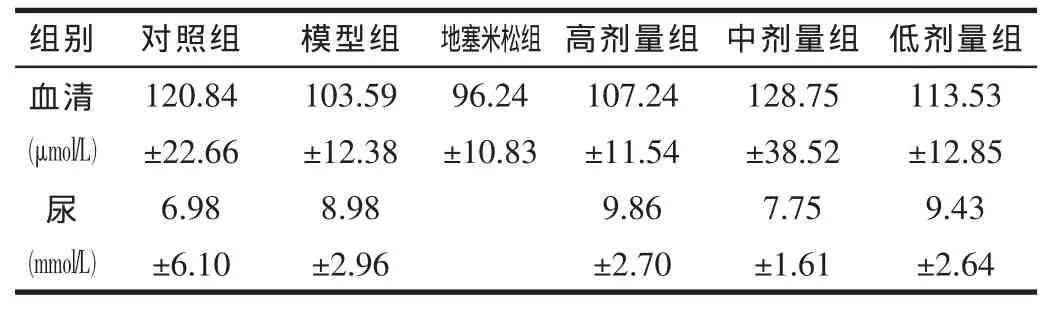
表3 各組血清及尿中肌酐水平比較 )
血清(μmol/L)尿(mmol/L)組別 對照組 模型組 地塞米松組120.84 103.59 96.24中劑量組 低劑量組128.75 113.53±22.66 ±12.38 ±10.83 ±11.54 ±38.52 ±12.85高劑量組107.24 6.98 9.86 7.75 9.43±6.10 ±2.70 ±1.61 ±2.64 8.98±2.96
對照組與模型組血清肌酐差異顯著 (P≤0.05)說明此模型對血清肌酐有影響;中劑量、低劑量組與對照組無差異,說明此2組對改善血清肌酐效果明顯;地米組與對照組差異顯著 (P≤0.05),說明地米對改善血清肌酐無效果。模型組、高劑量組、低劑量組尿肌酐升高明顯,中劑量組升高不明顯。
2.4尿素氮
表4 各組血清及尿中尿素氮水平比較 (,m m o l/L)
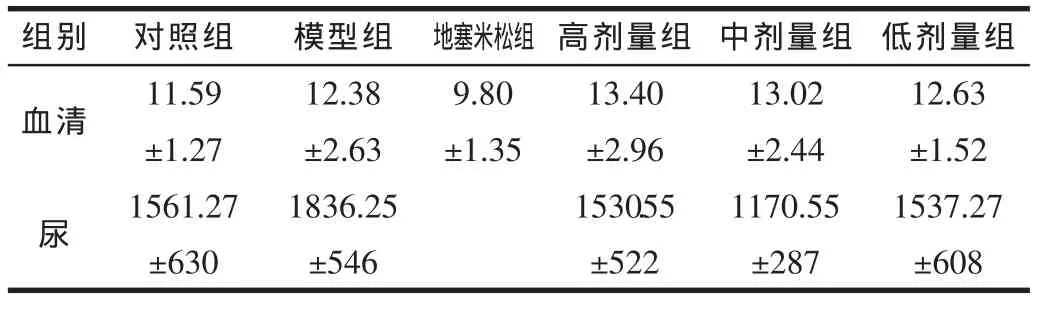
表4 各組血清及尿中尿素氮水平比較 (,m m o l/L)
組別 對照組 模型組 地塞米松組11.59 12.38 9.80血清尿 1561.27 1530.55 1170.55 1537.27±630 ±522 ±287 ±608中劑量組 低劑量組13.02 12.63±1.27 ±2.63 ±1.35 ±2.96 ±2.44 ±1.52高劑量組13.40 1836.25±546
地米組血清尿素氮明顯降低,與各組均差異顯著(P≤0.O5),說明地塞米松對改善血清尿素氮效果明顯。中劑量組尿尿素氮明顯降低,與模型組差異顯著(P≤0.05),說明中劑量組對改善尿尿素氮效果明顯。
2.5一氧化氮
表5 各組一氧化氮水平比較 (,μm o l/L)

表5 各組一氧化氮水平比較 (,μm o l/L)
組別 對照組 模型組 地塞米松組 高劑量組 中劑量組 低劑量組N0 53.72±10.83 79.50±22.40 92.99±29.36 48.32±11.96 55.33±19.38 78.12±23.87
對照組與模型組差異極顯著 (P≤0.1)說明此模型對N0影響極大;各劑量組與對照組比差異顯著 (P≤0.05),高劑量降低,中劑量略有升高,低劑量升高明顯。高、中劑量組與模型組比明顯降低。
2.6S O D
表6 各組血清及尿中SOD水平比較 (,×1 03U/L)
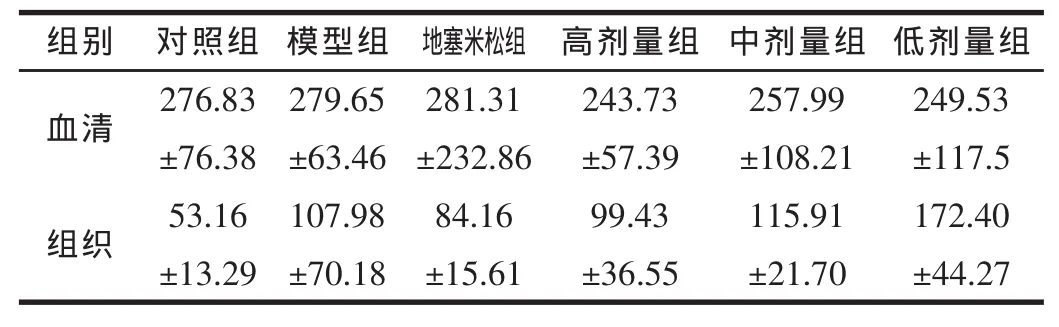
表6 各組血清及尿中SOD水平比較 (,×1 03U/L)
組別 對照組 模型組 地塞米松組 高劑量組 中劑量組 低劑量組276.83 279.65 281.31 243.73 257.99 249.53血清 ±76.38 ±63.46 ±232.86 ±57.39 ±108.21 ±117.5組織 53.16 107.98 84.16 99.43 115.91 172.40±13.29 ±70.18 ±15.61 ±36.55 ±21.70 ±44.27
模型組、地塞米松組與對照組比略有增高,而三個劑量組均略有下降。各組與對照組比均有增高,中劑量組、低劑量組增高明顯。
2.7MD A
表7 各組血清及尿中MDA水平比較 (,n m o l/m l)
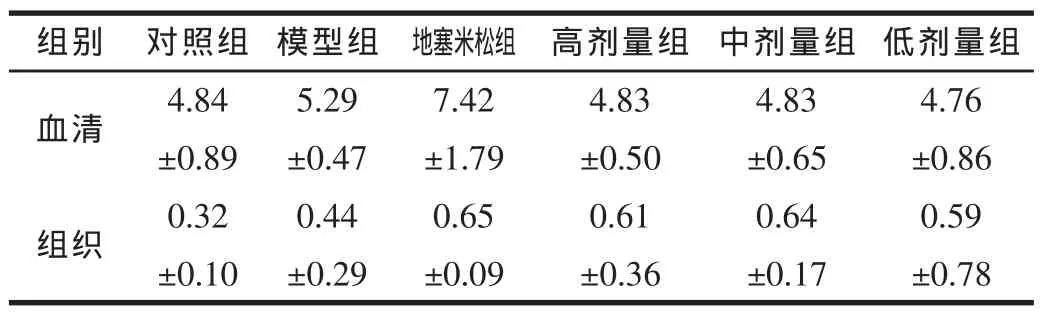
表7 各組血清及尿中MDA水平比較 (,n m o l/m l)
組別 對照組 模型組 地塞米松組 高劑量組 中劑量組 低劑量組4.84 5.29 7.42 4.83 4.83 4.76±0.89 ±0.47 ±1.79 ±0.50 ±0.65 ±0.86血清組織 0.32 0.44 0.65 0.61 0.64 0.59±0.10 ±0.29 ±0.09 ±0.36 ±0.17 ±0.78
模型組、地塞米松組MDA明顯增高,地塞米松組與各組均差異顯著 (P≤0.05);各劑量組與對照組無差異且略有降低。各組MDA均增高,地塞米松組與各劑量相接近,說明脂質過氧化增多。
2.8骨組織切片
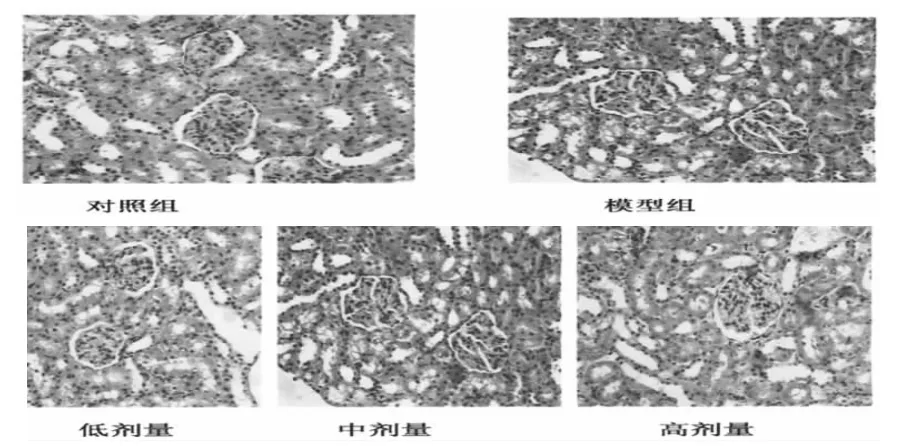
圖1各組骨組織切片HE染色結果
HE染色結果顯示:造模后與對照組相比,模型組腎小球體積增大,內皮細胞數目增多,近曲小管上皮細胞腫脹,小管管腔狹小,上皮細胞中有大量的蛋白樣物質沉積,證實腎臟發生玻璃樣變性。治療后,低劑量組與模型組比較,腎小球體積略縮小,近曲小管上皮細胞內蛋白沉積減少,上皮細胞玻璃樣變性程度減輕。而中劑量組,腎小球大小與對照組基本相似,
近曲小管上皮中也未見蛋白沉積,腎小球和腎小管的結構基本恢復到正常狀態,證實中劑量組藥物能夠改善和恢復腎臟結構。與中劑量組相比,高劑量組腎小管上皮細胞中有蛋白沉積,但玻璃樣變的程度要輕于模型組。
2.9毒性指標 按所能配的最大濃度配制 (相當于人的10倍量),一天給藥3次,后常規飼養,每三天稱重一次。觀察14天后全部處死,取血清檢測生化指標。
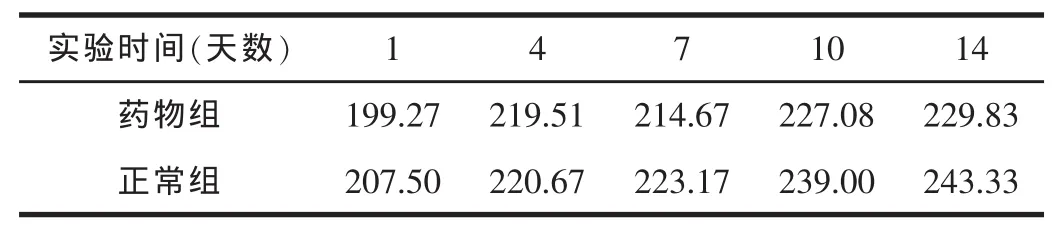
表8 兩組體重變化比較 (g)
第七天體重略比第四天降低外,其他均正常。
表9 兩組生化指標檢測比較
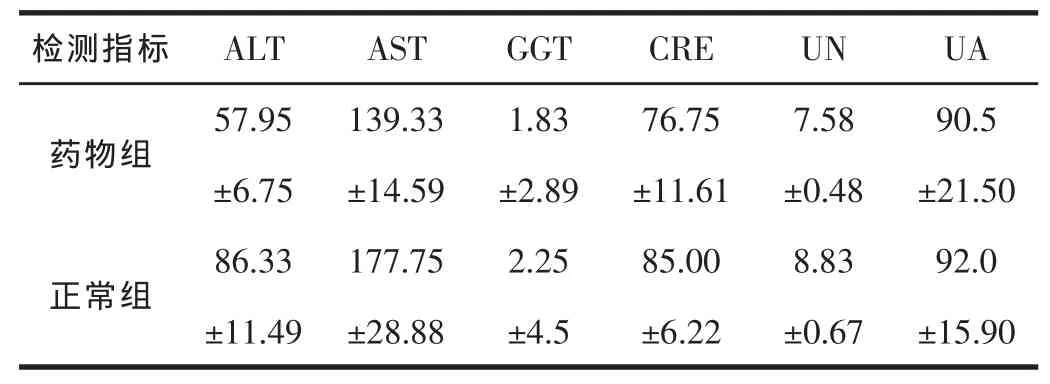
表9 兩組生化指標檢測比較
注:ALT(丙氨酸氨基轉移酶U/L)AST(天冬氨酸氨基轉移酶U/L)GGT(谷氨酰轉肽酶U/L)CRE(肌苷mmol/L)UN(尿素氮mmol/L)UA(尿酸μmol/L)
檢測指標 ALT AST 57.95 139.33 UA 90.5±6.75 ±14.59 ±2.89 ±11.61 ±0.48 ±21.50 GGT 1.83 CRE 76.75 UN 7.58藥物組正常組86.33 177.75 2.25 85.00 8.83 92.0±11.49 ±28.88 ±4.5 ±6.22 ±0.67 ±15.90
與正常組比尿酸基本未有變化,肌苷、尿素氮略有降低但未有顯著性差異;ALT(丙氨酸氨基轉移酶)、AST(天冬氨酸氨基轉移酶)、GGT(谷氨酰轉肽酶)有降低但差異不顯著。
3 討論
Heymann腎炎的臨床過程和病理類型與人類膜性腎病十分接近,作為人類膜性腎病的動物模型得到廣泛公認,制備該動物模型方法有主動型Heymann腎炎和被動型Heymann腎炎兩種,已經證明,Heymann腎炎發病機制包括多種細胞因子、補體激活、膜攻擊復合物形成、炎癥細胞以及炎性介質合成增加,引發一系列炎癥反應,最終導致腎小球基底膜損傷[1]。本研究采用了主動型Heymann腎炎模型,觀察徐氏腎炎靈膠囊不同劑量對模型動物的影響,結果顯示,徐氏腎炎靈膠囊各劑量組均可以降低腎炎大鼠尿素氮和尿蛋白。證實徐氏腎炎靈膠囊有對抗Heymann腎炎大鼠的蛋白尿作用。血清肌酐檢測中發現對照組與模型組差異顯著 (P≤0.05)說明此模型對血清肌酐有影響;中劑量、低劑量組與對照組無差異,說明此2組對改善血清肌酐效果明顯;在Heymann腎炎的機制探討中發現模型組大鼠尿蛋白量增加,各給藥組伴有血清腎皮質SOD含量減少,組織SOD含量增多,說明Heymann腎炎大鼠尿蛋白形成可能與抗氧化能力有關。血清、組織MDA含量均增多,說明Heymann腎炎大鼠尿蛋白形成可能與脂質過氧化增多有關。模型組炎癥因子NO有明顯的升高,徐氏腎炎靈膠囊各劑量組N0含量與模型組比較有顯著性差異,說明徐氏腎炎靈膠囊對于Heymann腎炎的治療機制有炎癥因子的表達參與,但具體影響因素不明。
HE染色結果顯示:造模后與對照組相比,模型組腎小球體積增大,內皮細胞數目增多,近曲小管上皮細胞腫脹,小管管腔狹小,上皮細胞中有大量的蛋白樣物質沉積,證實腎臟發生玻璃樣變性。治療后,低劑量組與模型組比較起來,腎小球體積略縮小,近曲小管上皮細胞內蛋白沉積減少,上皮細胞玻璃樣變性程度減輕。而中劑量組,腎小球大小與對照組基本相似,近曲小管上皮中也未見蛋白沉積,腎小球和腎小管的結構基本恢復到正常狀態,證實中劑量組藥物能夠改善和恢復腎臟結構。與中劑量組相比,高劑量組腎小管上皮細胞中有蛋白沉積,但玻璃樣變的程度要輕于模型組。
綜合以上切片和各種指標的觀察,都能看出中劑量藥物組對本腎炎模型有很好的治療作用,低劑量組略有改變,高劑量組改變不明顯。
毒性試驗通過體重、生活狀態觀察未見異常;生化指標檢測基本正常。
徐氏腎炎靈膠囊中的益母草、半邊蓮、玉米須,有清熱、涼血、利尿、消腫的功效,現代藥理研究證明能起到抑菌、抗炎、鎮靜、鎮痛、減少尿中蛋白的析出[2];牡丹皮、山萸肉、淮山藥、青蒿有活血、散瘀、補脾胃、益肺腎,能明顯改善血壓、止泄、止久咳之功效;當歸、牛膝、紅花有活血、和血、祛瘀、強補肝腎,對肝腎不足、腰膝酸軟、關節酸痛有顯著治療作用,故諸藥合用有清利濕熱、滋陰補腎、益氣活血、消腫止痛等作用[3]。本研究結果表明,徐氏腎炎靈膠囊組的療效明顯優于西藥對照組,說明徐氏腎炎靈膠囊具有對抗Heymamn腎炎大鼠蛋白尿作用,并有效降低血清肌苷,尿素氮與腎間質損傷程度,同時改善體重,有效控制復發。本研究為新藥開發及其臨床應用提供一定藥理學依據。
[1]陳灝珠.內科學[M].第4版,北京:人民出版社,2008.
[2]陳奇.中藥藥理研究方法學[M].北京:人民衛生出版社,2006.
[3]徐淑云,卞如濂、陳修.藥理學實驗方法[M].北京:人民衛生出版社,2006.

