人巨細胞病毒微小RNA miR?UL70?5P靶向抑制人即刻早期反應蛋白3的表達
柳中洋,齊瑩,郭鑫,蔣樹娟,黃郁晶,邵耀中,阮強
(中國醫科大學附屬盛京醫院病毒研究室,沈陽110004)
·論著·
人巨細胞病毒微小RNA miR?UL70?5P靶向抑制人即刻早期反應蛋白3的表達
柳中洋,齊瑩,郭鑫,蔣樹娟,黃郁晶,邵耀中,阮強
(中國醫科大學附屬盛京醫院病毒研究室,沈陽110004)
目的尋找人巨細胞病毒微小RNA miR?UL70?5P調控的靶mRNA,檢測miR?UL70?5P對靶mRNA蛋白質表達的調節作用。方法采用Hybrid?PCR方法從人巨細胞病毒感染的人胚肺成纖維細胞總RNA中篩選候選靶mRNA;采用熒光素酶實驗驗證miR?UL70?5p與候選靶mRNA的結合能力;采用Western blot方法檢測轉染miR?UL70?5P對部分靶mRNA蛋白質表達的調節作用。結果篩選并鑒定了人即刻早期反應蛋白3(IER3)等7種靶mRNA可與miR?UL70?5P特異性結合;在293T細胞中過表達的IER3可以被轉染的miR?UL70?5P下調30%。結論人巨細胞病毒表達的miR?UL70?5P在病毒感染宿主過程中具備抑制IER3蛋白質表達的能力。
人巨細胞病毒;微小RNAs;人即刻早期反應蛋白3
微小RNAs(microRNAs,miRNAs)是一類長度為22個堿基的核糖核酸,雖然不能夠翻譯表達蛋白質,但可以通過與信使RNA反向互補結合,阻礙其翻譯過程[1]。現已發現miRNAs在生命活動的各個方面發揮著精細的調節作用[2]。miRNAs在病毒中也有表達。人巨細胞病毒(human cytomegalovirus,HCMV)是人群感染率高達90%以上的DNA病毒。依據miRBase提供的資料,目前已經發現HCMV表達包括miR?UL70?5P在內的26種miRNAs。但是,miR?UL70?5P的生物學功能目前尚不清楚。本研究擬尋找HCMV miR?UL70?5P調控的靶mRNA,檢測miR?UL70?5P對靶mRNA蛋白質表達的調節作用。
1 材料與方法
1.1 材料
HCMV H株(本實驗室保存的臨床分離株);人胚肺成纖維細胞(human embryonic lung fibroblasts,HELF)(中國科學院上海細胞所)。pcr2.1載體(invi?trogen公司,美國);Top10感受態細菌(北京天根生化科技有限公司);熒光素酶報告質粒(appliedbio?systems公司,美國);熒光素酶活性檢測試劑(Pro?mega公司,美國);pBI?CMV2(Clontech公司,美國);蛋白質提取和檢測試劑(Thermo公司,美國);抗體(Abcam公司,美國)。
1.2 方法
1.2.1 使用hybrid?PCR篩選miR?UL70?5P的候選靶mRNA:用含15%胎牛血清的MEM培養HELF,密度為100%時接種HCMV H株。部分細胞在接種病毒前1 h用終濃度為100 μg/mL的放線菌酮處理,接毒后24 h使用Trizol法提取HCMV感染即刻早期(IE)總RNA;未經過放線菌酮處理的細胞在接毒后72 h,用Trizol法提取HCMV感染晚期(L)總RNA。使用TaKaRa公司的3′Full RACE試劑盒中的oligodT引物及逆轉錄酶將mRNA反轉錄成cDNA。設計并使用miR?UL70?5P的反向互補序列“TCTGGRCGRG?GCCGRGRCGC(R=A/G)”作為上游引物,oligodT引入的通用引物“ACCGTCGTTCCACTAGTGATTT”作為下游引物,以cDNA為模板進行PCR擴增,引物由北京invitrogen公司合成。PCR產物經過純化后(A9280,Promega公司,美國),用TA克隆的方法連接到pcr2.1載體。將連接產物轉化到感受態細菌中,挑取陽性克隆進行DNA測序。測序結果經過NCBI的blast軟件比對得到同源mRNA序列,作為備選的靶mRNA。
1.2.2 熒光素酶實驗驗證miR?UL70?5P與候選靶mRNA的結合能力:使用逆轉錄PCR方法擴增候選靶mRNA與miR?UL70?5p結合位點附近約300~500 bp左右的序列。在擴增引物的5′末端分別加入了BamHⅠ和HindⅢ酶切位點序列。純化PCR產物,進行BamHⅠ和HindⅢ雙酶切。將酶切產物連接到pMIR report載體上熒光素酶基因的3′非翻譯區(3′UTR區)的相應位點,得到“pMIR?靶mRNA”表達載體。用含10%胎牛血清的DMEM培養293T細胞,采用lip2000共轉染pMIR?靶mRNA、海腎熒光素酶質粒(TK)以及miR?UL70?5P的成熟體(銳博公司,廣州)到293T細胞。每個候選靶mRNA做3個復孔。使用線蟲的一種非特異性靶向miRNA作為陰性對照。使用pMIR空載體作為系統誤差對照。貼壁細胞通過裂解釋放熒光素酶(Dual?Luciferase? Reporter Assay E1960,Promega公司,美國),進行熒光素酶活性檢測(LB9507,Berthhold Technologies公司,德國)。先檢測每一樣本的螢火蟲熒光素酶熒光強度,后檢測海腎熒光素酶熒光強度。用“螢火蟲熒光素酶熒光值/海腎熒光素酶熒光值”得到消除了組內轉染誤差的終數據。以每個樣本的3個復孔所測終數據的平均值進行對比分析。
1.2.3 Western blot分析miR?UL70?5P對候選靶mRNA蛋白質表達的調控作用:根據與HCMV感染相關性及實驗可行性,選取人即刻早期反應蛋白3(immediate early response 3,IER3)進行Western blot實驗分析。將IER3mRNA全序列構建到pBI?CMV2蛋白質表達載體中,得到pBI?CMV2?IER3表達載體。共轉染pBI?CMV2?IER3和miR?UL70?5P成熟體至293T細胞中。使用線蟲的一種非特異性靶向miRNA成熟體作為miRNA陰性對照,使用pBI?CMV2自身表達的綠色熒光蛋白(green fluorescent protein,GFP)作為組內對照消除轉染誤差。轉染24 h后收集蛋白質(M?PER?Mammalian Protein Extrac?tion Reagent,PIERCE公司,美國)進行Western blot檢測。依次使用兔源多克隆抗體(Abcam公司,英國)和山羊抗兔的二抗(中杉金橋公司,北京)進行反應。使用ChemiDoc?MP System(Biorad,美國)進行成像,使用儀器配套軟件image lab進行實驗結果灰度分析處理。
2 結果
2.1 Hybrid?PCR篩選結果(表1)

表1 Hybrid?PCR篩選獲得的HCMV miR?UL70?5P候選靶mRNAsTab.1 Candidate target mRNAs of HCMV miR?UL70?5p obtained by Hybrid?PCR screening
共篩選獲得10種miR?UL70?5P的候選靶mRNA序列,8種來源于宿主細胞,2種來源于HCMV。其中,NQO2是一種黃素蛋白,功能是催化氧化還原反應;PP150是HCMV重要的衣殼蛋白,具有免疫原性,可引起宿主的體液免疫應答;核糖體蛋白L35構成核糖體亞基,參與蛋白質的合成;HCMV UL70是DNA復制引發酶,與HCMV的基因組復制有關;IER3是即刻早期反應蛋白,在輻射、感染等條件下迅速提高表達量,參與應激反應,并參與細胞凋亡的調控。這些靶基因涉及到細胞凋亡、HCMV感染與復制、細胞能量代謝、生物大分子合成等。
2.2 熒光素酶實驗檢測結果
miR?UL70?5P的轉染未造成PMIR空質粒螢火蟲熒光素熒光強度發生明顯改變(圖1)。除RO?MO1外,含有其它候選靶mRNA 3′UTR序列質粒的相對熒光值均表現為下調,說明候選靶mRNA與miR?UL70?5P確實存在結合關系。
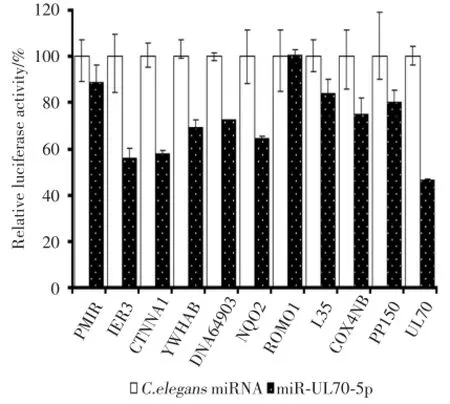
圖1 熒光素酶實驗檢測結果Fig.1 Result of Luciferase assay
2.3 Western blot結果
與作為miRNA參照的線蟲miRNA成熟體作用效果相比,載體內參照蛋白GFP的表達沒有受到轉染的miR?UL70?5P的影響;而載體中IER3的蛋白質表達量被miR?UL70?5P下調了36.4%(圖2)。

圖2 免疫印跡結果Fig.2 Result of Western blot
3 討論
HCMV的miRNA編碼區分散于病毒整個基因組中。已經進行功能研究的miRNA包括miR?UL112[3~7]、miR?UL148D[8]、miR?US4?5P[9]、miR?US5?1[10]、miR?US5?2[10]、miR?US25?1[11]、miR?US25?2?3P[12]和miR?US33[13]等。它們的主要功能在于影響病毒復制,為病毒建立免疫逃避和潛伏感染狀態創造有利條件。
Hybrid?PCR方法是本課題組建立的篩選miRNA靶mRNA的研究方法[14],具有快速、靈活等優點。用此方法可以對特定組織細胞、特定時間的mRNA樣本進行篩選。本研究中,對HCMV感染HELF細胞的即刻早期及晚期RNA進行了miR?UL70?5P候選靶mRNA的篩選,得到的靶mRNA來源包括宿主和病毒自身基因組,靶mRNA編碼蛋白質的功能涉及到能量代謝、細胞凋亡、病毒復制、病毒衣殼形成等各個方面,提示miR?UL70?5P可能通過以上相關機制影響病毒的感染狀態。
本研究只對HELF中miR?UL70?5p的靶mRNA進行了檢測。因為組織分化的原因,某些蛋白質在肺組織中并不表達,所以本研究結果只能反映肺組織受到HCMV感染時miR?UL70?5P與宿主及病毒自身基因相互作用的情況。在HCMV敏感的其它組織細胞中進行hybrid?PCR的篩選,將有利于揭示miR?UL70?5P在特定組織細胞中對HCMV感染調控的機理。
本研究對初篩得到的所有10個候選靶mRNA進行了熒光素酶實驗檢測。不同的靶mRNA與miR?UL70?5p的結合能力并不相同。一般來說,miRNA與靶mRNA結合的自由能越高,miRNA發揮轉錄抑制的作用越顯著,但是mRNA的三級空間結構和轉錄調控因子的空間占位效應可能會隱蔽起miRNA的結合位點,導致篩選得到的部分候選靶mRNA的3′UTR沒有對熒光素酶表達產生影響。熒光素酶實驗只可以驗證miRNA與相應mRNA靶位點之間的結合性,并不能反映其與完整靶mRNA發生的相互作用。使用Western blot實驗進行蛋白質水平的檢測來驗證miRNA對靶mRNA的轉錄后調控作用十分必要。
靶mRNA IER3編碼產物是一種即刻早期反應蛋白質,在感染、輻射、缺血等應激狀態下,表達值可以在15 min內迅速升高。研究發現,IER3蛋白在凋亡—抗凋亡過程中發揮雙向作用。在培養條件惡劣的情況下,高表達的IER3可促進細胞凋亡發生;而在培養條件優越的情況下,IER3則可抑制凋亡[15]。本研究通過Western blot方法證實了miR?UL70?5P對IER3蛋白質表達具有明顯的抑制作用。推測在HCMV感染肺組織過程中,miR?UL70?5P可能通過抑制病毒感染引起的IER3蛋白質表達來阻礙其誘導感染細胞的調亡,創造有利于病毒復制的微環境,從而確保病毒在宿主體內生存。
[1]Ambros V.microRNAs:tiny regulators with great potential[J].Cell,2001,107(7):823-826.
[2]鄧慶,黃健,韓澤廣.microRNA功能研究進展[J].生命科學研究,2006,10(2):91-94.
[3]Wilkinson GW,Tomasec P,Stanton RJ,et al.Modulation of natural killer cells by human cytomegalovirus[J].J Clin Virol,2008,41(3):206-212.
[4]Nachmani D,Lankry D,Wolf DG,et al.The human cytomegalovirus microRNA miR?UL112 acts synergistically with a cellular micro RNA to escape immune elimination[J].Nat Immunol,2010,11(9):806-813.
[5]Grey F,Meyers H,White EA,et al.A human cytomegalovirus?encoded microRNA regulates expression of multiple viral genes in?volved in replication[J].PLoS Pathog,2007,3(11):e163.
[6]Stern?Ginossar N,Elefant N,Zimmermann A,et al.Host immune system gene targeting by a viral miRNA[J].Science,2007,317(5836):376-381.
[7]Huang Y,Qi Y,Ma Y,et al.The expression of interleukin?32 is acti?vated by human cytomegalovirus infection and down regulated by hc?mv?miR?UL112?1[J].Virol J,2013,10:51.
[8]Wang YP,Qi Y,Huang YJ,et al.Identification of immediate early gene X?1 as a cellular target gene of hcmv?mir?UL148D[J].Int J Mol Med,2013,31(4):959-966.
[9]Kim S,Lee S,Shin J,et al.Human cytomegalovirus microRNA miR?US4?1 inhibits CD8(+)T cell responses by targeting the aminopep?tidase ERAP1[J].Nat Immunol,2011,12(10):984-991.
[10]Tirabassi R,Hook L,Landais I,et al.Human cytomegalovirus US7 is regulated synergistically by two virally encoded microRNAs and by two distinct mechanisms[J].J Virol,2011,85(22):11938-11944.
[11]Grey F,Tirabassi R,Meyers H,et al.A viral microRNA down?regu?lates multiple cell cycle genes through mRNA 5′UTRs[J].PLoS Pathog,2010,6(6):e1000967.
[12]Qi M,Qi Y,Ma Y,et al.Over?expression of human cytomegalovi?rus miR?US25?2?3p downregulates eIF4A1 and inhibits HCMV replication[J].FEBS Lett,2013,587(14):2266-2271.
[13]Shen ZZ,Pan X,Miao LF,et al.Comprehensive analysis of human cytomegalovirus microRNA expression during lytic and quiescent infection[J].PLoS One,2014,9(2):e88531.
[14]Huang Y,Qi Y,Ruan Q,et al.A rapid method to screen putative mRNA targets of any known microRNA[J].Virol J,2011,8:8.
[15]Wu MX.Roles of the stress?induced gene IEX?1 in regulation of cell death and oncogenesis[J].Apoptosis,2003,8(1):11-18.
(編輯 王又冬)
Human Cytomegalovirus microRNA miR?UL70?5P Suppresses the Expression of Immediate Early Response 3
LIU Zhong?yang,QI Ying,GUO Xin,JIANG Shu?juan,HUANG Yu?jing,SHAO Yao?zhong,RUAN Qiang
(Virus Laboratory,Shengjing Hospital,China Medical University,Shenyang 110004,China)
ObjectiveTo find the target message RNAs(mRNAs)of human cytomegalovirus(HCMV)microRNA(miRNA)miR?UL70?5P,and to detect regulation effects of miR?UL70?5p on protein expression of these target mRNAs.MethodsHybrid?PCR was used to screen the poten?tial target mRNAs in the pool of human embryo lung fibroblast(HELF)total RNAs.Luciferase report assay was used to identify the specific banding of miR?UL70?5P to the target mRNAs.Western blot was performed to validate the regulation effects of miR?UL70?5P on the protein expression of the target mRNAs.ResultsSeven mRNAs,including immediate early response 3(IER3),were identified as the targets of miR?UL70?5P.Over?ex?pressed IER3 in 293T cells could be down?regulated up to 30%by co?transfection of miR?UL70?5P.ConclusionHCMV miR?UL70?5p can sup?press the protein expression of its target mRNA,IER3,during infection.
cytomegalovirus;microRNAs;immediate early response 3
R373.9
A
0258-4646(2014)07-0577-04
國家自然科學基金(81171580);教育部高等學校博士學科點專項科研基金(20112104110012)
柳中洋(1985-),男,研究實習員,碩士.
阮強,E-mail:ruanq@sj?hospital.org
2014-04-14
網絡出版時間:

