碘催化合成對-正丁基苯胺的正交實驗研究
馬 琳
(1.寶雞文理學院化學化工學院,陜西寶雞721013;2.陜西省植物化學重點實驗室,陜西寶雞721013)
對-正丁基苯胺是重要的有機合成中間體之一,市場需求量較大。目前,工業化生產對-正丁基苯胺主要以苯胺和正丁醇為原料,采用ZnCl2作催化劑[1],存在腐蝕強、成本高的缺點。有研究報道,碘作為催化劑可用于多種有機反應[2-4]。作者以碘單質作催化劑合成對-正丁基苯胺[5],采用正交實驗優化了合成工藝條件,并為解決單質碘升華附著設備問題,嘗試以I2/Al2O3作催化劑合成對-正丁基苯胺。
1 實驗
1.1 試劑與儀器
正丁醇、苯胺、Al2O3均為分析純,碘(純度≥99.8%)。
FYX0.2型高壓釜(300mL),大連通產高壓釜容器制造有限公司;GC900A型氣相色譜儀,上海科創色譜儀器有限公司;GC6890型氣相色譜儀、MS5973型質譜儀,美國安捷倫公司。
1.2 方法
1.2.1 單質碘作催化劑
將混合原料(正丁醇與苯胺物質的量比為0.8∶1,由工業生產條件確定[1])加入高壓反應釜中,再加入催化劑碘。用氮氣置換釜內空氣3次,每次置換15 min。將反應釜溫度升至180℃,恒溫反應4h,然后將溫度升至設定反應溫度,恒溫反應一定時間。反應結束后待氣壓表讀數歸零,從取液口取樣,反應產物為淡棕紅色。
首先進行單因素實驗初步考察影響對-正丁基苯胺收率的主要因素,然后根據單因素實驗結果[5],選擇反應溫度、反應時間、碘量和攪拌速度作為考察因素,以對-正丁基苯胺收率為考核指標,進行4因素3水平正交實驗以優化合成條件[6],正交實驗的因素與水平見表1。
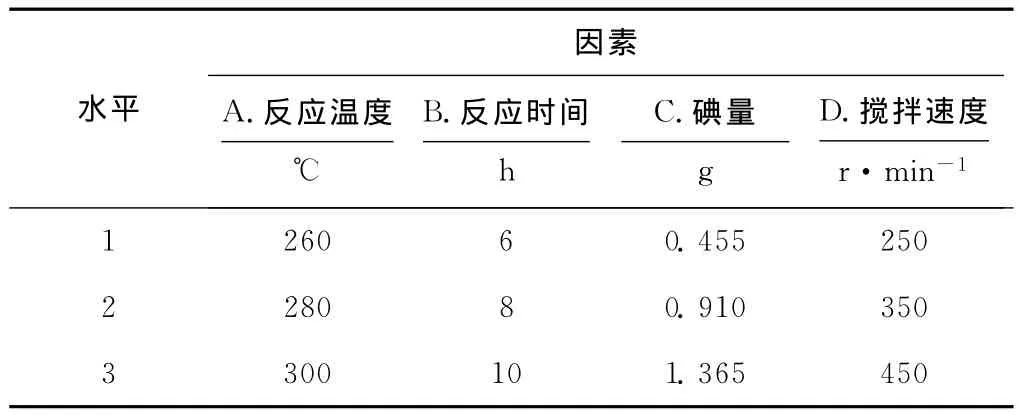
表1 正交實驗的因素與水平Tab .1 The factors and levels of the orthogonal experiment
1.2.2 I2/Al2O3作催化劑
1)I2/Al2O3的制備:稱取一定量烘干至恒質量的γ-Al2O3加入碘酒中,加熱回流6h,冷卻至室溫后抽濾,用無水乙醇淋洗,重復3次,再用蒸餾水洗至中性,60℃干燥12h[7]后迅速放入干燥器中,自然冷卻,即制得I2/Al2O3催化劑,稱量,按下式計算碘負載量[8]:
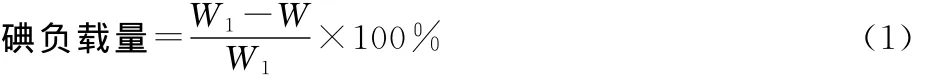
式中:W、W1分別為負載前、后活性炭的質量,g。
2)以I2/Al2O3代替單質碘作催化劑合成對-正丁基苯胺,反應條件選擇正交實驗確定的最優條件。
1.3 分析檢測
首先對反應產物進行GC-MS分析確定產品峰位置,然后用氣相色譜儀分析各峰產物,色譜定量采用峰面積歸一法,按式(2)~(4)計算對-正丁基苯胺的收率[9]:

式中:npt為時間為t時目標產物的量;∑npt為時間為t時總產物的量;At為時間為t時反應物的GC峰面積;A0為初始反應物的GC峰面積。
2 結果與討論
2.1 單質碘作催化劑
2.1.1 反應產物的確定
固定正丁醇與苯胺物質的量比為0.8∶1,在單因素實驗確定的較優條件[5][反應溫度280℃、反應時間8h、碘量0.455g(占苯胺質量的5‰)]下進行實驗。用氣相-質譜聯用儀(GC-MS)檢測反應產物,發現確有對-正丁基苯胺生成,并且確定目標產物的峰為峰3(圖1a)。進一步測定產物的氣相色譜,見圖1b。
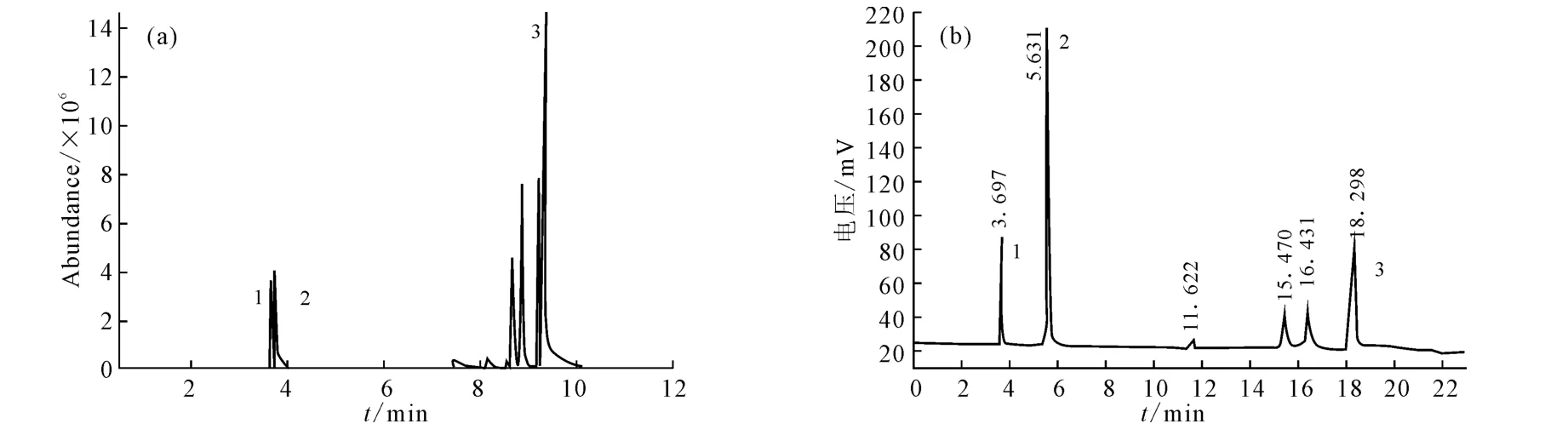
圖1 單質碘作催化劑時,產物的GC-MS(a)和GC(b)圖譜Fig.1 GC-MS(a)and GC(b)of the products using I2as catalyst
2.1.2 正交實驗結果與分析(表2)
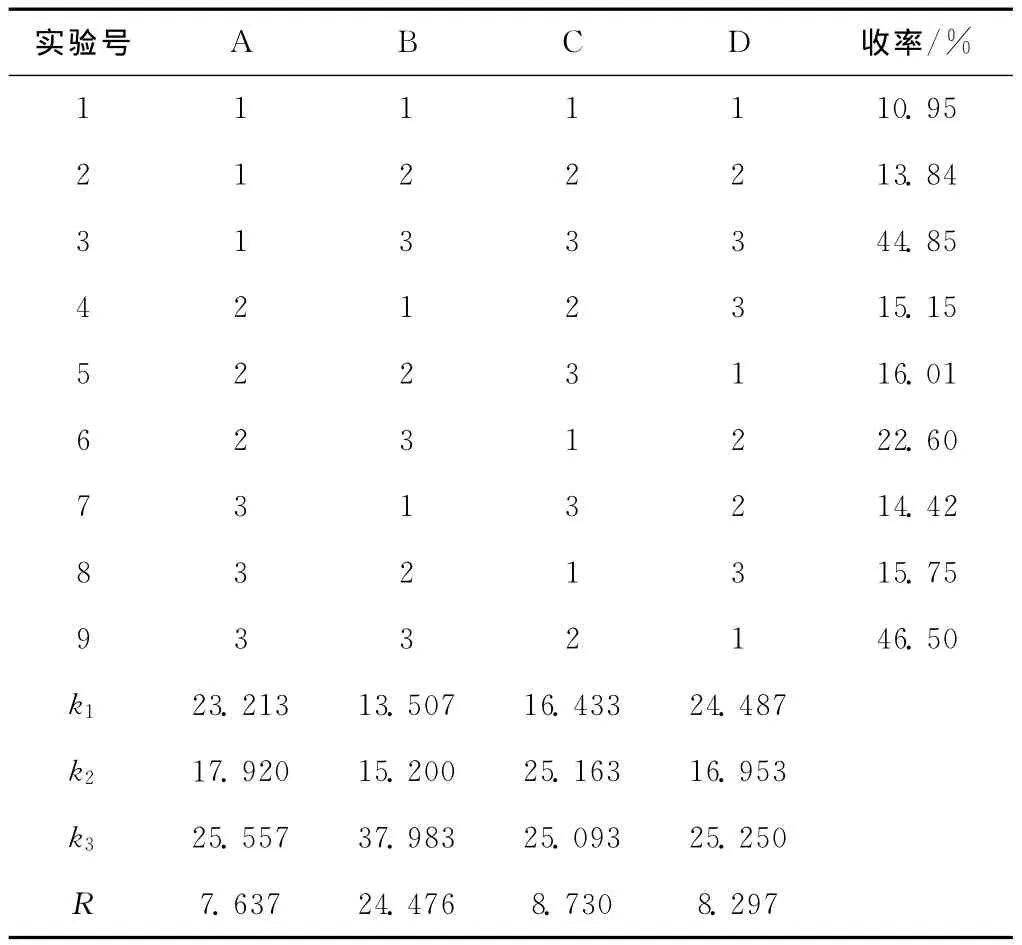
表2 正交實驗結果與分析Tab .2 The results and analysis of the orthogonal experiment
由表2可知,各因素對對-正丁基苯胺收率的影響大小依次是:反應時間>碘量>攪拌速度>反應溫度,最佳條件是A3B3C2D3,即反應溫度300℃、反應時間10h、碘量0.910g、攪拌速度450r·min-1。
在優化條件下進行3次平行實驗,對-正丁基苯胺收率分別為48.05%、50.12%、51.36%,平均收率49.84%,高于正交實驗的最高收率,表明所確定優化條件可靠。
2.2 I2/Al2O3作催化劑
根據碘作催化劑合成對-正丁基苯胺的正交實驗結果,在正丁醇與苯胺物質的量比為0.8∶1、反應溫度為300℃、反應時間為10h、催化劑I2/Al2O3用量為4.51g(碘負載量20%)、攪拌速度為450r·min-1的優化條件下合成對-正丁基苯胺。氣相色譜分析(圖2)表明:以I2/Al2O3作催化劑確有對-正丁基苯胺生成,3次平行實驗的結果見表3。
由表3可知,以I2/Al2O3作催化劑時,對-正丁基苯胺的收率達到55.51%。
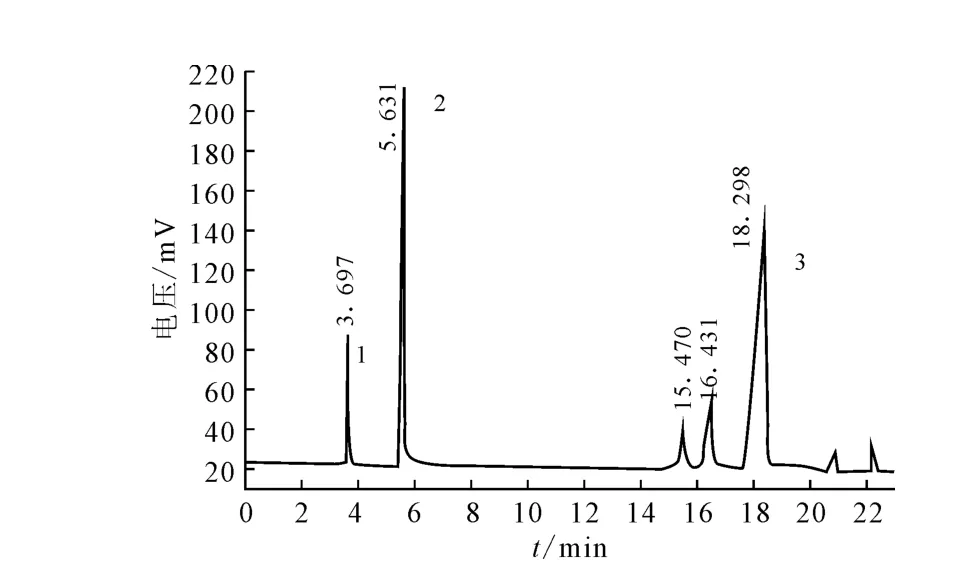
1.正丁醇 2.苯胺 3.對-正丁基苯胺圖2 I2/Al2O3作催化劑時,產物的GC圖譜Fig.2 GC of the products using I2/Al2O3as catalyst
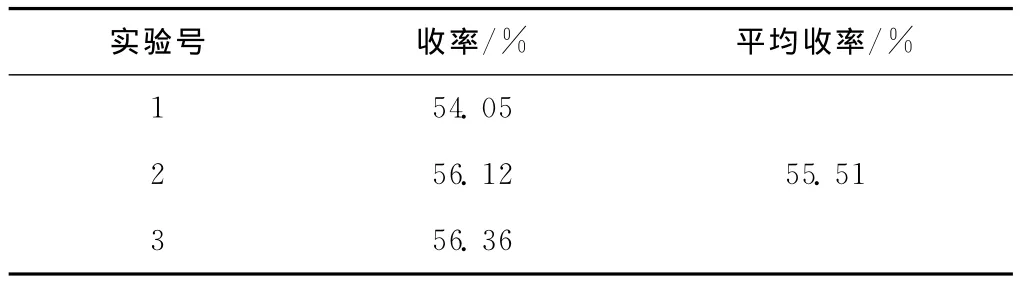
表3 I2/Al2O3作催化劑平行實驗結果Tab.3 The parrel experiment results for catalyst I2/Al2O3
2.3 討論
實驗證明,以單質碘或I2/Al2O3作催化劑均可催化正丁醇和苯胺反應生成對-正丁基苯胺,且都不腐蝕反應器。實驗結束后,打開高壓反應釜觀察發現:以單質碘作催化劑時,由于碘受熱升華易附著在設備上難以清洗,催化劑不易回收;以I2/Al2O3作催化劑,Al2O3不但起到碘催化劑載體的作用,而且還能吸附回收碘,使碘在反應釜上的附著量大大減少,環境友好,催化劑亦可重復利用。比較單質碘作催化劑和I2/Al2O3作催化劑的合成結果,發現I2/Al2O3催化合成目標產物的收率高于單質碘。后續可進一步優化I2/Al2O3催化合成對-正丁基苯胺的條件,亦可嘗試選用固定床反應器以進一步提高對-正丁基苯胺收率。
3 結論
以碘作催化劑、以正丁醇與苯胺為原料在高壓反應釜內催化合成對-正丁基苯胺,用GC-MS和氣相色譜對產物進行定性和定量分析。通過正交實驗確定最佳反應條件如下:反應溫度300℃、反應時間10h、碘量0.910g(占苯胺質量的10‰)、攪拌速度450r· min-1,在此條件下,對-正丁基苯胺收率為49.84%,并在以負載型催化劑I2/Al2O3代替單質碘時達到55.51%。
[1] 章思規.精細有機化學品技術手冊[M].北京:科學出版社,1991:264-267.
[2] 王宏社,苗建英,趙立芳.碘作為催化劑在有機合成中的應用[J].有機化學,2005,25(6):615-618.
[3] 劉星明,袁先友.碘催化劑在精細有機物合成中的研究進展[J].湖南科技學院學報,2008,29(4):55-58.
[4] 沈舒蘇,徐小平,紀順俊.分子碘催化的有機反應研究進展[J].有機化學,2009,29(5):806-811.
[5] 馬琳,張秀成,陳立宇.單質碘催化合成正丁基苯胺[J].重慶工學院學報(自然科學版),2008,22(2):52-54.
[6] 李云雁,胡傳榮.試驗設計與數據處理[M].北京:化學工業出版社,2008:128-142.
[7] 劉星明,袁先友.微波促進活性炭負載單質碘催化合成乙酰乙酸乙酯縮酮[J].湖南科技學院學報,2008,29(8):47-50.
[8] 田曉燕,胡奇林,田大年,等.活性炭負載單質碘催化合成季戊四醇雙縮酮[J].寧夏工程技術,2006,5(2):137-139.
[9] 唐培堃.精細有機合成化學及工藝學[M].第十二版.天津:天津大學出版社,2007:40-41.

