MR對聚丙烯酰胺面部注射后期移位的診斷價值
聞彩云 王智廷 周曉軍 曹國全 葛玉杰
MR對聚丙烯酰胺面部注射后期移位的診斷價值
聞彩云 王智廷 周曉軍 曹國全 葛玉杰
目前,聚丙烯酰胺(polyacrylamide hydrophilic gel,PAHG)在軟組織注射填充術(shù)中的應(yīng)用日益增多,術(shù)后并發(fā)癥也隨之增多,臨床對PAHG隆乳術(shù)后并發(fā)癥的影像學(xué)研究較多,但有關(guān)面部注射術(shù)后并發(fā)癥的影像學(xué)檢查報道尚少見。現(xiàn)將本院收治的11例(23處)PAHG面部注射患者(術(shù)后超過5年)的MR資料作一回顧性分析,現(xiàn)報道如下。
1 臨床資料
1.1 一般資料 選取2010-01—2012-03來我院就診的11例女性患者,年齡29~48歲,平均36歲。均于外院行PAHG面部注射術(shù),注入時間6~10年,平均7.8年,具體注射量均無原始病例記載,注射部位分別為嘴唇、顳部、頰部、額部、鼻部、頦部。
1.2 檢查方法 采用GE 3.0T超導(dǎo)MR掃描儀。掃描方法:患者取仰臥位,使用8通道頭顱線圈,分別行AX FSE T2WI-FS、AX FSE T1WI、3D space T2WI-FS序列掃描,部分隆鼻患者加掃SAG STIR序列、豐頰患者加掃COR STIR序列。2D掃描采用視野20cm×20cm或24cm×24cm,層厚4.0mm,間隔1.0mm;3D掃描采用層厚1.6mm。
1.3 結(jié)果 PAHG于T1WI表現(xiàn)為低信號,與肌肉、腺體信號相似;T2WI-FS、STIR則表現(xiàn)為明顯高信號,可清晰顯示移位于皮下、肌間隙、腺體內(nèi)的PAHG。本組11例患者23個PAHG注射處,除1例雙側(cè)顳部注射者判定為PAHG尚完整未發(fā)生移位外,其余均表現(xiàn)為不同程度PAHG移位:較多病例表現(xiàn)為PAHG向皮下(圖1)或周圍表淺的間隙(圖2)滲漏移位,較少病例PAHG表現(xiàn)為潛在較深的頜面部間隙(圖3)或腺體內(nèi)(圖4)游走移位。其中發(fā)生遠(yuǎn)處游走移位7例(8處,詳見表1)。
2 討論
臨床上關(guān)于注射PAHG發(fā)生移位的時間結(jié)論不一,國外一般為10~15年,國內(nèi)一般為5~10年[1]。因此本研究均選擇PAHG注射5年以上的患者作為觀察對象。林軍等[2]對PAHG隆乳術(shù)后并發(fā)癥研究,發(fā)現(xiàn)移位發(fā)生率占并發(fā)癥的7.6%,面部注射術(shù)后的并發(fā)癥亦以PAHG游走移位較多見。
郭偉[3]認(rèn)為,早期PAHG移位原因與手術(shù)操作不當(dāng)、術(shù)后處理不正確、受術(shù)者保護(hù)不當(dāng)?shù)纫穑笃谝莆豢赡苤饕c材料本身的物理特性有關(guān)。PAHG存在一定的流動性,可隨重力作用、肌肉收縮等因素沿組織間隙向身體的低位或沿肌束水平方向移動。盲視下注射PAHG后可因錯誤的注射層次、組織彈性、重力、體位、肌肉收縮、術(shù)后按摩等因素使PAHG沿面部表淺肌肉腱膜系統(tǒng)淺層向四周甚至面深部間隙擴(kuò)散、游走移位,導(dǎo)致注射后假體形態(tài)不穩(wěn),而術(shù)中、術(shù)后局部加壓過大等不當(dāng)處理更可加劇填充物蔓延。游離移位PAHG多數(shù)以大小不等分散的團(tuán)塊形式分布于頜面部組織間隙、脂肪或肌肉的結(jié)締組織內(nèi)。本組所觀察到的PAHG移位多屬此類。同時,由于手術(shù)不當(dāng),正常的組織結(jié)構(gòu)受到損傷,PAHG也會經(jīng)破損處向遠(yuǎn)處組織內(nèi)移位,部分甚至達(dá)到乳突、腮腺內(nèi)。本組中1例頰部注射患者頰部PAHG由雙耳前皮下、腮腺前緣進(jìn)入腮腺,可能是因手術(shù)中損傷了原本致密的腮腺鞘所致。
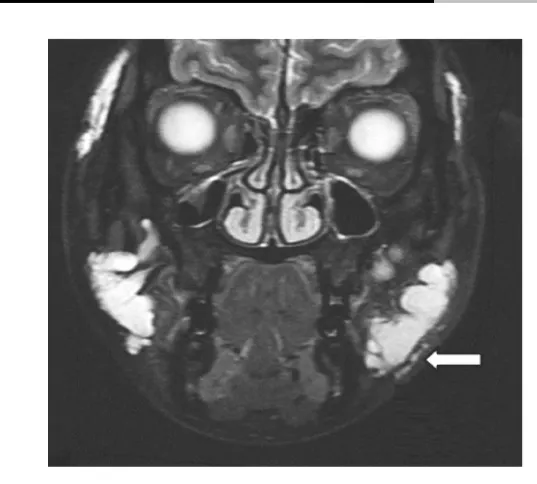
圖1 1例豐顳豐頰患者,左側(cè)頰部PAHG整體向下移位,同時頰部皮下可見線條狀PAHG滲漏移位(箭頭所示)
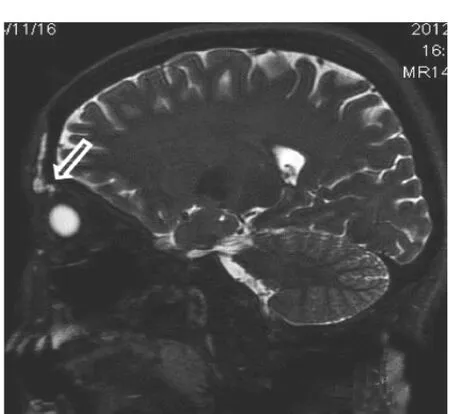
圖2 PAHG沿淺表間隙移位至右上瞼皮下、眼輪匝肌內(nèi)(箭頭所示)
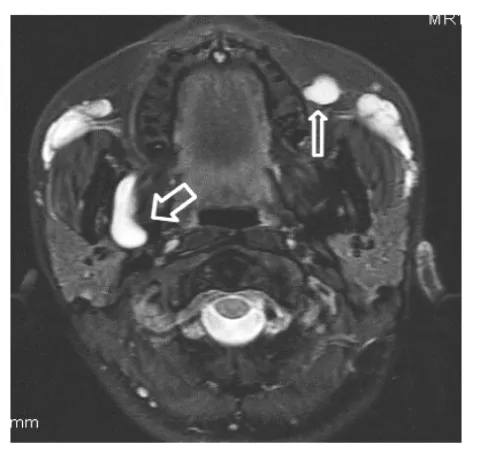
圖3 大塊PAHG游離移位至右側(cè)咽旁間隙(粗箭頭所示),同時左側(cè)頰部皮下亦可見團(tuán)塊狀PAHG游離移位(細(xì)箭頭所示)
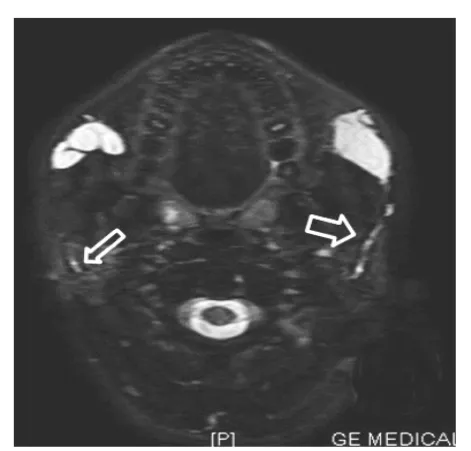
圖4 3D space圖像可見線條狀PAHG進(jìn)入雙側(cè)腮腺內(nèi)

表1 PAHG面部注射術(shù)后PAHG遠(yuǎn)處游走移位情況
MRI能清晰顯示移位PAHG的范圍及分布位置,提示皮下、肌間隙或腺體內(nèi)有無游離PAHG,并可確定其移位的范圍。3D SPACE序列成像具有薄層、無間隔掃描的特點,可獲得<1mm層厚的圖像,并能任意方向重建,較2D MR掃描更能直觀顯示細(xì)線狀的PAHG移位。但3D SPACE成像方法也存在一定缺陷,其對組織信號的抑制能力強(qiáng),除滲漏移位外的其他并發(fā)癥無明顯檢出率。
[1]郭金才,王玉榮.乳房假體破裂及注射PAHG擴(kuò)散的磁共振成像[J].放射學(xué)實踐,2004,19(5):338-340.
[2]林軍,錢云良,楊群,等.聚丙烯酰胺PAHG注射隆乳術(shù)后并發(fā)癥118例分析[J].中華整形外科雜志,2007,23(2):101.
[3]郭偉.聚丙烯酰胺PAHG注射隆乳術(shù)后并發(fā)PAHG遠(yuǎn)處移位16例分析[J].中華誤診學(xué)雜志,2008,8(31):7761-7762.
2012-05-25)
(本文編輯:歐陽卿)
325000 溫州醫(yī)科大學(xué)附屬第一醫(yī)院磁共振室

