靈芝三萜酸組分高效液相色譜指紋圖譜初探
魏曉霞 李鵬 孫紅 莊捷
(1福建省立醫院藥學部,福建福州 350001;2福建醫科大學藥學院天然藥物學系,350004)
靈芝三萜酸組分高效液相色譜指紋圖譜初探
魏曉霞1李鵬2孫紅1莊捷1
(1福建省立醫院藥學部,福建福州 350001;2福建醫科大學藥學院天然藥物學系,350004)
目的:建立靈芝三萜酸組分(GLA)的指紋圖譜,為其質量控制提供依據。方法:使用植物組織破碎法提取GLA,利用高效液相色譜法建立GLA的指紋圖譜。結果:GLA高效液相色譜指紋圖譜中有8個峰為其主要特征,其α值分別為0.68,0.73,0.90,0.95,1.00,1.12,1.36,1.46。結論:所建立的RP-HPLC指紋圖譜分析方法可為GLA的質量控制提供理論依據。
靈芝三萜酸;指紋圖譜;高效液相色譜法
靈芝(Ganoderma lucidum[Leys.ex Fr.]Karst)為多孔菌科(polyproraceae)、靈芝屬(Ganoderma)真菌植物赤芝(Ganoderma lucidum[Leys.ex Fr.] Karst)或紫芝(Ganoderma japonicum[Fr.]Lloyd)的干燥子實體[1]。靈芝性溫、味甘,多分布于閩、貴、云、冀、蘇、吉、浙等省,在我國已有悠久的藥用歷史,始載于《神農本草經》,具有補中益氣、扶正固本、滋補強壯之功效,是一種珍貴的中藥材[2]。三萜類化合物是靈芝主要成分之一。其中靈芝三萜酸組分(GLA)是靈芝三萜中的一大類成分,具有多種藥理活性,前期研究發現其具有一定抗腫瘤[3]和保肝作用[4],本實驗利用反相高效液相色譜(RP-HPLC)技術,建立GLA的高效液相色譜指紋圖譜,為GLA的質量控制提供實驗依據。
1 儀器與藥品
1.1 藥材
靈芝子實體精粉,3批次(批號GC-L3-20120821、GC-L3-20120922、GC-L3-20121010),由福建仙芝樓生物科技有限公司提供。
1.2 試劑
乙腈、甲醇為色譜純(國藥集團化學試劑有限公司);無水乙醇、乙酸乙酯、石油醚、冰乙酸均為分析純(國藥集團化學試劑有限公司);碳酸氫鈉為化學純(國藥集團化學試劑有限公司)。
1.3 儀器
AB204-E電子分析天平(Mettler Toledo公司);JHBE-50型閃式提取器(北京金鼐科技發展有限公司);HH-4型數顯恒溫水浴鍋(國華電器有限公司);RE-52A旋轉蒸發器(上海亞榮生化儀器廠);Agilent 1100高效液相色譜儀(美國Agilent公司),配二極管陣列檢測器,自動進樣器;處理軟件(Agilent化學工作站)。
2 方法
2.1 供試品制備
將靈芝子實體精粉經無水乙醇閃式提取、抽濾與減壓蒸餾后,無水乙醇提取浸膏拌硅藻土后,以石油醚索氏提取除雜后再用乙酸乙酯提取,乙酸乙酯提取液用飽和NaHCO3溶液萃取,NaHCO3層酸化后再用乙酸乙酯萃取,減壓濃縮真空干燥即得GLA[5]。共制備3批次來源于靈芝子實體精粉的GLA樣品備用。參照《中華人民共和國藥典》RP-HPLC的有關規定[6],精確稱取GLA樣品,用乙腈配成10 mg/mL供試品,0.45 μm微孔濾膜過濾,RP-HPLC進樣量5 μL。
2.2 色譜條件
依利特C18色譜柱(250 mm×4.6 mm,5 μm);填料Hypersil ODS 25 μm(柱號E1720569);流動相甲醇-水(含2%乙酸),梯度洗脫條件見表1;檢測波長252 nm;進樣量5 μL;流速0.8 mL/min;柱溫35℃。
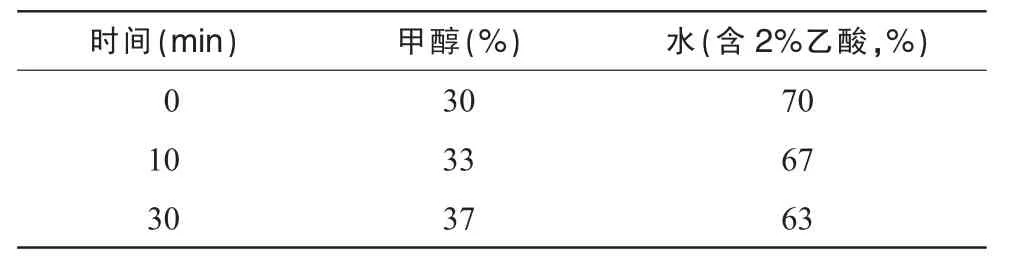
表1 線性梯度洗脫條件(體積百分比%)
2.3 HPLC分析
取3批次供試品溶液5 μL,注入高效液相色譜儀,自動積分記錄色譜圖(圖1、圖2、圖3)和各色譜峰的保留時間,以面積歸一化法計算各色譜峰的相對峰面積。
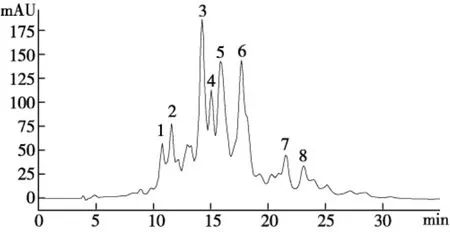
圖1 GLA的RP-HPLC圖(批次GC-L3-20120821)
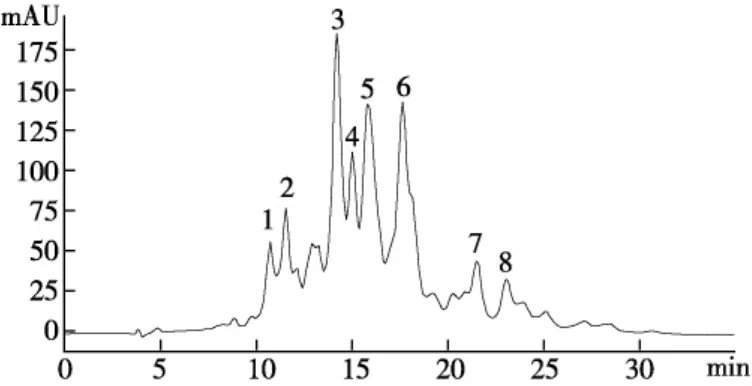
圖2 GLA的RP-HPLC圖(批次:GC-L3-20120922)

圖3 GLA的RP-HPLC圖(批次:GC-L3-20121010)
2.4 相對保留值指紋圖譜的確定
選擇一個保留時間居中且在各樣品中均存在的色譜峰作為參照物,指定它的相對保留時間(relative retention time)α=1,并分別求出樣品中各組分的相對保留值為:
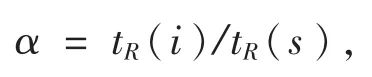
式中tR(i)為各組分的出峰時間,tR(s)為參照峰的出峰時間。
以某一樣品的色譜峰總面積為分母,各樣品中每個色譜峰面積為分子,求得該色譜峰的相對峰面積(ratio of peak area,RA),將它標在其α值項下,最后將各樣品的α按由小到大的次序依次排列成行。每個樣品色譜峰的相對保留值α和相對峰面積RA構成了其HPLC的指紋特征。
2.5 方法學考察
2.5.1 精密度試驗取同一GLA樣品,按2.1制備供試品,連續進樣5次,考察主要色譜峰的α和RA的一致性。相對標準偏差(RSD)是試驗可信度的一種考察標準,根據檢測數據,計算各自的RSD。
2.5.2 穩定性試驗取同一GLA樣品,按2.1制備供試品,分別在0 h,4 h,8 h,12 h和16 h檢測指紋圖譜,考察主要色譜峰的α和RA的一致性,并計算各自的RSD。
2.5.3 重現性試驗取同一批號GLA樣品5份,按2.1制備供試品,考察主要色譜峰的α和RA的一致性,并計算各自的RSD。
3 結果
3.1 GLA色譜圖
按2.3進行HPLC分析,得到3批次GLA高效液相色譜圖,見圖1、圖2、圖3。
3.2 指紋峰的標定
采用α標定指紋峰,以5號色譜峰作為參照峰,計算各待測峰的α及RA。結果見表2,表3。3批次GLA供試品中含量較高的峰集中在0.90~1.11區域,α值為0.90(峰3),0.95(峰4),1.00(峰5),1.12(峰6)處有4個較強峰;0.68(峰1),0.73(峰2),1.36(峰7),1.46(峰8)處有4個中等強峰。這8個色譜峰的RA均占總峰面積的3.3%以上,說明這8個峰的含量較高,可能是GLA組分中的主要成分。
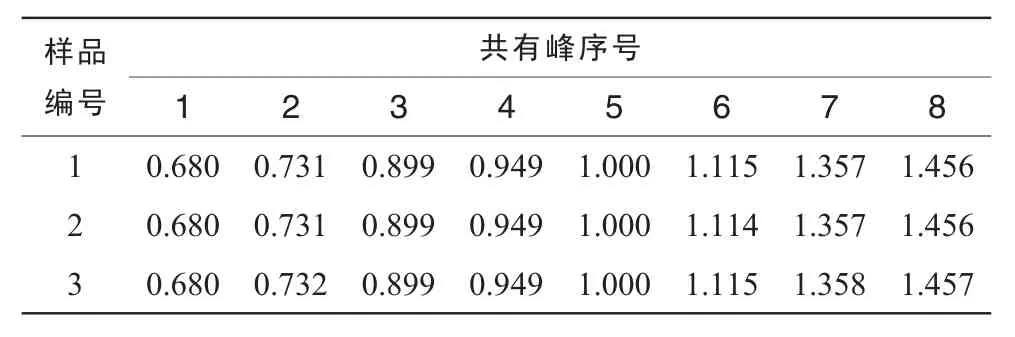
表2 GLA指紋圖譜共有峰相對保留時間(α)
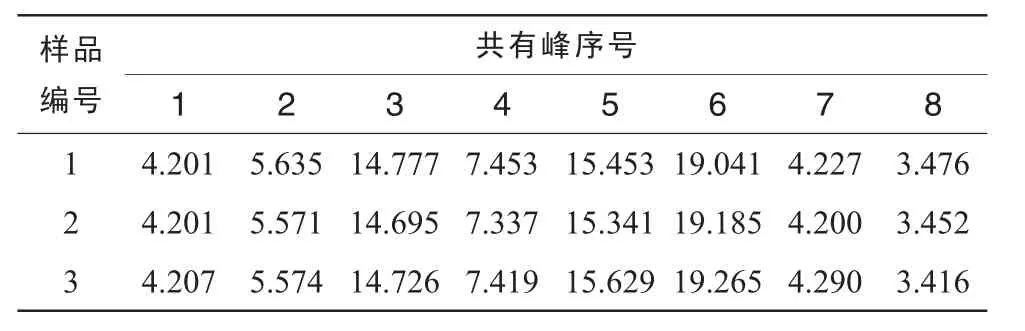
表3 GLA指紋圖譜共有峰相對峰面積(RA)
3.3 儀器精密度
分別取同一供試品溶液5 μL,連續進樣5次,色譜峰均自動積分。比較不同色譜圖中主要色譜峰的α和RA。結果表明,所標定色譜峰的α和RA基本一致,RSD均小于3%,符合指紋圖譜的檢測要求[7]。說明儀器系統精密度良好。見表4。
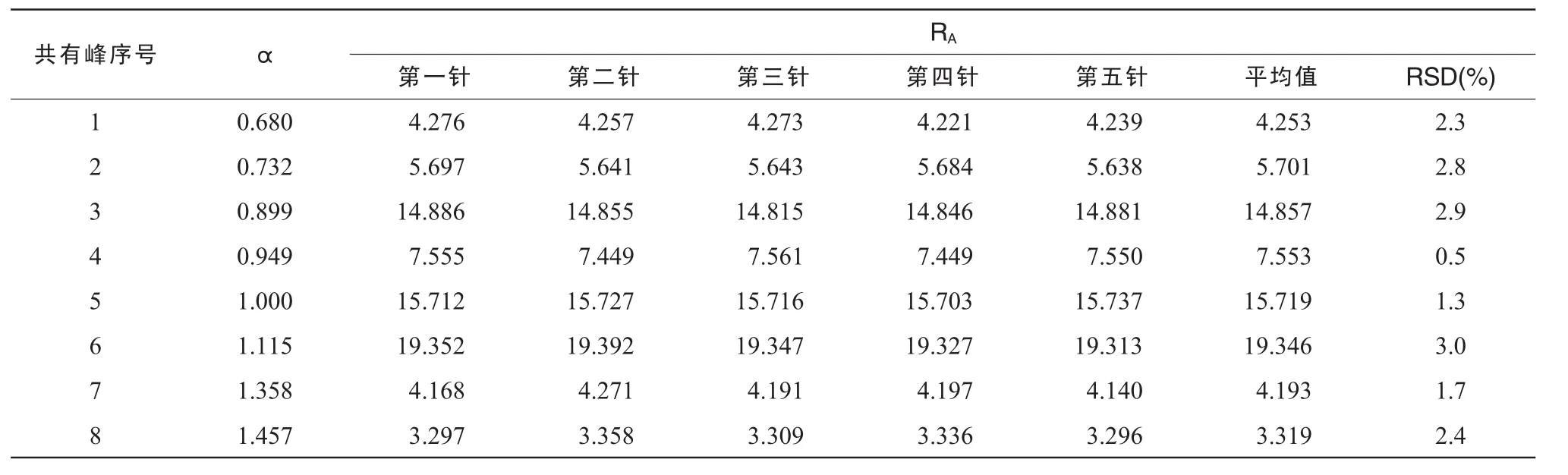
表4 GLA的精密度實驗數據
3.4 穩定性試驗
分別取同一供試品溶液5 μL,每隔4 h進樣一次,16 h內連續進樣5次,色譜峰均自動積分。比較不同色譜圖中主要色譜峰的α和RA。結果表明,所標定色譜峰的α和RA基本一致,RSD均小于3%,符合指紋圖譜的檢測要求[6]。說明GLA樣品性能比較穩定。見表5。
3.5 重現性試驗
取同一批號靈芝子實體精粉,按2.1項下方法制備5份供試品溶液。每份樣品進樣5 μL,色譜峰均自動積分。結果表明,所標定色譜峰的α和RA基本一致,RSD均小于3%,符合指紋圖譜的檢測要求。所考察的共有色譜峰的重現性良好。見表6。
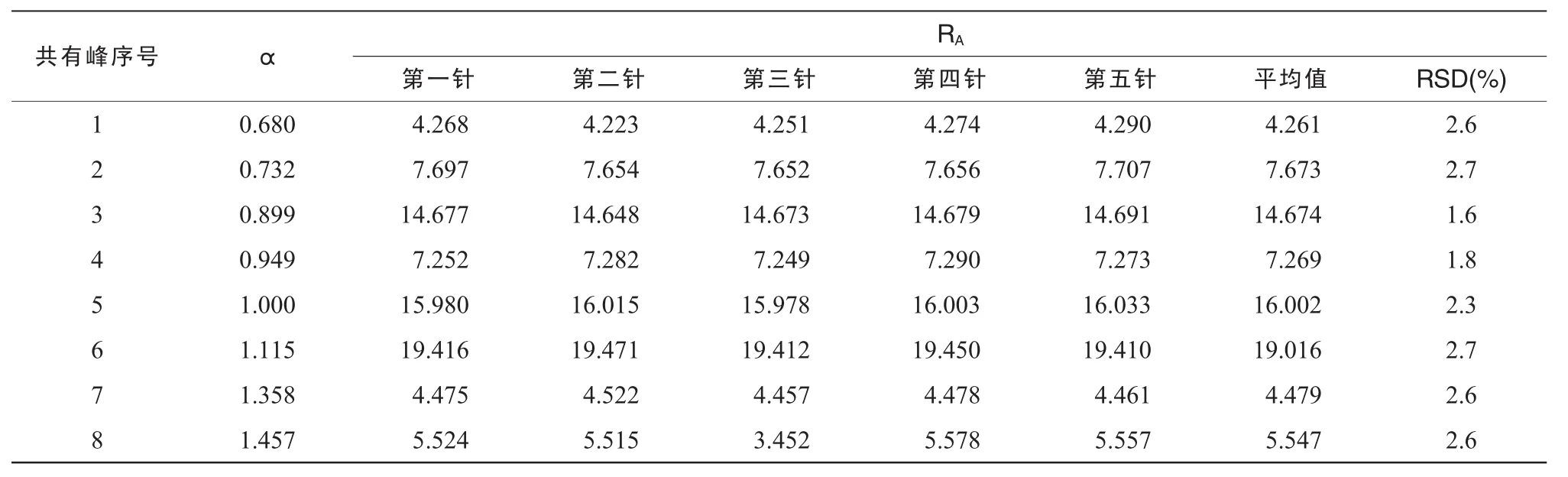
表5 穩定性實驗數據
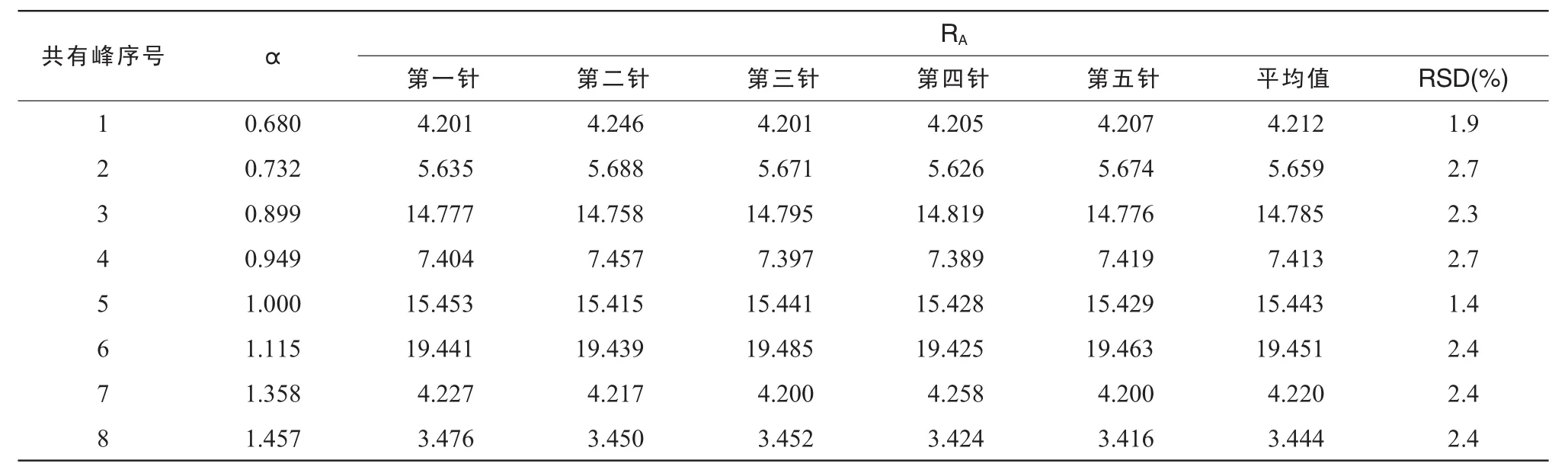
表6 GLA重現性實驗數據
4 討論
中藥的藥效是所含有的多種化學成分通過多靶點、多環節發揮綜合作用的結果,GLA的藥效是多種靈芝三萜酸類成分共同起作用的結果。僅分析測定一種或某幾種靈芝三萜酸來評價其質量是不全面的,本文建立的GLA高效液相色譜指紋圖譜是GLA中三萜酸類成分整體的綜合表達,更能全面評價GLA的質量。因此,GLA的RP-HPLC指紋圖譜是控制GLA質量的有效手段,具有一定必要性和先進性。本文所建立的方法得到的色譜指紋圖譜多數峰未達到基線分離,因此不適用于GLA的定量控制,但可以作為GLA質量控制中的定性控制方法。通過測定一種或某幾種靈芝三萜酸來作為GLA質量的定量控制方法,再結合本文建立的GLA質量的定性控制方法,可以全面控制GLA質量。3批次GLA樣品的指紋圖譜,各主要色譜峰的α分別為0.68,0.73,0.90,0.95,1.00,1.12,1.36,1.46。這8個色譜峰為3批次供試品的共有指紋峰,是鑒別GLA樣品的必要條件之一。
[1]國家藥典委員會.中華人民共和國藥典(2010年版)一部[S].北京:中國醫藥科技出版社,2010:174.
[2]江蘇新醫學院.中藥大辭典[M].上海:上海科學技術出版社,1985:1180-1182.
[3]魏曉霞,李鵬,許建華,等.靈芝三萜組分GLA體內外抗腫瘤作用的研究[J].福建醫科大學學報,2010,44(6):417-418.
[4]李鵬,魏曉霞,南婷婷,等.靈芝三萜酸對小鼠急性肝損傷的保護作用[J].中國醫院藥學雜志,2013,33(23):4-8.
[5]徐任生,陳仲良.中草藥有效成分提取與分離[M].2版.上海科學技術出版社:218-223.
[6]潘君漢.淺談中藥指紋圖譜的意義[J].中國藥業,2008,17(6):13-14.
[7]國家食品藥品監督管理局.關于印發《中藥注射劑指紋圖譜研究的技術要求(暫行)》的通知[J].中國藥品標準,2000,1(4):3.
Preliminary Study on HPLC Fingerprint of Triterpene acids Components from Ganoderma Lucidum
Wei Xiaoxia1,Li Peng2,Sun Hong1,Zhuang Jie1(1 Pharmacy Department of Fujian Provincial Hospital,Fujian Fuzhou 350001,China;2 Department of Natural Medicines of Pharmaceutical College of Medical University,350004)
Objective:To set up the fingerprint of triterpene acids components of ganoderma lucidum(GLA)and to provide a basis for its quality control. Methods:To extract the triterpene acids components of ganoderma lucidum by plant tissue crushing method and to establish the fingerprint of GLA by HPLC.Results:There were 8 characteristic peaks in HPLC fingerprint of GLA,their alpha values were 0.68,0.73,0.90,0.95,1.00,1.12,1.36 and 1.46 respectively.Conclusion: The established RP-HPLC fingerprint can provide a theoretical basis for the quality control of GLA.
Ganoderma lucidum;Triterpene acids;Fingerprint;HPLC
10.3969/j.issn.1672-5433.2014.04.006
2014-02-08)
國家自然科學青年基金(81202560);福建省教育廳科技計劃項目(JA11107);2011年福建省高校產學合作科技重大項目(2011Y4003)
魏曉霞,女,碩士。研究方向:腫瘤藥理。通訊作者E-mail:xxwei0321@163.com

