宮頸癌局部治療前新輔助化療的效果觀察
范克軍,于興江
宮頸癌是最常見(jiàn)的婦科惡性腫瘤,其發(fā)病率僅次于乳腺癌,在所有惡性腫瘤中占第7位。近年來(lái),宮頸癌的發(fā)病率呈升高和低齡化趨勢(shì),傳統(tǒng)的治療方法為手術(shù)加放療,病灶>4 cm及ⅡB期均需放療,但復(fù)發(fā)率高,且放療并發(fā)癥較多,嚴(yán)重影響患者生活質(zhì)量,尤其對(duì)年輕患者卵巢功能影響,有研究認(rèn)為合理的新輔助化療不僅可消滅微轉(zhuǎn)移灶,還可以縮小腫瘤體積和范圍,提高手術(shù)或放療效果。本文對(duì)2005年06月—2009年04月在筆者所在醫(yī)院41例局部晚期宮頸癌患者新輔助化療的療效進(jìn)行分析,并探討其在宮頸癌治療中的意義。
1 資料與方法
1.1 一般資料 選取2005年06月—2009年04月在筆者所在醫(yī)院手術(shù)前接受新輔助化療的宮頸癌患者41例;年齡26~71歲,中位年齡45歲;臨床分期:按照FIGO分期標(biāo)準(zhǔn)分期:ⅠB2期6例,ⅡA期12例,ⅡB期23例;病理分級(jí):G1者4例,G2者25例,G3者12例;病理類型:鱗癌37例,腺癌1例,腺鱗癌2例,小細(xì)胞癌1例。選取同時(shí)期直接手術(shù)宮頸癌患者25例為對(duì)照組;年齡31~74歲,中位年齡50歲;臨床分期:ⅠB2期12例,ⅡA期12例,ⅡB期1例;病理分級(jí):G1者2例,G2者10例,G3者13例;病理類型:鱗癌21例,腺癌1例,腺鱗癌2例,子宮內(nèi)膜樣腺癌1例。
1.2 治療方法
1.2.1 新輔助化療 術(shù)前動(dòng)脈介入化療者14例,經(jīng)皮一側(cè)股動(dòng)脈穿刺插管雙側(cè)髂內(nèi)動(dòng)脈灌注化療加或不加栓塞治療,采用順鉑為主的化療方案,化療后1周內(nèi)行手術(shù);靜脈化療者16例,采用BIP或PF方案,3周后手術(shù);動(dòng)脈介入聯(lián)合靜脈化療者11例,化療3周后手術(shù),方案同前。新輔助化療后經(jīng)臨床婦科檢查病灶縮小宮旁條件改善者行手術(shù)治療,若術(shù)后病理發(fā)現(xiàn)盆腔淋巴結(jié)陽(yáng)性、宮旁脈管有癌栓或?qū)m旁切緣及陰道切緣陽(yáng)性則行放療。
1.2.2 直接手術(shù) 直接手術(shù)者25例,手術(shù)方式為廣泛全子宮切除術(shù)+盆腔淋巴結(jié)切除術(shù),<40歲及要求保留卵巢的鱗癌患者保留一側(cè)或雙側(cè)卵巢,并行卵巢移位術(shù)。
1.3 療效判斷指標(biāo) 新輔助化療組患者接受化療前通過(guò)婦科檢查及影像學(xué)檢查測(cè)量病灶大小,術(shù)后根據(jù)病理測(cè)量病灶大小。根據(jù)WHO標(biāo)準(zhǔn):完全緩解(CR)指腫瘤完全消失,部分緩解(PR)指腫瘤縮小50%以上,穩(wěn)定(SD)指腫瘤增大或縮小不超過(guò)25%,且無(wú)新病灶出現(xiàn):進(jìn)展(PD)指腫瘤增大或縮小超過(guò)25%,或有新病灶出現(xiàn)[3]。有效為CR+PR。
1.4 統(tǒng)計(jì)學(xué)方法 采用SPSS 12.0軟件包進(jìn)行統(tǒng)計(jì)學(xué)分析,以t檢驗(yàn)比較手術(shù)時(shí)間和出血量,以χ2檢驗(yàn)比較其他計(jì)數(shù)資料。P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié) 果
2.1 兩組宮頸癌患者臨床病理特征 兩組患者的年齡、病理類型、分化程度差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05),臨床分期經(jīng)χ2檢驗(yàn)差異有統(tǒng)計(jì)學(xué)意義(P<0.01),新輔助化療組晚期病例較多(表1)。
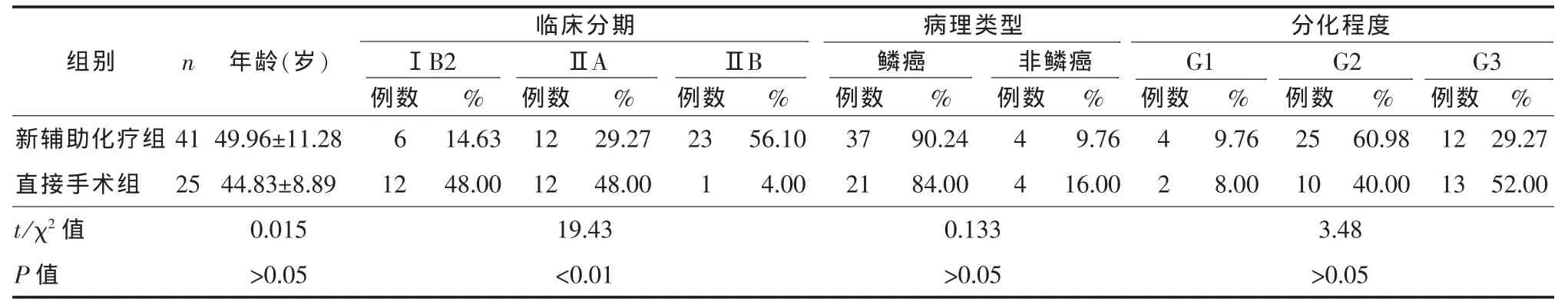
表1 66例宮頸癌患者臨床及病理特征
2.2 新輔助化療療效評(píng)價(jià) 41例接受新輔助化療者均成功施行了手術(shù),總有效率為 58.54%(24/41),其中 CR 為 4.88%(2/41),PR 53.66%(22/41),SD 36.59%(15/41),PD 4.88%(2/41),見(jiàn)表2。
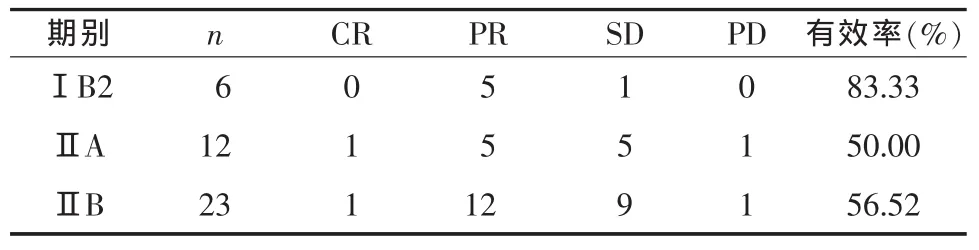
表2 41例宮頸癌新輔助化療效果
2.3 手術(shù)情況 所有患者均行廣泛全子宮切除術(shù)加盆腔淋巴結(jié)切除術(shù),41例行新輔助助化療者術(shù)中出血50~3500 ml,平 均 (1207±762) ml,手 術(shù) 時(shí) 間 150~350 min,平均 (247±56) min,對(duì)照組術(shù)中出血 150~2000 ml,平均 (878±522) ml,手術(shù)時(shí)間 150~600 min,平均 (233±94) min。兩組出血量及手術(shù)時(shí)間行t檢驗(yàn),差異均無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。術(shù)后病理:所有手術(shù)均無(wú)宮旁切緣及陰道切緣殘留,新輔助化療組淋巴結(jié)、 脈管轉(zhuǎn)移率為 36.59%(15/41),對(duì)照組轉(zhuǎn)移率 72.00%(18/25),根據(jù) χ2檢驗(yàn),χ2=6.43,差異有統(tǒng)計(jì)學(xué)意義 (P<0.05),見(jiàn)表3。
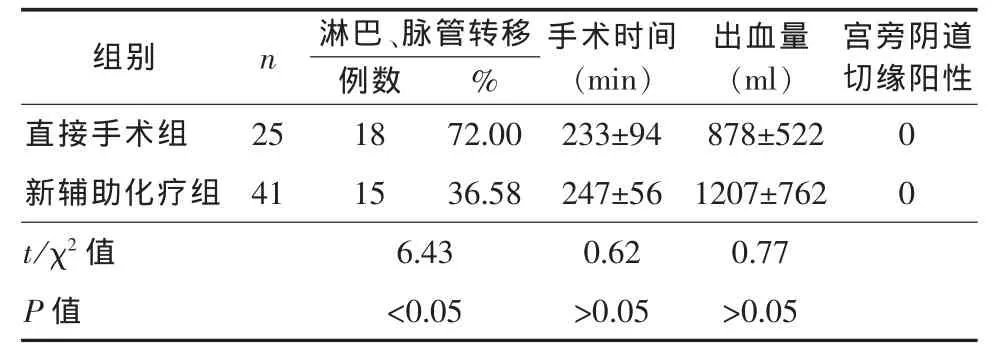
表3 兩組宮頸癌患者手術(shù)結(jié)果
3 討 論
新輔助化療是指在惡性腫瘤局部治療前 (手術(shù)或放療前)給予的全身化療,也稱早期化療、先期化療,主要用于乳腺癌、宮頸癌及頭頸部實(shí)體腫瘤的治療,即對(duì)無(wú)法手術(shù)切除或直接手術(shù)具有較大難度、估計(jì)不能達(dá)到理想的腫瘤細(xì)胞減滅術(shù)的患者,先行2~3個(gè)療程的化療后再評(píng)估能否施行根治性手術(shù)或放療[1]。近年來(lái),宮頸癌的新輔助化療越來(lái)越受到國(guó)內(nèi)外學(xué)者的重視,大量研究表明宮頸癌局部腫瘤體積大,其所伴隨的危險(xiǎn)因素增加[2],腫塊的大小與預(yù)后密切相關(guān)[3],對(duì)于腫瘤直徑>4 cm的ⅠB~ⅡA及ⅡB期患者,直接手術(shù)或放療或手術(shù)后放療遠(yuǎn)期效果均不太理想[4],而宮頸癌新輔助化療則主要應(yīng)用于該類患者。
本文中經(jīng)新輔助化療的41例患者均成功完成了手術(shù),以化療前婦檢或影像學(xué)測(cè)量病灶與術(shù)后病理測(cè)量病灶的大小變化評(píng)價(jià)療效,新輔助化療組有效率為58.45%,完全緩解率為4.87%。有文獻(xiàn)報(bào)道,以鉑類為基礎(chǔ)的聯(lián)合化療有效率多在80%以上,其中完全緩解率可達(dá)9%~18%[5],本文略低于文獻(xiàn)報(bào)道,可能與測(cè)量方法不同有關(guān)。多數(shù)文獻(xiàn)報(bào)道評(píng)價(jià)新輔助化療方法為化療后2~3周行婦科檢查或影像學(xué)測(cè)量病灶大小,本文以術(shù)后病理測(cè)量病灶的大小變化評(píng)價(jià)療效,筆者認(rèn)為更客觀、準(zhǔn)確一些。在決定手術(shù)后的輔助治療和判斷預(yù)后等方面,應(yīng)結(jié)合手術(shù)中發(fā)現(xiàn)和術(shù)后病理結(jié)果綜合考慮[6]。淋巴及脈管轉(zhuǎn)移是影響患者預(yù)后的重要因素。本文患者術(shù)后病理顯示淋巴脈管癌栓陽(yáng)性率新輔助化療組36.58%,顯著低于對(duì)照組 72.00%(P<0.05),Chen 等[7]研究提示,ⅠB2~ⅡB局部晚期宮頸癌患者新輔助化療組盆腔轉(zhuǎn)移和宮旁浸潤(rùn)率較直接手術(shù)組低,與本文結(jié)果相同。雖然本文未研究生存期,但此結(jié)果提示新輔助化療可能會(huì)改善患者的預(yù)后。手術(shù)時(shí)間兩組間差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05),新輔助化療組稍高于直接手術(shù)組,考慮與動(dòng)脈介入化療后1周內(nèi)手術(shù),組織處于充血狀態(tài)、栓塞造成宮旁組織纖維化或分期較晚有關(guān)。
本文結(jié)果證實(shí)了新輔助化療具有較好的療效,能有效地縮小腫瘤直徑,使原來(lái)不能手術(shù)的患者得到手術(shù)機(jī)會(huì),減少了淋巴脈管內(nèi)轉(zhuǎn)移,可能改善患者預(yù)后,且不增加手術(shù)時(shí)間及出血量。因此筆者認(rèn)為對(duì)于腫瘤直徑>4 cm的ⅠB~ⅡA及ⅡB期宮頸癌患者,新輔助化療聯(lián)合手術(shù)治療是其最好選擇。因本文例數(shù)較少,尚有許多不足,如未進(jìn)行化療療程、化療藥物及途徑選擇、生存期隨訪等研究,需在今后工作中進(jìn)一步完善。
[1] Parkin DM,BrayF,F(xiàn)erlay J,er al.Global cancer statistics[J].2002,CA Cancer J Clin,2005,55(1):74-108.
[2] Benedetti-Panici,SXXAmbia G,GREggi S,et al.Neo adjuvant chemotherapy and radical surgery in locally advanced cervical carcinoma:a polot study[J].Obster Gynecol,1988,71(3):344-348.
[3]明 蓉.宮頸癌新輔助化療及其對(duì)手術(shù)的影響[J].中國(guó)婦產(chǎn)科臨床雜志,2009,10(4):397-399.
[4] Huang HJ,Chang TC,Hong JH.Prognostic value of age and histologic type in neoadjuvant chemotherapy plus radical surgery for bulk(≥4cm) stage IB and Ⅱa cervical cancer[J].Int J Gynecol Cancer,2003,13(2):204.
[5]程曉東,呂衛(wèi)國(guó),葉 楓,等.局部晚期子宮頸癌新輔助化療價(jià)值的評(píng)估[J].中華婦產(chǎn)科雜志,2006,41(1):95-98.
[6]林仲秋,吳珠娜.FIGO2009外陰癌、宮頸癌和子宮內(nèi)膜癌新分期解讀[J].國(guó)際婦產(chǎn)科雜志,2009,36(4):411-412.
[7] Chen H,Liang C,Zhang L,et al.Clinical efficacy of modified preoperative neoadjuvant chemotherapy in the treatment of locally advanced cervical cancer: randomized study[J].Gynecol Oncol,2008,110(3):308-315.

