介孔Zn-Si 材料對(duì)水中亞甲基藍(lán)的吸附研究
帥超,廖運(yùn)文,2,高和軍,2,張孌孌,李宇飛
(1.化學(xué)合成與污染控制四川省重點(diǎn)實(shí)驗(yàn)室,四川 南充 637009;2.西華師范大學(xué) 應(yīng)用化學(xué)研究所,四川 南充 637009)
染料是工業(yè)廢水中常見的污染物,已經(jīng)嚴(yán)重的危害到人類賴以生存的環(huán)境[1-2]。隨著造紙、紡織、皮革以及塑料工業(yè)發(fā)展,工業(yè)廢水中的染料給環(huán)境帶來了嚴(yán)重的危害。其中,亞甲基藍(lán)是一種具有代表性的陽(yáng)離子型偶氮染料,存在于大量的工業(yè)廢水中,該染料以及其代謝中間產(chǎn)物具有致突變性、致癌性和其他毒性使其成為難處理的工業(yè)廢水[3-5]。過去幾十年,許多的研究者們通過對(duì)染料廢水的凈化研究,總結(jié)了一些常見的方法,例如:吸附、化學(xué)氧化、生物處理、離子交換和光降解等[6-7],在眾多的處理方法中,由于吸附法具有高效、操作簡(jiǎn)單以及吸附劑易回收等優(yōu)點(diǎn)[8],被認(rèn)為是去除染料廢水的最有效的方法之一。
介孔氧化硅因其具有均勻的孔道和高效的空催化和吸附領(lǐng)域中。但是,純的氧化硅材料由于框架結(jié)構(gòu)的化學(xué)惰性和孔壁無定型的本質(zhì)缺陷,使得其在工業(yè)中的應(yīng)用受到了極大限制[9]。為了提高氧化硅材料應(yīng)用的廣泛性,采取了與金屬離子摻雜的方法來提高它的性能,常用的金屬離子如Zn2+、Al3+、Fe2+等[10-11]。
本文以正硅酸乙酯和Zn(NO3)2·6H2O 為原料,采用傳統(tǒng)的化學(xué)沉淀法制備了介孔Zn-Si 材料,并研究了其對(duì)亞甲基藍(lán)的吸附能力。詳細(xì)的調(diào)查了pH、時(shí)間、溫度對(duì)吸附量的影響,探討了吸附過程的動(dòng)力學(xué)模型和等溫吸附模型。
1 實(shí)驗(yàn)部分
1.1 試劑與儀器
Zn(NO3)2·6H2O、十六烷三甲基溴化銨(CTAB)、正硅酸乙酯(TEOS)、亞甲基藍(lán)(MB)、濃鹽酸、氫氧化鈉均為分析純。
D/MAX Ultima ⅣX-射線衍射儀;Nicolet 6700傅里葉紅外光譜儀;DF-101S 集熱式恒溫加熱攪拌器;E-201-C 型pH 計(jì);UV-2550 型紫外可見分光光度計(jì)。
1.2 吸附劑合成
將3.6 g 十六烷三甲基溴化銨溶解到100 mL蒸餾水中,攪拌30 min 后得到澄清溶液。然后,稱取一定量的Zn(NO3)2·6H2O 溶解于20 mL 蒸餾水中,攪拌均勻后將其逐滴加入到上述澄清溶液中,持續(xù)攪拌得到均一的混合溶液。將一定量的正硅酸乙酯逐滴加到混合溶液,快速攪拌直到獲得澄清的溶液。向該澄清的溶液中,加入適量的氫氧化鈉溶液調(diào)節(jié)pH 值在10 左右。在60 ℃下,劇烈攪拌2 h后,用濃鹽酸將pH 值調(diào)節(jié)到7,高溫下繼續(xù)反應(yīng)3 h 后,將溶液冷卻、過濾、洗滌、干燥。隨后,在550 ℃下煅燒6 h 后獲得最終產(chǎn)品。實(shí)驗(yàn)通過調(diào)節(jié)Zn(NO3)2·6H2O 用量來制備不同摩爾比的介孔Zn/Si 材料。
1.3 吸附實(shí)驗(yàn)
取20 mL 的亞甲基藍(lán)溶液置入比色管中,加入2 mg 樣品,在25 ℃下攪拌一定時(shí)間,離心分離后,用紫外-可見分光光度計(jì)測(cè)定吸附后溶液的濃度。亞甲基藍(lán)的吸附量qt(mg/g)用下列公式計(jì)算:
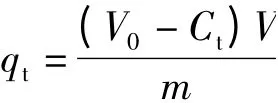
式中 qt——樣品對(duì)亞甲基藍(lán)染料的吸附量,mg/g;
C0、Ct——分別為亞甲基藍(lán)溶液吸附前、后的濃度,mg/L;
V——溶液的體積,mL;
m——吸附劑樣品的質(zhì)量,g。
2 結(jié)果與討論
2.1 Zn-Si 吸附劑樣品的結(jié)構(gòu)表征
由介孔Zn-Si 材料的XRD 圖(圖1)可知,所有樣品均在10 ~40°范圍內(nèi)有一個(gè)較寬的衍射峰,表明合成的介孔材料均為無定型結(jié)構(gòu),且摻入的Zn 完全進(jìn)入到SiO2的框架之中,沒有單獨(dú)Zn 及Zn 的氧化物特征峰存在[12]。

圖1 樣品的XRD 圖譜Fig.1 XRD patterns of samples

圖2 樣品的紅外圖譜Fig.2 FTIR patterns of samples
圖2 是Zn-Si 樣品的紅外譜圖。由圖2 可知,所有樣品均在2 921 cm-1和2 852 cm-1有吸收峰[13],表明樣品中存在 C—H 鍵的伸縮振動(dòng),而3 450 cm-1處的峰是由于Si—OH 基團(tuán)的氫鍵相互作用而產(chǎn)生的伸縮振動(dòng),在1 630 cm-1處的峰歸因于在介孔材料中H2O 的吸收[13],位于960 cm-1和470 cm-1的兩處峰是Si—O—Si 基團(tuán)伸縮振動(dòng)和彎曲振動(dòng)。介孔在Zn-Si 材料樣品中,隨著Zn 量的增加,470 cm-1處的吸收峰逐漸地消失,說明Zn 原子進(jìn)入了硅的骨架生成了Zn—Si—O 價(jià)鍵[13-14]。
2.2 pH 值的影響
染料溶液的pH 值是影響吸附量的一個(gè)重要因素,它決定著染料分子與吸附劑表面的電荷分布情況[15]。取20 mL、40 mg/L 的亞甲基藍(lán)溶液加入相同規(guī)格的錐形瓶中,調(diào)節(jié)pH 值在2.00 ~10.83,分別加入2 mg 的吸附劑,在25 ℃下攪拌1 h 后,離心分離。用紫外可見光譜測(cè)定溶液中殘余亞甲基藍(lán)的吸光度,計(jì)算吸附量,結(jié)果見圖3。
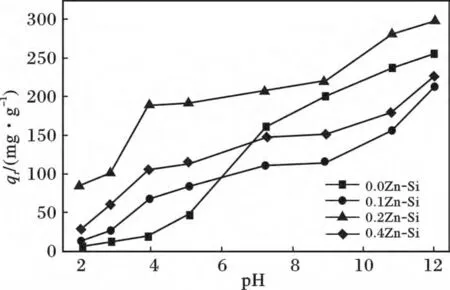
圖3 pH 對(duì)吸附的影響Fig.3 Effect of initial pH on the adsorption
由圖3 可知,隨著pH 值的增加,所有吸附劑樣品對(duì)亞甲基藍(lán)的吸附容量均逐漸增加,其中0.2Zn-Si 的吸附量整體高于0.0Zn-Si、0.1Zn-Si 和0.4Zn-Si,其在中性條件下便可高達(dá)209.22 mg/g。在酸性條件下,Zn 改性后的氧化硅分子吸附量明顯高于純氧化硅分子篩,這主要是由于Zn 提供活性位點(diǎn),增加了分子篩與亞甲基藍(lán)分子的結(jié)合位點(diǎn)。因此,Zn改性的氧化硅分子篩在不同pH 條件下均有較好的吸附性能。
2.3 吸附時(shí)間的影響
圖4 是時(shí)間對(duì)介孔Zn-Si 材料吸附量的影響。隨著吸附時(shí)間的延長(zhǎng),吸附劑對(duì)亞甲基藍(lán)的吸附量增加,在60 min 左右達(dá)到平衡。且介孔0.2Zn-Si 的平衡吸附容量可達(dá)到211.24 mg/g,其值遠(yuǎn)遠(yuǎn)大于介孔0.1Zn-Si 平衡吸附容量119.68 mg/g 和介孔0.4Zn-Si 的平衡吸附容量156.94 mg/g。因此,介孔0.2Zn-Si 是Zn 改性的氧化硅分子篩性能最優(yōu)的樣品。
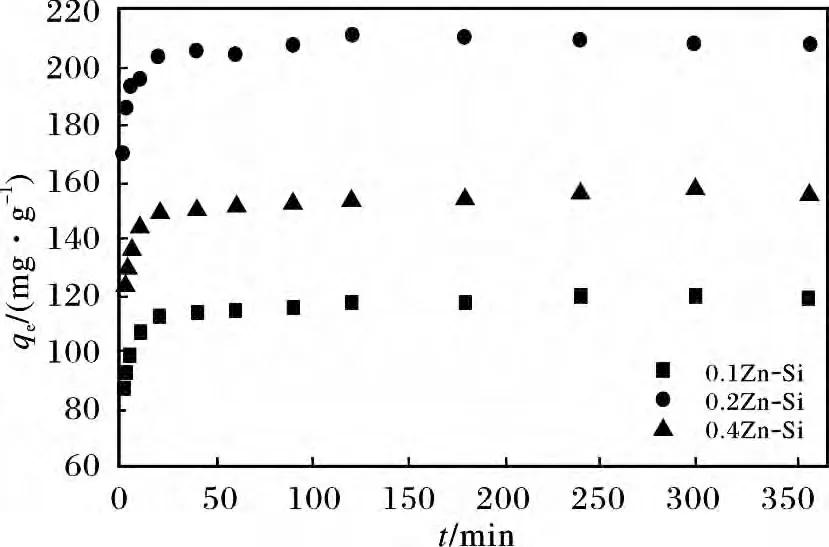
圖4 接觸時(shí)間對(duì)吸附的影響Fig.4 Effects of contact time on the adsorption
2.4 吸附動(dòng)力學(xué)
動(dòng)力學(xué)模型不僅可以推測(cè)吸附過程的吸附速率而且可以解釋吸附機(jī)理,通常采用準(zhǔn)一階方程和準(zhǔn)二階方程對(duì)動(dòng)力學(xué)數(shù)據(jù)進(jìn)行模擬分析。表1 是準(zhǔn)一級(jí)、準(zhǔn)二級(jí)吸附動(dòng)力學(xué)模型的相關(guān)參數(shù),準(zhǔn)二級(jí)動(dòng)力學(xué)模型的線性擬合決定系數(shù)(R2= 0.999 9)高于準(zhǔn)一級(jí)動(dòng)力學(xué)模型的線性擬合決定系數(shù),且理論計(jì)算的平衡吸附量與實(shí)際測(cè)得的平衡吸附容量相差不大。因此,假二級(jí)動(dòng)力學(xué)模型能更好的描述亞甲基藍(lán)在介孔Zn-Si 上的吸附過程。以上結(jié)果說明,Zn-Si 材料對(duì)MB 的吸附不是單一的物理吸附過程,同時(shí)存在化學(xué)吸附。
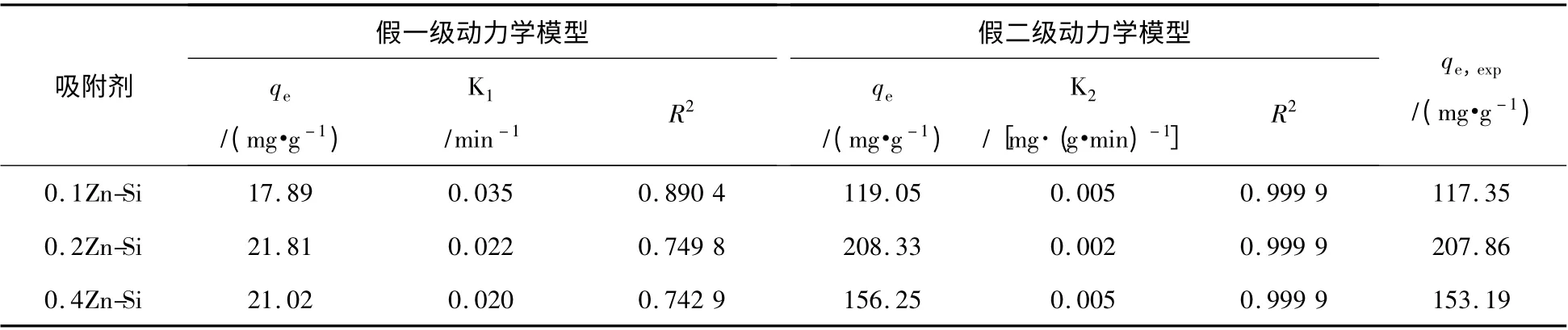
表1 吸附動(dòng)力學(xué)模型參數(shù)Table 1 Kinetic parameters for the adsorption of MBonto the Zn-Si samples
2.5 吸附等溫模型
為了深入的了解吸附劑與染料之間的相互作用,本文詳細(xì)的研究了介孔材料吸附等溫線。25,40,55 ℃下研究0.2Zn-Si 介孔材的吸附等溫線。由圖5 可知,隨著初始濃度的增加,吸附量逐漸增加直到平衡;而溫度的升高,吸附量也隨之增大。
實(shí)驗(yàn)采用Langmuir 和Freundlich 等溫吸附模型對(duì)等溫?cái)?shù)據(jù)進(jìn)行模擬。表2 為L(zhǎng)angmuir 和Freundlich 等溫吸附模型參數(shù),Langmuir 等溫吸附模型線性擬合決定系數(shù)(R2)大于Freundlich 方程線性擬合決定系數(shù)。因此,0.2Zn-Si 分子篩對(duì)亞甲基藍(lán)的吸附更符合Langmuir 等溫吸附模型。
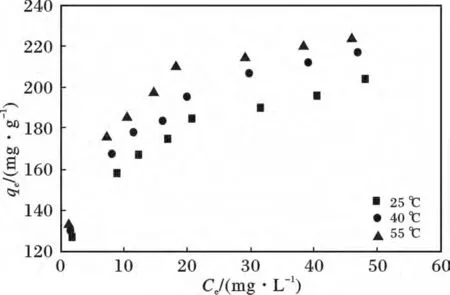
圖5 0.2Zn-Si 樣品的吸附等溫線Fig.5 Adsorption isotherm for the adsorption of MB onto 0.2Zn-Si sample
在Langmuir 等溫吸附模型中,25,40,55 ℃下的理論最大吸附量分別是212. 77,227. 27,232.56 mg/g,與實(shí)驗(yàn)所測(cè)得的結(jié)果基本一致。

表2 亞甲基藍(lán)的等溫吸附模型參數(shù)Table 2 Adsorption isotherm parameters of the adsorption of MB onto 0.2Zn-Si sample
3 結(jié)論
(1)在不同pH 值下,Zn-Si 復(fù)合材料對(duì)亞甲基藍(lán)均有較好的吸附性能。特別是0.2Zn-Si 樣品對(duì)亞甲基藍(lán)的吸附量可達(dá)到228.88 mg/g。
(2)0.2Zn-Si 樣品對(duì)亞甲基藍(lán)的吸附行為符合準(zhǔn)二級(jí)動(dòng)力學(xué)方程動(dòng)力學(xué)模型和Langmuir 等溫吸附模型,表明該吸附過程以單層吸附為主。
(3)Zn-Si 材料是一種高效的吸附劑,具有易分離、無污染、易制備和低消耗等特點(diǎn),因此該材料在以后廢水處理中存在廣泛的應(yīng)用前景。
[1] Vimones V,Lei S M,Jin B,et al.Kinetic study and equilibrium isotherm analysis of Congo Red adsorption by clay materials[J].Chem Eng J,2009,148:354-364.
[2] Seo Y M,Kin J H.Rapid dye adsorpion for dye-sensitized solar cells using a simple ultrasonication method[J]. J Ind Eng Chem,2013,19:488-492.
[3] Zhang X,Cheng C,Zhao J,et al. Polyether sulfone enwrapped graphene oxide porous particles for water treatment[J].Chem Eng J,2013,215/126:72-81.
[4] Lin Y F,Chen H W,Chien P S,et al. Application of bifunctional magnetic adsorbent to adsorb metal cations and anionic dyes in aqueous solution[J]. Hazard Mater,2011,185:1124-1130.
[5] 宋娟,李曉暉,寧喜斌.殼聚糖質(zhì)活性炭對(duì)亞甲基藍(lán)的吸附性能研究[J].應(yīng)用化工,2014,43(8):1446-1448.
[6] Gonzalez-Munoz M J,Rodriguez M A,Luque S,et al.Recovery of heavy metals from metal industry wastewaters by chemical precipitation and nanofiltration[J]. Desalination,2006,200:742-744.
[7] Kiefer R,Kalinitchev A I,Holl W H.Column performance of ion exchange resins with aminophosphonate functional groups for elimination of heavy metals[J]. React Funct Polym,2007,67:1421-1432.
[8] Gao H J,Kan T T,Zhao S Y,et al.Removal of anionic azo dyes from aqueous solution by functional ionic liquid cross-linked polymer[J]. J Hazard Mater,2013,261:83-90.
[9] Li D D,Min H Y,Jiang X,et al.One-pot synthesis of aluminum-containing ordered mesoprous silica MCM-41 using coal fly ash for phosphate adsorption[J].J Col Inter Sci,2013,404:42-48.
[10]Anunziata O A,Beltramone A R,Cussa J,et al.Synthesis and characterization of a novel composite:Polyindole included in nanostructured Al-MCM-41 material[J]. Micro Meso Mater,2012,153:191-197.
[11]Wang W S,Li Y B,Gao B J,et al.Effective removal of Fe(Ⅱ)impurity from rare earth solution using surface imprinted polymer[J]. Chem Eng Resear Des,2013,91:2759-2764.
[12]Liang X L,Yang R G,Li G Y,et al.Phenol hydroxylation over Fe-incorporated mesoporous materials prepared by coprecipitation[J].Micro Meso Mater,2013,182:62-72.
[13] Wu C,Kong Y,Gao F,et al. Synthesis,characterization and catalytic performance for phenol hydroxylation of Fe-MCM-41 with high iron content[J]. Micro Meso Mater,2008,113:163-170.
[14]Adam F,Andas J,Rahman I A. A study on the oxidation of phenol by heterogeneous iron silica catalyst[J]. Chem Eng J,2010,165:658-667.
[15]Chen Z H,F(xiàn)u J W,Wang M H,et al. Adsorption of cationic dye (methyene blue)from asolution using poly (cyclotriphosphazene-co-4,4-sulfonyldiphenol)nanospheres[J].Appl Surf Sci,2014,289:495-501.

