常規磁共振成像診斷無癥狀性出血轉化1例
劉彤彤,陳新,陳曉虹
1 病例介紹
患者,男性,66歲,農民。因“突發左側肢體無力2 h”入院。患者2 h前(2014-5-18 8∶30 am)晨起時無明顯誘因突然出現左側肢體麻木無力,摔倒在地,左側肢體不能抬起,頭部未著地,不能自行站起,無意識不清,無頭痛、惡心、嘔吐,無發熱,無視物雙影,無尿便失禁,癥狀未見好轉,遂來我院急診,查顱腦計算機斷層掃描(computed tomography,CT)未見出血灶(圖1A),考慮腦梗死可能,啟動“溶栓流程”。
既往史:體健,否認高血壓病、心臟病、糖尿病、腦血管病史;否認血液病病史;無吸煙、飲酒史;無頭痛、癲癇病史及腦血管病家族史。
急診查體:體溫36.8℃,脈搏70次/分,呼吸20次/分,血壓153/94 mmHg(右側);145/89 mmHg(左側),體重78 kg;心肺聽診未見異常,頸部血管聽診未聞及明顯雜音,腹平軟;神經系統查體:入院時(2014-5-18 10∶30 am)意識模糊,言語清楚,雙側瞳孔等大等圓;左側鼻唇溝淺,伸舌左偏,左上肢肌力0級、左下肢肌力1級;雙側膝腱反射對稱,雙側Babinski征陰性;美國國立衛生研究院卒中量表(National Institutes of Health Stroke Scale,NIHSS)評分9分。
輔助檢查:
實驗室檢查:血常規、凝血功能、肝功能、腎功能、電解質(2014-5-18)未見明顯異常,隨機靜脈血糖8.06 mmol/L(3.9~6.1 mmol/L)。血常規、肝功能、電解質、凝血功能(2014-5-19)未見異常;乙、丙、戊肝未見異常;尿常規未見明顯異常;血脂脂蛋白a 489.7 mg/L;空腹血糖6.46 mmol/L(3.9~6.1 mmol/L);同型半胱氨酸14.01 μmol/L(5~13.9 μmol/L),葉酸3.59 ng/ml(5.38~24 ng/ml)。
影像學檢查:
顱腦CT(2014-5-18 10∶30 am)未見明顯異常(圖1A);
心電圖未見明顯異常;
顱腦CT(2014-5-19 10∶20 am):右側額顳頂葉大范圍梗死灶(圖1B);
雙側頸動脈、椎動脈、鎖骨下動脈彩超(2014-5-23):左側頸總動脈中段潰瘍斑塊形成(多發);右側頸內動脈起始段閉塞;右側椎動脈開口處狹窄50%~69%。
顱腦磁共振成像(magnetic resonance imaging,MRI)及磁共振血管造影(magnetic resonance angiography,MRA)(2014-5-25):右側腦實質大面積梗死,內部T1高信號影(圖2);右側大腦中動脈及右側頸內動脈狹窄閉塞(圖3)。
經顱多普勒(transcranial Doppler,TCD)(2014-5-26):右側頸內動脈顱外段中度狹窄或閉塞;左側大腦前動脈輕度狹窄。
心臟彩超示:左心房輕度大,二尖瓣少量返流。左心功能未見明顯異常,射血分數(ejection fraction,EF):0.55。入院診斷:腦梗死
右側大腦中動脈供血區
大動脈粥樣硬化性
(TOAST分型)
動脈-動脈栓塞
診療經過:患者來院后急查顱腦CT未見出血,結合臨床癥狀考慮腦梗死超早期可能,急診查血常規、凝血功能、肝腎功能等未見異常,既往無明顯禁忌,啟動溶栓流程,給予重組組織型纖溶酶原激活劑(recombinant tissuetype plasminogen activator,rt-PA)阿替普酶70 mg(0.9 mg/kg),其中10% 1 min內靜脈推注,余液1 h內完成滴注,病后約3 h內完成用藥。溶栓過程中患者血壓平穩,神經功能缺損無加重,無頭痛,無牙齦出血,肢體肌力無明顯改善。24 h后復查顱腦CT(圖1B):右側大腦中動脈供血區大片狀低密度影,側腦室輕度受壓,未見顱內出血改變。血壓150/82 mmHg,神經系統查體較前未見明顯好轉:意識清,左側中樞性面癱,左側肢體肌力1級。溶栓24 h后開始早期治療,因考慮患者梗死面積大,權衡血栓及出血風險,給予阿司匹林0.2 g,以及降壓、改善缺氧耐受及穩定斑塊治療。為進一步明確患者病因完善相關心腦血管等輔助檢查,頸部血管彩超檢查提示左側頸總動脈中段潰瘍斑塊形成(多發),右側頸內動脈起始處閉塞,右側椎動脈開口處狹窄50%~69%。常規顱腦MRI(1.5T)及MRA(圖2~3)提示腦梗死部位見出血轉化;右側頸內動脈及大腦中動脈水平段未顯影,遠端可見部分顯示。考慮大面積腦梗死無癥狀性出血轉化,亞急性期可能性大;責任病變血管為同側頸內動脈閉塞可能性大,顱外頸動脈病變不除外。根據MRI影像表現及臨床癥狀,考慮為HI-2型[1],但同時考慮患者梗死面積較大,故治療上停用阿司匹林,住院期間未再繼續服用阿司匹林。經顱多普勒超聲提示右側頸內動脈顱外段重度狹窄或閉塞結合患者既往無相關心臟疾病病史及心臟相關輔助檢查,考慮病因為頸內動脈顱外段狹窄基礎上動脈到動脈栓塞,但不能除外急性原位血栓形成,栓子清除障礙可能;住院期間患者血壓平穩,肢體癱瘓無加重。出院時左上肢肌力1級、左下肢肌力2級。
出院診斷:右側腦梗死伴出血轉化

圖1 患者計算機斷層掃描成像注:A:急診首次CT(2014-5-18 10∶30 am)未見明顯異常;B:發病24 h后復查CT(2014-5-19 10∶20 am)提示右側額顳頂葉大范圍梗死灶(箭頭所示)。CT:計算機斷層掃描

圖2 患者磁共振成像注:A:T1加權成像可見低信號為主的混合信號,高信號位于半球深部鄰近側腦室體的前部,為不規則團塊樣改變(箭頭所示),整個腦室明顯受壓;B:T2加權成像,圖中可見腦梗死部位呈大片狀;C:FLAIR序列,圖中可見腦梗死呈大片狀高信號(箭頭所示)。FLAIR:液體衰減反轉恢復
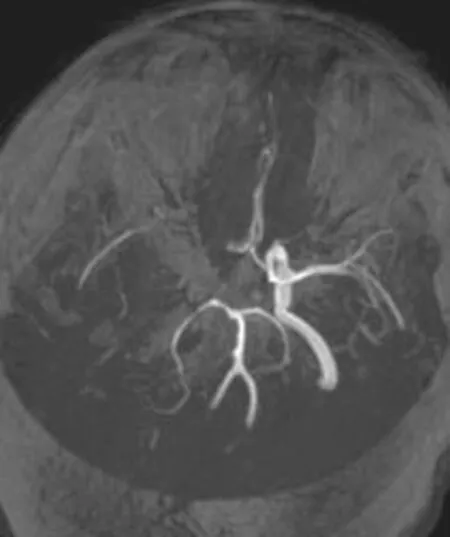
圖3 顱腦磁共振血管成像注:圖中可見后交通動脈未開放,右側頸內動脈及大腦中動脈水平段未顯影(箭頭所示),遠端可見部分顯示
大動脈粥樣硬化性
動脈-動脈栓塞
頸內動脈顱外段狹窄
病后3個月隨訪時,患者左上肢肌力2級、左下肢肌力3級,NIHSS評分:6分。
2 討論
腦梗死出血性轉化(hemorrhagic transformation of cerebral infarction,HTI)是腦梗死的一種并發癥,可以發生于溶栓或抗凝等藥物治療之后,亦可以是腦梗死自然轉歸過程的表現之一,根據歐洲協作急性卒中研究(European Cooperative Acute Stroke Study,ECASS)HTI的CT分型標準[1],HTI可分為出血性腦梗死(hemorrhagic infarction,HI)和腦實質出血(parenchymal hemorrhage,PH)。HI多為無癥狀性出血轉化,又分為沿梗死邊緣小點狀出血的HI-1型和梗死區內點片狀無占位效應的出血為HI-2型;PH為癥狀性出血轉化。大多HI為無癥狀性HTI[2],而大多數癥狀性顱內出血表現為PH型[3]。及時復查顱腦CT及MRI有助于發現早期的出血轉化。CT為常用的檢查手段,因掃描快速,費用低,對出血敏感,尤其適用于危重患者,目前仍是HTI的主要診斷手段。CT診斷盡管有一定的優勢,但不能顯示微小出血,因此可能漏檢HI-1類病灶。近年來有應用MRI進行HTI的相關研究[4],即便常規MRI,對出血轉化HI的檢出也較CT更有優勢。本例患者溶栓后24 h復查頭CT,證實大面積腦梗死診斷,但未見明顯的溶栓后出血轉化。溶栓后1周常規頭MRI及MRA檢查,在T1加權成像發現梗死區內出血改變。根據ECASS、美國國立神經病和卒中研究院(National Institute of Neurological Disorders and Stroke,NINDS)的診斷分類,以及結合溶栓后患者神經功能缺損未見加重及無頭痛等表現,考慮為HI-2型。結合T2加權成像、液體衰減反轉恢復(fluid attenuated inversion recovery,FLAIR)序列所見,考慮T1加權成像所見的出血轉化為亞急性期,不除外溶栓早期發生無癥狀性出血轉化的可能,即溶栓后首次24 h復查CT時可能有無癥狀性出血轉化。本例若不進行MRI掃描,則有可能延誤出血轉化的診斷,其中常規MRI-T1加權成像所見是診斷的重要依據。根據血紅蛋白代謝變化引起的MRI信號改變,MRI不僅可以診斷HI,還可以判斷梗死后出血的大致時間。
隨著MRI對出血轉化檢出率的提高,在一些腦梗死后HT的MRI研究中也使用歐洲ECASS分型方法[4]。腦梗死非溶栓治療出血轉化(HT)的MRI分型方法:Ⅰ級,前循環腦內梗死面積小于3.0 cm2,伴有點狀、斑片狀或皮質出血;Ⅱ級,梗死位于腦干或小腦,伴有點狀、斑片狀或皮質出血;Ⅲ級,前循環大面積梗死,伴有不同程度的出血[5]。但有研究發現以MRI為基準得出的結論與CT有所不同,同一病例MRI的HT分級可能與CT不同,主要是由于磁敏感偽影,MRI對HT敏感度增高的同時,其分級也會偏高,可將斑點狀出血劃分為塊狀血腫[6]。MRI可以診斷CT發現不了的微小出血灶。因此,目前亟需制訂HT的MRI分類標準及研究用于HT檢查的脈沖序列。建立主要基于MRI的HT預測模型[7]。
本病例提示,溶栓后早期即進行常規MRI掃描可及時發現無癥狀性出血轉化。除上述磁共振系列之外,還有一些磁共振技術可用于預測HT,例如FLAIR序列上的血管高信號[8],推測缺血后早期出現FLAIR序列高信號意味著血腦屏障(blood-brain barrier,BBB)破壞,進而更易發生HT[9]。磁敏感加權成像(susceptibility weighted imaging,SWI)上的微出血[10]等,都可能預示著HT的發生。如果應用MRI SWI,則顯示腦梗死中的出血更敏感,更清晰,明顯優于常規序列[11]。
1 Fiorelli M, Bastianello S, von Kunmaer R, et al. Hemorrhagic transformation within 36 hours of a cerebral infarct:relationships with early clinical deterioration and 3-month outcome in the European Cooperative Acute Stroke Study I (ECASSI)cohort[J]. Stroke, 1999, 30:2280-2284.
2 李曉嵐. 腦梗死后出血性轉化的臨床特征及危險因素分析[J]. 臨床和實驗醫學雜志, 2014, 13:45-48.
3 Campbell BC, Christensen S, Parsons MW, et al. Advanced imaging improves prediction of hemorrhage after stroke thrombolysis[J]. Ann Neurol, 2013, 73:510-519.
4 楊飛, 崔書君, 劉懷軍, 等. 腦梗死后出現轉變的CT、MRI比較[J]. 實用放射學雜志, 2011, 27:1632-1635, 1651.
5 卑貴光, 李柏松, 馬虹, 等. 腦梗死非溶栓治療出血性轉化的MR分型與預后相關性研究[J]. 中國臨床醫學影像雜志, 2011, 22:533-536.
6 Arnould MC, Grandin CB, Peeters A, et al.Comparison of CT and three MR sequence for detecting and categorizing early (48hours)hemorrhagic transformation in hyperacute ischemic stroke[J]. AJNR Am J Neuroradiol, 2004, 25:939-944.
7 全冠民, 袁濤, 劉懷軍. 急性腦梗死出血性轉化及MRI評估[J]. 國際醫學(臨床放射學分冊), 2006, 29:311-314.
8 Hohenhaus M, Schmidt WU, Brunecker P, et al.FLAIR vascular hyperintensities in acute ICA and MCA infarction:a marker for mismatch and stroke severity?[J]. Cerebrovasc Dis, 2012, 34:63-69.
9 Jha R, Battey TW, Pham L, et al. Fluid-attenuated inversion recovery hyperintensity correlates with matrix metalloproteinase-9 level and hemorrhagic transformation in acute ischemic stroke[J].Stroke, 2014, 45:1040-1045.
10 Shoamanesh A, Kwok CS, Lim PA, et al.Postthrombolysis intracranial hemorrhage risk of cerebral microbleeds in acute stroke patients:a systematic review and meta-analysis[J]. Int J Stroke, 2013, 8:348-356.
11 白敏, 隋慶蘭, 狄玉進, 等. 3.0T磁共振磁敏感成像在出血性腦梗死中的應用價值[J]. 醫學影像學雜志, 2011,21:171-174.
專家點評
目前計算機斷層掃描(computed tomography,CT)仍為診斷腦梗死后出血轉化的常用手段。本文報道1例由磁共振成像(magnetic resonance imaging,MRI)診斷的腦梗死出血性轉化的病例,提示常規MRI掃描可以及時發現無癥狀性出血轉化,并可以診斷CT發現不了的微小出血灶。本病例對臨床醫生評估出血轉化時選擇影像學方法有借鑒和提示作用,值得考慮。
專家 王瑞萍 教授
單位
遼寧省金秋醫院神經內科
wrp_sy@sina.com