乳腺化生性癌1例及文獻復習
李鳳陳
河北省滄州中西醫結合醫院CT/MRI室,河北滄州061000
乳腺化生性癌1例及文獻復習
李鳳陳
河北省滄州中西醫結合醫院CT/MRI室,河北滄州061000
乳腺癌;化生性癌;磁共振成像
1 病例報告
患者女性,40歲。因發現左乳腫物5個月,近2個月腫物突然增大就診入院。查體:左乳外側可觸及一腫物,大小5.0 cm×4.0 cm,質韌,邊界清晰,活動度差,無壓痛,周圍皮膚未見“橘皮樣”改變,左乳頭無凹陷;左鎖骨上、下及左腋窩未見明顯增大淋巴結;心、肺、腹部檢查陰性。實驗室檢查:血、尿常規及肝腎功能均正常。
鉬靶攝片示:左乳外3點不規則腫塊,大小3.2 cm×3.1 cm,邊界模糊,其內未見鈣化,左乳上象限血管較對側增粗,皮膚未見增厚,乳頭未見凹陷。超聲檢查:左乳3點腺體深層3.3 cm×2.5 cm× 1.6 cm低回聲腫物,形態不規則,部分邊緣呈淺分葉狀改變,部分邊緣成角,邊界欠清晰,內部回聲不均勻,內見多發液性暗區,乳腺彈性評分4~5分,阻力指數(resistance index,RI)0.89~1.0。MRI檢查:左乳外側橢圓形腫物,大小2.3 cm×1.9 cm×2.4 cm,病變信號欠均勻,T1W I呈低信號(圖1 A),T2W I呈等高混雜信號,周邊呈低信號,有假包膜(圖1 B),其內部見液化壞死區,邊界清晰,增強后呈明顯環形強化,內壁不規則(圖1 C);相應磁共振擴散加權成像(diffusion weighted imaging,DW I)呈周邊高信號,中心低信號,表觀彌散系數ADC值周邊減低,時間-信號強度曲線呈漸增型或平臺型(圖1 D)。入院后進行腫物穿刺活檢,考慮為化生性癌。
患者行改良根治術,手術所見:左乳外側腫物,大小2.5 cm×2.0 cm×1.5 cm,腫物與周圍界限清楚。病理檢查:左乳惡性腫物,免疫組化顯示:CD68(+),Ck-pan(+),E-cad(-),ER(-),PR(-),Vimentin(+),確診為化生性癌。術后行常規化療,隨訪3個月未見復發及轉移征象。
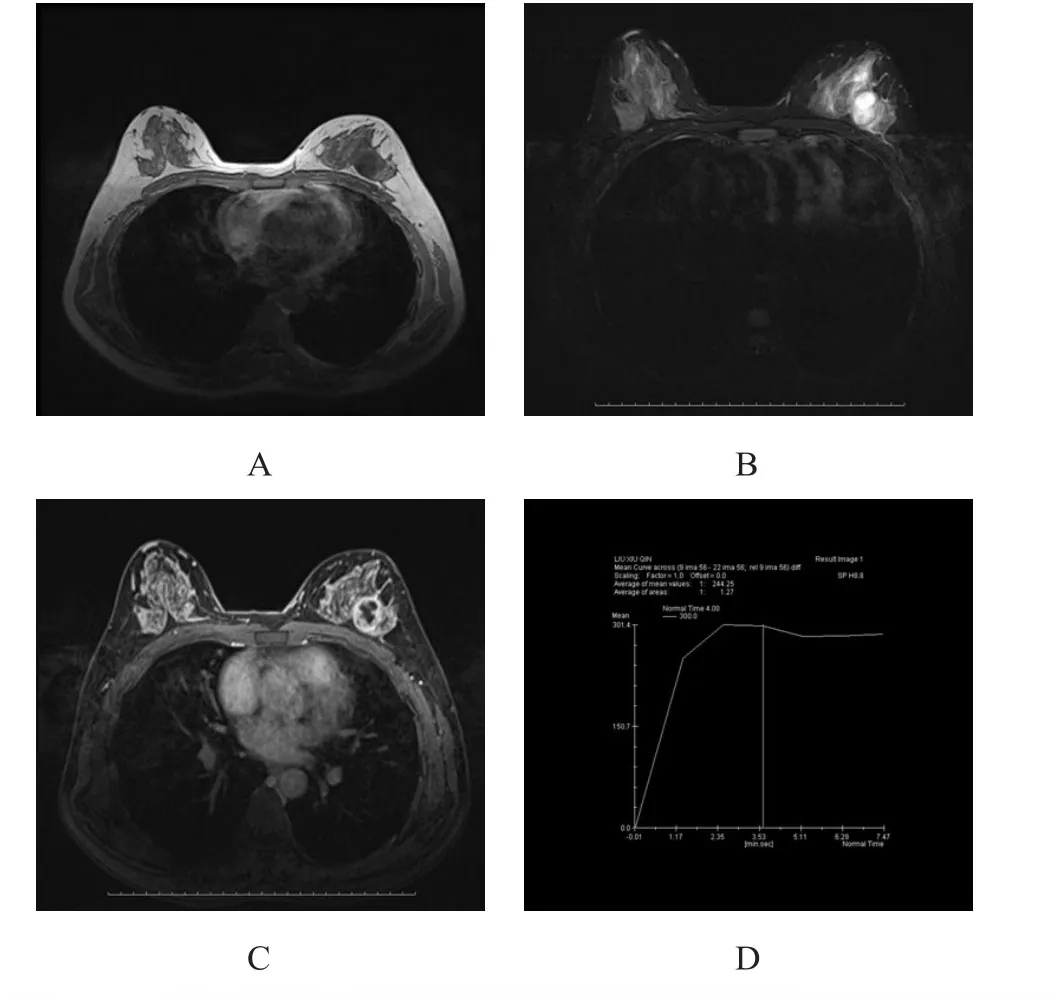
圖1 治療前的MRI表現
2 討論
化生性癌是一類異質性腫瘤,是由腺上皮向非腺上皮間葉組織轉化的一類浸潤性癌,病理類型罕見,5年生存率僅占35%,且惡性程度高。按照2012年第4版《WHO乳腺腫瘤組織學分類》[1]相關內容將非特殊型化生性癌分為低級別腺鱗癌、纖維瘤病樣化生性癌、鱗狀細胞癌、梭形細胞癌、伴間葉組織分化的化生性癌(包括軟骨樣分化、骨樣分化、間葉分化的其他類型)、混合性化生性癌、肌上皮癌。盡管國內外報道其影像學診斷不具有特征性表現,需手術或活檢證實[2-3],但筆者認為化生性癌有其相對的特異性表現。
此例患者鉬靶和超聲檢查結果均提示為惡性病變,從MRI表現上其有自身典型特點。Choi等[4]對21例化生性癌MRI表現進行研究,發現有57%的患者腫塊在T2W I上呈高信號;本例患者MRI檢查結果提示T2W I呈等高混雜信號(圖1 B),與上述文獻報道基本相符,可能是腫瘤發生壞死和囊變、瘤內存在膠凍樣物以及腫瘤向周圍生長等特征的反映。動態增強MRI檢查化生性癌多表現為環形強化,邊緣及實性部分明顯強化,囊性部分無強化[5];本例患者內部見液化壞死區,強化后呈明顯環形強化(圖1 C),也基本符合化生性癌動態增強的表現。因此,MRI檢查乳腺化生性癌的T2W I和動態增強對比圖像有一定的特征性,對乳腺化生性癌特別是鱗癌與其他乳腺腫瘤的鑒別有較高的價值[2,5]。此例患者術前超聲和鉬靶攝像均示腫物邊界模糊,術中見腫物與周圍界限清楚,而術前MRI就已顯示腫物有假包膜,邊緣清晰,這是文獻中未涉及的,體現出MRI較之超聲和X線檢查,對軟組織的對比分辨力高,能夠清晰顯示乳腺化生性腫物的細節。另外,本例患者左乳病變區MRI的時間-信號強度曲線呈漸增型或平臺型,與文獻[5]報道的流出型不同。
常見類型的乳腺癌MRI上T2W I多表現為稍高信號,邊緣可見分葉及毛刺,增強方式呈向心性強化,時間-信號曲線多為平臺型或流出型,ADC值減低[6];葉狀腫瘤是一種由纖維和上皮兩種組織共同構成的腫瘤[7],病變發現時一般體積較大,分葉較明顯,T2W I呈不均勻高信號,增強后多呈明顯均勻強化,出現液化壞死后呈環形強化,但時間-信號曲線多為漸增型或平臺型。可見常見類型的乳腺癌和葉狀腫瘤與化生性乳腺癌的MRI表現基本相同,難于鑒別。乳腺纖維瘤多表現為類圓形腫塊,邊界較清晰,MRI特征性的表現為T2W I上腫瘤內可見低信號分隔,時間-信號曲線呈漸增型或平臺型,DW I無明顯高信號,ADC值無明顯減低,雖然內部液化壞死時亦呈環形強化,但增強方式呈離心樣強化,其與化生性乳腺癌在MRI表現上有較多不同,相對易于區分。
乳腺化生性癌的惡性程度要大于浸潤性導管癌和浸潤性小葉癌[8],依據腫塊大小、淋巴結受累、轉移等得出的病理TNM分期是影響該病預后的主要因素。化生性癌治療方法以手術為主,術后放療有一定效果,但其對內分泌治療不敏感。
總之,乳腺化生性癌診斷的主要依據是病理切片及免疫組化檢查,其中免疫組化起到舉足輕重的作用。此例患者免疫組化ER(-)、PR(-),Ck-pan(+)及Vimentin(+),表明為上皮組織及間葉組織來源,符合化生性癌診斷。影像學檢查,特別是MRI對乳腺化生性癌的術前診斷有重要價值。
[1]齊曉偉,姜軍.2012年第4版《WHO乳腺腫瘤組織學分類》介紹[J].中華乳腺病雜志(電子版),2012,6 (5):62-64.
[2]高月,張清媛.化生性乳腺癌的研究進展[J].臨床腫瘤學雜志,2014,19(8):759.
[3]Yilmaz KB,Pak I,Irkkan C,et al.Metaplastic carcinoma of the breast:clinicopathological features and immunohistochemical analysis[J].J BUON,2011,16(4):652-656.
[4]Choi BB,Shu KS.Metaplastic carcinoma of the breast: multimodality imaging and histopathologic assessment [J].Acta Radiol,2012,53(1):5-11.
[5]劉佩芳,張淑平,邵真真,等.磁共振成像對形態學表現為良性特征的乳腺惡性腫瘤診斷價值[J].磁共振成像,2012,3(2):98-108.
[6]靳二虎.磁共振成像臨床應用入門[M].北京:人民衛生出版社,2009:203-211.
[7]鮑潤賢.中華影像醫學·乳腺卷[M].北京:人民衛生出版社,2010:196-199.
[8]Jung SY,Kim HY,Nam BH,et al.Worse prognosis of metaplastic breast cancer patients than other patients w ith triple-negative breast cancer[J].Breast Cancer Res Treat,2010,120(3):627-637.
R737.9
A
10.11877/j.issn.1672-1535.2015.13.04.23
2014-11-14)

