基于在線生理參數的黑曲霉生產葡萄糖酸鈉發酵動力學模型
平康康 路飛 王澤鍵 趙偉 儲炬 莊英萍 王永紅

摘要:對黑曲霉發酵生產葡萄糖酸鈉的發酵過程進行研究,并通過在線參數分析,發現在線生理參數攝氧率(OUR)和呼吸熵(RQ)可以用來表征發酵過程中底物葡萄糖消耗速率和得率的高低。基于此發現,將在線生理參數攝氧率(OUR)和呼吸熵(RQ)成功用于葡萄糖酸鈉發酵動力學特性表征和分析,得到了葡萄糖酸鈉發酵過程中葡萄糖消耗率和得率及葡萄糖酸生成的動力學方程,并對方程參數進行最優參數估計和非線性擬合。通過計算值與試驗數據的比較,發現試驗值和計算值可以很好地擬合。該模型可以很好地應用于葡萄糖酸鈉發酵工藝優化預測及后續放大過程。
關鍵詞:黑曲霉;葡萄糖酸鈉;在線生理參數;動力學模型
中圖分類號: S188+.4 文獻標志碼: A 文章編號:1002-1302(2015)07-0375-04
葡萄糖酸鈉是一種具有咸苦味、無腐蝕性、無揮發性、無毒、溫和的有機酸鈉鹽[1]。近年來,由于其在食品、飼料、醫藥及建筑等行業的廣泛應用[2-6],葡萄糖酸鈉越來越受到人們的關注。統計數字表明,葡萄糖酸鈉的市場需求量在逐年遞增[7-8]。目前工業上多采用黑曲霉發酵法生產葡萄糖酸鈉。黑曲霉代謝合成葡萄糖酸鈉的代謝過程可以簡化如圖1表示[9]。其反應方程式可以簡化如下:
C6H12O6+12O2→C6H12O7;
C6H12O7+NaOH→C6H12O6Na。
在此發酵過程中,氧氣不僅僅用于菌體生長和維持菌體的基本代謝,還作為生成葡萄糖酸反應的基本底物之一。因此發酵過程中的攝氧率(OUR)是非常重要的生理參數之一。用數學模型研究發酵動力學可以很好地揭示發酵過程中菌體生長、底物消耗和產物形成的規律,在預測微生物發酵過程和指導工藝優化方面起著很重要的作用[10];但是傳統的葡萄糖酸發酵動力學在預測和進行工藝優化時面臨較大的局限性,如產物和菌體量難以較快離線測定。本研究基于發酵過程中過程質譜儀檢測分析尾氣成分及經Biostar軟件采集計算所得的OUR、CER等生理參數,對黑曲霉發酵法生產葡萄糖酸鈉的過程進行在線參數分析,建立底物消耗動力學、產物生成動力學及得率的動力學方程。該模型可以很好地描述黑曲霉發酵生產葡萄糖酸的過程,可為工藝優化及自動化控制軟件設計提供較好的參考。
1 材料與方法
1.1 菌種
黑曲霉(Aspergillus niger),由山東福洋生物科技有限公司實驗室提供。
1.2 培養基組成
斜面孢子培養基:葡萄糖 60 g/L、尿素 2 g/L、KH2PO4 13 g/L、MgSO4·7H2O 0.02 g/L、玉米漿 1 g/L、CaCO3 5 g/L、瓊脂 2 g/L,調pH值至6.5~7.0,在0.1 MPa、121 ℃條件下滅菌30 min。控制培養溫度和濕度,溫度35 ℃,濕度40%,培養周期36~48 h。
種子培養基:葡萄糖 300 g/L、(NH4)2HPO4 1 g/L、KH2PO4 1 g/L、MgSO4·7H2O 0.02 g/L、玉米漿30 g/L。
發酵培養基:葡萄糖 300 g/L、(NH4)2HPO4 2 g/L、KH2PO4 2 g/L、MgSO4·7H2O 0.02 g/L、玉米漿 20 g/L。
1.3 分析檢測方法
菌濃度的測定:取50 mL發酵液,微孔濾膜(0.8 μm,上海迪清過濾技術有限公司)過濾,去離子水沖洗菌絲體5次,80 ℃ 烘干至質量恒定,電子天平稱質量。
葡萄糖的檢測:取發酵液過濾所得清液,稀釋到適當濃度,用菲林法[11]滴定。
葡萄糖酸鈉的檢測:取發酵液所得清液,稀釋適當倍數,HPLC(HP1100,安捷倫)測定,流動相為3 mol/L甲醇-0.25 mol/L 磷酸溶液(1 ∶1),流速1 mL/min,柱溫28 ℃,每次進樣20 μL。
pH值與溶氧(DO)的測定:pH值、DO均用梅特勒電極測定。
發酵過程尾氣的采集:采用Extrel過程質譜MAX300-LG對發酵過程中的進氣和尾氣進行實時在線采集分析,該質譜儀能夠精確測定發酵過程尾氣中的氬氣、氮氣、二氧化碳和氧氣等相對分子質量在300以內的可揮發性氣體。在使用之前用標準氣體對儀器的響應度進行標定[12-13]。
攝氧率(OUR)和二氧化碳的生成速率(CER)測定[14]:OUR和CER通過對發酵尾氣的分析數據計算得到。以進氣和尾氣中惰性氣體N2維持恒定建立平衡方程,求得OUR和CER的計算公式如下:
OUR=FinV[CO2,in-Cinertin×CO2,in1-(CO2,out+CCO2,out]×273273+Tin×11+h×Pin×1×10-5;
CER=FinV[Cinertin×CCO2,in1-(CO2,out+CCO2,out)-CCO2,in]×273273+Tin×11+h×Pin×1×10-5;
RQ=CEROUR。
式中:Fin為通氣速率;V是發酵液體積;Cinertin、CO2,in、CCO2,in分別是進氣中惰性氣體、氧氣及二氧化碳的體積分數;CO2,out、CCO2,out分別是出氣中氧氣及二氧化碳的體積分數;Pin為進氣的絕對壓強;Tin 是進氣溫度;h為進氣的相對濕度;RQ為呼吸熵。
1.4 培養方法
種子的培養:在無菌條件下,將孢子培養基斜面上的孢子用去離子水洗下,接入5 L發酵罐(裝液量3 L)的種子生長培養基中,在37 ℃、通風量300 L/h、pH值用10 mol/L氫氧化鈉調節維持在5.8的條件下培養18~20小時。
分批發酵培養:將制備好的種子培養液在無菌條件下按接種量10%轉入5 L發酵罐(裝液量3 L)中,溫度維持在 37 ℃,通風量300 L/h并保持一定攪拌轉速,pH值用10 mol/L氫氧化鈉調節維持在5.8的條件下培養至殘糖降至10 g/L以下時,發酵結束。
2 結果與分析
2.1 黑曲霉發酵過程在線參數分析
為了了解黑曲霉發酵葡萄糖酸鈉過程中,在線生理參數OUR、CER伴隨殘糖濃度、葡萄糖酸濃度變化而波動的規律,進行了不同攪拌轉速條件下的3組分批發酵試驗,結果見圖2、圖3和圖4。試驗組1:維持恒定轉速250 r/min;試驗組2:維持恒定轉速350 r/min;試驗組3:維持恒定轉速450 r/min。
在通氣量、溫度、壓力都一定的情況下,可以通過提高轉速改善供氧,了解發酵過程中底物葡萄糖濃度、產物葡萄糖酸鈉濃度和在線生理參數OUR、CER及RQ在發酵過程中的變化規律。從圖2可以看出,黑曲霉經過短暫延滯期后進入對數生長期,葡萄糖消耗速率和葡萄糖酸鈉生成速率都逐漸加快并達到較穩定值。隨著發酵的進行,OUR逐漸增大并在對數生長期結束的時候逐漸達到一個穩定值,CER在對數生長期結束時達到最大值,然后緩慢降低。從圖2可以看出,隨著發酵攪拌轉速提高,供氧能力增強[15],底物葡萄糖消耗速率和產物葡萄糖酸鈉生成速率明顯增大。而從圖3和圖4可以看出,250 r/min 試驗組OUR和CER最高分別在28.5 mmol/(h·L)和 3.1 mmol/(h·L) 左右,350 r/min試驗組OUR和CER最高分別在37.6 mmol/(h·L)和3.6 mmol/(h·L)左右,450 r/min試驗組OUR和CER最高分別在 45.2 mmol/(h·L) 和4.2 mmol/(h·L)左右,同時第3組試驗OUR和CER增長速率明顯快于前2組試驗。供氧能力提升導致耗糖速率和產酸速率的升高與OUR的增長有一致性。與此同時,供氧的改變并未導致3組試驗發酵末期CER有太大的差異,這主要是因為CER受菌濃度和菌體自身代謝所影響,發酵末期菌體增長基本停止,CER僅僅受菌體維持代謝強度影響。而3組試驗最高菌濃度分別為4.78、4.96、4.82 g/L,差別非常小。從試驗穩定期計算所得的RQ看,第1組試驗穩定期RQ為0.1左右,第2組試驗穩定期RQ為0.08左右,第3組試驗穩定期RQ為0.06左右。3組試驗穩定期間的產物得率分別為78.9%、843%和88.6%。即RQ降低的同時伴隨著底物轉化為產物的得率在升高。同時OUR和RQ的變化是在一定范圍內的,黑曲霉發酵法生產葡萄糖酸鈉的實際發酵過程中,OUR一般為0~80 mmol/(h·L),RQ一般為0.04~0.2。
2.2 基于在線參數的宏觀動力學的建立
2.2.1 底物消耗動力學 發酵過程中,底物消耗主要用于以下3個方面:一是菌體的生長消耗,二是用于產物的合成,三是用于菌體基本生命活動的維持。因此傳統的底物消耗動力學模型可以用如下方程來表示[16]:
-dSdt=1YX/S×dXdt+1YP/S×dPdt+mX。(3)
式中:S為葡萄糖質量濃度(g/L);t為時間(h);YX/S為葡萄糖用于菌體生長的得率常數;X為菌體濃度(g/L);YP/S為葡萄糖用于產物積累的得率常數;P為葡萄糖酸鈉濃度(g/L);m為維持常數。該方程雖然可以較好地描述葡萄糖酸鈉的發酵過程,但在實際發酵過程中,由于產物得率和菌體維持所用底物消耗并不為常數,得率和維持系數會隨著發酵條件的改變而改變。而且該方程用到的物理量如菌濃度X難以快速檢測,因此該方程在指導工藝優化的過程中作用十分有限。經過上述分析我們知道底物消耗和攝氧率(OUR)有密切的關系,我們提出如下經驗公式來描述黑曲霉發酵生產葡萄糖酸鈉過程中底物的消耗:
-dSdt=kOUR+h(8≤OUR≤80)。
即OUR在8~80范圍內,耗糖速率和OUR接近于線性關系,實際發酵過程中,OUR也在這個范圍內,為了進一步縮小方程造成的計算誤差,用如下二次項方程代替線性方程,可以取得更精確的計算值。
-dSdt=αOUR2+βOUR+λ。(4)
式中:S為葡萄糖濃度(mmol/L),OUR為攝氧率(mmol/L),α、β、λ均為為常數。
2.2.2 RQ與得率的相關性分析 如上所述,底物葡萄糖一部分用于產物葡萄糖酸鈉的合成,一部分用于菌體的生成,一部分用于菌體維持,葡萄糖生成葡萄糖酸是一個不生成CO2的過程,也就是說是一個RQ為0的反應過程。菌體量的增加和菌體的維持伴隨著CO2的釋放,葡萄糖酸鈉發酵過程中的RQ是葡萄糖3個代謝去向的共同結果,呼吸熵RQ就可以在一定程度上表征得率的高低。可以用如下方程來描述發酵過程中RQ和得率的關系:
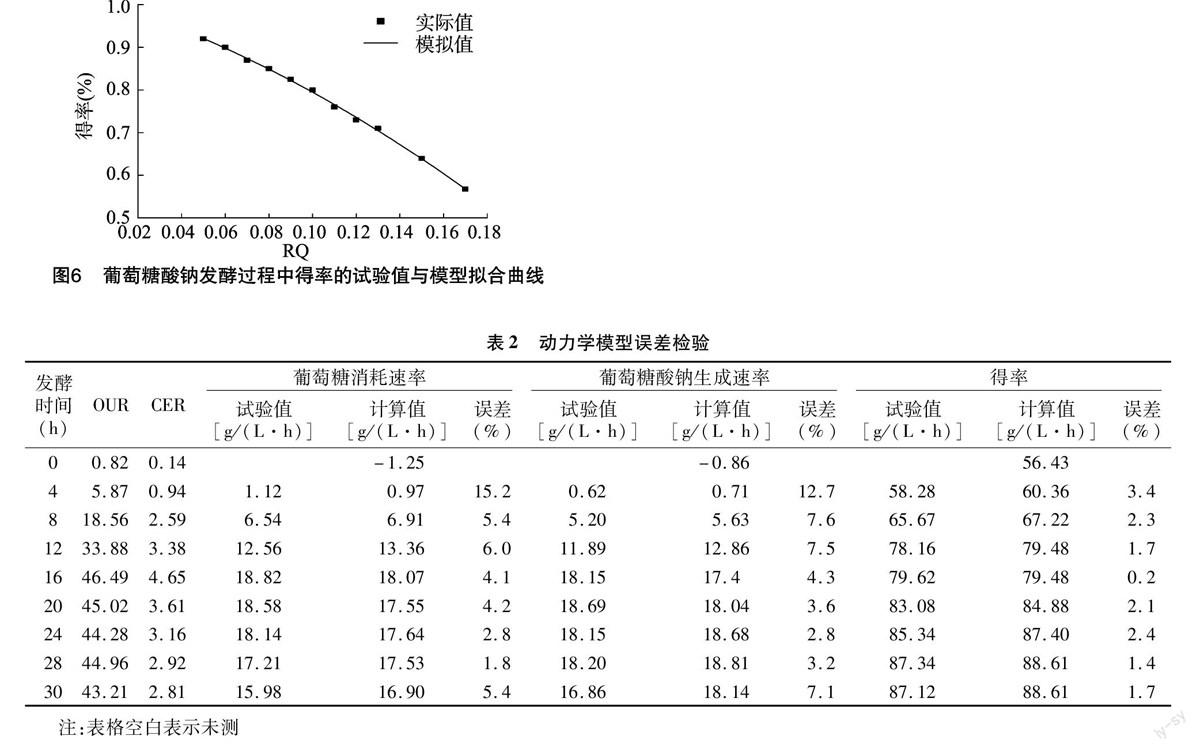
Yield=δRQ2+γRQ+(0.05≤RQ≤0.18)。(5)
式中,δ、γ、φ均為常數。
2.2.3 產物生成動力學 傳統發酵動力學認為,黑曲霉生產葡萄糖酸鈉是一個生長偶聯型,用如下方程來描述[17]:
dPdt=αdXdt+βX。(6)
式中:P為葡萄糖酸鈉濃度(g/L);α、β為動力學參數;αdXdt為與菌體生長率相關的產物形成率;βX為非伴隨菌體生長的產物形成率。該模型與傳統底物消耗動力學模型類似,在實際過程中也存在α、β為變量,菌濃度難以快速測定導致無法快速了解發酵過程產物生成的情況。因此根據式(6)又可進行如下描述:
dPdt=Yield×dSdt。(7)
將式(4)、式(5)帶入式(7)得,發酵過程中葡萄糖酸鈉生成動力學方程如下:
dPdt=(αOUR2+βOUR+γ)(δRQ2+γRQ+)。(8)
式中,P為葡萄糖酸鈉濃度(mmol/L)。
2.2.4 模型參數的求解 根據實際測得的數據,應用Origin軟件,采用通用全局優化算法,根據不同批次分批發酵的OUR和分別對應底物消耗速率曲線和得率與RQ相關性曲線進行非線性曲線擬合,得到擬合曲線,并得到參數最優估計值(表1)。
根據表1數據,得到黑曲霉發酵產葡萄糖酸鈉過程中動力學模型分別為:底物消耗動力學模型: -dSdt=-0.099 4OUR2+2.830 9OUR-10.893 5;發酵過程中得率模型:Yield=-6.093 2RQ2-1.603 3RQ+1.0161(0.04≤RQ≤0.2);產物合成動力學模型:dPdt=(-0.009 4OUR2+2.830 9OUR-10.893 5)(-6.093 2RQ2-1.603 3RQ+1.016 1)。
表1 葡萄糖酸鈉發酵動力學模型參數估計
參數αβλδγφ
估計值-0.009 42.830 9-10.893 5-6.093 2-1.603 31.016 1
圖5為不同OUR下的分批發酵過程中底物消耗曲線,圖6為不同RQ下得率變化曲線,其相關系數分別為0.994 8、0990 8。可見這2個模型能很好地描述葡萄糖酸鈉發酵過程中的底物消耗、產物生成得率情況。
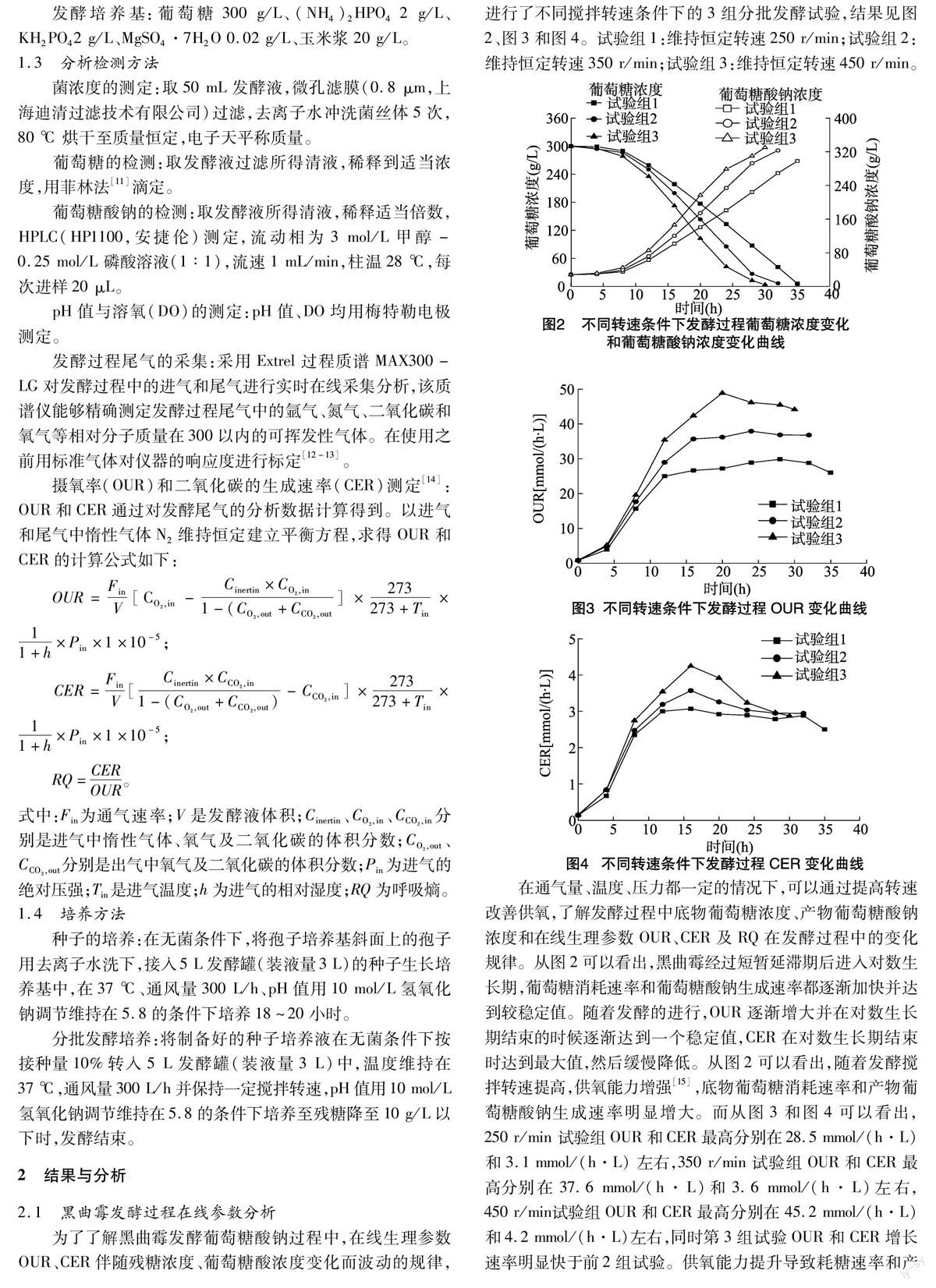
2.2.5 發酵動力學模型誤差檢驗 為了驗證模型的準確性,在相同的培養基條件下進行分批發酵的重復試驗,轉速設為450 r/min,通氣量為300 L/h,對分批發酵試驗過程中底物消耗速率和產物生成速率的實際測量值和模型計算值進行比較,結果見表2。
從表2可以看出,0 h種子剛接入發酵培養基內, 由于處
在延滯期的初始階段,OUR和CER值都很低,此時葡萄糖消耗速率和葡萄糖酸鈉產物生成速率都非常低,難以有效測出,同時經過模型計算所得耗糖速率和產物生成速率為負值。這主要是因為此時的OUR已經不在模型的適用范圍之內所致,但這并不妨礙該模型的實用性,因為在用黑曲霉發酵產葡萄糖酸鈉的實際過程中,除了延滯期的初始階段會有較低水平的OUR外,其他階段的OUR水平都在該模型使用范圍之內。除了0 h的數據誤差較大外,發酵周期內的其他時間葡萄糖消耗速率和葡萄糖酸鈉合成速率的實際測量值與模型計算值誤差都保持在10%以內。
3 結論與討論
微生物發酵是一個非常復雜的過程,菌體的生長,底物的消耗和產物的生成往往受多種因素的影響。通過將黑曲霉分批發酵葡萄糖酸鈉過程尾氣分析所得的OUR、CER及RQ等在線參數與發酵過程相關聯,本研究認為OUR越高,其發酵過程耗糖速率就越高,發酵周期相應越短;RQ越低,發酵過程得率就會越高。并根據此種關聯,提出了底物消耗速率、得率及產物生成速率與在線參數RQ、OUR相關的數學模型。相比于傳統的底物消耗模型和產物生成模型,該模型在實際發酵過程中可以很好地描述底物的消耗、發酵過程中得率的高低及產物生成速率而不用去考慮菌體量的多少。該模型優點在于方程變量可以通過計算機迅速得到,從而為發酵過程中工藝的優化提供有實際意義的指導。
參考文獻:
[1]Ramachandran S,Fontanille P,Pandey A,et al. Gluconic acid:properties,applications and microbial production[J]. Food Technology and Biotechnology,2006,44(2):185-195.
[2]Anastassiadis S,Morgunov I G. Gluconic acid production[J]. Recent patents on biotechnology,2007, 1(2):167-180.
[3]Singh O V,Kumar R. Biotechnological production of gluconic acid:future implications[J]. Applied Microbiology and Biotechnology,2007, 75(4):713-722.
[4]姜菲菲,李丕武,馬春玲,等,產葡萄糖酸鈉黑曲霉培養條件優化研究[J]. 中國釀造,2009,28(10):61-63.
[5]Blom R H,Pfeifer V F,Moyer A J,et al. Sodium gluconate production. Fermentation with Aspergillus niger[J]. Industrial & Engineering Chemistry,1952,44(2):435-440.
[6]黃道震,余麗秀.葡萄糖酸鈉的生產工藝及研究動態[J]. 河南化工,1999(5):35-36.
[7]黃騰華. 葡萄糖酸鈣和葡萄糖酸鈉發酵[J]. 發酵科技通訊,2006,35(3):22-23.
[8]蔡 皓,余 超,李 慶. 黑曲霉葡萄糖酸發酵的工藝控制方法[J]. 化學與生物工程,2008,25(6):63-66.
[9]張 靜. 黑曲霉發酵生產葡萄糖酸鈉的研究[D]. 無錫:江南大學,2008:7-10.
[10]周玉平,周 潔. 微生物連續發酵模型及其應用綜述[J]. 微生物學通報,2010,37(2):269-273.
[11]儲 炬,李友榮,俞俊棠. 葡萄糖氧化酶發酵動力學的研究[J]. 華東理工大學學報,1997(6):303-309.
[12]王然明,王澤建,田錫煒,等. 生物過程尾氣質譜儀在乳酸發酵工藝控制中的應用[J]. 華東理工大學學報 :自然科學版,2013(3):10-15.
[13]Wang Z J,Wang H Y,Li Y L,et al. Improved vitamin B12 production by step-wise reduction of oxygen uptake rate under dissolved oxygen limiting level during fermentation process[J]. Bioresource technology,2010,101(8):2845-2852.
[14]張嗣良,儲 炬. 多尺度微生物過程優化[M]. 北京:化學工業出版社,2003:97-150.
[15]溫 玲,路 飛,王澤建,等. 供氧水平對黑曲霉發酵生產葡萄糖酸鈉的影響[J]. 食品工業科技,2014,35(7):154-157.
[16]張小昊,童群義. 黑曲霉生產葡萄糖酸鈉的分批發酵動力學模型[J]. 食品工業科技,2010,31(12):221-223.
[17]Liu J Z,Weng L P,Zhang Q L,et al. A mathematical model for gluconic acid fermentation by Aspergillus niger[J]. Biochemical Engineering Journal,2003,14(2):137-141.

