基于Ag配合物的流動注射
扶昭富+李攻科??胡玉斐

摘 要 基于氫化可的松對Ag配合物-H2SO4體系化學發光信號的增敏作用,建立了一種測定血清中氫化可的松的流動注射-化學發光分析方法。當H2SO4濃度為1.0 mol/L,Ag配合物濃度為2.5×10
4 mol/L,流速為4.20 mL/min時,體系具有最強的化學發光。在最優實驗條件下,相對發光強度與氫化可的松濃度在3.0×10
~1.0×10
7 g/mL范圍內呈良好的線性關系,方法的檢出限為2.2×10
10 g/mL (3σ)。對5.0×10
8 g/mL氫化可的松連續平行測定11次,其相對標準偏差為0.6%。本方法成功地用于人血清中氫化可的松的含量測定,回收率為93.0%~110.0%,相對標準偏差在0.3%~3.2%之間。通過研究該體系的紫外可見吸收光譜和熒光發射光譜,探討了可能的化學發光機理。
關鍵詞 化學發光; 流動注射; 氫化可的松; Ag配合物; 血清
[HT][HK][FQ(32,X,DY-W][CD15] 2015-07-21收稿; 2015-08-06接受
本文系國家自然科學基金項目(Nos.21475153, 21107008, 91232703)及高等學校博士學科點專項項目(No.20120171110001)
* E-mail: cesgkl@mail.sysu.edu.cn; huyufei@mail.sysu.edu.cn[HT]
1 引 言
氫化可的松(Hydrocortisone,分子結構見圖1)是人腎上腺產生的一種腎上腺糖皮質激素,它在人體生理過程中起著至關重要的作用。氫化可的松主要作用包括參與免疫和代謝兩方面。在免疫方面,氫化可的松主要起抗炎和免疫抑制作用,影響體內免疫球蛋白的生成[1]; 在代謝行為方面,它主要是參與中間代謝(通常是分解代謝),例如減少體內組織對葡萄糖的吸收,通過加速葡萄糖異生酶在肝臟的合成加強葡萄糖異生作用[2]。血液中氫化可的松的濃度通常可以反映機體應激性亢進水平[3]。氫化可的松在臨床上可用于診斷與其濃度水平相關的疾病,如阿狄森病患者的腎上腺類固醇排泄水平低,庫欣綜合征患者體內氫化可的松生產過剩。此外,高血清水平(氫化可的松)也發現存在于應激反應,如精神疾病、肥胖、糖尿病、酗酒和懷孕人群。低水平的皮質醇見諸于腎上腺酶缺陷患者和長時間處于壓力下的人群[4]。
已報道的測定氫化可的松的方法包括免疫法[5,6]、液相色譜法[7,8]、氣相色譜-質譜聯用法[9]、液相色譜-質譜法[10~12]、毛細管電色譜[13]等。然而,這些方法都存在一定的缺陷,例如色譜法和質譜法需要昂貴的儀器,對環境的要求高; 免疫法易受樣品中相似結構的化合物的交叉反應影響。因此,建立一種簡單、快速、靈敏度高、選擇性好的氫化可的松檢測方法具有重要意義。化學發光檢測技術具有線性范圍寬、靈敏度高、檢測限低、儀器設備簡單和分析速度快等優點。結合流動注射技術(FI),化學發光法具有重現性好的特點,已廣泛應用于環境、醫藥等領域[14~18]。超常氧化態配合物通常可以在堿性環境中通過多齒配體的絡合作用而穩定存在[19~21]。
[Ag(HIO6)2]5
(Diperiodatoargentate,Ag配合物,簡寫為DPA)是一種超常氧化態配合物,也是一種強氧化劑,目前廣泛應用于無機,有機反應的動力學及反應機理研究[21]。由于具有強氧化性與良好的催化性能,DPA也逐漸引起分析研究者的關注。基于DPA和魯米諾的化學發光法測定氫化可的松已有報道[23],而發光試劑如魯米諾等的使用會影響方法的選擇性。
研究發現,氫化可的松可大大增強DPA在H2SO4介質中產生的微弱化學發光信號,該體系不需要發光試劑,方法的選擇性也較高。本研究基于該化學發光反應,結合流動注射技術,建立了一種靈敏的氫化可的松的分析方法,并成功應用于人血清中氫化可的松的檢測。通過熒光光譜和紫外光譜的研究,探討了可能的化學發光反應機理。
2 實驗部分
2.1 儀器與試劑
如圖2所示,流動注射化學發光(FI-CL)系統由兩個蠕動泵用于輸送試液,樣品注射通過一個帶定量環的六通閥實現。系統各部分的連接使用聚四氟乙烯管(直徑0.8 mm)。CL信號通過BPCL微弱發光檢測儀測量(中國科學院生物物理研究所); LS-45發光光譜儀 (美國Perkin Elmer 公司)。紫外分光光度儀(北京普析通用儀器有限責任公司)。
氫化可的松來源于德國Dr Ehrenstorfe公司,AgNO3,KIO4,K2S2O8和KOH購于上海第一化學試劑廠。所有試劑都為分析純,實驗用水均為二次蒸餾水。氫化可的松儲備液:準確稱取氫化可的松100 mg,用甲醇溶解,并定容至100 mL。
2.2 實驗過程
2.2.1 DPA的合成 按文獻[24]方法,將AgNO3 (1.36 g), KIO4 (3.24 g), K2S2O8 (3.00 g),KOH (8.00 g)與200.0 mL去離子水混合,加熱回流40 min,冷卻后過濾,得到DPA,低溫避光保存。通過其在λ=361 nm處的紫外吸光度計算其濃度(A=εcL, 摩爾吸光系數ε=1.26×104 L/(mol·cm)。
2.2.2 樣品處理 血清樣品由中山大學醫院提供。取適量血清,置于超濾管中,4000 r/min離心20 min,過濾,濾液用乙酸乙酯萃取3次,收集有機相并將其蒸干,加入適量水溶解,待測。
2.2.3 實驗方法 如圖2所示,在
950 V的負高壓下,時間間隔為0.1 s。以水為載流,經管道輸入流通池與DPA溶液在流通池中混合,開啟分析系統,待基線平穩后,切換閥,通過載流注入100 μL氫
圖2 FI-CL系統裝置圖
Fig.2 Schematic diagram of FI-CL system
P:蠕動泵(Peristaltic); V:進樣閥(Valve); F:流通池(Flow Cell); PMT:光電倍增管(Photomultiplier Tube); AMP: 信號放大器(Amplifier); HV: 高壓(High Voltage); REC: 記錄儀(Recorder); W:廢液(Waste); HV:
50 V。a: H2SO4; b: Hydrocortisone; c: Water; d: Diperiodatoargentate (DPA).化可的松標準溶液或樣品溶液與H2SO4的混合液,與DPA溶液在流通池中混合,產生化學發光,通過檢測系統記錄反應的發光信號,在線性范圍內,根據相對發光強度ΔI(ΔI=I-I0)進行定量分析。
3 結果與討論
3.1 化學發光反應動力學曲線
采用靜態注射法研究了氫化可的松-DPA-H2SO4體系的化學發光動力學曲線。用0.1 mL微量注射器將DPA溶液迅速注入到H2SO4和樣品(或水)(1∶1, V/V)的混合液中,產生顯著的化學發光。由圖3可見,這是一個快速反應過程,從試劑混合到發光強度達最大峰值所用時間僅為0.5 s,并在5 s內完成整個過程。因此,基于氫化可的松對DPA-H2SO4發光反應的增敏作用,結合流動注射技術可對氫化可的松進行測定。
3.2 條件優化
3.2.1 進樣體積及流速的選擇 進樣體積及流速能直接影響發光強度,結果表明,當進樣體積為200 μL時,可獲得最大的發光強度,所以實驗選定的最佳進樣體積為200 μL。實驗發現,發光強度隨流速的增加而增大,但考慮到精確性與試劑用量,選擇4.20 mL/min進行后續實驗。
3.2.2 反應介質的選擇 考察了常見的酸性介質HCl、HNO3、H3PO4、多聚磷酸和H2SO4對該體系反應的化學發光強度的影響。研究表明,DPA在酸性環境中能產生微弱的化學發光,氫化可的松的加入能大大增強化學發光信號。在H2SO4介質中,體系的發光強度最大且穩定,而在其它介質中未觀察到明顯的發光信號,故選用H2SO4為反應介質。固定其它條件,考察0.05~2.0 mol/L H2SO4溶液對化學發光強度的影響。如圖4所示,隨著H2SO4濃度增大,氫化可的松的相對發光強度也增大; 當H2SO4濃度達到1.0 mol/L時,相對發光強度達到最大值; 繼續增大H2SO4濃度,化學發光強度反而減小。因此,H2SO4溶液的最佳濃度選用1.0 mol/L。
3.2.3 DPA濃度的選擇 DPA在體系中是氧化劑,其濃度對發光信號的影響很大。在5.0×10
1.0×10
3 mol/L范圍內,考察了DPA溶液濃度對化學發光信號的影響。由圖5可見,當DPA溶液濃度低于2.5×10
4 mol/L, 相對發光強度隨DPA溶液濃度的增加而增大,當其濃度達到2.5×10
4 mol/L時,相對發光強度達到最大發光值; 繼續增大DPA的濃度,發光強度反而會減小,其原因可能是DPA為橘紅色溶液,濃度過大會導致自吸收。因此DPA溶液的濃度選用2.5×10
4 mol/L。
3.3 分析特性
在最佳實驗條件下,氫化可的松的質量濃度在0.3 ~10 ng/mL范圍內與相對發光強度呈良好的線性關系,回歸方程為I=7.62C-18.58 (ng/mL, R2=0.9991 )。對濃度為50 ng/mL氫化可的松平行測定11次,相對標準偏差為0.6%。方法的檢出限為0.22 ng/mL。
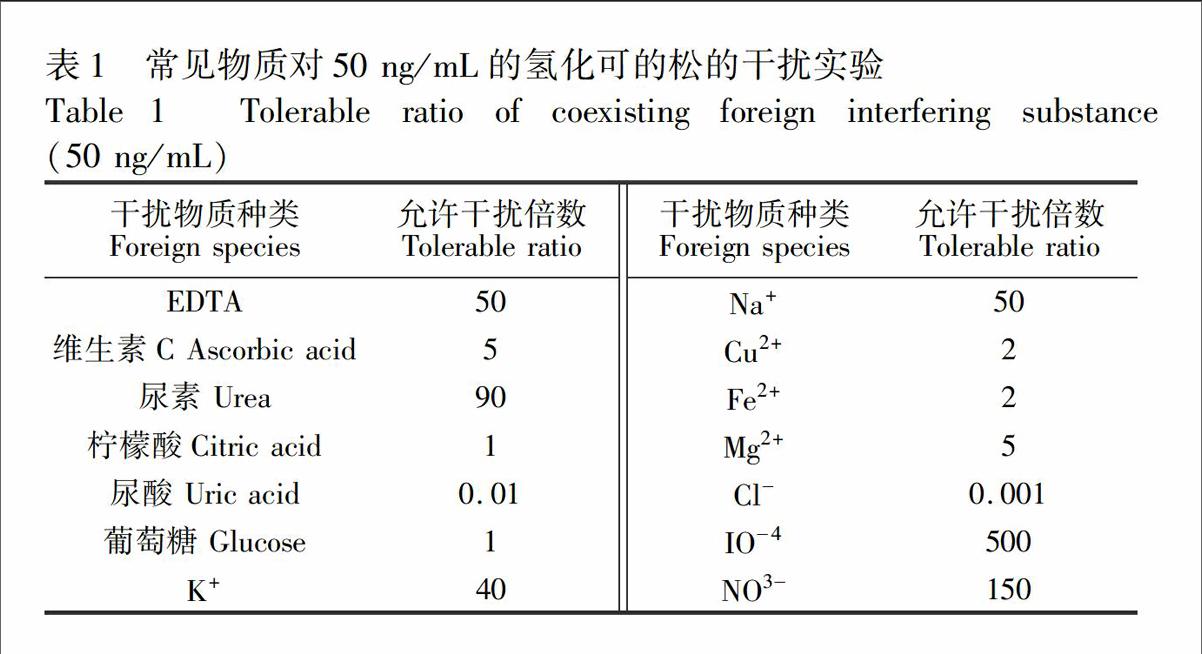
3.4 干擾測定
在選定的最優條件下,考察了人血清樣品中常見組分對該化學發光體系的干擾情況,結果見表1。對于50 ng/mL氫化可的松,相對誤差小于5%的條件下,部分物質及離子對氫化可的松的測定有一定的干擾,特別是尿酸和Cl
,故在對血清進行實際檢測時需要進行樣品前處理。
3.5 樣品分析
標準加入回收實驗: 在0.5 mL血清樣品或注射液樣品中加入適量氫化可的松標準溶液,攪拌混勻
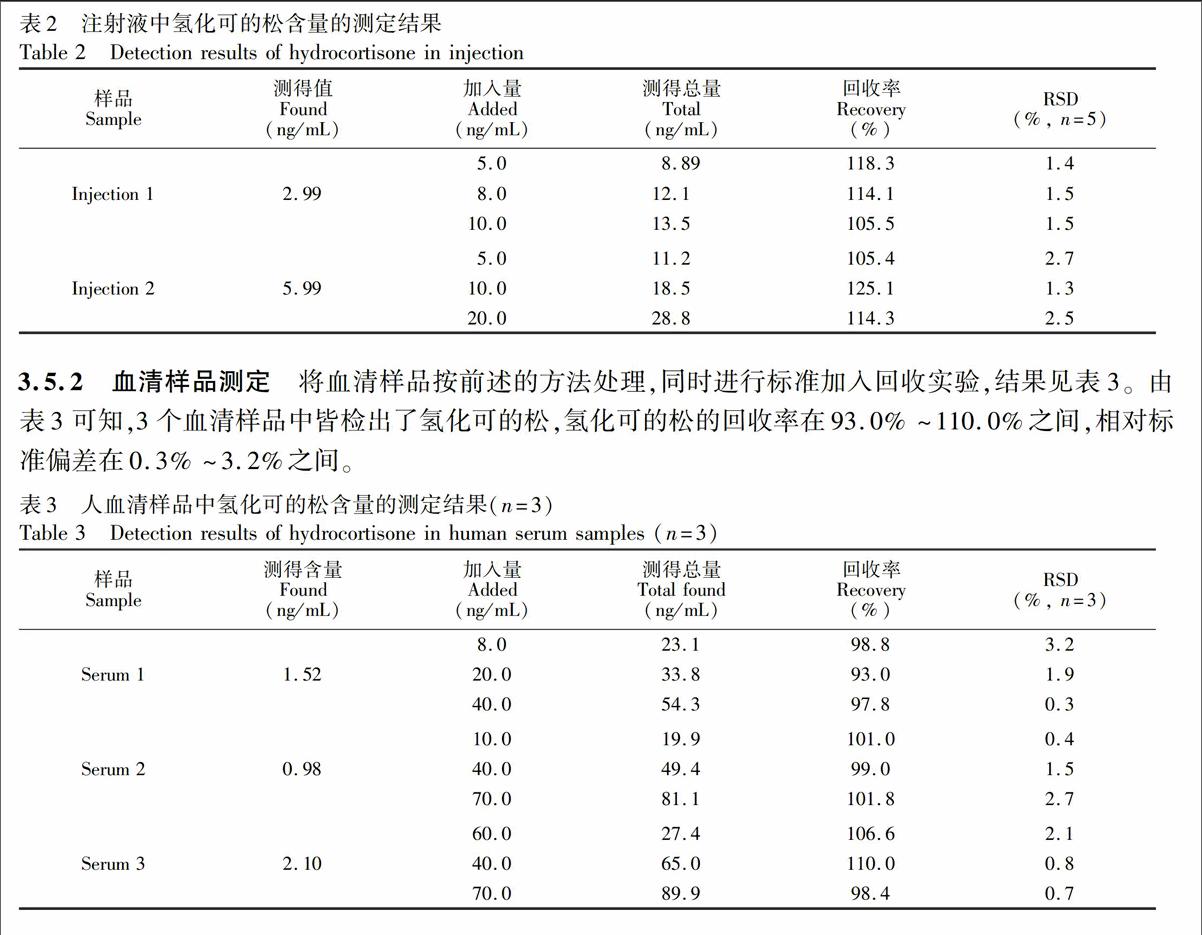
3.5.1 注射液測定 將氫化可的松注射液(每管25 mg)用水稀釋至不同濃度,按照實驗方法測定,同時進行標準加入回收實驗。由表2可知,氫化可的松的回收率在105.4%~125.1%之間,相對標準偏差在1.3%~2.7%之間。
3.5.2 血清樣品測定 將血清樣品按前述的方法處理,同時進行標準加入回收實驗,結果見表3。由表3可知,3個血清樣品中皆檢出了氫化可的松,氫化可的松的回收率在93.0%~110.0%之間,相對標準偏差在0.3%~3.2%之間。
3.6 化學發光機理探討
3.6.1 紫外可見吸收光譜圖研究 氫化可的松-DPA-H2SO4體系的紫外可見吸收光譜圖如圖6所示。DPA的吸收峰在364 nm處,當加入H2SO4后,DPA溶液的顏色逐漸褪去,其吸收峰減弱,表明H2SO4與DPA發生了化學反應。氫化可的松的吸收峰在249 nm處,當其與DPA或DPA-H2SO4混合后,其紫外光譜明顯不同于氫化可的松和DPA或DPA-H2SO4紫外吸收光譜圖的簡單加合,說明氫化可的松與DPA發生了反應。
3.6.2 熒光光譜研究 在300~475 nm范圍內,氫化可的松-DPA-H2SO4體系的熒光光譜圖見圖7。H2SO4和DPA在300~475 nm波長范圍內均無熒光,但DPA存在基體光譜峰,兩者混合之后,DPA的基體光譜峰發生了明顯的變化,可推斷DPA與H2SO4可發生化學反應。氫化可的松在紫外光激發下能產生特征熒光,其最大激發波長和發射波長分別為289 和361 nm; 當其與H2SO4混合,由于酸效應使熒
光發射峰強度降低,但無明顯位移,可以推斷H2SO4與氫化可的松之間并未產生化學反應; 當其與DPA混合時,僅在460 nm處產生一個弱發射峰,存在明顯的位移,由此可以推斷,DPA與氫化可的松發生了強的相互作用,這可能是反應過程中產生的激發態(O2)2*所引起的[25,26]。將DPA、H2SO4和氫化可的松三者混合所得到的熒光光譜也表明三者之間發生了化學反應在反應過程中可能產生了O2·
O2·
之間結合可能產生富電子中間體:激發態(O2)2*,(O2)2*返回基態生成O2[27,28]。
紫外可見光譜和熒光光譜測試表明,在H2SO4介質中,DPA與氫化可的松發生了化學反應,Shi等[29]的研究表明, DPA有兩種存在形式:[Ag(HIO6)2]5
和 [Ag(HIO6)(OH)(H2O)]2
(圖8),后者是活性中心并能發生復合反應。氫化可的松分子可以獲得激發態(O2)2*的部分能量從而被激發。DPA-H2SO4-氫化可的松體系產生的發光可能來源于DPA和氫化可的松獲得(O2)2*的能量, 并被激發,返回基態時,能量以光的形式釋放,產生CL發射[25~28]。
4 結 論
本研究基于H2SO4介質中氫化可的松對DPA信號的增強作用,提出了一種測定氫化可的松的流動注射化學發光法。研究結果表明,本方法具有設備簡單、操作方便、靈敏度高、線性范圍寬等優點,適用于實際樣品分析。
References
1 Nagae M, Fuda H, Ura K, Kawamura H, Adachi S, Hara A, Yamauchi K. Fish Physiol. Biochem., 1994, 13(1): 41-48
2 Jost C M, Picon R I. Br. Vet. J., 1970, 125: 321-326
3 Attia M S, El-Swafy E, Youssef A O, Hefny H A, Khalil M H. J. Fluoresc., 2014, 24(2): 337-344
4 Turpeinen U, Hmlinen E. Best Pract. Res. Cl. En., 2013, 27(6): 795-801
5 Zangheri M, Cevenini L, Anfossi L, Baggiani C, Simoni P, Di Nardo F, Roda A. Biosens. Bioelectron., 2015, 64: 63-68
6 Yadav R, Mohan K, Kumar V, Sarkar M, Nitu K, Meyer H H D, Prakash B S. Domest. Anim. Endocrin., 2013, 45(2): 72-78
7 Saracino M A, Iacono C, Somaini L, Gerra G, Ghedini N, Raggi M A. J. Pharmaceut. Biomed., 2014, 88: 643-648
8 Ronowicz J, Kupcewicz B, Pakowski A, Bilski P, Siódmiak T, Marsza M, Krysiski J. Chem. Pap., 2014, 68(7): 861-870
9 Amendola L, Garribba F, Botrè F. Anal. Chim. Acta, 2003, 489(2): 233-243
10 Snchez-Guijo A, Hartmann M F, Shi L, Remer T, Wudy S A. Anal. Bioanal. Chem., 2014, 406(3): 793-801
11 Chen Z, Li J, Zhang J, Xing X, Gao W, Lu Z, Deng H. J. Chromatogr. B., 2013, 929: 187-194
12 ZHOU Jian,WANG Min,TANG Xiao-Yan,MAO Xue-Fei,DAI Xin-Hua. Chinese J. Anal. Chem., 2013, 41(9): 1439-1443
周 劍, 王 敏, 湯曉艷, 毛雪飛, 戴新華. 分析化學, 2013, 41(9): 1439-1443
13 SUN Xue-Ting, SHANG Shao-Ming, CHEN Xiu-Ying, WANG Yun, LI Juan. Chinese J. Anal.Chem., 2014, 42(1): 36-40
孫雪婷, 商少明, 陳秀英, 汪 云, 李 娟. 分析化學, 2014, 42(1): 36-40
14 Iranifam M. Revisiting Flow-Chemiluminescence Techniques: Pharmaceutical Analysis, Luminescence. 2013, 28(6): 798-820
15 Christodouleas D, Fotakis C, Economou A, Papadopoulos K, Timotheou-Potamia M, Calokerinos A. Anal. Lett., 2011, 44(1-3): 176-215
16 XIAO Hu-Yong, CHEN Jia, WEI Guo-Fen, HU Qin-Qin, AI Yong-Qing, HAN Yun, ZHOU Xing-Wang, L Jian-Quan. Chinese J. Anal. Chem., 2013, 41(3): 432-435
肖虎勇,陳 佳, 魏國芬, 胡芹芹, 艾永青, 韓 韻, 周興旺,呂鑒泉. 分析化學, 2013, 41(3): 432-435
17 Tang Y, Song H, Su Y, Lv Y. Anal. Chem., 2013, 85(24): 11876-11884
18 Ocaa-Gonzlez J A, Ramos-Payn M, Fernndez-Torres R, Villar Navarro M, Bello-López M . Talanta, 2014, 122: 214-222
19 Zhao F, Zhao W, Xiong W. Luminescence, 2013, 28(2): 108-113
20 Shetti N P, Hosamani R R, Nandibewoor S T. The Open Catalysis Journal, 2009, 2(1): 130-139
21 Sivaramakrishna A, Clayton H S, Muralikrishna U. ChemInform., 2011, 42(28): doi: 10.1002/chin.201128221
22 Shi H, Guo Y, Kang W. J. Solution Chem., 2011, 40(7): 1371-1381
23 Shi H, Xu X, Ding Y, Liu S, Li L, Kang W. Anal. Biochem., 2009, 387(2): 178-183
24 Balikungeri A, Pelletier M, Monnier D. Inorg. Chim. Acta, 1977, 22(1): 7-14
25 Sun H, Chen P, Wang F, Wen H. Talanta, 2009, 79(2): 134-140
26 Liang S, Zhao L, Zhang B, Lin J. J. Phys. Chem. A, 2008, 112(4): 618-623
27 Zhao F, Zhao W, Xiong W. Luminescence, 2013, 28(2): 108-113
28 Chen P, Sun H. Drug Test. Anal., 2010, 2(1): 24-27
29 Shi H, Shen S, Sun H, Liu Z, Li L. J. Inorg. Biochem., 2007, 101(1): 165-172

