胰島素泵強化治療對老年2型糖尿病足患者血糖波動、氧化應激損傷的影響
馬麗輝
糖尿病足是糖尿病患者常見的慢性并發癥之 一,由于自身局部神經異常以及下肢微血管病變導致足部淺層或深層組織被破壞,臨床表現為足部潰
瘍且常伴有感染,若不及時控制,則有可能造成需要截肢的后果[1]。胰島素泵治療已經普遍應用在糖尿病危重患者的相關治療中并且取得了良好的臨床療效[2],但在糖尿病合并足潰瘍患者中的應用鮮有報道。本研究通過胰島素泵短期強化治療糖尿病合并足潰瘍患者,探討其對患者氧化應激狀態的影響以及評價其臨床應用療效,為臨床防治提供參考。
1 對象與方法
1.1 研究對象 2012年6月—2014年6月我院收治的老年2型糖尿病(T2DM)足潰瘍80例,年齡60~82(65.9±5.7)歲;其中男48例,女32例;所有患者均為Wagner分級[3]Ⅰ~Ⅲ級;潰瘍面積1~20(9.3±1.4)cm2;糖尿病足潰瘍的診斷標準參照人民衛生出版社出版的第二版《內分泌學》[4]相關標準:符合1999年世界衛生組織制定的糖尿病診斷標準;沒有出現周圍血管病變和周圍的神經病變,但足部已經出現感染、潰爛、化膿等癥狀。排除標準:肝腎功能不全、血液病、自身免疫系統疾病。將80例糖尿病合并足潰瘍患者隨機分為觀察組40例和對照組40例,觀察組男23例,女17例;對照組男25例,女15例。經醫院倫理委員會批準,并經患者同意填寫知情同意書。兩組年齡、性別構成、體重指數(BMI)、糖尿病病程、潰瘍病程、潰瘍面積、糖化血紅蛋白、空腹血糖、餐后2 h血糖、胰島素抵抗指數、空腹胰島素水平等一般臨床資料比較均無統計學差異(P>0.05),具有可比性。見表1。
表1 兩組老年2型糖尿病足潰瘍一般臨床資料比較(±s)
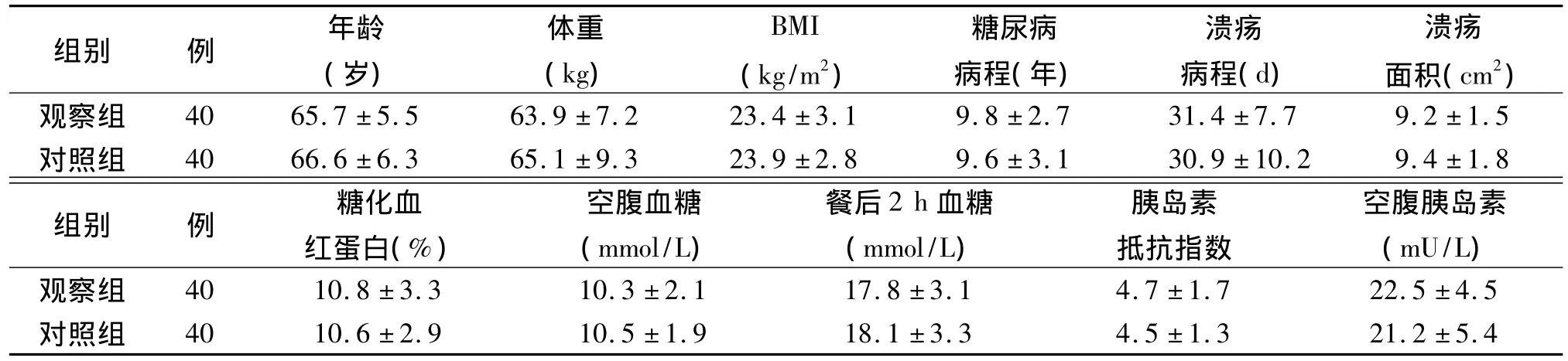
表1 兩組老年2型糖尿病足潰瘍一般臨床資料比較(±s)
注:對照組接受常規皮下注射胰島素治療,觀察組接受短期胰島素泵強化治療
組別 例 年齡(歲)體重(kg)BMI(kg/m2)糖尿病病程(年)潰瘍病程(d)潰瘍面積(cm2)觀察組 40 65.7 ±5.5 63.9 ±7.2 23.4 ±3.1 9.8 ±2.7 31.4 ±7.7 9.2 ±1.5對照組 40 66.6 ±6.3 65.1 ±9.3 23.9 ±2.8 9.6 ±3.1 30.9 ±10.2 9.4 ±1.8組別 例 糖化血紅蛋白(%)空腹血糖(mmol/L)餐后2 h血糖(mmol/L)胰島素抵抗指數空腹胰島素(mU/L)觀察組 40 10.8 ±3.3 10.3 ±2.1 17.8 ±3.1 4.7 ±1.7 22.5 ±4.5對照組 40 10.6 ±2.9 10.5 ±1.9 18.1 ±3.3 4.5 ±1.3 21.2 ±5.4
1.2 方法
1.2.1 治療方法:所有患者入院后均給予糖尿病飲食、潰瘍局部創面的常規消毒及換藥、抗感染及營養支持等常規治療等。觀察組根據《中國胰島素泵治療指南(2010)》[5],采用血糖動態監測系統(美國美敦力公司生產的Minimed)監測患者血糖72 h,然后給予胰島素泵的強化治療:用胰島素泵皮下輸注生物合成人胰島素(諾和靈R,諾和諾德中國制藥生產),強化治療10~14 d,讓患者的睡前血糖和FPG(空腹血糖)保持在 3.6 ~7.5 mmol/L,2 hPG(餐后2 h血糖)保持在<8.0 mmol/L。每天采用血糖儀監測睡前及三餐前后的血糖,按照血糖的水平及時調整胰島素的劑量。對照組接受常規皮下注射胰島素治療,在三餐前給予諾和靈R皮下注射、睡前給予諾和靈N(諾和諾德中國制藥生產)皮下注射。兩組均根據患者的實際飲食情況、生理狀態,并依據血糖監測的結果適時調整胰島素劑量。
1.2.2 觀察指標及檢測方法:應用動態血糖儀(美敦力公司研制)檢測兩組治療前后的72 h的血糖水平,依據檢測結果計算相應的血糖波動參數:血糖標準差(SDBG)、平均血糖波動幅度(MAGE)及最大血糖波動幅度(LAGE);記錄治療前及治療后1、2周的血漿丙二醛含量(MDA)、超氧化物歧化酶水平(SOD)、8-異前列腺素 F2α(8-iso-PGF2α)水平、潰瘍面積;MDA測定采用比色法(試劑由南京建成生物工程研究所提供),SOD測定采用酶速率法(南京建成生物制品公司提供);8-iso-PGF2α采用酶聯免疫吸附法測定(試劑盒產自美國Cayman公司)。
1.3 療效評價 記錄治療前及治療2周后患者潰瘍面積的變化情況。療效評判標準[6]為:①治愈:潰瘍面積縮小≥75%,愈合部分上皮化;②好轉:患者潰瘍面積縮小50% ~75%;③無顯著變化:潰瘍面積減少≤50%;④惡化:潰瘍面積不減少反而有增大趨勢。愈合良好率=(治愈人數+好轉人數)/本組治療的總人數×100%。
1.4 統計學方法 采用SPSS 19.0統計軟件包進行統計學分析,定量資料以均數±標準差(±s)表示,組間比較采用t檢驗,定性資料采用χ2檢驗;重復測量資料采用重復測量設計的方差分析,相關性分析采用pearson線性相關分析,α=0.05為檢驗水準。
2 結果
2.1 兩組治療前后血糖波動相關參數的比較 與治療前比較,兩組SDBG、MAGE及LAGE均顯著下降(P<0.05),觀察組MAGE較對照組下降更為明顯(P <0.05);見表2。
2.2 兩組治療前及治療后1、2周氧化應激損傷指標及潰瘍面積的比較 兩組治療1、2周氧化應激損傷指標及潰瘍面積均比治療前顯著改善(P<0.05)。觀察組治療1、2周后的 MDA、8-iso-PGF2α低于對照組(P<0.05),治療后1、2周后的SOD高于對照組(P<0.05);潰瘍面積在治療后1、2周亦顯著小于對照組(P<0.05);見表3。
表2 兩組老年2型糖尿病足潰瘍治療前后血糖波動相關參數的比較(±s,mmol/L)
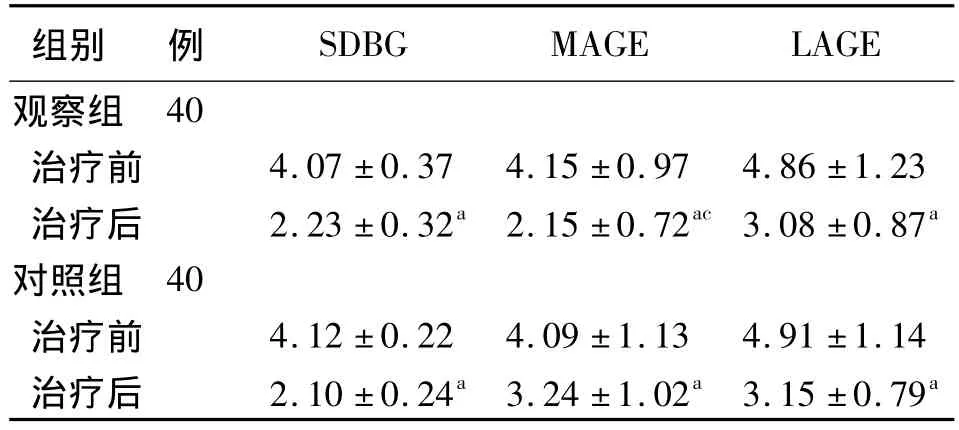
表2 兩組老年2型糖尿病足潰瘍治療前后血糖波動相關參數的比較(±s,mmol/L)
注:SDBG:血糖標準差;MAGE:平均血糖波動幅度;LAGE:最大血糖波動幅度。對照組接受常規皮下注射胰島素治療,觀察組接受短期胰島素泵強化治療。與治療前比較,aP<0.05;與對照組比較,cP<0.05
組別 例SDBG MAGE LAGE觀察組40治療前 4.07 ±0.37 4.15 ±0.97 4.86 ±1.23治療后 2.23 ±0.32a 2.15 ±0.72ac3.08 ±0.87a對照組 40治療前 4.12 ±0.22 4.09 ±1.13 4.91 ±1.14治療后 2.10 ±0.24a 3.24 ±1.02a 3.15 ±0.79a
表3 兩組老年2型糖尿病足潰瘍治療前后氧化應激損傷指標及潰瘍面積的比較(±s)
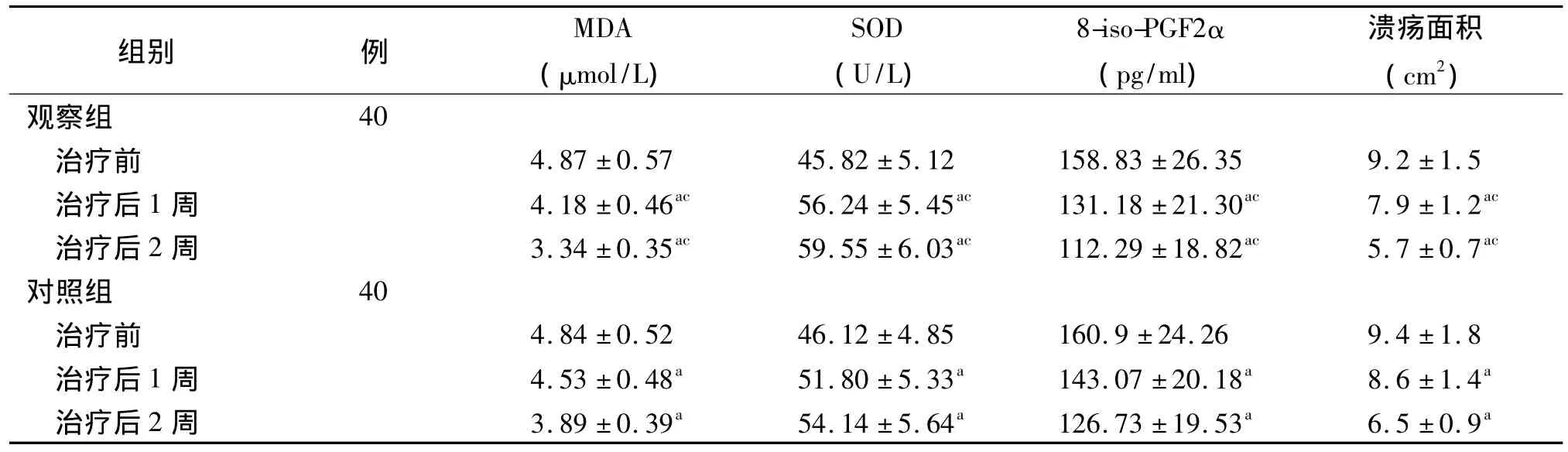
表3 兩組老年2型糖尿病足潰瘍治療前后氧化應激損傷指標及潰瘍面積的比較(±s)
注:MDA:丙二醛;SOD:超氧化物歧化酶水平;8-iso-PGF2α:8-異前列腺素F2α水平。對照組接受常規皮下注射胰島素治療,觀察組接受短期胰島素泵強化治療。與治療前比較,aP<0.05;與對照組比較,cP<0.05
組別 例MDA(μmol/L)SOD(U/L)8-iso-PGF2α(pg/ml)潰瘍面積(cm2)觀察組40治療前 4.87 ±0.57 45.82 ±5.12 158.83 ±26.35 9.2 ±1.5治療后 1 周 4.18 ±0.46ac 56.24 ±5.45ac 131.18 ±21.30ac 7.9 ±1.2ac治療后 2 周 3.34 ±0.35ac 59.55 ±6.03ac 112.29 ±18.82ac 5.7 ±0.7ac對照組 40治療前 4.84 ±0.52 46.12 ±4.85 160.9 ±24.26 9.4 ±1.8治療后 1 周 4.53 ±0.48a 51.80 ±5.33a 143.07 ±20.18a 8.6 ±1.4a治療后 2 周 3.89 ±0.39a 54.14 ±5.64a 126.73 ±19.53a 6.5 ±0.9a
2.3 兩組患者治療2周后療效的比較 治療2周后,觀察組治療后潰瘍愈合良好率明顯高于對照組(χ2=4.261,P=0.041)。見表4。

表4 兩組老年2型糖尿病足潰瘍治療2周后療效的比較(例)
2.4 血糖波動、氧化應激及潰瘍面積的pearson線性相關分析 治療前 MAGE與 MDA、8-iso-PGF2α呈正相關(r=0.762,P=0.000;r=0.578,P=0.000),而與 SOD 呈負相關(r= -0.664,P=0.000);治療后MAGE與MDA、8-iso-PGF2α呈正相關(r=0.356,P=0.000;r=0.312,P=0.002),而與SOD呈負相關(r= -0.297,P=0.000)。治療前MDA、8-iso-PGF2α與潰瘍面積呈正相關(r=0.489,P=0.000;r=0.762,P=0.000);而 SOD 與潰瘍面積呈負相關(r= -0.517,P=0.000);治療后 MDA、8-iso-PGF2α與潰瘍面積呈正相關(r=0.376,P=0.000;r=0.469,P=0.000);而 SOD 與潰瘍面積呈負相關(r= -0.352,P=0.000)。此外,治療前后的MAGE與潰瘍面積亦呈正相關(r=0.629,P=0.000;r=0.482,P=0.000)。
3 討論
2型糖尿病患者足潰瘍致殘率較高,Zgonis等[7]報道此類患者發生截肢的風險是非糖尿病患者的30倍。此類患者由于自身血糖控制較差,血糖波動大,常常處于氧化應激狀態,氧化應激不僅與糖尿病發病的病理生理過程密切相關,其導致的氧化應激損傷還影響器官及組織細胞的修復及愈合。葛奎等[8]在糖尿病大鼠模型的燙傷創面愈合研究發現,氧化應激中產生的氧自由基不僅阻礙創面愈合,還能夠加重組織創面的感染,與對照組比較,處于明顯氧化應激狀態下的實驗組燙傷創面的愈合明顯延遲;廖炎與樂園[9]在探討氧化應激與器官損傷的關系時指出,氧化應激中產生的活性氧(ROS)能夠活化各種轉錄因子如核因子(NF)-κB,從而調節各種前炎癥基因的表達,誘發炎癥反應參與組織損傷。簡茂強等[10]報道顯示氧化應激狀態能夠降低皮膚的通透性及防御能力,表皮下微循環功能亦有顯著下降,增加了遭受外界侵害的風險。
近些年的多項研究已經證實,2型糖尿病患者中氧化應激的產生與機體血糖波動密切相關[11-15],且血糖波動可能作為一個始動因素,誘發氧化應激反應的產生,加重微循環血管內皮細胞的損傷,對預后產生不利影響[16-17],且目前的研究已經將血糖波動作為2型糖尿病患者治療不佳及相關并發癥出現的獨立預測因素,并且這種預測價值是獨立于HbA1c、餐后血糖及 FPG 的[18-19]。Zsuga 等[20]報道了糖尿病合并缺血性腦中風患者血糖波動產生的氧化應激損傷,使患者神經功能恢復不良,給患者長期預后帶來不利影響。目前,MDA被認為是一種靈敏反映脂質過氧化損傷及體內活性氧濃度的生化指標,是脂質過氧化過程的最終產物,它能夠使脂質、核酸及各種蛋白質發生交聯,引起細胞突變死亡[21];SOD則被認為是一類抗氧化應激損傷的酶促防御系統,是抗氧化損害的主要防御力量,其活性高低可以反映機體細胞組織抗氧化損傷的效應。8-iso-PGF2α是一種反映氧化應激損傷指標“金標準”,其主要來源于機體過多的氧自由基攻擊細胞膜中花生四烯酸后裂解生成的特異活性物質,8-iso-PGF2α在組織及體液中含量穩定,不受藥物及食物的干擾,是評估機體氧化應激損傷的理想指標[22]。在血糖波動的參數中,MAGE是以血糖波動的峰值至波動谷值的方向來計算其波動的幅度,是所有血糖波動幅度的平均值,可以不依賴血糖的整體水平而真正反映患者血糖波動的程度,因此,MAGE被認為是患者血糖波動的“金標準”[23]。
胰島素泵在臨床又被稱為“人工胰”,CSII可以模擬自身胰島素的生理分泌功能,能夠持續的對胰島素進行基礎分泌以及餐后的脈沖式釋放,在整個胰島素釋放的程序中,可完全貼近人體生理過程[24],該泵可減輕患者的血糖波動,從而降低或者減輕患者的應激反應,此外還能適當改善患者的胰島素抵抗,有效的控制血糖水平,在降低足潰瘍患者高滲狀態以及抑制細菌繁殖方面具有重要意義。何晏清等[25]報道顯示初診2型糖尿病患者應用胰島素泵短期強化治療不僅能使血糖平穩下降,改善胰島β細胞功能,還能夠抑制作為反映氧化應激損傷指標的8-iso-PGF2α的產生,該因子能夠誘導血管平滑肌細胞中的DNA合成增加,引起血管平滑肌增生造成管腔狹窄,最終引起微循環供血不足,周圍組織細胞缺血缺氧。張曉軍和裴先鋒[26]亦報道胰島素泵短期強化治療能夠顯著改善糖尿病患者血糖的各種指標,顯著提高血漿SOD水平從而提升了抗氧化損傷的防御能力。本研究顯示,與治療前比較,兩組患者SDBG、MAGE及LAGE均顯著下降,觀察組MAGE較對照組下降更為明顯;觀察組治療1、2周后的MDA、8-iso-PGF2α低于對照組,治療1、2周后的SOD高于對照組;潰瘍面積在治療1、2周后亦顯著小于對照組;這些均提示胰島素泵短期強化治療能夠顯著控制老年T2DM合并足潰瘍患者的血糖波動、抑制或緩解患者氧化應激狀態,進而加速了患者潰瘍面的愈合。
本研究中pearson線性分析顯示患者治療前后的MAGE與MDA、8-iso-PGF2α及潰瘍面積呈正相關,而與 SOD呈負相關;治療前后的 MDA、8-iso-PGF2α與潰瘍面積呈正相關;而SOD與潰瘍面積呈負相關,這些均提示2型糖尿病足潰瘍患者潰瘍愈合與血糖波動及氧化應激密切相關,推測患者存在一種“血糖波動-氧化應激-潰瘍愈合”作用鏈,鏈的上游因素(血糖波動及氧化應激)直接影響了潰瘍愈合,而在這些環節中,血糖波動引起的氧化應激至關重要。血糖波動引起氧化應激的失衡的機制尚不明確,可能的原因是:①血糖波動異常可引起胰島素抵抗程度增加,而胰島素抵抗能夠使患者處于氧化應激狀態,從而誘發患者出現慢性炎癥狀態[23,27-29];②血糖波動異常可激活蛋白激酶 C,誘導內皮細胞DNA的氧化損傷及細胞凋亡,同時激活鈣調節通道誘發大量氧自由基生成[21-23];③血糖異常波動可使氨基己糖通路、多元醇通路激活、并通過使蛋白激酶C活化以及終末糖基化產物途徑誘導機體氧化應激出現[30-31]。
綜上所述,老年T2DM合并足潰瘍的愈合可能受到血糖波動及氧化應激損傷的不利影響,胰島素泵短期強化治療能夠較好的控制老年T2DM合并足潰瘍患者的血糖波動、減輕患者氧化應激程度進而促進患者潰瘍的預后。
[1]Sohn M W,Budiman-Mak E,Stuck R M,et al.Diagnostic accuracy of existing methods for identifying diabetic foot ulcers from inpatient and outpatient datasets[J].J Foot Ankle Res,2010,3:27.
[2]Xu W,Weng J.Current role of short-term intensive insu-lin strategies in newly diagnosed type 2 diabetes[J].J Diabetes,2013,5(3):268-274.
[3]趙文州,何陸,郎蘇,等.不同Wagner分級糖尿病足患者自我管理行為現況評分比較[J].中國醫藥導刊,2012,14(10):1729-1730.
[4]廖二元.內分泌學:上冊[M].2版.北京:人民衛生出版社,2004:124-125.
[5]佚名.中國胰島素泵治療指南(2010)[J].中國醫學前沿雜志(電子版),2011,12(4):78-86.
[6]韋華,王民登,李鳳玲,等.高壓氧對糖尿病足潰瘍臨床效果及血漿纖溶系統的影響[J].重慶醫學,2012,41(5):480-482.
[7]Zgonis T,Stapleton J J,Girard-Powell V A,et al.Surgical management of diabetic foot infectionns and amputations[J].AORN J,2008,87(5):935-946.
[8]葛奎,牛軼雯,謝挺,等.氧化應激對糖尿病大鼠燙傷創面愈合的影響[J].同濟大學學報(醫學版),2008,29(5):31-34.
[9]廖炎,樂園.氧化應激與器官損害[J].中國現代醫學雜志,2013,23(18):57-61.
[10]簡茂強,Peter M Elias.氧化應激與表皮通透屏障功能降低性皮膚病[J].中國皮膚性病學雜志,2013,27(4):408-410.
[11]劉杰.糖尿病足綜合治療35例臨床觀察[J].中國綜合臨床,2012,28(2):197-198.
[12]代雪梅,沈霞蔚,肖醉萱.2型糖尿病患者糖尿病足發病的相關因素分析[J].疑難病雜志,2013,12(4):310-311.
[13]唐繼全,甘干達,羅平,等.帶腓淺神經外踝上皮瓣修復糖尿病足創面[J].華南國防醫學雜志,2011,25(1):84-85.
[14]李德梅,李敬會,李麗娜,等.通心絡膠囊聯合中藥浴足治療老年2型糖尿病下肢動脈閉塞癥療效觀察[J].疑難病雜志,2012,11(9):712-714.
[15]吳石白,白關小宏,王良宸,等.負壓封閉引流技術治療重度糖尿病足壞疽的臨床觀察[J].中國綜合臨床,2011,27(10):1066-1069.
[16]Gohel M G,Chacko A N.Serum GGT activity and hsCRP level in patients with type 2 diabetes mellitus with good and poor glycemic control:An evidence linking oxidative stress,inflammation and glycemic control[J].J Diabetes Metab Disord,2013,12(1):56.
[17]鄭煒,龍艷,蘇珂.血糖波動與糖尿病微血管病變的研究進展[J].山東醫藥,2011,51(28):113-114.
[18]丁林,呂肖鋒,張星光,等.胰島素泵強化治療對2型糖尿病合并冠心病患者血糖波動、內皮脂肪酶及超敏C反應蛋白的影響[J].解放軍醫藥雜志,2014,26(8):33-36.
[19]Zhang W,Zhao S,Li Y,et al.Acute blood glucose fluctuation induces myocardial apoptosis through oxidative stress and nuclear factor-κB activation[J].Cardiology,2013,124(1):11-17.
[20]Zsuga J,Gesztelyi R,Kemeny-Beke A,et al.Different effect of hyperglycemia on stroke outcome in non-diabetic and diabetic patients-a cohort study[J].Neurol Res,2012,34(1):72-79.
[21]張潔,董閃閃,康巖,等.2型糖尿病腎病患者血糖波動與氧化應激的相關性研究[J].中國全科醫學,2013,16(29):3410-3413.
[22]Dandona P,Ghanim H,Bandyopadhyay A,et al.Insulin suppresses endotoxin-induced oxidative,nitrosative,and inflammatory stress in humans[J].Diabetes Care,2010,33(11):2416-2423.
[23]張名揚,呂肖鋒,張微微,等.2型糖尿病合并急性腦梗死患者血糖波動對體內氧化應激水平的影響及意義[J].中國全科醫學,2014,17(7):784-787.
[24]黃海,祝開思,王平,等.新診斷的2型糖尿病患者胰島素強化治療前后氧化應激水平的變化[J].中國糖尿病雜志,2011,19(5):338-339.
[25]何晏清,文莉,韓瑛,等.短期胰島素泵強化治療對初診2型糖尿病患者氧化應激的影響[J].山西醫科大學學報,2013,44(12):948-950.
[26]張曉軍,裴先鋒.初診2型糖尿病患者采用短期胰島素泵強化治療對其胰島功能及其氧化應激的影響[J].海南醫學院學報,2012,18(10):1430-1432.
[27]劉金鋼.肥胖癥與2型糖尿病外科治療的規范和推廣[J].中華消化外科雜志,2013,12(12):897-900.
[28]王剛,楊波.糖尿病心肌纖維化的機制及干預[J].中國循證心血管醫學雜志,2013,5(6):669-670.
[29]Rizzo M R,Barbieri M,Marfella R,et al.Reduction of oxidative stress and inflammation by blunting daily acute glucose fluctuations in patients with type 2 diabetes:role of dipeptidyl peptidase-IV inhibition[J].Diabetes Care,2012,35(10):2076-2082.
[30]Monnier L,Mas E,Ginet C,et al.Activation of oxidative stress by acute glucose fluctuations compared with sustained chronic hyperglycemia in patients with type 2 diabetes[J].JAMA,2006,295(14):1681-1687.
[31]朱震宏,蔣曉真,顧哲.2型糖尿病大血管病變與血糖波動和炎癥因子相關分析[J].實用糖尿病雜志,2012,8(2):55-56.

