肝動脈熱灌注化療栓塞對原發性肝癌碘化油沉積及療效的影響*
王振軍,胡鴻濤,黎海亮
鄭州大學附屬腫瘤醫院放射介入科;河南省腫瘤醫院放射介入科 鄭州450003
動脈化療栓塞(transarterial chemoembolization,TACE)在國內外被認為是原發性肝癌的有效治療手段之一[1]。臨床研究[2-4]顯示TACE 對肝癌的療效與碘化油的沉積呈正相關,即碘化油充盈愈完全,患者生存率愈高。近年來,經動脈熱灌注化療后TACE 治療原發性肝癌表現出安全、高效、可提高患者免疫功能的特點,日益受到重視[5-6]。作者就肝動脈熱灌注化療后TACE 治療對中晚期原發性肝癌的臨床療效進行分析,同時就熱灌注化療對碘化油沉積的影響做進一步的探討,現報道如下。
1 對象與方法
1.1 研究對象 入組標準:原發性肝癌,無血管侵犯、肝外臟器轉移,肝功能Child-Pugh 分級為A、B級,預計生存期在6個月以上且為初診患者。依據上述標準,選取2010年1月至2012年10月在河南省腫瘤醫院治療的96例原發性肝癌患者,其中男84例,女12例;年齡26~75歲,中位年齡55歲;其中86例依據臨床資料、影像學(CT、B 超、DSA、MRI等)檢查結合血清AFP 測定明確診斷,余10例經肝穿刺活檢確診;均無治療相關禁忌證。將96例患者分為兩組。熱灌注組48例,其中男43例,女5例,瘤體最大徑≤5 cm15例,>5 cm33例;單發腫瘤患者12例,多發腫瘤患者36例;肝功能Child-Pugh 分級為A 級者28例,B 級者20例。對照組48例,其中男41例,女7例,瘤體最大徑≤5 cm 16例,>5 cm 32例;單發腫瘤患者10例,多發腫瘤患者38例;肝功能Child-Pugh 分級為A 級者26例,B 級者22例。該研究通過了醫院倫理委員會審查,所有入組患者均在術前簽署知情同意書。
1.2 治療方法 患者均采用經皮穿刺動脈插管,對肝動脈及可能存在的腫瘤供血動脈行動脈造影,確定腫瘤供血動脈后,將導管超選擇至腫瘤供血動脈內(必要時使用微導管)。熱灌注組:將鹽酸吉西他濱(1 000 mg/m2)用生理鹽水稀釋后加入熱灌注化療桶中(HGC-3000 腫瘤介入熱療機,珠海),以0.5~1.0 mL/s 流率進行熱灌注,將動脈導管入口處的溫度設定在51℃,而到達腫瘤的溫度維持在41~43℃,隨后用鹽酸吉西他濱200 mg/m2、卡鉑200 mg/m2、碘化油5~20 mL 混合后經腫瘤供血動脈行超選擇性肝動脈化療栓塞。對照組:直接行常溫下而不是行熱灌注化療,其他治療流程及用藥均與熱灌注組相同。患者的介入治療設定為每4 周重復1次,直至患者病情完全緩解或不能耐受。
1.3 觀察指標 ①肝功能變化:治療前、治療后第3天及30天測定丙氨酸轉氨酶(ALT)、谷草轉氨酶(AST)水平。②影像學療效評價:治療后第30天行CT 掃描,依據實體腫瘤的療效評價標準(RECIST)[5]評估客觀療效,臨床有效率=(完全緩解+部分緩解)/總例數×100%。③介入次數。④碘化油沉積情況的評估:治療1、3個月后CT 評估碘化油沉積情況。根據文獻[7]報道將碘化油在腫瘤內部沉積分為4 型。Ⅰ型:碘化油均一沉積于腫瘤內;Ⅱ型:碘化油缺損性沉積,腫瘤內碘化油總量>80%;Ⅲ型:碘化油沉積為散在斑片狀,腫瘤內總量為30%~79%;Ⅳ型:腫瘤內碘化油總量<30%。Ⅰ+Ⅱ型為有效。⑤生存期:從首次治療時開始,直至患者死亡或隨訪結束。
1.4 統計學處理 采用SPSS 18.0 進行數據分析,兩組不同時間點ALT、AST 水平的比較采用重復測量數據的方差分析,臨床有效率和碘化油沉積的比較采用χ2檢驗,介入治療次數的比較采用兩獨立樣本t 檢驗,Kaplan-Meier 法繪制生存曲線并進行logrank 檢驗,檢驗水準α=0.05。
2 結果
2.1 肝功能的變化 治療30 d 內兩組均無患者死亡。兩組患者在治療后第3天ALT、AST 水平較治療前急劇升高,熱灌注組升高幅度更大;治療后第30天兩組ALT、AST 恢復正常。見表1。

表1 兩組治療前后肝功能的變化 U/L
2.2 影像學療效評價 熱灌注組患者病情完全緩解、部分緩解、穩定和進展分別為0、36、7、5例,臨床有效率為75.00%(36/48);對照組分別為0、19、18、11例,臨床有效率為39.58%(19/48)。兩組臨床有效率差異有統計學意義(χ2= 12.303,P<0.001)。
2.3 介入治療次數 熱灌注組行介入治療(2.79 ±1.25)次,對照組(3.46 ±1.50)次,熱灌注組明顯少于對照組(t=2.360,P=0.020)。
2.4 碘化油沉積情況 見表2、3。治療1、3個月后熱灌注組碘化油有效沉積率均高于對照組。
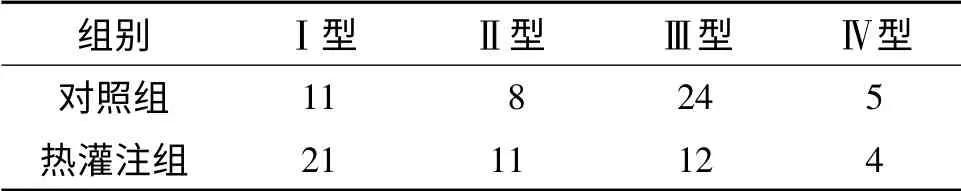
表2 兩組患者治療1個月后碘化油沉積情況比較例

表3 兩組患者治療3個月后碘化油沉積情況比較
2.5 生存分析 對96例患者進行3~32個月隨訪,失訪5例,其中熱灌注組3例、對照組2例。兩組生存曲線差異有統計學意義(χ2=23.411,P<0.001),熱灌注組中位生存期為24個月(95%CI 為20~29個月),對照組為19個月(95%CI 為18~20個月),熱灌注組明顯長于對照組。
3 討論
TACE 可以充分栓塞肝癌病變血管,減少局部血供,其臨床療效與腫瘤內碘化油滯留量成正比[2],患者生存率與碘化油沉積情況呈正相關[3-4]。Choi 等[8]對27例肝癌患者先行肝動脈化療栓塞,然后手術切除,病理和CT 檢查的對比發現碘化油沉積濃密的病灶腫瘤壞死程度達98%,碘化油沉積區無存活的腫瘤組織,而碘化油沉積少的病灶壞死程度只有64%。因此如何提高腫瘤內碘化油滯留量成為提高TACE 療效的關鍵問題。
碘化油可長期停滯于癌組織的血管間隙和毛細血管內,栓塞腫瘤的供血毛細血管。此外,碘化油攜帶抗癌藥物,可在腫瘤組織內形成高濃度的化療環境,殺死腫瘤細胞。但是常規化療灌注用的栓塞劑和溶劑均為常溫,血液溫度高于其溫度,在對患者進行動脈血管內化療灌注和化療栓塞時容易對腫瘤血管造成冷刺激,導致血管痙攣或血流減慢,致使栓塞劑不易完全充填,而一旦術后冷刺激因素消失,血流會突然出現一個加速和加壓,則可能導致部分栓塞劑被沖刷,進一步消弱栓塞效果。既往報道[5-6]證實熱灌注化療可以提高TACE 的效果,熱灌注溫度為41~45℃時效果最佳,一方面熱灌注對腫瘤細胞起到殺傷作用,而正常的肝細胞因能耐受則不會出現不可逆性損傷;另一方面,化療藥物與熱療的協同作用被最大化。
該研究中,作者對肝動脈熱灌注化療后TACE治療對中晚期原發性肝癌的臨床療效進行了觀察。術中作者將動脈導管入口處的溫度設定在51℃(通過熱灌注儀進行設定),從而保證到達腫瘤局部的溫度維持在41~43℃,CT 顯示治療1個月及3個月后熱灌注組患者碘化油有效沉積率均明顯高于對照組,說明熱灌注后立即進行碘化油栓塞可明顯提高腫瘤局部碘化油的沉積率和密集率,而正常肝實質內藥物沉積明顯減少。與對照組比較,熱灌注組臨床有效率提高,中位生存期延長,介入治療次數減少,說明熱灌注化療后TACE 可明顯提高碘化油的沉積率和密集率,從而減少介入栓塞治療次數,同時也減少了介入治療對肝功能造成的損傷。原因可能為[5-6]:①熱刺激使得正常肝動脈痙攣收縮,而腫瘤供血動脈因發育不完善出現擴張。②熱刺激使腫瘤毛細血管滲透性增加,可使更多的碘化油沉積于腫瘤內,并進一步加強了腫瘤末梢血管交通支的栓塞,最終可使栓塞趨于完全。③熱灌注化療栓塞除了使碘化油沉積增多外,還可使其在腫瘤內的分布更均勻,這兩種因素均可以延長碘化油的充填時間[7]。此外,熱灌注可以有選擇性地使瘤體溫度增高,腫瘤細胞會因高溫死亡[9]。局部熱灌注化療還可以進一步加強化療藥活性,改變細胞膜的通透性,促使靶細胞與化療藥的結合,增強化療藥物殺傷癌細胞的作用。與此同時,熱灌注可提升患者自身免疫力,全面抑制化療后腫瘤細胞的復活。
總之,熱灌注化療后TACE 可顯著提高肝癌內碘化油的沉積率,促進腫瘤壞死,減少介入治療次數,顯著延長患者生存期,這是一種把熱療、栓塞和化療融為一體治療原發性肝癌既安全又有效的方法,值得臨床推廣應用。
[1]周霖,王華明,艾鼎倫,等.原發性肝癌患者肝動脈化療栓塞術后肝功能失代償的臨床分析[J].解放軍醫學雜志,2014,39(2):149
[2]張正宇,鄧燕賢,徐軍紅,等.肝癌患者化療栓塞后肝功能嚴重失代償的相關因素分析[J].實用放射學雜志,2015,31(2):287
[3]王建平,侯魯強,劉軍偉,等.肝癌碘油栓塞后碘油沉積量與療效的相關性[J].實用醫藥雜志,2008,25(3):308
[4]劉嶸,王建華,周康榮,等.肝動脈化療栓塞治療原發性肝癌中碘油沉積良好患者療效觀察[J].介入放射學雜志,2001,10(4):212
[5]駱俊朋,胡鴻濤,郭晨陽,等.吉西他濱熱化療灌注聯合卡鉑化療栓塞治療原發性肝癌臨床應用研究[J].介入放射學雜志,2013,22(6):470
[6]駱俊朋,胡鴻濤,郭晨陽,等.吉西他濱熱化療灌注聯合TAE 治療原發性肝細胞癌[J].中國介入影像與治療學,2013,10(3):142
[7]王軍,張緒敬,李東民,等.介入熱灌注化療栓塞治療肝臟惡性腫瘤療效分析[J].介入放射學雜志,2006,15(7):405
[8]Choi BI,Kim HC,Han JK,et al.Therapeutic effect of transcatheter oily chemoembolization therapy for encapsulated nodular hepatocellular carcinoma:CT and pathologic findings[J].Radiology.1992,182(3):709
[9]鄒勁林,呂寶軍,楊光偉,等.介入熱灌注化療對中晚期肝癌患者免疫功能的影響[J].中國實用醫藥,2009,4(35):19

