分析化學(xué)中玻璃器皿及分析儀器的校正教學(xué)
馮建波 吳春艷
摘要:玻璃器皿及分析儀器的校正在分析檢驗(yàn)工作中具有極其重要的作用。結(jié)合具體校正實(shí)驗(yàn)過程,闡述了用衡量法對(duì)單標(biāo)線容量瓶和用純化水校正滴定管操作,并給出了滴定管校正曲線及其繪制步驟;講解了繪制鐠釹濾光片的吸收曲線和分光光度計(jì)其他性能校正。
關(guān)鍵詞:玻璃器皿;分析儀器;校正;操作
中圖分類號(hào):G718.5 ? ? 文獻(xiàn)標(biāo)志碼:A ? ? 文章編號(hào):1674-9324(2015)45-0242-04
分析化學(xué)是一門傳統(tǒng)的專業(yè)基礎(chǔ)課,理論教學(xué)和實(shí)踐教學(xué)已日臻完善。近幾年來我院學(xué)生參加了全國(guó)職業(yè)院校技能大賽——《化學(xué)檢驗(yàn)工》技能競(jìng)賽,從競(jìng)賽的實(shí)際情況及我院工業(yè)分析與檢驗(yàn)專業(yè)畢業(yè)生在企業(yè)從事分析檢測(cè)工作情況反饋意見來看,同學(xué)們對(duì)玻璃器皿和分析儀器的校正工作知道甚少,更不知道校正操作及其重要性。而使用校正過玻璃器皿和分析儀器是提供可靠分析數(shù)據(jù)的保障,也是保證分析誤差最小化的措施之一,在分析檢驗(yàn)工作中具有極其重要的作用。因此,在今后分析化學(xué)中要加強(qiáng)玻璃器皿和分析儀器校正的相關(guān)教學(xué)。
在分析化學(xué)教學(xué)中涉及到準(zhǔn)確計(jì)量的玻璃器皿和分析儀器可歸納為以下幾類:
1.稱量類:機(jī)械天平(已處于淘汰狀態(tài))、電子天平等。
2.計(jì)量類:量筒、量杯、單標(biāo)線容量瓶、滴定管、分度吸量管等。
3.電化學(xué)類:恒電流庫侖儀、酸度計(jì)等。
4.光化學(xué)類:可見光-紫外分光光度計(jì)、原子吸收分光光度計(jì)等。
5.色譜類:氣相色譜儀、液相色譜儀。
下面重點(diǎn)講解單標(biāo)線容量瓶、滴定管、可見光分光光度計(jì)的校正教學(xué)。
一、單標(biāo)線容量瓶校正操作(衡量法)
采用衡量法。衡量法是用天平稱量單標(biāo)線容量瓶中純化水的質(zhì)量,然后按照該溫度下純化水的密度,計(jì)算出單標(biāo)線容量瓶的容積。
1.單標(biāo)線容量瓶外觀要求。單標(biāo)線容量瓶的玻璃應(yīng)清澈、透明。應(yīng)具有下列標(biāo)記:廠名和商標(biāo),標(biāo)準(zhǔn)溫度(20℃),標(biāo)稱總?cè)萘颗c單位,準(zhǔn)確度等級(jí)A或B。
2.單標(biāo)線容量瓶的瓶口與瓶塞之間的密合性要求。當(dāng)純化水注至標(biāo)線,將瓶塞塞緊,當(dāng)用手指壓緊瓶塞,上下顛倒10次,再次顛倒時(shí),在倒置狀態(tài)下保持10秒,結(jié)束后,用濾紙?jiān)谌优c瓶口周圍擦看,不應(yīng)有水滲出。
3.單標(biāo)線容量瓶校正。取洗凈干燥的單標(biāo)線容量瓶,稱重后加入純化水,使液面達(dá)標(biāo)線以下約5mm處,用毛細(xì)滴管將液面準(zhǔn)確地調(diào)至標(biāo)線,準(zhǔn)確稱重單標(biāo)線容量瓶與純化水的重量。計(jì)算純化水的質(zhì)量,用實(shí)驗(yàn)溫度時(shí)1mL水質(zhì)量(查附表1)來除水質(zhì)量,即可計(jì)算出單標(biāo)線容量瓶的實(shí)際毫升數(shù),即20℃時(shí)真實(shí)容積。
二、滴定管校正操作
1.滴定管玻璃應(yīng)清澈、透明,分度線和所量數(shù)值應(yīng)清晰、完整、耐久,分度線應(yīng)平直,分格均勻并必須與器軸相垂直,相鄰兩分度線的中心距離應(yīng)大于1 mm。
2.滴定管應(yīng)具有下列標(biāo)記:廠名和商標(biāo),標(biāo)準(zhǔn)溫度(20℃),等待時(shí)間txxS,標(biāo)稱總?cè)萘颗c單位XXmL,準(zhǔn)確度等級(jí)A、B或Ex。
3.滴定管活塞密合性:當(dāng)純化水注至最高標(biāo)線時(shí),活塞在任意關(guān)閉情況下(不涂油脂)停留20分鐘,漏水量應(yīng)不超過一小格。
4.滴定管容量允差:純化水流出時(shí)間和等待時(shí)間,分度線寬度等均應(yīng)符合下表規(guī)定。
5.滴定管的標(biāo)定:加純化水于滴定管中,使液面達(dá)到最高標(biāo)線以上約5mm處,用活塞慢慢地將液面準(zhǔn)確地調(diào)至零位。將已稱量的稱量杯放在滴定管尖端下,完全開啟活塞,當(dāng)液面降至距檢定分度線以上5mm處,關(guān)閉活塞等待30S,然后在10S內(nèi)用活塞將液面準(zhǔn)確調(diào)至被檢定分度線,準(zhǔn)確稱重稱量杯與純化水的質(zhì)量,計(jì)算純化水質(zhì)量。用同樣方法測(cè)其他刻度處的純化水質(zhì)量。
數(shù)據(jù)處理:由附表1查得K■,按下列公式計(jì)算滴定管各段純化水校正值。
△V=m*K■-V1
△V:校正值mL
V:滴定管讀數(shù)mL
m:稱出純化水質(zhì)量g
K■:換算系數(shù),由附表1查得。
不同容量滴定管標(biāo)定點(diǎn)確定:
1~10mL滴定管:半容量和總?cè)萘慷c(diǎn)。
25mL滴定管:
A級(jí);0~5mL、0~10mL、0~15mL、0~20mL、0~25mL
B級(jí);0~12.5mL、0~25mL
50mL滴定管:
A級(jí);0~10mL、0~20mL、0~30mL、0~40mL、0~50mL
B級(jí);0~12.5mL、0~25mL、0~37.5mL、0~50Ml
三、滴定管校正曲線
對(duì)于已經(jīng)校正為合格的滴定管,在實(shí)際滴定中要考慮玻璃受熱膨脹等因素的影響,為準(zhǔn)確滴定,需要作滴定管校正曲線。
首先把要校正滴定管編號(hào),清洗干凈,活塞涂上凡士林,檢漏,裝入新煮沸冷至室溫的蒸餾水至刻度上,記錄蒸餾水溫度,排氣泡,調(diào)液面至0.00mL刻度處。然后由滴定管放出10.00mL蒸餾水至事先稱重的具塞瓶中,蓋上瓶塞,再稱出裝蒸餾水后的質(zhì)量,兩次之差,即為放出蒸餾水的質(zhì)量。用同樣的方法稱出滴定管由0到20.00mL,0到25.00mL,0到30.00mL,0到40.00mL,0到50.00mL刻度間蒸餾水的質(zhì)量。用實(shí)驗(yàn)溫度蒸餾水質(zhì)量除以相對(duì)應(yīng)溫度下校正的水密度,即可得滴定管各部分容積的實(shí)際毫升數(shù)。
V校=V實(shí)-V讀
V實(shí)=M/ρ
M=M瓶+水-M瓶
V校:校準(zhǔn)點(diǎn)的校正值mL
V實(shí):校準(zhǔn)點(diǎn)的實(shí)際容積mL
V讀:校準(zhǔn)點(diǎn)的放出體積讀數(shù)mL
M:校準(zhǔn)點(diǎn)的放出蒸餾水質(zhì)量g
M瓶+水:校準(zhǔn)點(diǎn)的放出蒸餾水質(zhì)量和瓶質(zhì)量g
M瓶:空瓶質(zhì)量g
ρ:水的密度g/mL
例:在15℃由滴定管放出10.03mL水,稱其質(zhì)量為10.04g,15℃的校正值為0.99792g/mL,因此可計(jì)算出放出水的實(shí)際體積為10.04/0.99792=10.06(mL),因此滴定管這段體積的誤差為10.06-10.03=+0.03mL,使用時(shí)實(shí)際應(yīng)為10.03+0.03=10.06(mL),這才是真實(shí)體積。
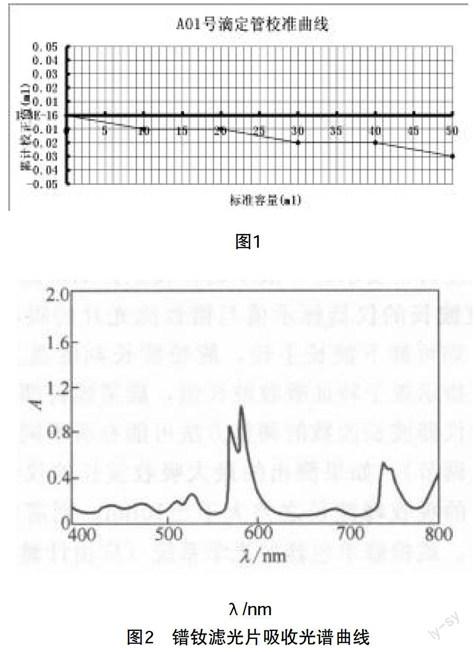
下面是一支50mL、A級(jí)“編號(hào)A01”滴定管校正實(shí)例。
滴定管校正曲線的繪制步驟如下:
(1)在Excel表輸入數(shù)據(jù)
00
10 ? ? ?-0.01
20 ? ? ?-0.01
30 ? ? ?-0.02
40 ? ? ?-0.02
50 ? ? ?-0.03
(2)插入圖形
選中數(shù)據(jù)區(qū)→插入→圖表→XY散點(diǎn)圖→選中折線散點(diǎn)圖→下一步→下一步→輸入標(biāo)題“A01號(hào)滴定管校準(zhǔn)曲線”,X軸名稱“標(biāo)準(zhǔn)容量(mL)”,Y軸名稱“累計(jì)校正值(mL)”→完成。
(3)設(shè)計(jì)刻度線
縱座標(biāo)軸處右鍵→座標(biāo)軸格式→刻度最小值-0.05,最大值+0.05,主要刻度單位0.01,次要刻度單位默認(rèn)。
橫座標(biāo)軸處右鍵→座標(biāo)軸格式→刻度最小值0,最大值50,主要刻度單位5,次要刻度單位1。
(4)設(shè)計(jì)網(wǎng)格線
右鍵單擊圖部分→圖表選項(xiàng)→X軸選主要網(wǎng)格線,次要網(wǎng)格線→Y軸選主要網(wǎng)格線。
(5)去掉灰色底色
右鍵單擊圖區(qū)→數(shù)據(jù)糸列格式→線形→自定義→樣式、顏色、粗細(xì)→數(shù)據(jù)標(biāo)記→自定義→→樣式、前景色、背景色。
四、分光光度計(jì)的校檢
為保證測(cè)試結(jié)果的準(zhǔn)確可靠,新購(gòu)買或使用半年的分光光度計(jì)應(yīng)定期進(jìn)行校檢,校檢內(nèi)容包括:波長(zhǎng)校檢、透射比正準(zhǔn)確度的檢驗(yàn)、穩(wěn)定度的檢驗(yàn)、吸收池(比色皿)配套性檢驗(yàn)。
1.波長(zhǎng)校檢。分光光度計(jì)出廠運(yùn)輸、使用過程中,由于機(jī)械振動(dòng)、溫度變化、燈絲變形、燈座松動(dòng),經(jīng)常會(huì)使測(cè)量波長(zhǎng)同實(shí)際波長(zhǎng)不符,導(dǎo)致測(cè)定誤差,影響測(cè)定結(jié)果的精度,為此經(jīng)常需要校檢。
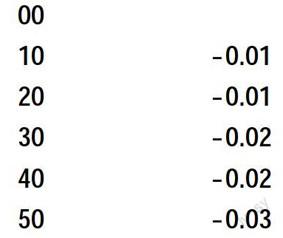
在可見光區(qū)檢驗(yàn)波長(zhǎng)準(zhǔn)確度的方法是繪制鐠釹濾光片的吸收曲線(見圖2)。鐠釹濾光片的吸收峰為528.7nm和807.7nm。如果測(cè)出的峰的最大吸收波長(zhǎng)與儀器標(biāo)示值相差±3nm以上,則需要細(xì)微調(diào)節(jié)波長(zhǎng)刻度校正螺絲(不同型號(hào)的儀器調(diào)整方法有所不同,應(yīng)按儀器說明書進(jìn)行)。如果測(cè)定最大吸收波長(zhǎng)與儀器波長(zhǎng)標(biāo)示值相差大于±10nm,則需調(diào)整鎢燈燈泡的位置,或檢修單色器的光學(xué)系統(tǒng)。
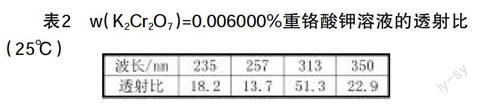
2.透射比正準(zhǔn)確度的檢驗(yàn)。透射比正確度檢驗(yàn)的具體操作是:質(zhì)量分?jǐn)?shù)w(K2Cr2O7)=0.006000%重鉻酸鉀的0.001mol·L-1HClO4標(biāo)準(zhǔn)溶液,以0.001mol·L-1HClO4標(biāo)準(zhǔn)溶液為參比液,以1cm的石英比色皿分別在235nm、257nm、313nm、350nm波長(zhǎng)處測(cè)定透射比,與表2所列標(biāo)準(zhǔn)溶液的標(biāo)準(zhǔn)值比較,根據(jù)儀器的級(jí)別,其誤差應(yīng)在允許的范圍內(nèi)。
3.穩(wěn)定度的檢驗(yàn)。在儀器測(cè)量波長(zhǎng)范圍兩端向中間靠10nm處,例如儀器工作波長(zhǎng)范圍為320nm至820nm,則在330nm和810nm處,調(diào)零點(diǎn)后,蓋上樣品室蓋(打開光門),使光電管受光,調(diào)透射比為95%;若是數(shù)顯式分光光度計(jì),調(diào)透射比至100%,觀察3min讀取透射比的變化,即為光電流穩(wěn)定度。
4.吸收池(比色皿)配套性檢驗(yàn)。在定量分析中,尤其是在紫外光區(qū)測(cè)定時(shí),需要對(duì)吸收池(比色皿)配套性檢驗(yàn),以消除吸收池的誤差,提高測(cè)定的準(zhǔn)確度。
操作是:石英吸收池在220nm處裝蒸餾水;在350nm處裝質(zhì)量分?jǐn)?shù)w(K2Cr2O7)=0.006000%重鉻酸鉀的0.001mol·L-1HClO4標(biāo)準(zhǔn)溶液;玻璃吸收池在600nm處裝蒸餾水;在400nm處裝質(zhì)量分?jǐn)?shù)w(K2Cr2O7)=0.006000%重鉻酸鉀的0.001mol·L-1HClO4標(biāo)準(zhǔn)溶液,以一個(gè)吸收池為參比池,調(diào)節(jié)透射比為100%,測(cè)量其他各吸收池的透射比,透射比的偏差小于0.5%的吸收池可配成一套。
參考文獻(xiàn):
[1]JJJG196-2006.常用玻璃量器檢定規(guī)程[S].
[2]吳萬先.校正滴定管幾種方法的討論[J].化工標(biāo)準(zhǔn)與質(zhì)量管理,1991,(7).
[3]黃一石.儀器分析[M].北京:化工工業(yè)出版社,2013.
[4]高職高專化學(xué)教材編寫組.分析化學(xué)實(shí)驗(yàn)[M].北京:高等教育出版社,2014.
[5]高職高專化學(xué)教材編寫組.分析化學(xué)[M].北京:高等教育出版社,2014.

