石墨爐原子吸收法結合絡合萃取測定芒硝中的鉛
楊華劍, 胡曉燕, 金 錚, 楊 悅, 吳曉平
(臨海市食品藥品檢驗檢測中心,浙江臨海317000)
?
石墨爐原子吸收法結合絡合萃取測定芒硝中的鉛
楊華劍, 胡曉燕, 金 錚, 楊 悅, 吳曉平*
(臨海市食品藥品檢驗檢測中心,浙江臨海317000)
摘要:目的 建立石墨爐原子吸收(GFAAS)法,結合絡合萃取來測定芒硝中的鉛。方法 將芒硝與1%吡咯烷二硫代甲酸銨(APDC)絡合,形成的鉛絡合物以甲基異丁基酮(MIBK)將其萃取出。再以20%鹽酸將鉛從MIBK中反萃取,萃取液用石墨爐原子吸收測定。結果 該方法下鉛的線性范圍為0~50 μg/L,r=0.999 1,加樣回收試驗低、中、高濃度的平均回收率分別為89.9%、95.0%、99.4%,方法檢出限0.045 mg/kg。結論 該方法精確、簡便、快速,可用于芒硝中鉛的測定。
關鍵詞:芒硝;鉛;石墨爐原子吸收;絡合萃取
芒硝Natrii Sulfas為硫酸鹽類礦物芒硝族芒硝經加工精制而成的結晶體,主要含十水硫酸鈉(Na2SO4.10H2O),具有瀉下通便、潤燥軟堅、清火消腫之功效,常用于實熱積滯、腹滿脹痛、大便燥結、腸癰腫痛,尚可外治乳癰,痔瘡腫痛等[1]。
芒硝源于自然環境下生長的礦物,存在有害殘留或污染物質的概率較高,其安全性尤其值得關注,而鉛為中藥材常見有害殘留或污染物質之一,通常采用石墨爐原子吸收法(GFAAS)或ICP-MS法測定。有文獻報道[2],采用ICP-MS法分析測定芒硝中的鉛,但該方法由于儀器昂貴,很難普遍使用,而迄今幾乎沒有原子吸收法測定芒硝中的鉛的研究,其原因是芒硝主要含有硫酸鈉,按照《中國藥典》2010年版附錄中的原子吸收法測定時,背景嚴重干擾測定。國內外已有對海水、腌制食品等高鹽樣品中鉛的原子吸收法測定報道,主要有絡合萃取[3-5]、固相萃取[6-8]、共沉淀[9-11]、吸附分離[12-13]、分散液液微萃取[14]、固化懸浮有機微萃取[15-16]、薄膜擴散梯度技術[17]等,將鉛從高鹽基體中分離出,從而更好地去除高鹽背景的干擾。另外,絡合萃取通過螯合劑改變鉛在水相和有機相之間的分配系數,實現高鹽樣品中的鉛與高鹽基體有效分離,方法簡單、成本低,目前芒硝中鉛的絡合萃取原子吸收法測定尚未見報道。本實驗采用吡咯烷二硫代甲酸銨-甲基異丁基甲酮(APDC-MIBK)絡合萃取體系萃取芒硝中的微量鉛,再利用稀鹽酸從MIBK中反萃取鉛,可有效消除硫酸鈉等無機鹽的干擾,實現了石墨爐原子吸收法測定芒硝中的鉛。
1 儀器與試劑
PerkinE1mer-AA 900Z原子吸收光譜儀、THGA石墨管(美國PerkinE1mer公司);Mi11i-Q水處理系統(美國Mi1ipore公司)。
鉛標準溶液(1 000 μg/mL,產品編號GBW08619)。鹽酸為優級純、硝酸鈀為化學純、甲基異丁基甲酮為分析純(國藥集團化學試劑有限公司);吡咯烷二硫代甲酸銨(純度99%,阿拉丁試劑上海有限公司);實驗用水為超純水(Mi11i-Q水處理系統)。芒硝(市內5家零售藥店,散裝),由中心執業中藥師郭勇鑒定為正品藥材。
2 方法
2.1 溶液配制
標準使用液:取鉛標準溶液適量,2%鹽酸溶液逐級稀釋至50 μg/L,即得。
基體改進劑溶液:稱取二水硝酸鈀30 mg,0.5 mL硝酸溶解,超純水定容至25 mL,搖勻,即得0.1%硝酸鈀基體改進劑溶液。
1%APDC溶液:稱取APDC 250 mg,超純水溶解定容至25 mL,搖勻,即得。
20%鹽酸溶液:取鹽酸200 mL,加水稀釋至1 000 mL,即得。
2.2 供試品溶液的制備 將本品研細,精密稱取0.5 g,置于50 mL量瓶中,1%鹽酸溶液溶解,定容。再取5 mL,置于10 mL比色管中,加入1% APDC溶液1 mL,混勻。溶液略混濁時,用1 mo1/L氫氧化鈉溶液調至剛澄清,加入MIBK溶液1 mL,渦旋30 s,靜置分層后棄去水相,加入20%鹽酸4 mL,渦旋60 s,靜置分層后棄去有機相,水相用水定容至5 mL,即得。
2.3 儀器參數 波長283.31 nm;燈電流10 mA;狹縫寬度0.7 nm;背景校正zeeman;進樣量20 μL;基體改進劑0.1%硝酸鈀溶液[18]5 μL。石墨爐升溫程序見表1。
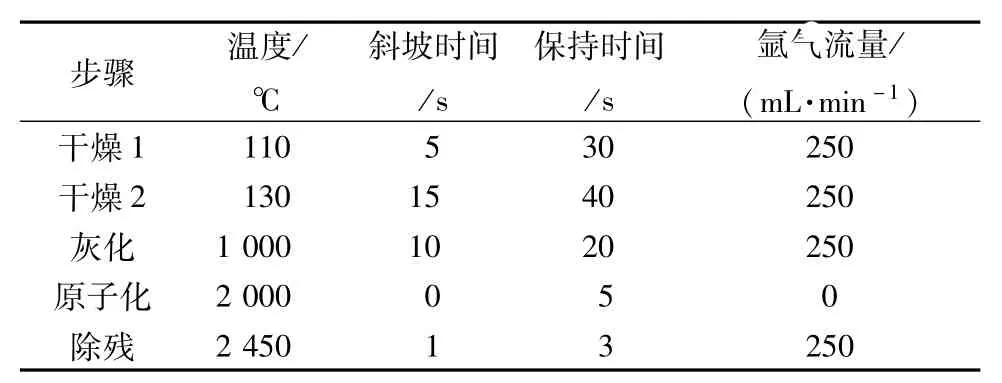
表1 升溫程序Tab.1 Tem perature program
3 結果與討論
3.1 試驗條件的優化 對芒硝中鉛測定方法的各個影響參數進行優化,確定最佳試驗條件。
3.1.1 pH對鉛絡合的影響 在APDC-MIBK萃取體系中,APDC與鉛絡合后,被MIBK溶劑萃取,該絡合過程受溶液pH的影響。本實驗以40 μg/L鉛溶液為測試對象,用1 mo1/L氫氧化鈉分別調節pH為0.8、1.6、2、2.5、3.5、4.0、5.2、6.3、7.5,按“2.2”項下方法用MIBK萃取后,直接測定有機相吸光度,結果見圖1。由圖可知,當pH 為1.6~3.5時,MIBK對鉛絡合物的萃取效率最大;pH≤1.6時,加入1%APDC溶液后體系變渾濁;pH≥2.5時,體系澄清。因此,確定在前處理過程中加入1%APDC溶液后,再用1 mo1/L氫氧化鈉調節至溶液剛好澄清。
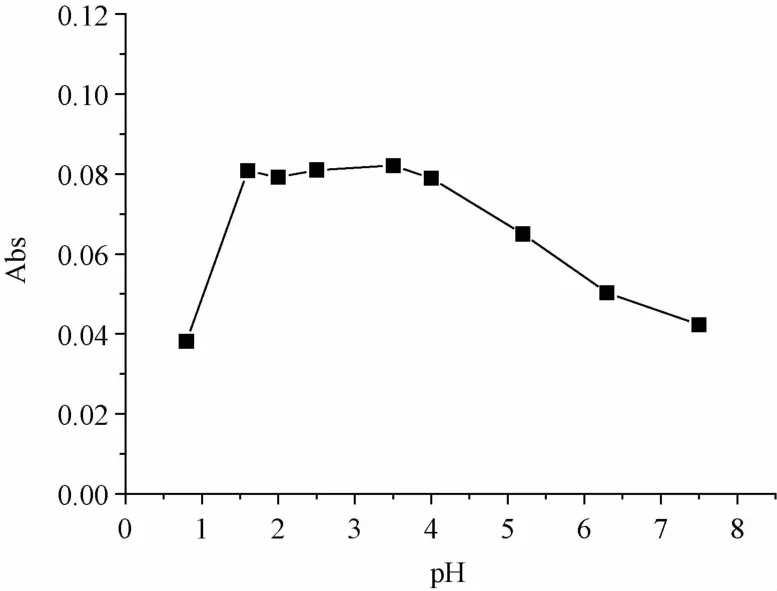
圖1 pH對絡合萃取的影響Fig.1 Effect of pH on chelating extraction
3.1.2 APDC濃度的影響 以APDC為絡合劑時,其加入量應保證能夠將鉛完全絡合以便萃取。本實驗以40 μg/L鉛溶液為測試對象,分別加入質量濃度為0.1%、0.3%、0.5%、1%、1.5%、2%的APDC溶液1 mL,MIBK萃取后測定有機相吸光度,結果見圖2。由圖可知,APDC質量濃度超過0.3%時,鉛的吸光度就不再隨其增加而增加。為確保對芒硝中鉛的完全絡合,最終確定APDC的質量濃度為1%。
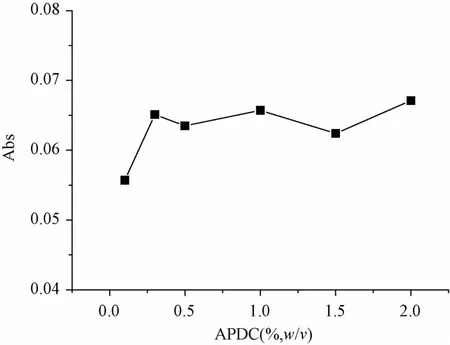
圖2 APDC質量濃度對絡合萃取的影響Fig.2 Effect of APDC concentration on chelating extraction
3.1.3 MIBK加入量的影響 樣品前處理過程中選擇MIBK作為萃取劑,可將產生的ADPC-Pb絡合物萃取到有機相中。本實驗以40 μg/L鉛溶液為測試對象,萃取劑MIBK的加入量分別為100、150、200、250、500、1 000、2 000 μL,即濃縮比(樣品體積/MIBK體積)分別為50、35、25、20、10、5、2.5,然后測定有機相濃度并計算萃取率。當濃縮比≤20時,萃取率可以達到90%左右;濃縮比≤5時,萃取率可以達到95%以上。因此,確定濃縮比為5,即1 mLMIBK溶液。
3.1.4 鹽酸體積分數對反萃取的影響 本實驗以40 μg/L鉛溶液為測試對象,萃取至MIBK中后,分別用4%、8%、16%、20%、24%鹽酸溶液進行反萃取,測定并計算回收率,當達到20%時,基本萃取完全,結果見圖3。因此,確定鹽酸體積分數為20%。
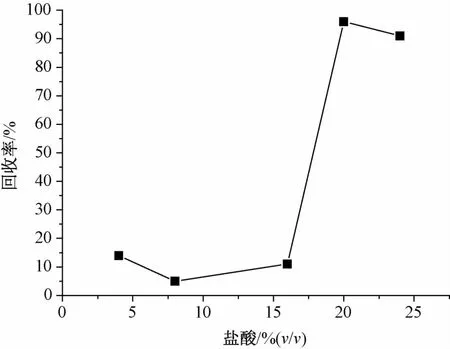
圖3 鹽酸體積分數對反萃取的影響Fig.3 Effect of hydrochloric acid concentration on stripping
3.1.5 硝酸鈀基體改進劑的影響 采用石墨爐原子吸收法測定鉛時,硝酸鈀作為基體改進劑能有效提高灰化溫度,消除背景干擾[18]。本實驗以5 μL 0.1%硝酸鈀溶液為基體改進劑時,原子吸收圖譜峰型平滑對稱,供試品溶液與標準溶液的出峰時間基本一致,精密度良好。
3.2 方法學考察
3.2.1 線性和范圍 按“2.1”、“2.3”項下方法和參數測定標準溶液,繪制標準曲線。結果,回歸方程為y=0.001 74x+0.000 98,r=0.999 1,鉛濃度在0~50 μg/L范圍內線性關系良好。
3.2.2 檢出限 在石墨爐原子吸收法中,檢出限的定義為3SD/k。其中,SD是指對標準空白溶液進行11次測量得到的值,k是指標準曲線的斜率。Pb的檢出限為0.45 μg/L,方法檢出限為0.045 mg/kg。
3.2.3 回收率試驗 按“2.2”項下方法制備供試品溶液3份,分別加入1.00 μg/mL鉛標準溶液0.50、1.00、1.80 mL,配制高、中、低3個質量濃度,每個質量濃度平行3份,測定鉛的加樣回收率,計算RSD,結果見表2。由表可知,該方法回收率良好。
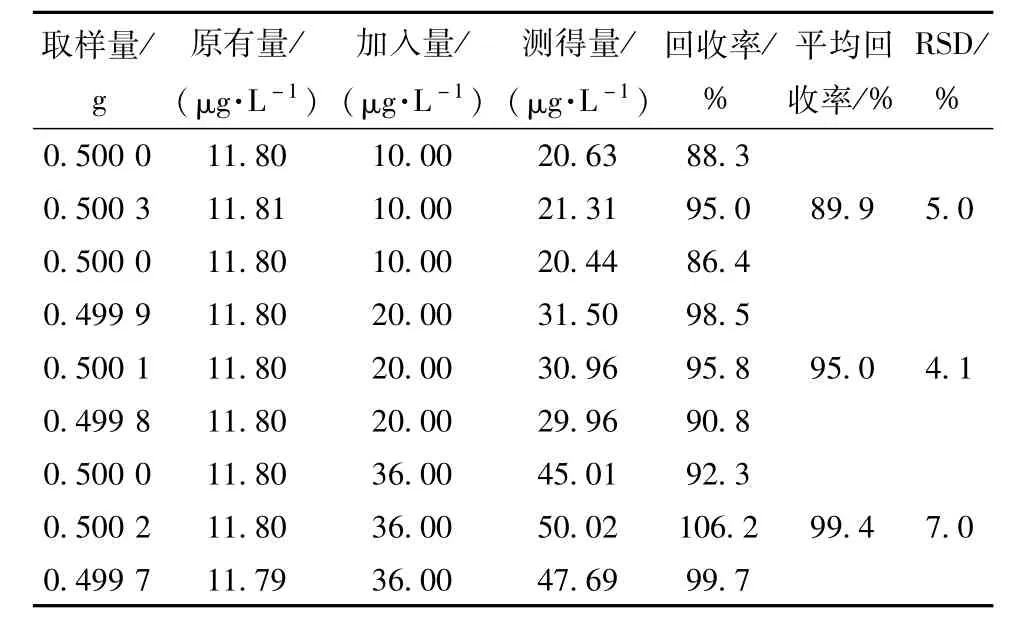
表2 回收率試驗結果(n=3)Tab.2 Results of recovery tests(n=3)
3.2.4 精密度試驗 選擇20 μg/L鉛標準液,按“2.2”項下方法萃取與反萃取后,測定7次。結果,其RSD為1.62%,表明儀器精密度良好。
3.3 樣品測定 取市購芒硝樣品5批,按“2.2”項下方法制備供試品溶液進行測定。結果,5批樣品中鉛的含有量為分別為1.18、1.08、4.20、3.37、2.12 mg/kg,小于一般中藥材規定的5 mg/kg限量。而且,采用本方法制備的供試品溶液時,石墨爐原子吸收測定時背景干擾基本消除,見圖4、圖5。
4 結論
本實驗建立了石墨爐原子吸收法測定芒硝中的鉛,通過APDC-MIBK絡合萃取,稀鹽酸反萃取,可有效消除芒硝中無機鹽的背景干擾。在優化的最佳實驗條件下,該方法精密度高,測定結果準確,加樣回收率符合要求,而且操作簡便,分析速度快,能滿足分析測試要求,適用于芒硝中鉛的測定。
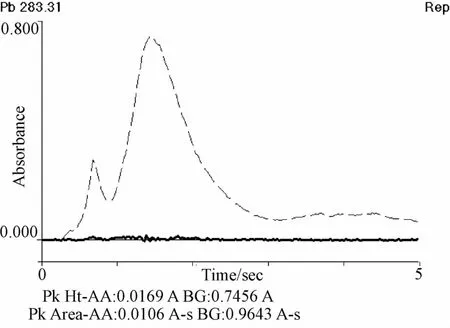
圖4 未經萃取時芒硝中鉛的原子吸收圖譜Fig.4 Absorbance peak profile of Pb in Natrii Sulfas w ithout extraction
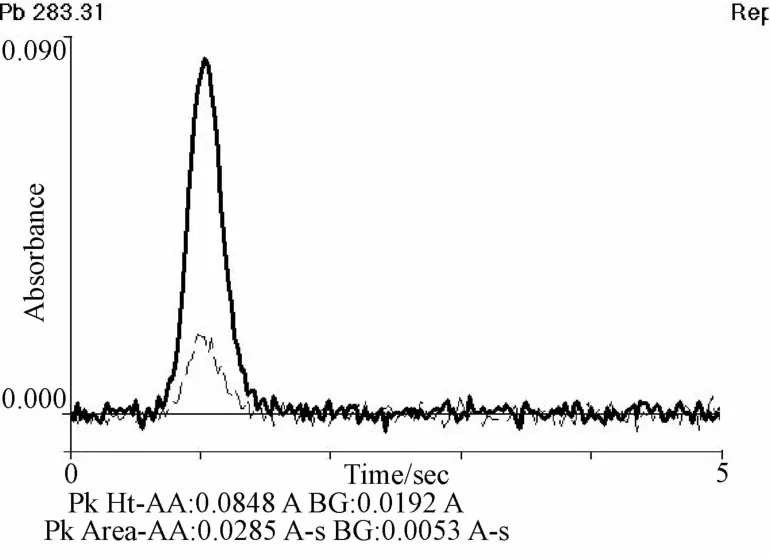
圖5 絡合萃取后芒硝中鉛的原子吸收圖譜Fig.5 Absorbance peak profile of Pb in Natrii Sulfas after chelating extraction
參考文獻:
[1] 國家藥典委員會.中華人民共和國藥典:2010年版一部[S].北京:中國醫藥科技出版社,2010:118-119
[2] 李 沁,吳春敏,鄒義栩,等.礦物藥芒硝中無機元素的ICP-MS分析[J].藥物分析雜志,2013,33(11):1887-1892.
[3] 李秀婷,王 冬.石墨爐原子吸收法測定高鹽食品中的微量鉛[J].糧油食品科技,2003,11(4):35-36.
[4] Anthemidis A.Automatic sequentia1 injection 1iquid-1iquid micro-extraction system for on-1ine f1ame atomic absorption spectrometric determination of trace meta1 in water samp1es[J].Talanta,2008,77(2):541-545.
[5] Naeemu11ah,Kazi T G,Afridi H I,et al.Simu1taneous determination of si1ver and other heavymeta1s in aquatic environment receiving wastewater from industria1 area,app1ying an enrichmentmethod[J].Arabian J Chem,2014,http://dx.doi. org/10.1016/j.arabjc.2014.10.027
[6] Baytak S,Türker A R.Determination of 1ead and nicke1 in environmenta1samp1es by f1ame atomic absorption spectrometry after co1umn so1id-phase extraction on Ambersorb-572 with EDTA [J].JHazard Mater,2006,129(1-3):130-136.
[7] Mahmoud M E,Kenawy IMM,HafezMM A H,etal.Remova1preconcentration and determination of trace heavy meta1 ions in water samp1es by AAS via chemica11y modified si1ica ge1N-(1-carboxy-6-hydroxy)benzy1idenepropy1amine ion-exchanger [J].Desalination,2010,250(1):62-70.
[8] ?ahan S,?ahin U.An automated so1id phase extraction coup1ed with e1ectrotherma1 atomic absorption spectrometric determination of Pb(II)in high sa1t content samp1es[J].Talanta,2011,86:128-132.
[9] Doner G,Ege A.Determination of copper,cadmium and 1ead in seawater and minera1water by f1ame atomic absorption spectrometry after coprecipitation with a1uminum hydroxide[J].A-nal Chim Acta,2005,547(1):14-17.
[10] Saracog1u S,Soy1ak M,Peker D S K,et al.A pre-concentration procedure using coprecipitation for determination of 1ead and iron in severa1samp1es using f1ame atomic absorption spectrometry[J].Anal Chim Acta,2006,575(1):133-137.
[11] Baysa1A,Akman S,Ca1isir F.A nove1s1urry samp1ing ana1ysis of 1ead in different water samp1es by e1ectrotherma1atomic absorption spectrometry after coprecipitated with coba1t/pyrro1idine dithiocarbamate comp1ex[J].J Hazard Mater,2008,158(2-3):454-459.
[12] Saitoh T,Satoh F,Hiraide M.Concentration of heavy meta1 ions in water using thermoresponsive che1ating po1ymer[J].Talanta,2003,61(6):811-817.
[13] Tokman N,Akman S,Ozerog1u C.Determination of 1ead,copper and manganese by graphite furnace atomic absorption spectrometry after separation/concentration using a water-so1ub1e po1ymer[J].Talanta,2004,63(3):699-703.
[14] Naseri M T,Mi1ani Hosseini M R,Assadi Y,et al.Rapid determination of 1ead in water samp1es by dispersive 1iquid-1iquid microextraction coup1ed with e1ectrotherma1 atomic absorption spectrometry[J].Talanta,2008,75(1):56-62.
[15] Dadfarnia S,Sa1manzadeh AM,Shabani AM H.A nove1separation/preconcentration system based on so1idification of f1oating organic drop microextraction for determination of 1ead by graphite furnace atomic absorption spectrometry[J].Anal Chim Acta,2008,623(2):163-167.
[16] Chamsaz M,Akhoundzadeh J,Arbab-Zavar M H.Preconcentration of 1ead using so1idification of f1oating organic drop and its determination by e1ectrotherma1 atomic absorption spectrometry [J].JAdv Res,2013,4(4):361-366.
[17] Chen H,Guo L,Zhang M,etal.Determination of 1ead in soybean sauces by the diffusive gradients in thin fi1ms technique [J].Food Chem,2014,165:9-13.
[18] 吳曉平,楊華劍.硝酸鈀基體改進劑在原子吸收石墨爐法測定黃芪中鉛的應用[J].中成藥,2014,36(8):1696-1700.
[綜 述]
Determ ination of lead in Natrii Sulfas by GFAAS combined w ith chelating extraction
YANG Hua-jian, HU Xiao-yan, JIN Zheng, YANG Yue, WU Xiao-ping*
(Linhai Center for Food and Drug Control,Linhai317OOO,China)
ABSTRACT:AIM To estab1ish amethod for the determination of 1ead in Natrii Sulfas by graphite furnace atomic absorption spectrometry(GFAAS)combined with che1ating extraction.METHODS Natrii Sulfas was che1ated with 1% ammonium pyrro1idinedithiocarbamate(APDC).The obtained comp1ex was extracted from N.Sulfas with methy1 isobuty1ketone(MIBK).Then 1ead was stripped from MIBK with 20% hydroch1oric acid and detected by GFAAS.RESULTS The 1inearity of this method ranged from 0 to 50 μg/L.The corre1ation coefficient was 0.999 1.The 1imit of detection was 0.045 mg/kg.The average recoveries were 89.9%,95.0% and 99.4% at 1ow,medium and high concentrations,respective1y.CONCLUSION Thismethod is accurate,simp1e and rapid,which can be used for the determination of 1ead in Natrii Sulfas.
KEY WORDS:Natrii Sulfas;1ead;GFAAS;che1ating extraction
*通信作者:吳曉平(1968—),男,副主任技師,從事食品藥品檢驗與分析。Te1:(0576)85306113
作者簡介:楊華劍(1983—),男,工程師,從事食品藥品檢測工作。Te1:13867626365,E-mai1:yhjzju@126.com
收稿日期:2015-04-07
doi:10.3969/j.issn.1001-1528.2016.01.031
中圖分類號:R284.1
文獻標志碼:A
文章編號:1001-1528(2016)01-0137-05

