人ASPP2重組腺病毒質量控制研究
王 爽,許堅吉,劉曉霓,陳德喜
(首都醫科大學附屬北京佑安醫院北京市肝病研究所,北京 100069)
?
人ASPP2重組腺病毒質量控制研究
王爽,許堅吉,劉曉霓,陳德喜
(首都醫科大學附屬北京佑安醫院北京市肝病研究所,北京100069)
摘要:目的對人ASPP2重組腺病毒制劑進行質量分析,并針對其關鍵質量特性建立質控方法。方法采用PCR法對重組腺病毒的載體結構特征基因E2B和目的基因ASPP2進行擴增,瓊脂糖電泳進行分子量鑒定;采用UV-SDS法測定重組腺病毒的病毒顆粒數;采用組織培養半數感染劑量法(TCID50)測定重組腺病毒的感染滴度;采用Western blot法對重組腺病毒感染靶細胞后目的蛋白ASPP2的表達情況進行檢測;通過MTT實驗觀察重組腺病毒對肝癌細胞的生物學效應;采用A549細胞進行重組腺病毒的復制型病毒檢測。結果腺病毒載體E2B基因和目的基因ASPP2的鑒定結果與理論值相符;重組腺病毒的病毒顆粒數為每毫升5.6×1012VP,病毒滴度為每毫升2×1011IU,比活性為3.5%;病毒感染靶細胞24 h后可檢測出ASPP2蛋白的表達;重組腺病毒對肝癌細胞具有生長抑制作用;復制型腺病毒(RCA)水平小于1 RCA/3.0×1010VP,符合中國食品藥品監督管理局(SFDA)的標準。結論>建立了人ASPP2重組腺病毒的關鍵特征的質量控制方法,為該重組腺病毒質量標準的建立及相關應用奠定了基礎。
關鍵詞:基因治療;腺病毒;ASPP2;質量控制;病毒比活;MTT
基因治療是指運用DNA轉移來治療甚至預防人類疾患。將DNA送入細胞的方法雖然很多,但進行基因治療時,必須讓多數的細胞都獲得DNA,一般的DNA傳送方法都無法達到此目標。由于病毒感染細胞的效率很高,因此適合做基因治療的載體,將預轉導的基因送入細胞內。腺病毒載體是現在基因治療最為常用的治療載體之一。腺病毒雖然不能長時間穩定表達,但其轉移效率高的特點使其目前在治療惡性腫瘤方面具有了其它病毒載體難以替代的優勢[1-2]。
ASPP2是p53凋亡刺激蛋白(apoptosis stimulating protein of p53, ASPP)家族的一員,能特異性地調節 p53 依賴性凋亡作用。早在10多年前,ASPP2就被發現是p53的結合蛋白[4],它作為p53介導凋亡的正調節子的作用已經被明確證實。同時,ASPP2的生理學重要性也已經通過ASPP2缺陷型鼠的產生及特征分析展現出來[5-6]。我們現在已經知道ASPP2是一種單倍劑量不足型腫瘤抑制因子,在鼠的發育和腫瘤形成過程中是p53的重要激活劑。臨床研究顯示包括肝癌在內的多種腫瘤組織ASPP2表達下降,與腫瘤的發展、轉移和預后密切相關[7-9],ASPP2可能是未來癌癥治療的一個新的重要靶點。
我們前期構建并大量擴增純化了人ASPP2重組腺病毒,本實驗依據《人基因治療和制劑質量控制技術指導原則》[10]及《中國藥典》三部(2010版)相關要求,結合該重組腺病毒的特點,針對關鍵質量特征,從重組腺病毒的鑒定、病毒顆粒數、滴度檢測、目的蛋白表達、生物學活性以及復制型腺病毒(RCA)檢測幾方面對人ASPP2重組腺病毒進行質量分析,建立關鍵質量特征的質量控制方法,為其下一步研究奠定質量基礎。
1材料與方法
1.1試劑與儀器
DMEM高糖培養基、胎牛血清、胰酶、青鏈霉素購自美國Gibco公司;人ASPP2重組腺病毒由陜西師范大學生命科學學院夏海濱教授基因治療研究室構建;人胚腎293T細胞、人肺癌A549、人肝癌HepG2和Huh7細胞株為本室保存。10 cm細胞培養皿、96孔、24孔細胞培養板購自美國Corning公司;ASPP2單克隆抗體購自美國Sigma公司;通用型基因組DNA提取試劑盒購自康為世紀公司;MTT 噻唑藍購自美國Sigma公司。Nikon ECLIPSE TE2000-U倒置熒光顯微鏡;BioTeke ND5000超微量紫外可見分光光度計;Thermo Scientific 8000型恒溫CO2培養箱;BACKMAN L-80XP 超速離心機;BioTeke CYTATION3細胞成像多功能檢測系統;BIO-RAD DNA Engine PCR儀;Alpha Imager凝膠成像儀;Thermo Scientific Multiskan GO全波長酶標儀。
1.2方法
1.2.1PCR-電泳法鑒定腺病毒E2B和人ASPP2基因重組腺病毒由載體DNA和目的基因兩部分構成。按照試劑盒方法提取病毒基因組DNA,通過對重組腺病毒載體結構基因E2B和目的基因ASPP2進行PCR擴增。PCR產物經1%瓊脂糖凝膠電泳分子量鑒定。以滅菌純水代替模板同步反應作為陰性對照。
E2B區引物序列為:上游引物5′-TCGTTTCTCAGCAGCTGTTG-3′,下游引物5′-CATCTGAACTCAAAGCGTGG-3′,擴增片段大小為880 bp。擴增條件為:94℃變性5 min;94℃變性20 s,55℃復性30 s,72℃延伸1 min,共40個循環;72℃延伸5 min[10]。
ASPP2的引物序列為:上游引物5′ -AGCTGCCATGGAGACCATCT-3′,下游引物5′- ACTGTTCTCCGTACTGGCAC-3′,擴增片段大小為220 bp。擴增條件為:95℃變性3 min;94℃變性1 min,55℃復性1 min,72℃延伸1 min,共3個循環;94℃變性30 s,55℃復性45 s,72℃延伸45 s,共27個循環;72℃延伸5 min。
1.2.2UV-SDS法測定人ASPP2重組腺病毒病毒顆粒數用病毒保存液配制0.2% SDS;取等量的人ASPP2重組腺病毒待測液與0.2% SDS液混合;振蕩混勻,56 ℃水浴中放置10 min;等溫度降至室溫時,瞬時離心。病毒保存液配制的0.2% SDS作為空白對照,測定波長260和280 nm處的吸光度值,平行實驗2次。按公式計算:病毒顆粒數=A260 nm×稀釋倍數×1.1×1012。
1.2.3半數組織培養感染劑量(TCID50)法測定病毒滴度在實驗前24 h,向96孔板每孔加入100 μL人胚腎293T細胞懸液,1×103個細胞;待測病毒液的稀釋,按10倍稀釋度(106~1013)稀釋病毒樣品;從孵箱中取出96孔板,在顯微鏡下確定每孔的細胞均生長良好。吸棄舊培養液,然后依次將106~1013稀釋的病毒加入96孔板中,每一稀釋度占用一行,每行10孔重復,每孔加入90 μL 病毒稀釋液,而每行的第11~12孔均加入90 μL不含病毒的完全培養基作為對照;37℃培養10 d后觀察細胞病變現象,并對CPE孔進行計數,計算每行的陽性率,計算病毒滴度(Spearman-Karber Method):病毒滴度=10(x+0.8)IU/mL,x=101~1012依次稀釋度下CPE陽性率總和。公式使用條件:陰性對照沒有CPE和生長抑制現象;加入最小稀釋濃度病毒液的孔均有CPE。
1.2.4Western blot方法檢測人ASPP2重組腺病毒目的蛋白的表達取人ASPP2重組腺病毒,以MOI=100感染人肝癌HepG2和Huh7細胞,24 h后提取細胞蛋白;用BCA法進行蛋白定量;經8% SDS-PAGE,后將蛋白轉至PVDF膜上;用ASPP2單克隆抗體1 ∶1 000稀釋,二抗1 ∶2 000稀釋;室溫下孵育一抗2 h,用1×TBST洗膜3次;室溫下孵育二抗1 h,用1×TBST洗膜3次;用ECL試劑盒檢測,壓片后顯影。
1.2.5人ASPP2重組腺病毒生物學活性測定培養肝癌Huh7細胞和HepG2細胞至對數生長期,消化并計數,將細胞懸液以每孔細胞數2 500個/100 μL培養液接種4塊96孔板;次日加入相應滴度的病毒液(Huh7細胞病毒終濃度為1×107和1×108pfu·mL-1,HepG2細胞病毒終濃度為5×106和5×107pfu·mL-1),每個滴度同時做3個復孔;在病毒加入后的24、48、72、96 h時傾倒培養液,每孔加MTT(5 g·L-1)20 μL后,于37℃孵育4 h;傾倒板中液體并向每孔加入150 μL DMSO,振蕩10 min,用酶標儀在490 nm波長處檢測數值。實驗重復3次。計算公式:生長抑制率/%=(1-ASPP2干預組/陰性對照)×100%
1.2.6復制性腺病毒(RCA)的檢測收集A549細胞并配成濃度為4×108·L-1的細胞懸液,共132 mL。接種細胞于11個12孔板,每孔4×105個細胞,置于孵箱,37℃、5% CO2培養過夜。將3×1010VP待測樣品稀釋于120 mL DMEM完全培養基。移去12孔板內的培養基,并加入1 mL待檢樣品,一共感染10個12孔板。同時設定一板陰性對照,每孔加入1 mL完全培養基,置于孵箱,37℃培養14 d。在d 7補液,每孔加1 mL完全DMEM。結果判定:加入待檢樣品的10板均無致細胞病變效應(CPE)出現,同時陰性對照的細胞正常,無CPE產生,則判定病毒樣品的RCA檢測合格。
2結果
2.1人ASPP2重組腺病毒鑒定
經1%瓊脂糖凝膠電泳分析,ASPP2基因擴增產物可見220 bp的特異性條帶,E2B基因擴增產物可見880 bp的特異性條帶,與預期的擴增片段長度相符。見Fig 1。
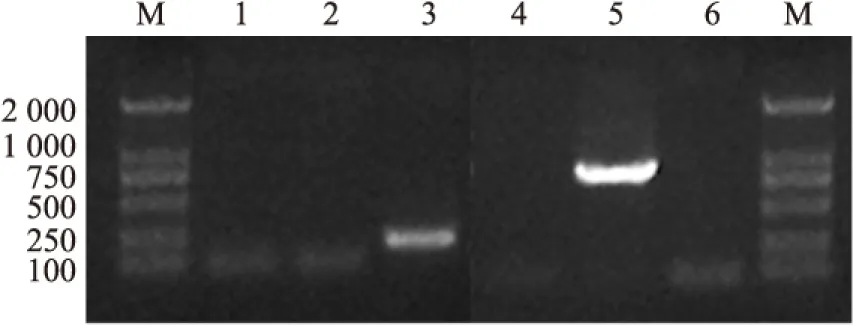
Fig 1 Electrophoretic profile of PCR products of ASPP2 and E2B genes
1:negative control(ASPP2 gene);2:PCR products of 293T cells(ASPP2 gene);3:recombinant adenovirus(ASPP2 gene);4:PCR products of 293T cells(E2B gene);5:recombinant adenovirus(E2B gene);6:negative control(E2B gene);M:DNA marker 2000.
2.2人ASPP2重組腺病毒的顆粒數與滴度測定
病毒可以通過測定吸光度值來計算病毒總顆粒數,進行適當稀釋后,使病毒液在260 nm處的吸光度值處于0~1.0之間,根據公式:病毒顆粒數=A260 nm×稀釋倍數×1.1×1012計算重組ASPP2腺病毒的病毒顆粒數為5.6×1012VP/mL。同時計算A260/A280的比值為1.21,落在規定值的1.2~1.3之間,初步分析結果顯示人ASPP2重組腺病毒純度達到要求。病毒滴度的測定采用SFDA和FDA推薦的TCID50法,此方法已被用于測定許多病毒的滴度,病毒稀釋液與細胞在96孔板進行培養,然后監測每孔是否出現CPE。根據公式計算后得到人ASPP2重組腺病毒的病毒滴度為2×1011IU/mL。病毒比活即病毒感染滴度與病毒顆粒數的比值(IU/VP)。目前,SFDA規定重組腺病毒作為基因治療制品的比活性應高于3.3%。人ASPP2重組腺病毒的比活值為3.5%,符合SFDA規定的要求。
2.3人ASPP2重組腺病毒目的蛋白的表達情況
在確定目的基因存在后,還需要進一步驗證存在于制劑中的目的基因經腺病毒載體介導后,是否可在靶細胞中表達目的蛋白。本實驗通過人ASPP2重組腺病毒感染人肝癌HepG2和Huh7細胞后,檢測細胞中目的蛋白的過表達情況。結果顯示在病毒感染24 h,ASPP2腺病毒感染細胞比未感染細胞存在ASPP2蛋白的高表達現象。見Fig 2。
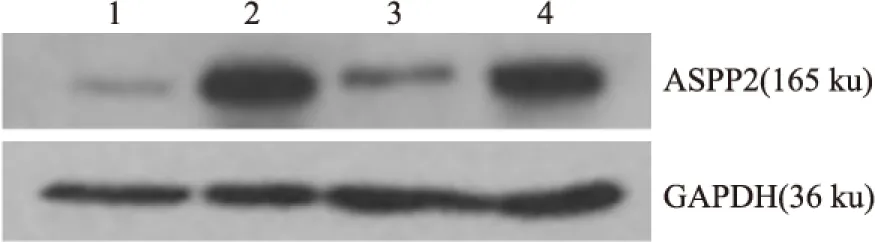
Fig 2 ASPP2 protein expression in infected HepG2 and Huh7 cells by human ASPP2 recombinant adenovirus
1:HepG2 cells;2:HepG2 cells infected by human ASPP2 recombinant adenovirus;3:Huh7 cells;4:Huh7 cells infected by human ASPP2 recombinant adenovirus
2.4生物學活性
效應實驗除了基因表達檢測外,還應觀察表達的目的蛋白是否產生特定的生物學功能。結果顯示,與陰性對照腺病毒相比,人ASPP2重組腺病毒(劑量)在不同時間段都存在不同程度的生長抑制情況。當人ASPP2重組腺病毒在5×107pfu/mL滴度下作用HepG2細胞72 h時的生長抑制率為50.5%;當人ASPP2重組腺病毒在1×108pfu/mL滴度下作用Huh7細胞72h時的生長抑制率為61.69%,說明ASPP2對肝癌HepG2和Huh7細胞具有明顯的生長抑制作用。見Fig 3。

Fig 3 Growth inhibitory effect of ASPP2 recombinant adenovirus on HepG2 and Huh7 cells
2.5復制型腺病毒(RCA)檢測
由于復制型腺病毒(RCA)數量會隨著293細胞的傳代次數增加而增加,而RCA的產生會嚴重干擾重組腺病毒載體的使用效果,并帶來安全隱患。RCA檢測是重組腺病毒制品安全性檢查的核心指標。目前,SFDA和FDA推薦采用A549細胞生物學方法檢測RCA。非復制型腺病毒不會造成A549細胞產生CPE。規定標準為:每3.0×1010VP中應不高于1RCA(即≤1RCA/3.0×1010VP)。Fig 4顯示,實驗組加入重組腺病毒樣品后,持續培養2周后未見CPE,而對照組293細胞則出現明顯的CPE。結果表明重組ASPP2腺病毒中的RCA符合SFDA標準。
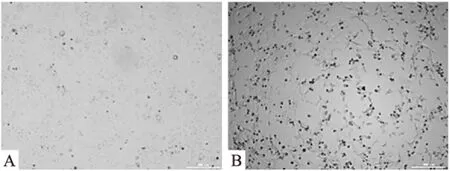
Fig 4 RCA detection of ASPP2 recombinant adenovirus(×40)
A:Human ASPP2 recombinant adenovirus infected A549 cells for 14 days;B:Human ASPP2 recombinant adenovirus infected 293 cells for 7 days
3討論
癌癥是一種獲得性遺傳疾病,通過引入治療性腫瘤抑制基因或使癌基因失活,基因治療有望成為一種非常有效的抗腫瘤治療方式。其可產生針對每個腫瘤的精確遺傳結構,因此能產生較低的全身毒性[11]。在眾多腫瘤抑制基因中,p53是最具潛力的治療性基因之一,作為“基因組衛士”,它在受到癌基因、DNA損傷以及氧化應激等刺激下,通過誘導細胞周期抑制、衰老以及凋亡等途徑來發揮作用。而作為p53的結合蛋白,ASPP2在p53介導的凋亡基因轉錄的激活和細胞周期抑制上扮演重要角色[2],同時ASPP2也具有p53非依賴的腫瘤抑制作用[12-13],ASPP2可能成為未來腫瘤治療的靶點之一。
臨床應用腺病毒能夠高水平瞬時表達外源基因,腺病毒能夠促進分裂、不分裂細胞系的局部和系統性的基因遞送和傳導。與逆轉錄病毒不同,重組腺病毒基因組能夠插入大量的外源DNA堿基,且不整合到宿主染色體上,這也是重組腺病毒的最大安全優勢。作為基因治療載體必需符合兩個必要條件,一是進入細胞后無法復制,不會產生具有感染力的病毒。另一是能在試管內繁殖,并被組裝成具有感染力的病毒顆粒[14]。因此,批量擴增的腺病毒制劑則需要嚴格的質量控制以保證藥物安全有效。
腺病毒顆粒數的檢測多采用A260紫外光吸收法,通過病毒基因組的光吸收值來計算,該方法要求病毒濃度和純度都要足夠高,同時此種方法不能區分感染型和缺陷型病毒顆粒。滴度代表具有感染能力的病毒顆粒數,它更為直觀地反映能進入細胞表達目的蛋白的病毒顆粒,即有效劑量,是衡量腺病毒特性更為重要的指標。我們選擇SFDA和FDA推薦的TCID50方法測定病毒滴度。這一方法的原理基于最高稀釋度下293細胞中病變效應(CPE)的形成。該方法只需10 d就可以獲得結果,而且人為因素對結果的影響較小,結果的重復性更高。同時將滴度與顆粒數相比可得到腺病毒制品的比活性,FDA和SFDA推薦增加比活的概念來完善對此類產品的質控,規定重組臨床級制品的比活性必須大于3.3%。在重組腺病毒的擴增中,嚴格控制病毒種子的代數,盡量減少RCA的產生,以保證制劑的安全。
基因治療的體外藥效測定是評價其有效性的關鍵指標。一般情況下,在體外將重組病毒感染細胞并培養后,可通過Western blot定性實驗或ELISA定量實驗檢測培養上清中的目的蛋白的表達。本實驗中,將ASPP2重組腺病毒感染HepG2和Huh7細胞后,采用Western blot方法鑒定出目的基因在靶細胞中獲得有效表達。在生物學活性測定中,為驗證試驗品是否具有抗腫瘤作用,我們選擇了兩種肝癌細胞HepG2和Huh7,將ASPP2重組腺病毒同時作用這兩種細胞,觀察到其可抑制腫瘤細胞的生長,證實了其體外具有抗腫瘤活性。
本實驗根據《人基因治療和制劑質量控制技術指導原則》及《中國藥典》三部(2010版)相關要求,針對人ASPP2重組腺病毒的關鍵質量屬性建立了質控方法,初步為該制品質量標準的建立和完善,保證其安全、有效、質量可控以及后續研究奠定了基礎。
參考文獻:
[1]Kay M A, Glorioso J C, Naldini L. Viral vectors for gene therapy: the art of turning infectious agents into vehicles of therapeutics[J].NatMed,2001,7(1): 33-40.
[2]席聰,安睿,李海勛,等. rAAV-PR39-ADM防治大鼠腦缺血/再灌注損傷的研究[J].中國藥理學通報,2015,31(5):641-7.
[2]Xi C, An R, Li H X, et al. Research on prevention and treatment effect of Raav-PR39-ADM in cerebral ischemia reperfusion injury in rats[J].ChinPharmacolBull, 2015,31(5):641-7.
[3]Samuels-Lev Y, O′Connor D J, Bergamaschi D,et al. ASPP proteins specifically stimulate the apoptotic function of p53[J].MolCell, 2001, 8(4): 781-94.
[4]Gorina S, Pavletich N P. Structure of the p53 tumor suppressor bound to the ankyrin and SH3 domains of 53BP2[J].Science, 1996, 274(5289): 1001-5.
[5]Vives V, Su J, Zhong S. ASPP2 is a haploinsufficient tumor suppressor that cooperates with p53 to suppress tumor growth[J].GenesDev,2006,20(10): 1262-7.
[6]Kampa K M, Acoba J D, Chen D, et al. Apoptosis-stimulating protein of p53(ASPP2) heterozygous mice are tumor-prone and have attenuated cellular damage-response thresholds[J].ProcNatlAcadSciUSA, 2009,106(11): 4390-5.
[7]Ma L, Chen Z M, Li X Y, et al. Nucleostemin and ASPP2 expression is correlated with pituitary adenoma proliferation[J].OncolLett, 2013,6(5): 1313-8.
[8]Mak V C, Lee L, Siu M K, et al. Downregulation of ASPP2 in choriocarcinoma contributes to increased migratory potential through Src signaling pathway activation[J].Carcinogenesis, 2013,34(9): 2170-7.
[9]Schittenhelm M M, Illing B, Ahmut F, et al. Attenuated expression of apoptosis stimulating protein of p53-2(ASPP2) in human acute leukemia is associated with therapy failure[J].PLoSOne, 2013, 8(11): e80193.
[10]中國生物制品標準化委員會. 人基因治療研究和制劑質量控制技術指導原則[R]. 北京:國家食品藥品監督管理局, 2003.
[10]The State Biological Products Standardization Commission of the People’s Republic of China. Guidance for human gene therapy research and its products quality control[R]. Beijing: SFDA , 2003.
[11]Chen G X, Zhang S, He X H,et al. Clinical utility of recombinant adenoviral human p53 gene therapy: current perspectives[J].OncoTargetsTher, 2014, 7: 1901-9.
[12]Trigiante G, Lu X. ASPP[corrected] and cancer[J].NatRevCancer,2006, 6(3): 217-26.
[13]Sullivan A, Lu X, ASPP: a new family of oncogenes and tumour suppressor genes[J].BrJCancer, 2007,96(2): 196-200.
[14]林建偉,王饒高. 第二屆藥品技術審評研討會論文集[C]. 北京,2003.
[14]Lin J W, Wang R G. Proceedings of the second symposium on drug technical review[C]. Beijing, 2003.
Quality control of human ASPP2 recombinant adenovirus
WANG Shuang,XU Jian-ji,LIU Xiao-ni, CHEN De-xi
(BeijingInstituteofHepatologyandBeijingYouanHospital,CapitalMedicalUniversity,Beijing100069,China)
Abstract:AimTo analyze the key quality and establish methods for essential quality control of human recombinant ASPP2 adenovirus. MethodsThe viral structural gene of E2B and target gene of ASPP2 were identified by PCR; The number of virus particles was measured by UV-SDS methods; Infectious titer was determined by TCID50 assay; Target protein of ASPP2 was observed by Western blot assay; The biological effects of recombinant adenovirus on liver cancer cells were evaluated by MTT assay; A549 cells were used to check replication of the competent adenovirus(RCA) by the observation of the cytopathic effect.ResultsPCR analysis of E2B and ASPP2 was in consistent with theoretical values; Particle numbers of virus were 5.6×1012VP/mL, infectious titer was 2×1011IU/mL and specific activity was 3.5%; ASPP2 protein expression could be detected when cells were infected with virus for 24 h; Growth inhibition of liver cancer cells could be found by adding recombinant ASPP2 adenovirus; The level of RCA was less than 1 RCA/3.0×1010VP, in line with the standards of China Food and Drug Administration(SFDA).ConclusionThe quality control methods were established aiming at key characters of human recombinant ASPP2 adenovirus, which may provide foundations for its quality standard and future applications.
Key words:gene therapy; adenovirus; ASPP2; quality control;virus specific activity;MTT
收稿日期:2016-01-06,修回日期:2016-02-01
基金項目:國家自然科學基金資助項目(No 81272266);北京市衛生系統高層次衛生技術人才培養項目資助(No 2015-3-101);國家自然科學基金國際(地區)合作與交流項目(No 81361120401);北京市肝病研究所自主課題基金(No BJIH-01604)
作者簡介:王爽(1984-),女,博士生,助理研究員,研究方向:腫瘤生物學,E-mail:wsh1029@126.com;
doi:10.3969/j.issn.1001-1978.2016.06.027
文獻標志碼:A
文章編號:1001-1978(2016)06-0881-05
中國圖書分類號:R373.1;R394.2;R459.9;R735.7
網絡出版時間:2016-5-25 15:39網絡出版地址:http://www.cnki.net/kcms/detail/34.1086.R.20160525.1539.054.html
◇實驗方法學◇
劉曉霓(1972-),女,博士,研究員,研究方向:抗腫瘤藥理學,通訊作者,E-mail:lxnlxm@126.com;
陳德喜(1962-),男,博士,教授,研究方向:肝病基礎和臨床,通訊作者,E-mail:dexi09@yahoo.com

