Ni基催化劑管式固定床甲烷重整反應器中積炭效應的數值模擬
曹 軍,張 莉,徐 宏,邢耀華
(華東理工大學 機械與動力工程學院,上海 200237)
?
Ni基催化劑管式固定床甲烷重整反應器中積炭效應的數值模擬
曹軍,張莉,徐宏,邢耀華
(華東理工大學 機械與動力工程學院,上海 200237)
在綜合考慮積炭效應對催化劑孔隙率以及催化劑活性影響的基礎上,通過建立包含動量、能量、質量傳遞以及化學反應動力學方程的多物理場耦合數值模型,從熱質傳遞的角度,計算了Ni基催化劑管式固定床甲烷重整反應器中的積炭效應,闡明了包含多孔介質催化劑段的反應通道中的速度、溫度及壓力場分布,并指出了在通道中隨氣體流動擴散的可移動炭以及催化劑表面沉積炭濃度分布規律,分析了積炭對催化劑孔隙率、活性以及反應通道壓降的影響,并進一步討論了甲烷濃度以及溫度對積炭產生的影響,最后提出了消減積炭的方法。
管式固定床反應器;積炭效應;孔隙率;催化劑活性;數值模擬
目前,天然氣制液體燃料(Gas to liquid,GTL)技術受到人們的廣泛關注。在GTL工藝中,首先通過甲烷水蒸氣重整[1]、甲烷部分氧化重整[2]、甲烷二氧化碳重整[3]、甲烷自熱重整[4]、甲烷三重整[5]等天然氣重整工藝,實現天然氣向合成氣的轉化,再經由進一步的費-托合成工藝[6-7]轉化為液體燃料。GTL工藝在降低天然氣的輸運和存儲成本的同時,在一定程度上實現了天然氣對石油的替代,成為天然氣利用的一種重要方式[8-10]。
在天然氣的重整工藝中,Ni基催化劑由于其良好的活性和較低的價格,被普遍認為最具大規模工業化應用前景,引起了研究者的廣泛關注。但在重整反應的高溫下,由于甲烷裂解等原因,很容易產生積炭,附著在Ni基催化劑表面,覆蓋活性點位,阻塞載體空隙,從而極大降低了催化活性,并影響反應速率[11-12]。

現有關于積炭效應的研究主要集中在通過調節催化劑組分、孔結構、載體表面酸堿度、晶粒尺寸等,以及改變催化劑前處理方法來抑制積炭的產生,對反應過程中積炭的分布規律及其產生和消減機制的討論較少,缺乏系統描述積炭效應的理論分析模型。
筆者在綜合考慮積炭對催化劑孔隙率以及催化劑活性影響的基礎上,建立和求解包含有動量、能量、質量傳遞以及積炭反應的多物理場耦合數值模型,分析Ni基催化劑管式固定床甲烷重整反應器中的積炭效應,明確了積炭在反應物流動方向上的分布規律,闡明了積炭對催化劑活性及催化劑多孔結構孔隙率的影響,考察了甲烷入口濃度及反應溫度對積炭的影響,提出了除改善催化劑化學組分構成之外的抑制積炭的措施。
1 Ni基催化劑管式固定床甲烷重整反應器中積炭效應數學模型的建立與求解
1.1數學模型
為了研究管式固定床天然氣重整反應器中由于CH4裂解產生的積炭效應,建立如圖1所示的二維軸對稱數學模型。假設管式反應器長度為Lb、半徑為Rb,中間部分長度為Lc填充有球形顆粒狀Ni/Al2O3催化劑,催化劑顆粒直徑為dp。原料氣CH4以一定的溫度和壓力從反應通道入口流入,經過自由流動段之后,流入催化劑段發生反應,然后再經由自由流動段流出反應通道。CH4裂解所需要的熱量由外部高溫煙氣提供。

圖1 計算中所用的二維軸對稱管式反應器模型
1.2積炭反應的動力學方程
天然氣重整反應中的積炭主要來自CH4的裂解以及CO歧化反應,尤其是CH4的裂解。CH4裂解反應如式(1)所示,式(2)為其反應動力學方程[20]。
CH4?C+2H2;ΔH=74.9kJ/mol
(1)
(2)
式(2)中k、kp和kH分別可由式(3)~(5)計算。
(3)
(4)
(5)
1.3控制方程
基于上述產生積炭的理論,通過求解包含有動量、能量和質量傳遞,以及積炭產生化學反應動力學方程的多物理場耦合數值模型,即可分析管式固定床反應器中由于CH4裂解產生的積炭分布。在進行數學模型的構建時,需要有以下4點假設。
(1)反應物及產物氣體在相應的反應溫度和壓力下均滿足理想氣體狀態方程;
(2)反應物及產物氣體均為可壓縮,并處于層流狀態;
(3)催化劑顆粒為直徑一致的圓球,整個催化劑床層可視為均勻的多孔介質結構,孔隙率為ε,滲透率為κ;
(4)固體催化劑床層與周圍氣體處于熱平衡狀態。
基于上述假設,數學模型中用到的主要控制方程包括管式反應器中的自由流動區域的控制方程式(6)~(9)、管式反應器催化劑段(發生積炭反應的多孔介質區域)的控制方程式(10)~(13)。
(6)
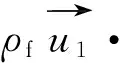
(7)
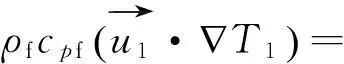
(8)

(9)
(10)

(11)
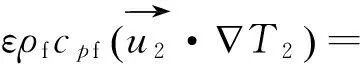
(12)

(13)
混合氣體的密度ρf、比熱容cpf和導熱系數λf分別用式(14)~(16)計算。
(14)
(15)
(16)
多孔結構催化劑床層的等效導熱系數λeff由混合氣體及固體催化劑的導熱系數λf及λs通過孔隙率加權求和后得出,如式(17)所示。
λeff=ελf+(1-ε)λs
(17)
對于CH4裂解積炭,在考慮了催化劑活性a對其影響之后,不同組分的反應速率可分別表示為式(18)~(20),甲烷裂解反應的吸熱量qt可表示為式(21)。
rCH4=-rm·a
(18)
rC=rm·a
(19)
rH2=2rm·a
(20)
qt=ΔH·rm·a
(21)
1.4積炭對催化劑活性及孔隙率影響的表征
積炭產生之后附著在催化劑表面,將會影響催化劑活性,積炭濃度CC與催化劑活性a之間的關系可用式(22)表示[20],其中的ka可由式(23)計算。
(22)
(23)
附著在催化劑表面的積炭濃度對多孔介質催化劑孔隙率ε和滲透率κ的影響可分別由式(24)、(25)表示[20]。
(24)
(25)
通過以上方程即可實現積炭效應對催化劑活性,孔隙率及滲透率影響的耦合計算。
1.5邊界條件
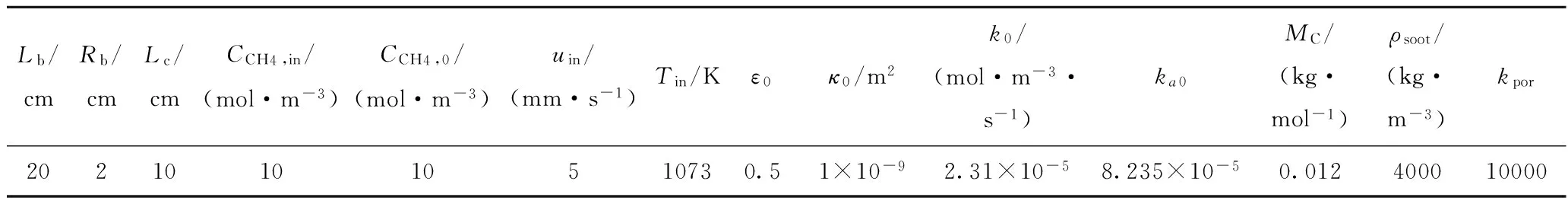
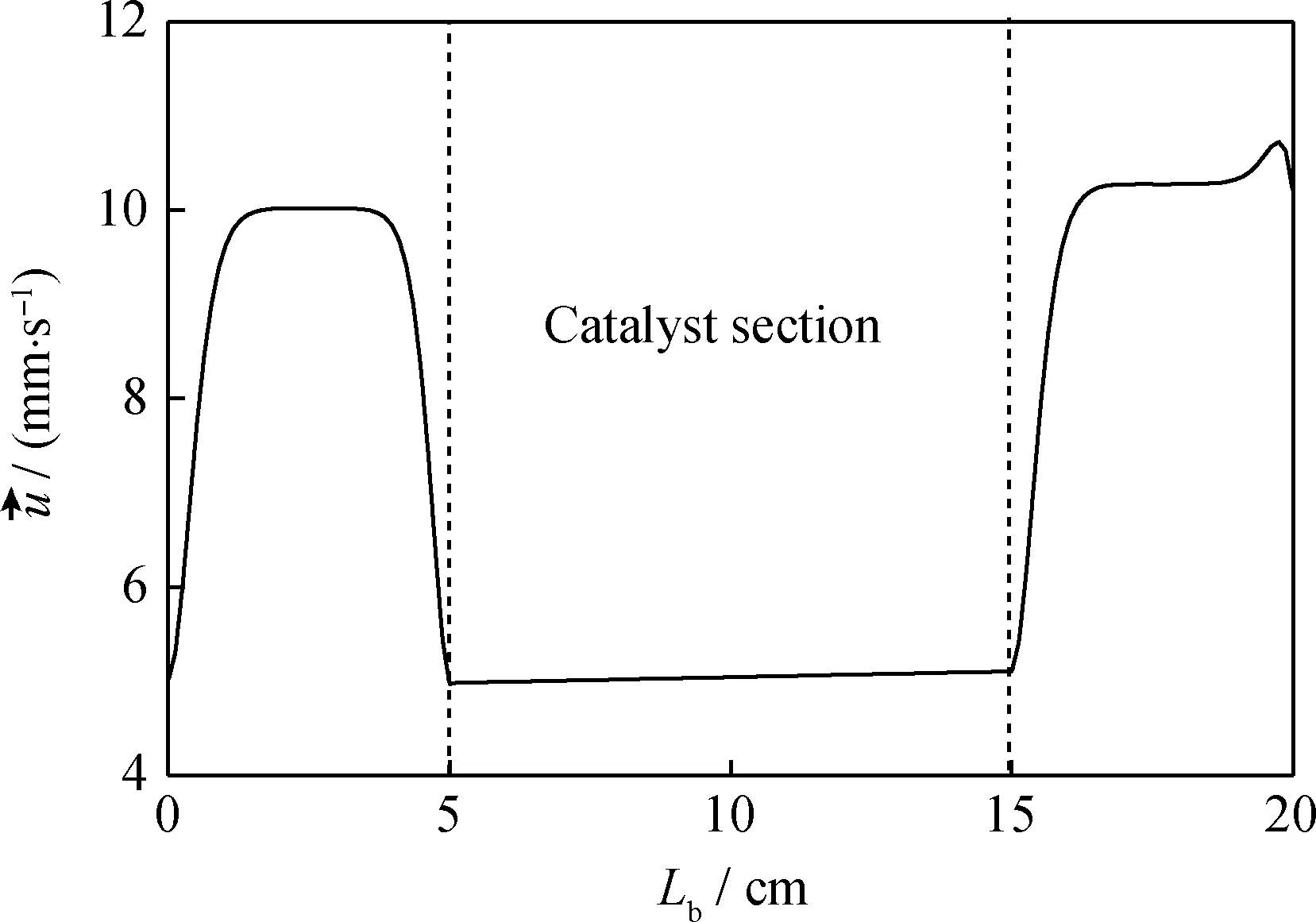
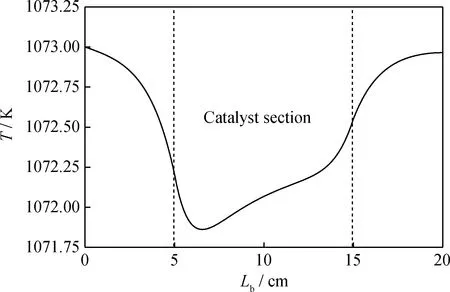
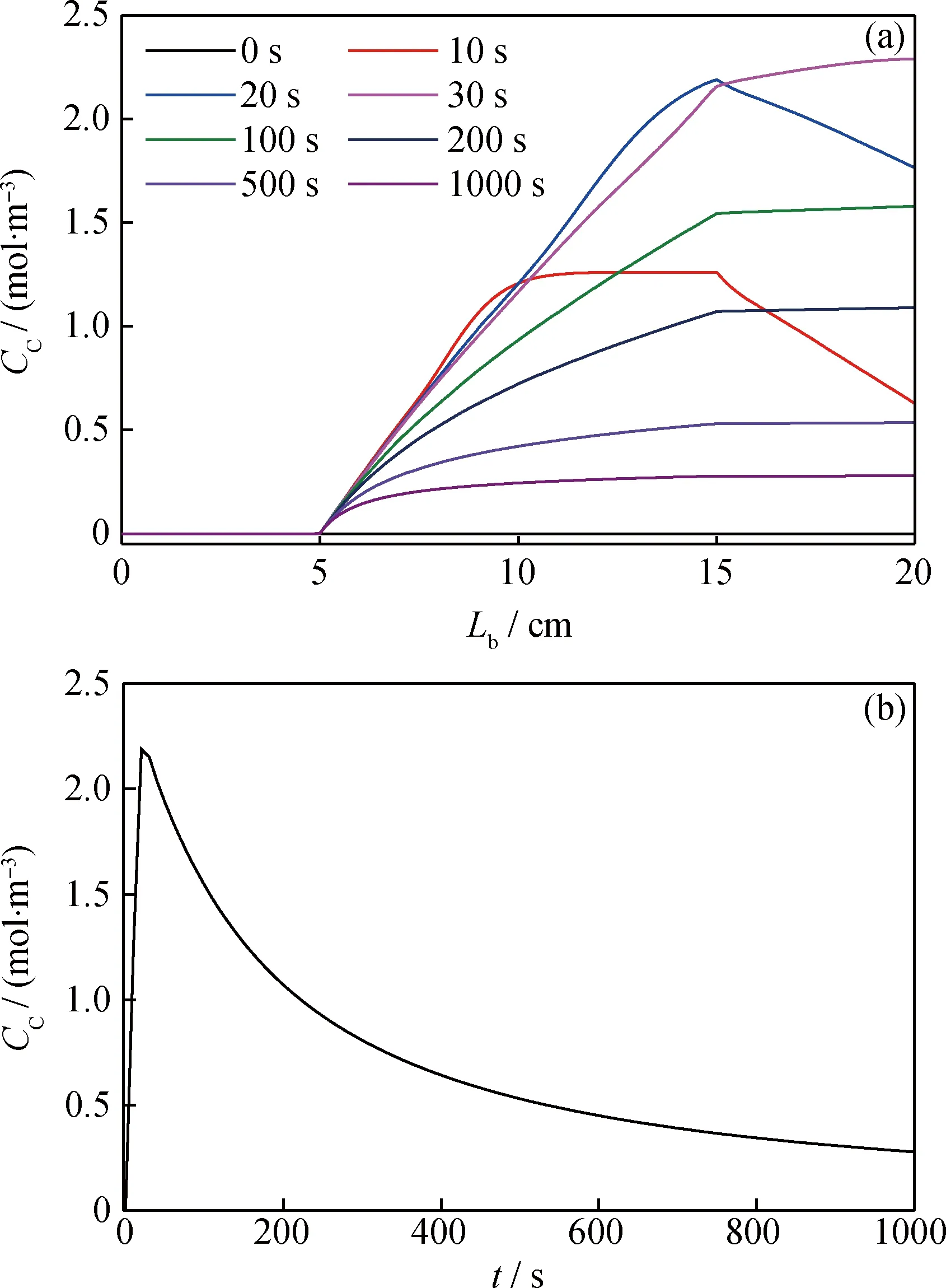
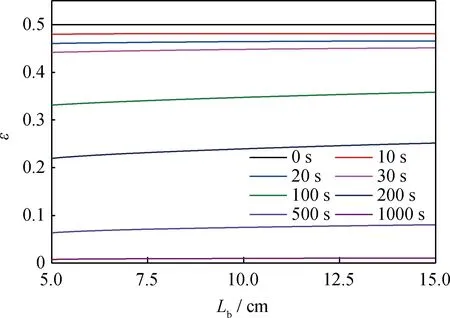
對于發生積炭反應的管式固定床反應器模型,其入口(z=0,0 u=uin,v=0,T=Tin,CCH4=CCH4,in, CC=0,CH2=0 (26) (27) (28) (29) 1.6計算參數及模型求解 在模型求解過程中,如無特別說明,用到的反應器尺寸及其他主要計算參數列于表1。利用有限元方法建立數學模型并對其開展計算分析,所有計算結果均經過了網格無關性驗證。 2.1管式固定床天然氣重整反應器反應通道中的流動及傳熱特性 積炭產生之后覆蓋在催化劑表面,造成催化劑多孔結構孔隙率和滲透率的改變,進而改變管式固定床天然氣重整反應器通道中的速度和壓力分布。圖2為反應進行200 s時反應通道中的速度場分布。可以看到,反應氣體在進入催化劑段后,速度明顯下降,但是當氣體流出催化劑段之后,速度明顯增大,且反應通道出口區域流速高于入口區域。這是由于在氣體的流動過程中,CH4不斷裂解產生H2,造成混合氣體體積膨脹,從而使得氣流流動速度增加。 表1 管式固定床天然氣重整反應器積炭反應數學模型中用到的計算參數[20] 圖2 管式固定床反應器中心軸線上的氣體速度分布 圖3所示為在保持入口流速恒定為5 mm/s時,不同時刻管式反應器通道中的壓力分布以及反應通道中壓降隨時間的變化。從圖3(a)可以看到,在反應通道自由流動的入口和出口區域的壓降幾乎可以忽略,整個通道中的主要壓降集中在催化劑段,且壓力呈線性下降的趨勢;隨著時間的延長,催化劑層中的積炭逐漸增多,催化劑段的壓降也不斷增大。從圖3(b)可見,隨著時間的延長,由于積炭不斷產生,維持相同流速所需的壓力則急劇上升,反應進行600 s之后,已經達到近1000 kPa。因此,積炭的生成會明顯地提高驅動氣體流動的泵功,造成能源浪費。在反應速率滿足要求的前提下,增大催化劑填充的孔隙率,可在一定程度上延長其使用壽命,并降低維持流速所需的功耗。 圖3 管式固定床天然氣重整反應器反應通道中的壓力分布及積炭效應對壓降的影響 圖4所示為反應進行200 s之后管式固定床天然氣重整反應器反應通道中心軸線處的溫度分布。可以看出,由于CH4裂解反應為吸熱反應,加之催化劑段入口區域反應劇烈,吸熱現象更為顯著,因此當氣體流入催化劑段后溫度明顯下降;隨著反應進行,由于積炭及反應物濃度下降,在流動方向上反應速率降低,吸熱減弱,當外界保持一定的熱流量時,催化劑段溫度相比于入口段有一定的上升。在催化劑段前方入口區域則由于氣體本身的導熱,造成反應氣體溫度從進入管式反應器之后就有一定量的下降。 圖4 管式固定床天然氣重整反應器反應通道中心軸線上的溫度分布 2.2管式固定床天然氣重整反應器反應通道中的積炭分布規律 CH4裂解產生的炭可以分為兩個部分。一部分由于氣流的吹掃及自身的擴散作用,會隨著氣體的流動被帶出反應通道;另一部分則沉積在催化劑表面,成為影響反應速率和催化劑活性的重要因素,其分布狀態對于催化劑結構的設計具有重要意義。 圖5(a)為CH4裂解反應從開始到1000 s的過程中,反應通道中隨著氣流帶出通道的炭顆粒的濃度分布,圖5(b)為不同時刻通道出口處可移動炭顆粒濃度分布。 從圖5(a)可以看到,隨著反應的不斷進行,CH4裂解產生的部分積炭由于氣流的吹掃作用,從反應通道的上游被帶到下游,可移動炭顆粒濃度沿著氣體流動方向不斷增加,在反應管的出口處達到最高;在反應進行30 s之后,由于積炭造成催化劑失活,裂解反應速率下降,產生炭的速率減慢,在通道中的可移動炭顆粒濃度也逐漸降低。從圖5(b)可以看到,由于初始階段反應比較劇烈,催化劑活性高,生成的炭顆粒濃度也很高,但是在一段時間之后,反應速率逐漸下降,炭顆粒濃度也不斷下降。 對于影響催化劑性能的沉積在催化劑表面的積炭濃度分布,可以通過催化劑段孔隙率的變化來表征。圖6為不同時刻催化劑段沿著氣體流動方向的孔隙率分布。可以看到,隨著反應時間的延長,積炭不斷增加,整個催化劑段的孔隙率均下降。在同一時刻,催化劑孔隙率則沿著氣體流動方向逐漸增加,催化劑入口段孔隙率最小。這是由于入口段CH4裂解積炭反應劇烈,產生的積炭更多,雖然有一部分隨著氣流被帶出通道,但還有很多附著在催化劑表面形成積炭。積炭更容易在入口段形成的規律,為積炭的消除提供了一個基本思路。 圖5 反應通道中可移動炭顆粒濃度(CC)沿通道分布和通道出口處CC隨時間的變化 圖6 管式固定床天然氣重整反應器催化劑段沿氣流方向的孔隙率變化 管式固定床天然氣重整反應器催化劑段孔隙率隨反應時間的變化如圖7(a)所示。從圖7(a)可見,由于積炭的逐漸累積,催化劑孔隙率呈指數規律不斷下降,到1000 s時已經接近0,即催化劑空隙已經完全被堵死,反應無法繼續進行。除了對孔隙率造成影響之外,積炭還會極大的影響催化劑的反應活性,圖7(b)為催化劑段出口區域的催化劑活性隨時間的變化。從圖7(b)可以看到,由于積炭的累積,在反應進行1000 s之后,該區域催化劑活性接近于零,催化劑已經失活。由此可見,消除催化劑積炭是重整過程中需要解決的一個重要問題。 圖7 CH4重整反應積炭對催化劑孔隙率(ε)及催化活性(α)的影響 2.3產生積炭的影響因素 2.3.1CH4濃度的影響 反應器CH4入口濃度是影響積炭產生的一個重要因素。圖8為在CH4反應進行100 s之后,CH4入口摩爾濃度在10~30 mol/m3變化時,催化劑段出口處孔隙率的變化。可以看出,由于反應物濃度增加造成產生的積炭量增大,催化劑段出口處孔隙率隨著CH4入口濃度的增大不斷下降。當CH4摩爾濃度從10 mol/m3增大到30 mol/m3時,該處孔隙率從0.36降低為0.20。因此,在Ni基催化劑CH4重整反應中,雖然提高CH4入口濃度會有利于重整反應向正向進行,但同時會發生嚴重的積炭效應,CH4入口濃度應該選擇在一個合理的范圍。 圖8 管式固定床天然氣重整反應器CH4入口濃度(CCH4,in)對催化劑段出口處孔隙率(ε)的影響 2.3.2溫度的影響 對CH4入口溫度及環境溫度分別均為800℃、900℃及1000℃時,反應進行到100 s時刻,反應通道中催化劑段的孔隙率示于圖9。可以看出,由于CH4裂解為吸熱反應,提高溫度將會增大CH4裂解反應的速率,使反應向正向進行,從而產生更多的積炭,造成同一時刻催化劑段的孔隙率更低。因此,適當降低反應溫度是減少積炭產生的一種方法。然而,由于CH4重整制合成氣反應也是吸熱反應,以CH4-CO2重整為例,如式(30)所示,降低溫度不利于合成氣的轉化。因此,在實際中應該選擇折中的反應溫度,在保證反應轉化率的同時,適度降低溫度來消減積炭的產生,從而提高催化劑的使用壽命。 圖9 不同CH4入口溫度時管式固定床天然氣重整反應器催化劑段的孔隙率(ε) CH4+CO2?2CO+2H2;ΔH=247.3 kJ/mol (30) (1)采用管式固定床反應器進行天然氣重整反應時,反應氣體在進入多孔介質催化劑段后,速度明顯下降,但是流出催化劑段之后,速度又明顯增大,且反應通道出口區域流速高于入口區域。這是由于在反應氣流動過程中,CH4不斷裂解產生H2,造成混合氣體體積膨脹,從而使得氣流流動速度增加。由于CH4裂解反應為吸熱反應,加之催化劑段入口區域反應劇烈,吸熱現象更為顯著,因此當氣體流入催化劑段后溫度下降明顯。 (2)由于氣流吹掃作用,CH4裂解產生的可移動炭顆粒濃度沿氣流方向不斷增加;由于催化劑入口段CH4裂解反應劇烈,催化劑表面的積炭濃度最大,其多孔結構孔隙率及活性的下降幅度也最多;沿著氣流方向,積炭的影響逐漸減弱。 (3)隨著積炭的增多,保持恒定流速所需的入口壓力急劇增大,如果不采取有效措施,甚至會造成通道阻塞,使得反應停滯。 (4)催化劑段入口處孔隙率隨著CH4濃度的增大而下降,高CH4濃度有利于重整反應向正向進行,但同時會發生嚴重的積炭效應。 (5)高溫有利于CH4重整反應正向進行(吸熱反應),但同時也促進積炭的生成,實際操作中應該選擇適中合理的溫度。 (6)改變催化劑結構進而改變其中的流場分布,讓更多的炭顆粒通過氣流吹掃及擴散作用帶出反應通道,以及合理的溫度設置,是在不改變催化劑組分情況下的兩種消減積炭的方法。 符號說明: a——催化劑活性,mol/m3; Ci——組分濃度,mol/m3; ΔH——反應焓值,J/mol; k——反應速率系數,mol/(m3·s); k0——化學反應速率,mol/(m3·s); kH——無量綱反應系數; kp——壓力系數,Pa; Lb——反應通道長度,cm; Lc——催化劑段填充長度,cm; MC——積炭的摩爾質量,kg/mol; p——壓力,Pa; pCH4——CH4分壓,Pa; pH2——H2分壓,Pa; qt——甲烷裂解反應的吸熱量,kJ; rm——甲烷裂解反應速率,mol/(m3·s); ri——組分反應速率,mol/(m3·s); Rb——反應管半徑,cm; Rg——氣體常數,J/(mol· K); T——反應溫度,K; Tf——外界環境溫度,K; ρ——密度,kg/m3; ρf——混合氣體密度,kg/m3; ρsoot——積炭密度,kg/m3; ε——催化劑孔隙率; κ——催化劑滲透率,m-2; ε0——催化劑初始孔隙率; κ0——催化劑初始滲透率,m-2; λf——混合氣體的導熱系數,W/(m· K); λs——固體催化劑的導熱系數,W/(m· K); λeff——催化劑床層等效導熱系數,W/(m· K); 下角標 in——進口; 0——初始; 1——自由流動區域; 2——催化劑多孔介質區域。 [1]SEUNG W J,WON J Y,MIN W J,et al.Optimization of a counter-flow microchannel reactor using hydrogen assisted catalytic combustion for steam reforming of methane[J].International Journal of Hydrogen Energy,2014,39(12):6470-6478 [2]SHASHI K,SURENDRA K,JITENDRA K P.Hydrogen production by partial oxidation of methane:Modeling and simulation[J].International Journal of Hydrogen Energy,2009,34(16):6655-6668. [3]GODINI H R,XIAO S,KIM M,et al.Dual-membrane reactor for methane oxidative coupling and dry methane reforming:Reactor integration and process intensification[J].Chemical Engineering and Processing:Process Intensification,2013,74:153-164. [4]AKBARI M H,SHARAFIAN A H,ANDISHEH T M.A microreactor modeling analysis and optimization for methane autothermal reforming in fuel cell applications[J].Chemical Engineering Journal,2011,166(3):1116-1125. [5]WALKER D M,PETTIT S L,WOLAN J T,et al.Synthesis gas production to desired hydrogen to carbon monoxide ratios by tri-reforming of methane using Ni-MgO-(Ce,Zr)O2catalysts[J].Applied Catalysis A:General,2012,445-446:61-68. [6]RAHIMPOUR M R,KHADEMI M H,BAHMANPOUR A M.A comparison of conventional and optimized thermally coupled reactors for Fischer-Tropsch synthesis in GTL technology[J].Chemical Engineering Science,2010,65(23):6206-6214. [7]BHATELIA T,LI C,SUN Y,et al.Chain length dependent olefin re-adsorption model for Fischer-Tropsch synthesis over Co-Al2O3catalyst[J].Fuel Processing Technology,2014,125:277-289. [8]WOOD D A,NWAOHA C,TOWER B F.Gas to liquids(GTL):A review of an industry offering several routes for monetizing natural gas[J].Journal of Natural Gas Science and Engineering,2012,9:196-208. [9]ARUTYUNOV V S,AVCHENKOV I S,SEDOV I V,et al.New concept for small-scale GTL[J].Chemical Engineering Journal,2015,282:206-212. [10]DAVIS B H.Fischer-Tropsch synthesis:Overview of reactors development and future potentials[J].Topics in Catalysis,2005,32(3):143-168. [11]WU W,LIOU Y C,YANG H T.Design and evaluation of a heat-integrated hydrogen production system by reforming methane and carbon-dioxide[J].Journal of the Taiwan Institute of Chemical Engineers,2013,44(6):929-935. [12]RAHNAMA H,FARNIAEI M,ABBASI M,et al.Modeling of synthesis gas and hydrogen production in a thermally coupling of steam and tri-reforming of methane with membranes[J].Journal of Natural Gas Science and Engineering,2014,20(4):1779-1792. [13]KOO K Y,ROH H S,JUNG U H,et al.Combined H2O and CO2reforming of CH4over nano-sized Ni/MgO-Al2O3catalysts for synthesis gas production for gas to liquid(GTL):Effect of Mg/Al mixed ratio on coke formation[J].Catalysis Today,2009,146(1-2):166-171. [14]MESHKANI F,REZAEI M,ANDACHE M.Investigation of the catalytic performance of Ni/MgO catalysts in partial oxidation,dry reforming and combined reforming of methane[J].Journal of Industrial and Engineering Chemistry,2014,20(4):1251-1260. [15]ROH H S,KOO K Y,YOON W L.Combined reforming of methane over co-precipitated Ni-CeO2,Ni-ZrO2and Ni-Ce0.8Zr0.2O2catalyst to produce synthesis gas for gas to liquid(GTL)process[J].Catalyst Today,2009,146(1-2):71-75. [16]KOO K Y,LEE S H,JUNG U H,et al.Syngas production via combined steam and carbon dioxide reforming of methane over Ni-Ce/MgAl2O4catalysts with enhanced coke resistance[J].Fuel Processing Technology,2014,119:151-157. [17]SON I H,LEE S J,SOON A,et al.Steam treatment on Ni/γ-Al2O3for enhanced carbon resistance in combined steam and carbon dioxide reforming of methane[J].Applied Catalyst B:Environmental,2013,134-135:103-109. [18]KANG K M,KIM H W,SHIM I W,et al.Catalytic test of supported Ni catalysts with core/shell structure for dry reforming of methane[J].Fuel Processing Technology,2011,92(6):1236-1243. [19]BAO Z H,LU Y W,HAN J,et al.Highly active stable Ni-based bimodal pore catalyst for dry reforming of methane[J].Applied Catalyst A:General,2015,491:116-126. [20]NURUNNABI M,KADO S,SUZUKI K,et al.Synergistic effect of Pd and Ni on resistance to carbon deposition over NiO-MgO solid solution supported Pd catalysts in oxidative steam reforming of methane under pressurized conditions[J].Catalysis Communications,2006,7(7):488-493. Numerical Simulation of the Carbon Deposition Effect inTubular Fixed Bed Methane Reforming Reactor Over Ni-Catalyst CAO Jun,ZHANG Li,XU Hong,XING Yaohua (School of Mechanical and Power Engineering,East China University of Science and Technology,Shanghai 200237,China) Based on the effects of carbon deposition on catalyst porosity and activity,a multiphysics-coupled numerical model containing the equations of momentum,energy and mass transfer,as well as the chemical reaction kinetics was developed,to simulate the carbon deposition effect in tubular fixed bed methane reforming reactor over Ni-catalyst in the viewpoint of heat and mass transfer.The velocity and temperature field,as well as the pressure distribution in the reaction channel with porous media catalyst section were explained in detail.The distribution rules of movable coke,which is caused by the convection and diffusion,and the deposited coke on catalyst surface in the reaction channel were both pointed out.Meanwhile,the effects of carbon deposition on the porosity and catalyst activity of porous catalyst,as well as the pressure drop in reaction channel,were all discussed.Finally,the effects of methane inlet concentration and temperature on the carbon deposition effect were further analyzed,and the methods for coke elimination were proposed.The developed analytical model described the generation and distribution rules of carbon deposition effect systematically,which is helpful for the further research on the carbon elimination in CH4reforming reaction over Ni-catalyst. tubular fixed bed reactor; carbon deposition effect; porosity; catalyst activity; numerical simulation 2015-06-16 中央高校基本科研業務費探索基金項目(WG1414044)資助 曹軍,男,助理研究員,博士,從事過程強化技術及高效過程裝備研發;Tel:021-64253810,E-mail:caojun@ecust.edu.cn 徐宏,男,教授,博士,從事石油化工中強化傳熱傳質方面的研究;Tel:021-64253810;E-mail:hxu@ecust.edu.cn 1001-8719(2016)05-0951-08 TE09 Adoi:10.3969/j.issn.1001-8719.2016.05.012
2 結果與討論

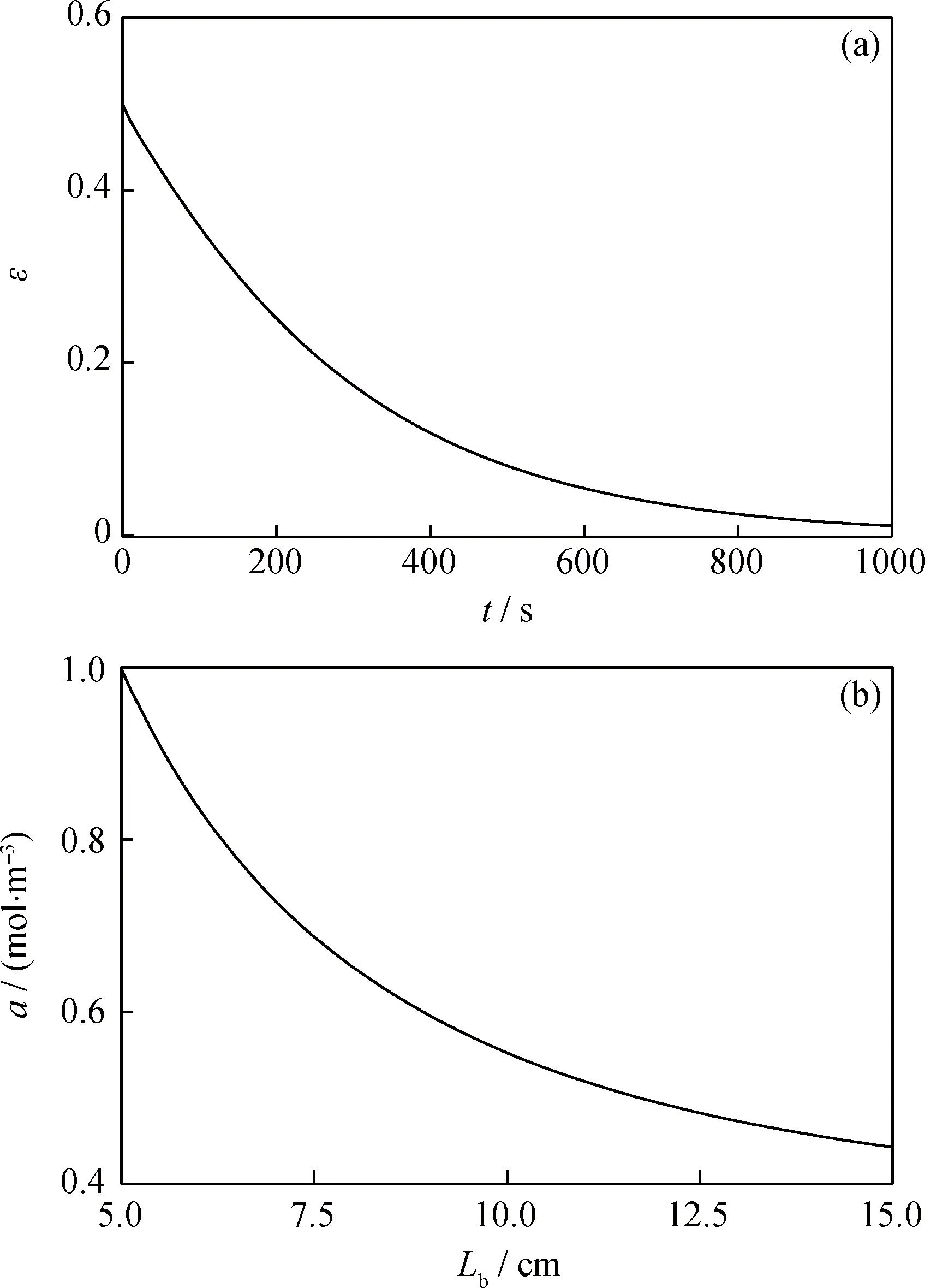
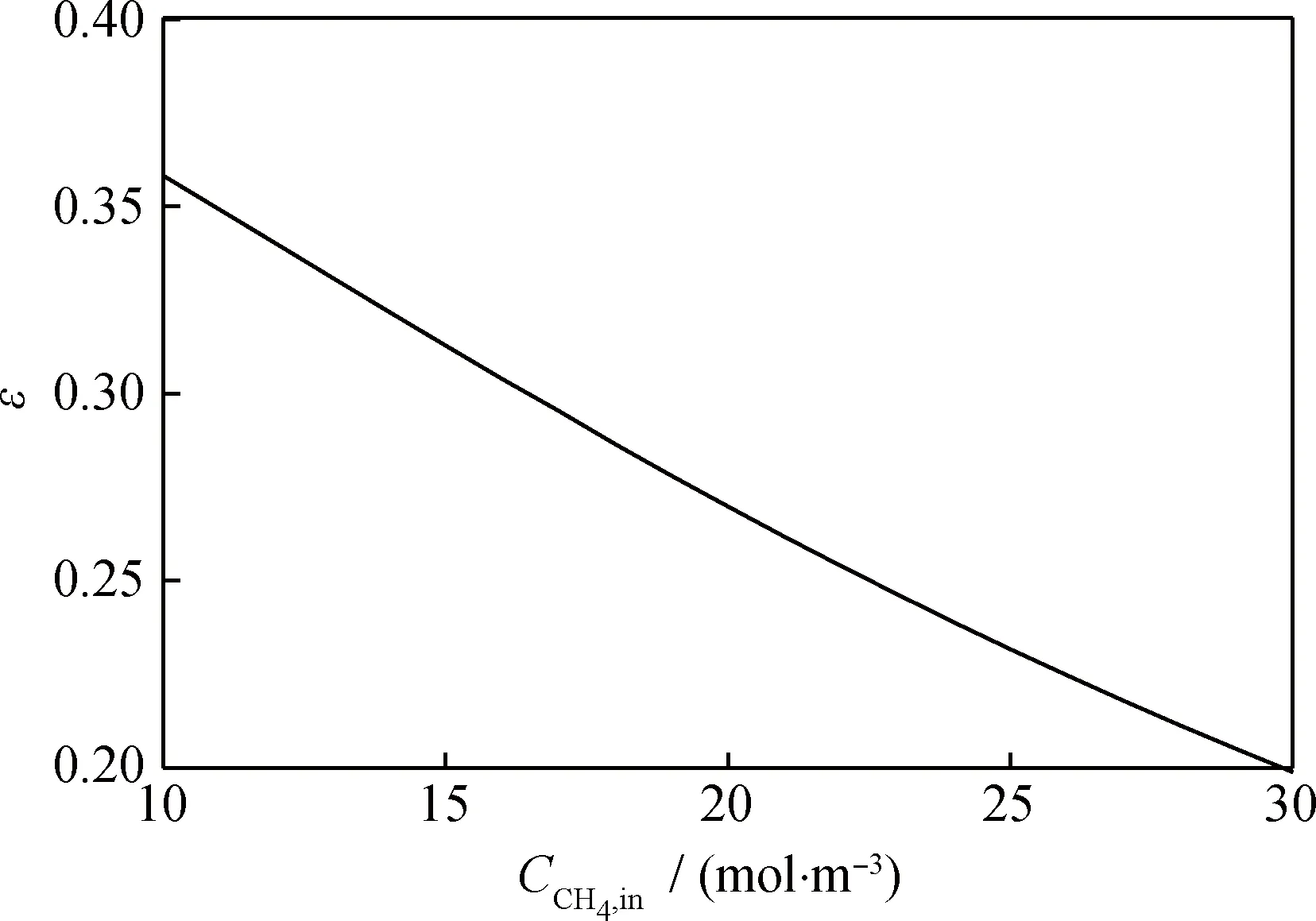
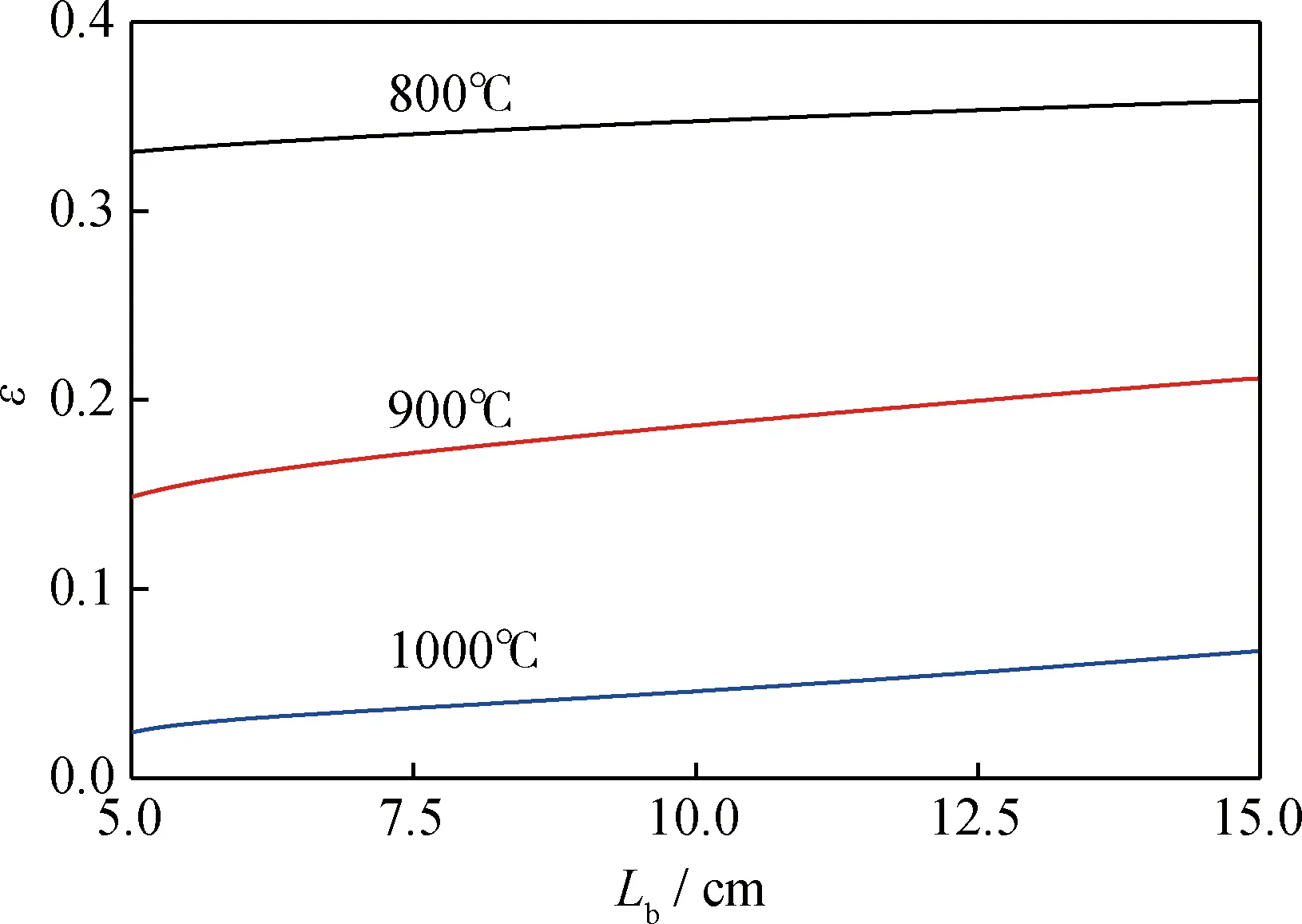
3 結 論


