芍藥苷對HepG2肝癌細胞凋亡的誘導作用
張亞武,權柯
1蘭州大學第二醫院膽胰外科,甘肅蘭州730000;2甘肅中醫藥大學
芍藥苷對HepG2肝癌細胞凋亡的誘導作用
張亞武1,權柯2
1蘭州大學第二醫院膽胰外科,甘肅蘭州730000;2甘肅中醫藥大學
目的:探討芍藥苷(Paeoni florin)對H epG 2肝癌細胞凋亡的誘導作用,并考察其作用機制。方法:用不同濃度芍藥苷(0.5,2 m g/m L)對HepG 2肝癌細胞進行培養,采用MTT法檢測細胞活力,酶標法檢測Caspase 3活性,western blot法檢測N F-κB信號通路相關蛋白表達。結果:隨著給藥濃度的增加,芍藥苷能逐漸降低H epG 2肝癌細胞活力,在48小時抑制率最高;并能提高Caspase 3活性,抑制細胞核內N F-κB p65磷酸化,IκBα磷酸化,從而促進細胞凋亡。結論:芍藥苷可能通過N F-κB信號通路誘導H epG 2肝癌細胞凋亡,達到抗腫瘤效果。
HepG 2肝癌細胞;凋亡;NF-κB信號通路;磷酸化;芍藥苷
肝癌是常見的惡性腫瘤之一,目前其主要治療手段為手術,但術后易復發,轉移率較高。因此,尋求有效治療肝癌,降低復發率的藥物成為研究熱點。
芍藥苷(Paeonif1orin,PF)是從毛茛科植物芍藥(Paeonia Lactiflora Pa11)中提取的有效單體成份,能抗各種腫瘤活性[1-4]。已有報道芍藥苷可上調Bax,p53表達,下調Bc1-2表達,促進HepG2肝癌細胞凋亡[1],但其具體機制尚不可知。并且芍藥苷可通過抑制NF-κB信號通路,抑制胃癌細胞增殖[2-3],本研究在此基礎上探討芍藥苷是否通過抑制NF-κB信號通路來誘導HepG2肝癌細胞凋亡。
1 材料與方法
1.1細胞系與藥物HepG2肝癌細胞購自美國標準生物品收藏中心(ATCC),細胞培養在含10%胎牛血清的DMEM培養基中。芍藥苷購自中國藥品生物制品檢定所。
1.2試劑與儀器四唑鹽試劑(MTT)(sigma公司);BCA法蛋白定量試劑盒(碧云天生物技術研究所);ECL超敏發光液(碧云天生物技術研究所);小鼠p65抗體(碧云天生物技術研究所);β-actin(碧云天生物技術研究所);兔IκBα抗體(Epitmics公司);兔抗pp65抗體(Epitmics公司);Caspase 3分光光度法檢測試劑盒(南京凱基生物技術有限公司);胎牛血清(Gbico公司);DMEM培養基(Gbico公司);CO2培養箱(Thermo Scientific公司);超凈工作臺(Thermo Scientific公司);Tecan Infinite F200/M200型多功能酶標儀(瑞士TECAN集團公司);ChemiDocTM XRS凝膠成像系統(Bio-Rad公司)。
1.3方法
1.3.1MTT實驗將80%左右融合的HepG2肝癌細胞,消化,細胞濃度調整為4×103個/mL,接種,37℃5% CO2培養箱中培養24小時。加入含PF,終濃度為0.5、1、2mg/mL的DMEM培養基中,繼續培養24、48、72小時,加MTT(5mg/mL)20μL,培養4小時后棄上清,加DMSO 150 μL,10分鐘左右后570 nm處測定OD值。計算藥物對細胞生長的抑制率。
1.3.2Caspase 3酶活性檢測將80%左右融合的HepG2肝癌細胞,消化,細胞濃度調整為4×103個/mL,接種,37℃5%CO2培養箱中培養48小時。加入含PF,終濃度為0.5、1、2 mg/mL的DMEM培養基中,按照Caspase 3酶活性檢測試劑盒說明書進行操作,收集細胞,裂解,加底物,顯色,于405 nm處測定吸光度。
1.3.3w est ern bl ot收集細胞,加入RIPA裂解液,收獲蛋白。根據BCA試劑盒對蛋白濃度進行測定。跑SDS凝膠電泳,后濕法磚膜。孵一抗過夜,二抗1小時后,在膜上滴加ECL曝光液,在凝膠成像系統中曝光。用“Quantity one”軟件對各抗體條帶灰度值進行統計。
1.4統計學方法數據采用SPSS 17.0軟件統計分析。計量資料以(±s)表示,采用t檢驗,P<0.05表示差異有統計學意義。
2 結果
2.1芍藥苷對H epG 2肝癌細胞增殖抑制作用隨著給藥濃度的增加,芍藥苷對HepG2肝癌細胞抑制作用逐漸增強,在2 mg/mL時抑制率最大;隨著24、48、72小時給藥時間的增加,芍藥苷對HepG2肝癌細胞抑制作用也逐漸增強,其中48、72小時作用強度一致,所以在后續實驗中選取48小時作為給藥濃度,見表1。
表1 芍藥苷對H epG 2肝癌細胞增殖抑制作用(±s)
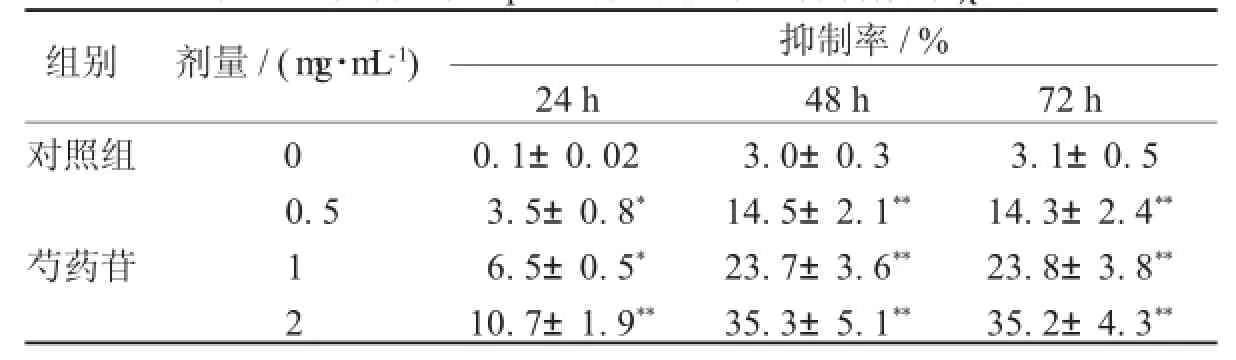
表1 芍藥苷對H epG 2肝癌細胞增殖抑制作用(±s)
注:與前一劑量組比較,*表示P<0.05,**表示P<0.01。
組別劑量/(m g·m L-1)抑制率/% 24 h48 h72 h對照組00.1±0.023.0±0.33.1±0.5 0.53.5±0.8*14.5±2.1**14.3±2.4**芍藥苷16.5±0.5*23.7±3.6**23.8±3.8**2 10.7±1.9**35.3±5.1**35.2±4.3**
2.2芍藥苷對HepG 2肝癌細胞Caspase 3活性的影響芍藥苷(0.5、1、2 mg/mL)能提高HepG2肝癌細胞Caspase 3活性,并呈劑量依賴性,差異具有統計學意義(P<0.01),見圖1。
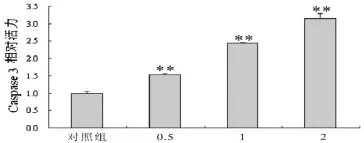
圖1 芍藥苷對HepG 2肝癌細胞Caspase 3活性的影響
2.3芍藥苷對HepG 2肝癌細胞NF-κB通路的影響芍藥苷能抑制HepG2肝癌細胞細胞核NF-κB p65蛋白磷酸化,并呈劑量依賴性,差異具有統計學意義(P<0.05),而對細胞核內p65表達無任何影響,差異無統計學意義(P>0.05)。因此繼續探討NF-κB p65上游蛋白的影響,結果發現芍藥苷能抑制HepG2肝癌細胞IκBα蛋白磷酸化,并呈劑量依賴性,差異具有統計學意義(P<0.05),但對IκBα自身表達無任何影響,見圖2。
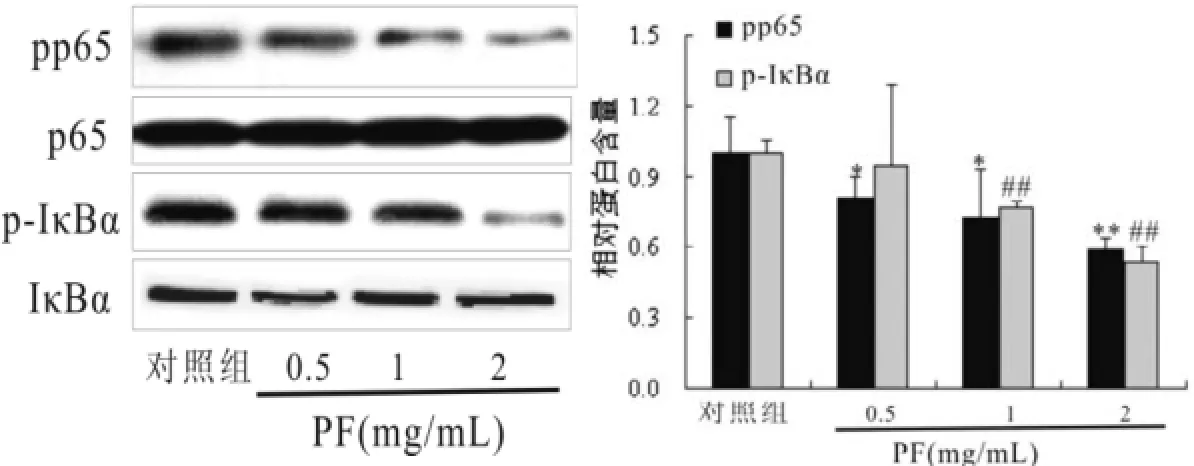
圖2 芍藥苷對H epG 2肝癌細胞N F-κB通路的影響
3 結論
肝癌是常見的惡性腫瘤之一,其危害僅次于肺癌,目前其主要治療手段為手術,但即使獲得手術切除機會,其復發、轉移率依然較高[5-9]。因此,尋求有效治療肝癌,降低復發率的藥物成為當務之急。而抗腫瘤藥物包括化療藥物、激素、生物制劑都能引起腫瘤細胞發生調亡。凋亡對腫瘤的抑制起重要作用,并且抑制NF-κB活性促進細胞凋亡是治療腫瘤的有效手段之一[10]。芍藥苷可通過抑制NF-κB信號通路來抑制胃癌細胞增殖[2-3],所以本研究擬嘗試用不同濃度(0.5、1、2 mg/mL)芍藥苷對HepG2肝癌細胞進行培養,結果表明隨著給藥濃度的增加,芍藥苷可逐漸降低細胞活力,抑制腫瘤細胞的增殖,在48小時時抑制率達到最高點。
Caspase 3是caspase家族中最重要的凋亡執行者之一,其被合成后通常以非活化的酶原形式存在于細胞質中,在多種凋亡信號刺激下經蛋白水解作用被激活成活化形式,可對多種蛋白底物進行降解,在細胞凋亡過程中起關鍵作用,被認為是整個凋亡級聯反應的一個關鍵調節點[11]。Caspase 3在HepG2肝癌細胞中活性高于給藥組[12-14],在本研究中,與對照組比較,芍藥苷(0.5、1、2 mg/mL)呈劑量依賴性抑制Caspase 3活性。
NF-κB是一類廣泛存在于腫瘤細胞內的重要轉錄因子,是多信號轉導途徑的匯聚點,參與組織細胞的免疫調節,炎癥反應,生長分化和凋亡等[15-16]。未受刺激時與IκB結合,當受到刺激時,IκB磷酸化,釋放NF-κB,使之恢復轉錄活性并從細胞質轉移到細胞核內,調節相關基因的表達。NF-κB在各種腫瘤細胞中均過表達[17],朱開梅等[18]報道八角中莽草酸可通過抑制NF-κB p65活性,抑制人肝癌HepG2細胞增殖。本研究結果表明芍藥苷能抑制HepG2肝癌細胞NF-κBp65,IκBα蛋白磷酸化,最終提高Caspase 3活性,誘導腫瘤細胞凋亡。
因此,芍藥苷可能通過NF-κB信號通路,提高Caspase 3活性,促進HepG2肝癌細胞的凋亡。
[1]晏雪生,李瀚旻,彭亞琴,等.芍藥苷對人肝癌細胞Hep-G2凋亡及其調控基因的影響[J].中華中醫藥學刊,2007,25(7): 1346-1347.
[2]方申存,戴偉,吳昊,等.芍藥苷對人胃癌SG C7901/V CR細胞增殖抑制作用及其機制研究[J].南京醫科大學學報:自然版,2010,30(5):636-640.
[3]Fang S,Zhu W,Zhang Y,et al.Paeoni florin modulates multi drug resistance of a human gastric cancer cell line vi a the inhibition of NF-κB activation[J].Mol Med Rep,2012,5(2):351-356.
[4]Lu JT,He W,SongSS,et al.Paeoni florin inhibited the tumor invasion and metastasis in human hepato cellular carcinoma cells[J].Brat is l Lek Listy,2014,115(7):427-433.
[5]郭明,伍周玲,王春歌,等.黃芩苷-金屬配合物的合成及其抗腫瘤活性研究[J].藥學學報,2014,49(3):337-345.
[6]吳菲,林國楨,張晉昕.我國惡性腫瘤發病現狀及趨勢[J].中國腫瘤,2012,21(2):81-85.
[7]魏沙.2002—2010年我國城市惡性腫瘤死亡率變化趨勢分析[J].實用預防醫學,2013,20(1):111-113.
[8]李鐘聲.原發性肝細胞癌的治療進展[J].安徽醫學,2009, 30(7):830-832.
[9]蔡欣然,黃長玉,周良藝.原發性肝癌根治術后不同復發時期高危因素及療效研究[J].實用腫瘤雜志,2010,25(5): 560-563.
[10]Baud V,Karin M.Is N F-kappaB a good target for cancer therapy?Hopes and pitfalls[J].Nat Rev Drug Discov,2009,8(1):33-40.
[11]Porter A G,Janicke RU.Emerging roles of caspase-3 in apopt os is[J].Cell Death Differ,1999,6(2):99-104.
[12]Xiang Q,M aY,Dong J,et al.Carnosic acid induces apopt osi s associ at ed with mit ochondri al dysfuncti on and Akt inact i vation in HepG 2 cell s[J].Int J Food Sci Nutr,2015,66(1):76-84.
[13]Zhang H,Guo Z,Han L,et al.The antitumor effect and mechanism of tai pei ni ne A,a new C19-dit erpenoid al kal oi d fr om Aconi tumt ai pei cum,on the HepG 2 hum an hepat ocel l ul ar carci nom a cel l l i ne[J].J BU O N,2014,19(3):705-712.
[14]Sudan S,Rupasi nghe H P.Fl avonoi d-enri ched appl e fraction A F4 i nduces cell cycle arrest,DNA topoisomerase II inhi bition,and apoptosis in human liver cancer HepG 2 cells[J].Nutr Cancer,2014,66(7):1237-1246.
[15]Zhang Y H,Yan HQ,Wang F,et al.TIPE2 inhi bits TN F-α i nduced hepatocellular carcinoma cell metastasis via Erk1/2 downregul at i on and N F-κB activation[J]. Int J Oncol,2015,46(1):254-264.
[16]Shan RF,Zhou Y F,Peng A F,et al.Inhi bition of Aurora-B suppresses H epG 2 cell invasi on and migration via the PI3K/A kt/N F-κB si gnaling pathway in vitro[J]. Exp Ther Med,2014 8(3):1005-1009.
[17]崔嵩,劉學鋒,吳斌.N F-κB在腫瘤中的研究進展[J].現代腫瘤醫學,2009,17(1):134-137.
[18]朱開梅,顧生玖,顧小文,等.八角中莽草酸對人肝癌H epG 2細胞增殖及N F-κB蛋白表達的影響[J].中國實驗方劑學雜志,2014,20(1):126-129.
Apoptotic Induction Effects of Paeoniflorin on Hepatoma Carcinoma Cells
ZHANG Yawu1,QUAN Ke2
1 Biliary Pancreatic Surgery Department of Lanzhou University Second Hospital,Lanzhou 730000,China;2 Gansu University of Traditional Chinese Medicine
Objective:To explore apoptotic induction effects of paeoniflorin on hepatoma carcinoma cells(HepG2),and to investigate its mechanism.Methods:HepG2 cells were cultivated with different concentrations of paeoniflorin(0.5,2 mg/mL),cell viability was detected by MTT method,Caspase 3 activity measured by enzyme linked immunosorbent assay and the expression of NF-κB signaling pathway related protein by western blot method. Results:As the concentrations of the drug increased,paeoniflorin could decrease the viability of HepG2 cells gradually,and the inhibition rate reached the highest within 48 hours;it increased Caspase 3 activity,inhibited the phosphorylation of NF-κB p65 and IκBα,thereby to promote cellular apoptosis.Conclusion:Paeoniflorin could obtain anti-tumor effects by inducing the apoptosis of HepG2 cells via NF-κB signaling pathway.
hepatoma carcinoma cells;apoptosis;NF-κB signaling pathway;phosphorylation;paeoniflorin
R735.7
A
1004-6852(2016)05-0023-03
2015-02-19
張亞武(1971—),男,碩士學位,副主任醫師。研究方向:消化道腫瘤的診治。

