局部晚期鼻咽癌TP方案誘導化療及同期放化療初步觀察*
李金偉肖海王蓉曾紅學
局部晚期鼻咽癌TP方案誘導化療及同期放化療初步觀察*
李金偉①肖海②王蓉②曾紅學①
目的:觀察局部晚期鼻咽癌誘導化療及不同化療方案的依從性及不良反應。方法:將60例局部晚期鼻咽癌患者按照隨機數字表法分為A、B、C三組,A組TP誘導化療+同期順鉑放化療,B組順鉑同期放化療,C組TP同期放化療。放療為調強放療,GTVnx 68~72 Gy,GTVnd 65~70 Gy。觀察三組治療依從性及不良反應情況。結果:三組完成化療數比例分別為80.0%、95.0%、90.0%,放療全部足量完成,依從性均好,最常見反應為胃腸道反應、口咽黏膜炎、骨髓抑制、皮膚損傷,三組比較差異均無統計學意義(P>0.05)。但同時中重度不良反應發生率A組最高,B組最低,差異有統計學意義(P<0.05)。結論:局部晚期鼻咽癌誘導化療后同期放化療及順鉑同期放化療、TP同期放化療依從性均良好,前者同時中重度不良反應發生率較高,順鉑同期放化療最輕。
局部晚期鼻咽癌; 同期放化療; 誘導化療; 不良反應
First-author's address:Ganzhou Tumor Hospital,Ganzhou 341000,China
調強放療在劑量學和生物效應方面較常規放療有絕對優勢,顯著提高局部控制率,是鼻咽癌治療首選[1-4]。INT0099試驗確立了同期放化療作為局部晚期鼻咽癌標準治療[5]。誘導化療取得較高局部緩解率,對生存率貢獻結論不一,誘導化療及同期化療方案、與同期化療的配合模式仍存在爭議[6-10]。為此對2014年1-11月筆者醫院60例局部晚期鼻咽癌,通過行與不行誘導化療,及同期化療的不同方案,記錄不良反應發生率,觀察依從性,現報告如下。
1 資料與方法
1.1 納入與排除標準 納入標準:(1)經鼻咽組織病理確診的初治鼻咽癌;(2)分期Ⅲ期及Ⅳa期(2008分期);(3)無嚴重并發疾病;(4)KPS≥70;(5)年齡≤70歲;(6)既往無放化療史。排除標準:(1)妊娠哺乳期鼻咽癌;(2)既往或同時第二原發癌。
1.2 一般資料 選擇2014年1-11月筆者所在醫院收治的60例局部晚期鼻咽癌患者,按照隨機數字表法分為A、B、C三組,每組20例。三組患者性別、年齡、分期等一般資料比較,差異均無統計學意義(P>0.05),具有可比性,見表1。
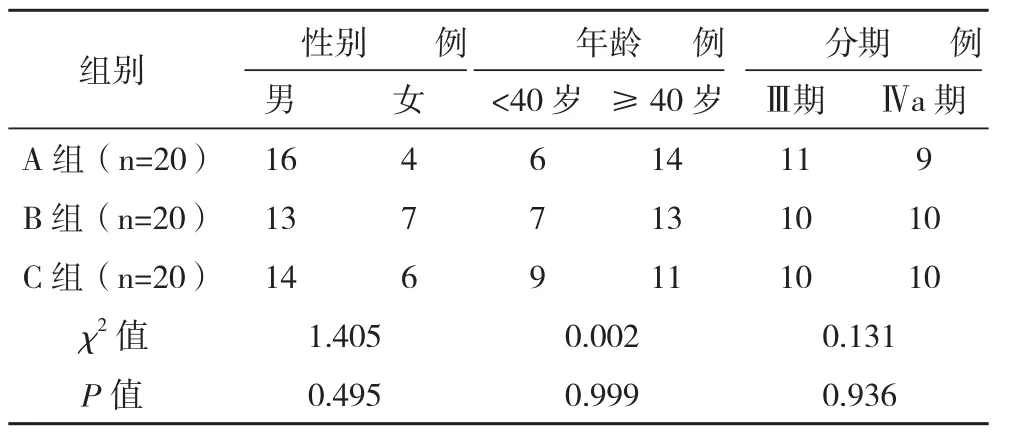
表1 三組患者臨床資料 例
1.3 方法 A組誘導化療,多西他賽75 mg/m2d1+順鉑75 mg/m2d1、22,2周期后同期放化療,順鉑100 mg/m2,d1、d22;B組同期順鉑100 mg/m2,d1、d22;C組多西他賽75 mg/m2+順鉑75 mg/m2,d1、d22同期放化療。放療采用調強放療,GTVnx 68~72 Gy,GTVnd 65~70 Gy,CTV1 60 Gy,CTV2 54~56 Gy,31~33次。
1.4 觀察指標 記錄比較三組不良反應發生情況,不良反應采用2003美國毒副反應標準(CTCAE3.0)。
1.5 統計學處理 采用SPSS 16.0軟件對所得數據進行統計分析,計量資料用(±s)表示,比較采用t檢驗;計數資料以率(%)表示,比較采用 χ2檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 治療完成情況
2.1.1 化療 化療完成率計算:A組以完成4次化療例數,B、C組以完成2次化療的例數,與總例數之比。B組完成率較高,但三組比較差異均無統計學意義( χ2=1.680,P=0.432>0.05),見表2。
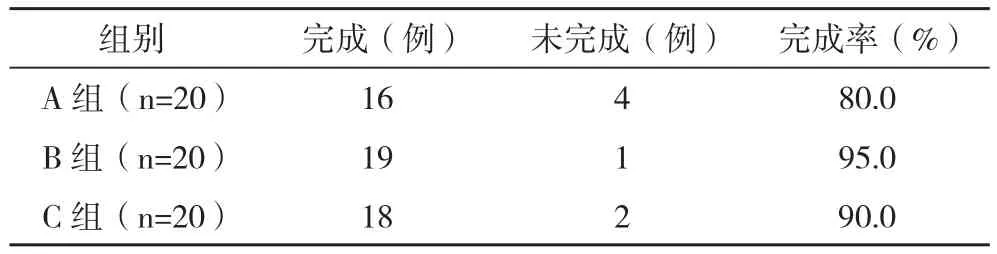
表2 三組化療完成情況比較
2.1.2 放療 所有患者均完成足量放療,三組放療劑量、放療總天數比較,差異均無統計學意義(P<0.05),見表3。
表3 三組放療劑量、放療總天數比較(±s)
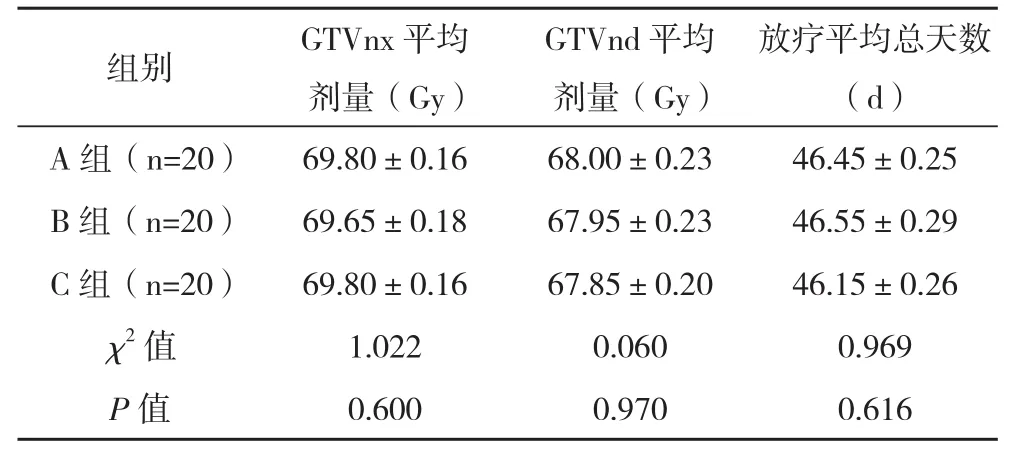
表3 三組放療劑量、放療總天數比較(±s)
?
2.2 不良反應 最常見為胃腸道反應、口咽黏膜炎、骨髓抑制、皮膚損傷。A、B、C三組3~4度胃腸道反應、3~4度骨髓抑制、2~3度口腔黏膜炎、2~3度皮膚損傷比較,差異均無統計學意義(P>0.05)。但同時中重度不良反應發生率A組最高,B組最低,差異有統計學意義(P<0.05)。見表4。
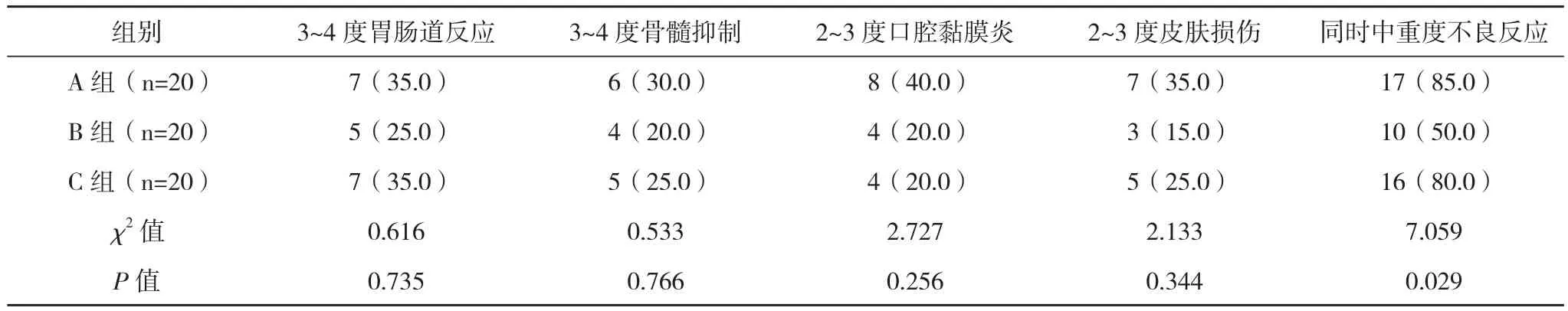
表4 三組不良反應發生情況比較 例(%)
3 討論
調強放療的應用,使鼻咽癌局控率顯著提高,遠處轉移成為失敗主要原因[11-12],因而降低遠處轉移備受關注。各種研究與放療聯合的方式有誘導化療、同期化療及不同方案的組合。
北美開展的Ⅲ期臨床研究INT0099試驗及以后臨床試驗結果,同期放化療成為局部晚期鼻咽癌的標準治療方式。誘導化療有降低腫瘤負荷,提高腫瘤對射線的敏感性,并可殺滅可能潛在的微轉移腫瘤細胞,降低遠處轉移,因此許多臨床試驗探索誘導化療聯合同期放化療的模式[13-17],但是誘導化療也可能無效,可能導致腫瘤加速增殖,使腫瘤細胞產生耐藥性,錯過放療最佳時期。單藥DDP的同步放化療作為局部晚期鼻咽癌的標準治療方式,較誘導化療的優勢在于根治性放療及早參與,腫瘤血管未破壞,與化療有協同作用,沒有誘導化療后腫瘤加速增殖的情況。雖然使患者總生存獲益,但遠處轉移仍是治療失敗的主要原因[18]。單藥順鉑強度小,對預防或治療亞臨床轉移灶作用小,增加強度的同步化療,可能在預防遠處轉移起一定作用,有利于迅速降低腫瘤負荷,改善局部血液循環,改善細胞乏氧狀態,增加放射敏感性,故有學者采用同期TP方案化療替代單藥順鉑,試圖通過增加同期化療強度來降低遠處轉移,提高療效[13-14]。誘導化療后同期化療及順鉑同期化療、TP同期化療一起研究目前尚未見報道。
李權[19]對130例局部晚期鼻咽癌誘導化療與IMRT同期化療研究,結果誘導化療聯合IMRT同期化療及IMRT同期化療兩組的急性不良反應比較,差異無統計學意義(P>0.05)。Hui等[20]開展的TP誘導化療+順鉑同期放化療與單藥順鉑同期放化療臨床隨機對照研究結果顯示:誘導化療+同期放化療組中3~4度粒細胞減少發生率較高,但兩組粒細胞減少及其他急性不良反應發生率比較無差異均無統計學意義(P>0.05)。本研究中,三組完成全部預期化療數比例分別為80.0%、95.0%、90.0%,放療全部足量按時完成,差異均無統計學意義(P>0.05),依從性均較好。出現的最常見的反應為胃腸道反應、口咽黏膜炎、骨髓抑制、皮膚損傷。A、B、C三組3~4度胃腸道反應、3~4度骨髓抑制、2~3度口腔黏膜炎、2~3度皮膚損傷比較,差異均無統計學意義(P>0.05)。但三組同時發生中重度不良反應發生率,A組最高,B組最低,差異有統計學意義(P<0.05)。不良反應經預防性用藥和積極處理,患者一般均能耐受。
本研究中三組目前納入的病例數較少,觀察時間較短,期待大樣本、隨訪時間更長的臨床研究,進一步優化治療計劃和改變化療方案。
[1]林海群,李寶生,魏玉梅,等.同期推量調強放療聯合化療治療中晚期鼻咽癌的療效分析[J].中華腫瘤防治雜志,2009,16(18):1408-1411.
[2]吳芳,王仁生,馮國生,等.初治鼻咽癌調強放療的前瞻性多中心臨床研究[J].中華放射腫瘤學雜志,2012,21(3):407-411.
[3]高穎川,朱小東,李齡,等.339例鼻咽癌調強放療臨床療效分析[J].中國腫瘤臨床,2012,39(24):2029-2035.
[4]蘇勝發,趙充,韓非.鼻咽癌適形調強放療遠期療效分析[J].中華腫瘤防治雜志,2013,20(11):853-858.
[5] Al-Sarraf M,Leblanc M,Giri P G,et al.Chemoradiotherapy versus radiotherapy in patients with advanced nasopharyngeal cancer:phase Ⅲ randomized intergroup study 0099[J].J Clin Oncol,1998,16(4):1310-1317.
[6]龍斌,譚兵,周憲,等.放化療聯合治療局部晚期鼻咽癌的臨床觀察[J].中國腫瘤臨床,2012,39(20):1556-1558.
[7]杜清華,王仁生.局部晚期鼻咽癌誘導化療的研究進展[J].廣東醫學,2012,33(17):2685-2688.
[8] Guo L,Lin H X,Xu M,et al.PhaseⅠstudy of TPF neoadjuvant chemotherapy followed by radical radiotherapy in advanced nasopharyngeal carcinoma[J].Chin J Cancer,2010,29(2):136-139.
[9] Airoldi M,Gabriele P,Gabriele A M,et al.Induction chemotherapy with carboplatin and taxol followed by radiotherapy and concurrent weekly carboplatin+taxol in locally advanced nasopharyngeal carcinomaf[J].Cancer Chemother Pharmacol,2011,67(5):1027-1034.
[10] Bae W K,Hwang J E,Shim H J,et al.PhaseⅡstudy of docetaxel,cisplatin,and 5-FU induction chemotherapy followed by chemoradiotherapy in locoregionally advanced nasopharyngeal cancer[J].Cancer Chemother Pharmacol,2010,65(3):589-595.
[11] Wang R,Wu F,Lu H,et al.Definitive intensity-modulated radiation therapy for nasopharyngeal carcinoma: long-term outcome of a multicenter prospective study[J].Journal of Cancer Research and Clinical Oncology,2013,139(1):139-145.
[12] Wu F,Wang R,Lu H,et al.Concurrent chemoradiotherapy in locoregionally advanced nasopharyngeal carcinoma:treatment outcomes of a prospective,multicentric clinical study[J]. Radiotherapy and Oncology:Journal of the European Society for Therapeutic Radiology and Oncology,2014,112(1):106-111.
[13]莫清華,孫建湘,金軍,等.TP方案同期化放療治療局部晚期鼻咽癌的臨床研究[J].現代腫瘤醫學,2008,16(11):1895-1897.
[14]張兵,唐滟,謝軍,等.局部晚期鼻咽癌同步放化療臨床療效[J].醫學臨床研究,2011,28(1):32-34.
[15] Guo S S,Tang L Q,Chen Q Y,et al.Induction chemotherapy followed by concurrent chemoradiotherapy versus concurrent chemoradiotherapy alone in stage Ⅲ-Ⅳb nasopharyngeal carcinoma patients with Epstein-Barr virus DNA≥4000 copies/ml:a matched study[J].Oncotarget,2016,7(20):29 739-29 748.
[16] Wee C W,Keam B,Heo D S,et al.Locoregionally advanced nasopharyngeal carcinoma treated with intensity-modulated radiotherapy plus concurrent weekly cisplatin with or without neoadjuvant chemotherapy[J].Radiation Oncology Journal,2015,33(2):98-108.
[17] Tan T,Lim W T,Fong K W,et al.Concurrent chemoradiation with or without induction gemcitabine, Carboplatin,and Paclitaxel: a randomized, phase 2/3 trial in locally advanced nasopharyngeal carcinoma[J].International Journal of Radiation Oncology Biology Physics,2015,91(5):952-960.
[18] Wang J,Shi M,Hsia Y,et al.Failure patterns and survival in patients with nasopharyngeal carcinoma treated with intensity modulated radiation in Northwest China: a pilot study[J]. Radiation Oncology,2012,7(1):2.
[19]李權.局部晚期鼻咽癌患者誘導化療與IMRT同期化療的遠期療效觀察[J].武漢大學學報(醫學版),2015,36(1):62-65.
[20] Hui E P,Ma B B,Leung S F,et al.Randomized phase II trial of concurrent cisplatin-radiotherapy with or without neoadjuvant docetaxel and cisplatin in advanced nasopharyngeal carcinoma[J]. Journal of Clinical Oncology:Official Journal of the American Society of Clinical Oncology,2009,27(2):242-249.
Preliminary Research of TP-based Induction Chemotherapy and Concurrent Chemotherapy in the Treatment of Locally Advanced NPC
L I J in-wei,XIAO Hai,WANG Rong,et al.//Medical Innovation of China,2016,13(27):010-013
Objective:To observe the adherence and adverse reactions of induction chemotherapy and different concurrent chemotherapy regimens for locally advanced nasopharyngeal carcinoma(NPC). Method:A total of 60 patients with locally advanced NPC were randomly divided into A,B,C groups,20 cases in each group.Group A was given TP-based induction chemotherapy,followed by concurrent chemoradiotherapy with cisplatin;Group B was given Cisplatin-based concurrent chemoradiotherapy.Group C was given TP-based concurrent radiochemotherapy.Radiotherapy was used by IMRT,GTVnx 68-72 Gy,GTVnd 65-70 Gy.The treatment compliance and incidence of adverse reactions of three groups were observed.Result:Group A,B and C completed the expected number of chemotherapy rates were 80.0%,95.0%,90.0%.Radiotherapy were completed at sufficient amount,compliance was good,the most common were gastrointestinal,oropharyngeal mucositis,myelosuppression,skin damage.In severe injuries differences were no statistical difference(P>0.05).But all adverse reactions rates were statistically different,group A was the highest,group B was the lowest,there was statistical significance(P<0.05).Conclusion:Locally advanced NPC treated by TP-based induction chemotherapy followed by cisplatin-based concurrent chemoradiotherapy,cisplatin-based concurrent radiochemotherapy,TP-based concurrent chemoradiotherapy,the compliance of treatment are good.The moderate and severe adverse reactions of the former is highest,cisplatin-based concurrent chemotherapy is lightest.
Locally advanced nasopharyngeal carcinoma; Concurrent chemoradiotherapy; Induction chemotherapy; Adverse reactions
10.3969/j.issn.1674-4985.2016.27.003
贛州市科技局科技計劃項目
(贛市科發【2012】36號-194)
①江西省贛州市腫瘤醫院 江西 贛州 341000
②贛南醫學院
李金偉
(2015-12-01) (本文編輯:程旭然)

