白蘞的化學成分研究
白學莉,單文靜
(遼寧省大連市第五人民醫院,遼寧大連 116021)
白蘞的化學成分研究
白學莉,單文靜
(遼寧省大連市第五人民醫院,遼寧大連 116021)
目的研究中藥白蘞的化學成分。方法采用大孔吸附樹脂、硅膠柱色譜、聚酰胺色譜、葡聚糖凝膠(sephadex LH-20)柱色譜、十八烷基硅烷鍵合硅膠(ODS)色譜等手段進行分離純化,根據化合物的理化性質和波譜學等方法鑒定中藥白蘞所含化學成分的結構。結果從白蘞植物的70%乙醇提取物中分離得到9個化合物,分別鑒定為尿苷(uridine,1),腺苷(adenosine,2),阿魏酸(ferulic acid,3),原兒茶酸(protocatechuate,4),沒食子酸(gallic acid,5),大黃素-8-O- -D-吡喃葡萄糖苷(emodin-8-O- -D-glucopyranoside,6),咖啡酸(caffeic acid,7), -谷甾醇( -sitosterol,8),7 -羥基- -谷甾醇(7 -hydroxy- -sitosterol,9)。結論化合物4和化合物9是從蛇葡萄屬(Ampelopsis Michx.)植物中首次分離得到,化合物1~3和化合物7為首次從白蘞Ampelopsis japonica(Thunb.)Makino植物中分離得到。
白蘞;化學成分;成分分離;結構鑒定
白蘞又名兔核、白根、昆侖、貓兒卵、鵝抱蛋、見腫消、穿山老鼠、白水罐、山地瓜、鐵老鼠、母雞帶仔、老鼠瓜薯、山栗子、人卦牛、白漿罐、野紅薯、地老鼠、野著薯、母雞抱蛋、五爪藤等,首載于《神農本草經》,引為下品。白蘞廣泛分布于我國東北、華北、華東、華中及西南地區[1-2]。2015年版《中國藥典(一部)》收載的白蘞為葡萄科白蘞Ampelopsis japonica(Thunb.)Makino的塊根,具有清熱解毒、消腫散結、生肌止痛之功效,用于癰疽發背、療瘡、瘰癘、水火燙傷。白蘞入藥歷史悠久,早在《名醫別錄》中就有記載,是歷代醫家治療疔癰的重要藥物。現代藥理學研究表明,白蘞具有明確的抗腫瘤、抗菌、抗病毒等活性[3-7],同時可外用治療瘡瘍[8]。現代化學研究表明,白蘞主要含有酚酸、蒽醌、黃酮、皂苷類物質,同時還含有揮發油類成分[9-11]。其中,酚酸類成分沒食子酸和蒽醌類成分大黃素被認為是其主要的活性成分,用于白蘞的質量評價[12-14]。為了進一步分析白蘞的化學成分,為其開發利用提供理論依據,本研究中對白蘞的70%乙醇提取物的化學成分進行了分析,共分離純化出9個化合物,通過理化性質和波譜學手段鑒定了全部化合物的結構。現報道如下。
1 儀器與材料
1.1 儀器
BRUKER-ARX-300型和BRUKER-ARX-500型核磁共振波譜儀(TMS作內標,布魯克科技有限公司);Waters Prep150型高效液相色譜儀(檢測器2489 UV/Visible Detector,沃特世科技有限公司);制備色譜柱YMCODS-A柱(250 mm×10 mm,5 μm,YMC科技有限公司);分析色譜柱YMCODS-A型(150 mm×4.6 mm,5 μm,YMC科技有限公司);RE-3000B型旋轉蒸發儀(上海亞榮生化儀器廠);柱色譜硅膠(100-200目,200~300目),薄層色譜硅膠H(300~400目)及薄層色譜硅膠(GF25),均購于青島海洋化工有限公司;ODS柱色譜填料(60~80 μm,Welch科技有限公司);Sephadex LH-20(北京綠百草科技發展有限公司);AB-8大孔吸附樹脂(河北華眾化工有限公司)。
1.2 材料
白蘞藥材購于遼寧省藥材公司,經大連210醫院藥學部徐保利副主任藥師鑒定為蛇葡萄屬(Ampelopsis Michx.)葡萄科白蘞Ampelopsisjaponica(Thunb.)Makino的塊根。
2 方法與結果
2.1 方法
取中藥材白蘞10.0 kg,粉碎,以8倍量(80 L)70%乙醇浸泡0.5 h時后加熱回流提取3次,每次2 h,合并提取液并減壓濃縮得浸膏約2.1 kg,浸膏加水50 L溶解稀釋,溶液分別依次采用氯仿、乙酸乙酯和正丁醇進行萃取,并對各萃取部分進行減壓濃縮至浸膏,對正丁醇萃取部分浸膏采用大孔吸附樹脂及硅膠柱色譜技術,二氯甲烷∶甲醇(500∶1~1∶1),經過薄層色譜法合并分離物,進一步經過ODS柱色譜,制備液相色譜,以甲醇-水為洗脫系統進行單體成分純化,分離各化合物,采用核磁共振光譜技術進行結構鑒定。
2.2 分析結果
采用2.1項下方法分離,得化合物1(14 mg),2(22 mg),3(26 mg),4(12 mg),5(5 mg),6(20 mg),7(10 mg),8(9 mg)和9(12 mg),結構鑒定分別為尿苷(uridine,1),腺苷(adenosine,2),阿魏酸(ferulic Acid,3),原兒茶酸(protocatechuate,4),沒食子酸(gallic acid,5),大黃素-8-O-β-D-吡喃葡萄糖苷(emodin-8-O-β-D-glucopyranoside,6),咖啡酸(caffeic acid,7),β-谷甾醇(β-sitosterol,8),7 β-羥基-β-谷甾醇(7 βhydroxy-β-sitosterol,9)。化合物結構見圖1。
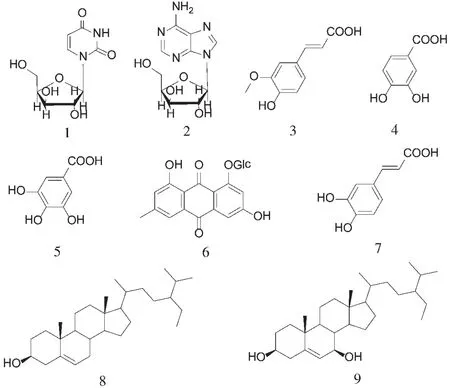
圖1 化合物1~9結構
2.3 各化合物鑒定
2.3.1 化合物1
淡黃色油狀(甲醇)。1H-NMR(300 MHz,DMSO-d6) δ:11.13(1H,s,N-H),5.63(1H,d,J=8.0 Hz,H-5),7.87(1H,d,J=8.0 Hz,H-6),5.76(1H,d,J=5.5 Hz,H-1′);13C-NMR(75 MHz,DMSO-d6)δ:151.6(C-2),163.2(C-4),102.6(C-5),141.6 (C-6),88.5(C-1′),74.3(C-2′),70.7(C-3′),85.6(C-4′),61.7(C-5′)。與文獻[15]報道結果一致,故鑒定該化合物為尿苷(uridine)。
2.3.2 化合物2
無色油狀(甲醇)。13C-NMR(300 MHz,DMSO-d6) δ:152.8(C-2),149.5(C-4),119.8(C-5),156.6 (C-6),140.4(C-8),88.4(C-1′),73.9(C-2′), 71.1(C-3′),86.4(C-4′),62.1(C-5′)。與文獻[16]報道的數據基本一致,故鑒定該化合物為腺苷。
2.3.3 化合物3
白色針狀結晶(MeOH)。1H-NMR(CD3OD-d4,500 MHz)δH:7.76(1H,d,J=16.1 Hz,H-7),6.47 (1H,d,J=16.1 Hz,H-8),7.01(1H,d,J=8.1 Hz,H-5),7.21(1H,dd,J=8.1,2.0 Hz,H-6),7.32(1H,d,J=2.0 Hz,H-2),4.08(3H,s)。與文獻[17]報道的數據基本一致,故鑒定該化合物為阿魏酸。
2.3.4 化合物4
白色結晶(MeOH)。三氯化鐵-鐵氰化鉀反應呈陽性,提示有酚羥基;溴甲酚綠反應呈陽性,提示有羧基存在;SnCl2反應呈陽性,提示有鄰酚羥基存在。與原兒茶醛對照品共薄層,Rf值一致,故鑒定該化合物為原兒茶酸。
2.3.5化合物5
白色結晶(MeOH)。三氯化鐵-鐵氰化鉀反應呈陽性,提示含有酚羥基;溴甲酚綠反應呈陽性,提示有羧基存在。與沒食子酸對照品共薄層,二者Rf值一致,故鑒定該化合物為沒食子酸。
2.3.6 化合物6
黃色針晶(甲醇),Borntr?ger′s反應、三氯化鐵反應、Molish反應均呈陽性。均與已知對照品共薄層,其Rf值一致,故鑒定該化合物為大黃素-8-O-β-D-吡喃葡萄糖苷。
2.3.7 化合物7
白色針狀結晶(MeOH)。1H-NMR(DMSO-d6,500 MHz)δH:7.43(1H,d,J=16.1 Hz,H-7),6.16(1H,d,J=16.1 Hz,H-8),6.03(1H,dd,J=9.0,2.8 Hz,H-2),6.74(1H,d,J=9.0 Hz,H-5),6.98(1H,dd,J=9.0,3.0 Hz,H-6),9.06(1H,s,H-9);13C-NMR (DMSO-d6,500 MHz)δC:168.2(C-9),116.1(C-8),144.5(C-7),121.2(C-6),115.4(C-5),148.3(C-4),145.9(C-3),114.5(C-2),126(C-1)。與文獻[17]報道結果一致,故鑒定該化合物為咖啡酸。
2.3.8 化合物8
白色針狀結晶(MeOH),mp 137~138℃,Liebermann-Burchard反應陽性。與β-谷甾醇對照品共薄層,Rf值相同,斑點顏色一致。與β-谷甾醇對照品混合,熔點不下降,故鑒定該化合物為β-谷甾醇。
2.3.9 化合物9
白色粉末(MeOH),mp 213~214℃。1H-NMR (CDCl3-d,500 MHz)δH:3.55(1H,m,H-3),5.30 (1H,s,H-6),3.85(1H,m,H-7),0.70(3H,s,CH3-18),1.05(3H,s,CH3-19),0.93(3H,d,J=6.5Hz,CH3-21),0.83(3H,d,J=7.0Hz,CH3-26),0.81(3H,d,J=7.0Hz,CH3-27),0.85(3H,t,J=7.5 Hz,CH3-29);13C-NMR (125 MHz,CDCl3-d)δC:C1~C29(36.9,31.6,71.4,41.7,143.5,125.4,73.3,40.9,48.3,36.4,21.1,39.5,42.9,55.4,26.4,28.5,56.0,11.8,19.1,36.1,18.8,34.0,26.1,45.8,29.1,19.8,19.0,23.1,12.0)。與文獻[18]報道的數據基本一致,故鑒定該化合物為7β-羥基-β1-谷甾醇。
3 討論
白蘞為傳統中藥,具有抗腫瘤、抗菌及抗病毒等活性。本試驗中采用傳統中藥化學研究手段從中藥白蘞Ampelopsis japonica(Thunb.)Makino中分離得到9個化合物單體成分,并應用光譜學技術對所有化學成分的結構進行鑒定,其中化合物4和化合物9是從蛇葡萄屬(AmpelopsisMichx.)植物中首次分離得到,化合物1~3和化合物7為首次從白蘞植物中分離得到。從白蘞及蛇葡萄屬植物中首次分離的單體成分主要為酚酸類及生物堿類成分,酚酸類成分是主要活性成分,具有抗菌、降糖、抗腫瘤等活性。首次分離的活性成分如阿魏酸、咖啡酸等可為白蘞藥材的質量控制和質量評價提供新的指標,同時可為中藥白蘞的開發提供理論基礎。
[1]中國醫學科學院藥物研究所.中藥志(第一冊)[M].北京:人民衛生出版社,1959:404.
[2]江蘇新醫學院.中藥大辭典(上冊)[M].上海:上海人民出版社,1977:69.
[3]賈敏,張寒.白蘞、烏頭單用及合用對人胃腺癌細胞SGC-7901增殖、凋亡的影響[J].現代中西醫結合雜志,2011,20(27):3388-3390.
[4]杭佳,張夢美,葉曉川,等.白蘞藥效成分沒食子酸抑制人肝癌HepG2細胞生長及作用機制研究[J].中國實驗方劑學雜志,2013,19(1):291-295.
[5]張夢美,葉曉川,黃必勝,等.白蘞抗腫瘤活性部位的篩選研究[J].湖北中醫藥大學學報,2012,14(2):40-42.
[6]張波,周芳亮,盧芳國,等.96種中藥材對流感病毒神經氨酸酶活性的影響[J].中華中醫藥雜志,2014,29(9):2788-2792.
[7]朱長俊,朱紅薇.白蘞正丁醇提取物抗菌作用研究[J].中國民族民間醫藥雜志,2011,20(1):67-68.
[8]湯佩佩,郭曉芳,白明,等.白蘞外用對瘡瘍模型的影響[J].中華中醫藥雜志,2012,27(3):702-705.
[9]米君令,吳純潔,孫靈根,等.白蘞化學成分研究[J].中國實驗方劑學雜志,2013,19(18):86-89.
[10]陳愛軍,劉運美,蔡鳳桃,等.白蘞研究進展[J].中國民族民間醫藥雜志,2014,23(13):10-11.
[11]高歡,王文娜,孫琦,等.白蘞揮發油化學成分分析[J].特產研究,2014,36(1):52-54.
[12]樂佳美,熊筱娟,畢寶寶,等.RP-HPLC測定不同產地白蘞藥材中沒食子酸的含量[J].安徽農業科學,2015,43(4):108-110.
[13]張小燕,杭佳,葉曉川,等.HPLC切換波長法同時測定白蘞中沒食子酸、原兒茶醛、兒茶素和白藜蘆醇的含量[J].藥物分析雜志,2014,34(3):428-431.
[14]陳愛軍,劉運美,曾雷,等.反相高效液相色譜法測定白蘞藥材中大黃素的含量[J].湖南中醫雜志,2014,30(12):147-148.
[15]付明,王登宇,胡興,等.徐長卿化學成分研究[J].中藥材,2015,38(1):97-100.
[16]姜泓,劉珂,孟舒,等.人工蛹蟲草子實體化學成分[J].藥學學報,2000,35(9):663-668.
[17]董琳,王金輝,劉明生.裸花紫珠葉中的酚酸類化學成分[J].沈陽藥科大學學報,2010,287(4):290-291.
[18]彭金詠,范國榮,吳玉田.白花敗醬草化學成分研究[J].中藥材,2005,28(10):24-25.
Study on the Constituents of Ampelopsis Japonica(Thunb.)Makino
Bai Xueli,Shan Wenjing
(Dalian Fifth People′s Hospital,Dalian,Liaoning,China116021)
Objective To study the chemical constituents of the Ampelopsis japonica(Thunb.)Makino.MethodsSeparation and purification were carried out by macroporous adsorption resin,silica gel column chromatography,polyamide chromatography,Sephadex LH-20 column chromatography,octadecyl silanebondedsilicagel(ODS)chromatography.Thephysico-chemical properties andspectroscopic methods were used to identify the structure ofAmpelopsis japonica(Thunb.)Makino.Results9 compounds were obtained from the 70%ethanol-water extracts of theAmpelopsis japonica(Thunb.)Makino.The structures were determined as Uridine(1),Adenosine(2), FerulicAcid(3),protocatechuate(4),gallicacid(5),emodin-8-O-β-D-glucopyranoside(6),Caffeicacid(7),β-sitosterol(8)and 7β-hydroxy-β-sitosterol(9)by comparison of their spectral data with the reported data,respectively.Conclusion s Compounds 4 and 9 were isolated from genus Ampelopsis for the first time,compound 1-3 and 7 were isolated from Ampelopsis japonica(Thunb.)Makino for the first time.
Ampelopsis Radix(Thunb.)Makino;chemical constituents;structural identification;constituent isolation
R284.1;R282.71
A
1006-4931(2017)01-0016-03
10.3969/j.issn.1006-4931.2017.01.005
2016-09-18;
2016-10-25)
白學莉(1972-),女,主管藥師,研究方向為中藥質量標準,(電話)0411-84211244(電子信箱)baixueli0411@163.com。

