水熱法制備SnO2納米顆粒的CO氧化性能
柴澍靖,李 靜,白雪芹,李新剛
(天津大學化工學院,天津市應用催化科學與工程重點實驗室,天津 300354)
隨著工業革命以及科學技術的發展,環境污染問題日益嚴重。CO是空氣中常見的有害氣體,無色無味,其密度和空氣相近,傳播性較強[1]。CO與人體血紅蛋白的結合能力約為O2的210倍[2]。當空氣中φ(CO)達到200×10-6時,3 h后就會出現輕微頭疼;當φ(CO)達到1.28%時,1~3 min內即可致人死亡。由于CO對人類生命健康威脅較大,低濃度的CO消除很早就引起了學者的關注。
催化消除是最有效的CO消除途徑[3-4]。一直以來貴金屬催化劑,以其高催化活性吸引著廣大研究者的關注[5-8]。但是貴金屬催化劑價格昂貴,高溫易燒結失活等問題阻礙了其在工業上的推廣應用。因此金屬氧化物催化劑,如Co3O4[4]、Fe2O3[9]、CeO2[10]和CuO[11],以其低成本和良好的熱穩定性成為近年來的研究熱點[12]。
二氧化錫(SnO2)是n型半導體材料,常用于CO氣敏材料[13],電極材料[14]以及太陽能電池材料[15]。在催化領域,由于其具有良好的熱穩定性及抗水性,常被用作貴金屬載體如Au/SnO2、Pd/SnO2[16],催化劑助劑[17],此外,通過形成復合金屬氧化物,SnO2體系也表現出了極高的反應活性[18-19]。本課題組的劉程等[20]通過將Ce摻雜進入SnO2晶格得到了活性極高的甲烷氧化催化劑,摻雜Ce后可以提高SnO2氧流動性,產生表面和體相的氧空位,同時活化了催化劑表面的氧物種和Sn4+。
但是目前關于SnO2基體本身的研究工作報道較少,本工作主要是以SnO2材料為模型,采用簡單的一步水熱法對其尺寸進行調控,并利用X射線衍射(XRD)、透射電鏡(TEM)、N2物理吸脫附(BET)和H2程序升溫還原(H2-TPR)手段,考察納米尺寸對其表面狀態及催化性能的影響,為其作為催化劑載體材料以及摻雜型復合金屬氧化物催化劑的設計提供重要的理論參考。
1 實驗部分
1.1 催化劑的制備
稱取五水合四氯化錫試劑,在40 ℃的水浴溫度下,配制成0.1 mol·L-1的溶液。溶解均勻后在磁力攪拌下逐滴加入氨水調節pH值至7,得到白色沉淀。用去離子水抽濾洗滌Cl-離子,至濾液滴入0.1 mol·L-1的AgNO3溶液無沉淀產生。將濾餅溶于氨水中,滴加配置好的0.05 mol·L-1的CTAB溶液,40 ℃水浴攪拌1 h。將前驅體溶液移入水熱釜,190 ℃水熱處理12 h。將水熱產物干燥過夜,然后在馬弗爐中2 ℃·min-1升溫至300 ℃保持1 h,再升溫至500 ℃焙燒3 h。將此催化劑標記為Nano-SnO2。
對照組樣品采用氨水沉淀法制備,同樣抽濾洗去Cl-離子,將濾餅干燥過夜,然后馬弗爐中500 ℃,焙燒4 h。將此催化劑標記為SnO2。
所用CTAB為上海阿拉丁生化科技股份有限公司生產,其余試劑均為天津市光復精細化工研究所生產,純度均為分析純。
1.2 催化劑表征
1.2.1熱重-差熱(TG/DTA)測試
對催化劑的TG/DTA測試所用儀器為Perkin Elmer公司生產的Diamond TG/DTA熱重分析儀。樣品用量10 mg,空氣氣速100 mL·min-1,升溫速率10 ℃·min-1。
1.2.2X射線衍射分析(XRD)測試
XRD測試是在德國布魯克AXS有限公司生產的型號為D8-S4衍射儀上進行。操作電壓和電流分別為40 kV和40 mA,采用Cu_Kα作為射線源,掃描范圍2θ=10°~90°,采集步長0.02°。
1.2.3比表面積(BET)測試
催化劑的比表面積測試在Quantachrome NOVA-2000物理吸附儀上進行。測試前催化劑于300 ℃脫氣預處理4 h,然后在液氮溫度(-196 ℃)下利用氮氣吸附/脫附測試,樣品比表面積采用多點BET方法計算得出。
1.2.4透射電子顯微鏡(TEM)測試
催化劑的形貌測試是在JEM-2100F場發射透射顯微鏡上進行的,加速電壓200 kV。樣品測試前經過超聲分散在乙醇溶液中,然后將其沉積到銅網上,干燥后進行測試。
1.2.5H2程序升溫還原(H2-TPR)測試
催化劑的H2-TPR測試在天津先權公司的TP-5080全自動化學吸附儀上進行,尾氣進入TCD檢測儀前,經過CaO和NaOH凈化處理。測試條件:樣品用量30 mg,還原氣為8% H2/N2混合氣,氣速30 mL·min-1,并以10 ℃·min-1的升溫速率從室溫加熱到900 ℃。
1.3 催化劑的CO氧化性能測試
催化劑的CO氧化性能測試在微型反應評價裝置上進行。樣品用量100 mg,測試氣體組成為1% CO/24% O2/N2(150 mL·min-1)。空速約為93 000 mL·g-1·h-1。反應前在350 ℃,25% O2/N2(150 mL·min-1)氣氛條件下預處理0.5 h。反應尾氣用紅外線氣體分析儀進行檢測。CO轉化率通過公式(1)計算。
XCO=[CO2]outlet/([CO]outlet+[CO2]outlet)
(1)
式(1)中[CO]outlet和[CO2]outlet分別表示反應尾氣中CO和CO2的濃度。
確定溫度下的反應速率(r)采用公式(2)計算。
(2)
式(2)中,Q表示反應氣流量,XCO表示CO轉化率,m表示催化劑質量。
2 結果與討論
2.1 熱重分析
由于Nano-SnO2樣品在制備的過程中加入CTAB作為模板劑,因此在表征催化劑之前要確認模板劑已完全焙燒脫除。圖1是對于干燥后的水熱產物進行的熱重測試。
從TG/DTA結果可以看出,樣品有2個失量臺階,對應溫度區間分別為200~300 ℃和300~500 ℃。第1個失量臺階失量比例高達30%,此過程應包含脫水和有機物的劇烈燃燒;第2個失量臺階失量比例不到10%,可能是模板劑的完全燃燒脫除。因此在焙燒溫度設定上,采用緩慢升溫,并在300 ℃停留1 h,再緩慢升溫至500 ℃的方法。使催化劑表面的CTAB模板劑得以完全脫除,并且不會在劇烈燃燒的過程中局部過熱導致納米顆粒燒結團聚。
2.2 催化劑結構分析
圖2為SnO2和Nano-SnO2催化劑的XRD衍射譜圖。圖2中SnO2和Nano-SnO2催化劑的衍射峰均可以歸屬為金紅石型SnO2相(JCPDS no.41-1445),未觀察到其他雜相的衍射峰。這表明,通過水熱法也合成出了與沉淀法一樣的金紅石型SnO2。本研究又觀察到Nano-SnO2催化劑的衍射峰變寬,衍射峰變寬表明催化劑的結構對稱性下降了,晶粒尺寸減小了。通過謝樂公式進一步計算得出,Nano-SnO2的晶粒大小約為5.5 nm,而SnO2的晶粒大小在23.1 nm左右。
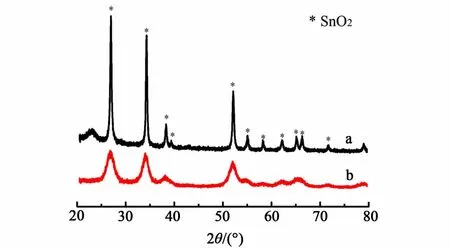
圖2 SnO2 (a)及Nano-SnO2 (b)的XRD譜圖Fig.2 XRD patterns of SnO2 (a) and nano-SnO2 (b)
圖3和圖4分別展示了SnO2和Nano-SnO2催化劑的N2吸附-脫附曲線和BJH孔徑分布曲線。SnO2和Nano-SnO2樣品均表現出了典型的Ⅳ型吸附等溫線。不同的是SnO2樣品的滯后環為H3型,沒有明顯的飽和吸附平臺,孔結構不規整;Nano-SnO2樣品的滯后環為H2型,具有飽和吸附平臺,孔徑分布較均勻,可能為尺寸均一的球形顆粒聚集而成。孔徑分布曲線證實了這點,SnO2樣品的堆積孔徑分布在3.65和11.52 nm處,且分布范圍較寬,孔結構不一致,而Nano-SnO2樣品的堆積孔徑為3.88 nm,分布范圍窄,孔結構相近。表1列出了催化劑的晶粒尺寸和比表面積的具體數值,SnO2的BET比表面積為20 m2·g-1,與文獻[19]報道相一致。Nano-SnO2催化劑的BET比表面積大幅提高,達到了79 m2·g-1,這意味著將有更多的活性位暴露出來,有利于SnO2活性的提高。

表1 催化劑樣品的平均晶粒尺寸和比表面積Table 1 Average grain size and specific surface area of the catalysts
2.3 催化劑形貌分析
圖5a)和圖5b)是SnO2催化劑的TEM圖,圖5c)和圖5d)是Nano-SnO2催化劑的TEM圖。從中可以看出通過水熱法本研究合成出了粒徑均一、分散度良好的SnO2納米顆粒。且Nano-SnO2催化劑的晶粒尺寸明顯小于純SnO2催化劑的晶粒尺寸,這與表1中所列的晶粒尺寸結果相一致。
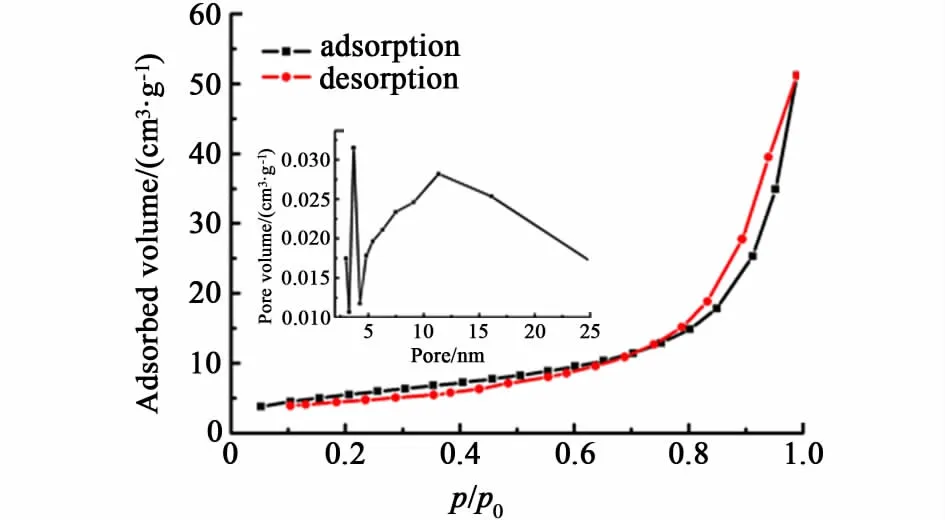
圖3 SnO2的N2吸附-脫附曲線和BJH孔徑分布曲線Fig.3 N2 adsorption-desorption isotherms and BJH pore size distribution of SnO2
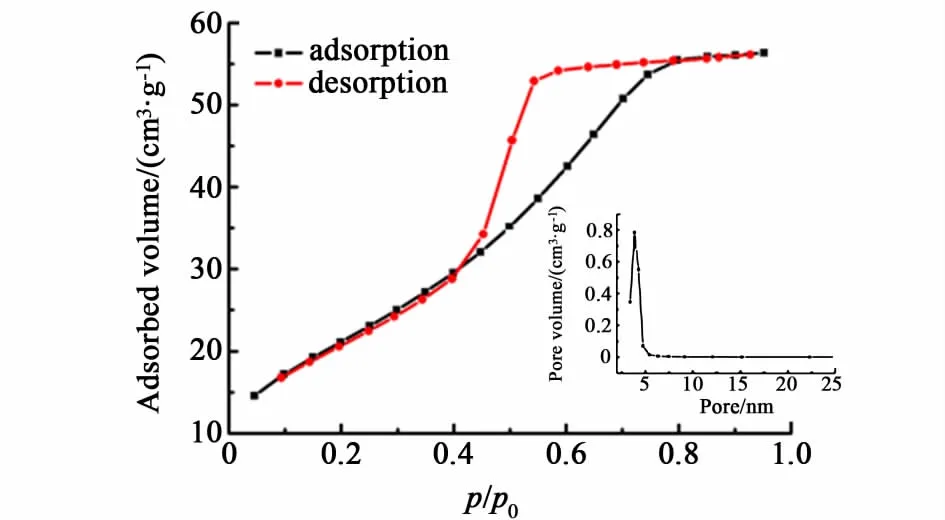
圖4 Nano-SnO2的N2吸附-脫附曲線和BJH孔徑分布曲線Fig.4 N2 adsorption-desorption isotherms and BJH pore size distribution of nano-SnO2
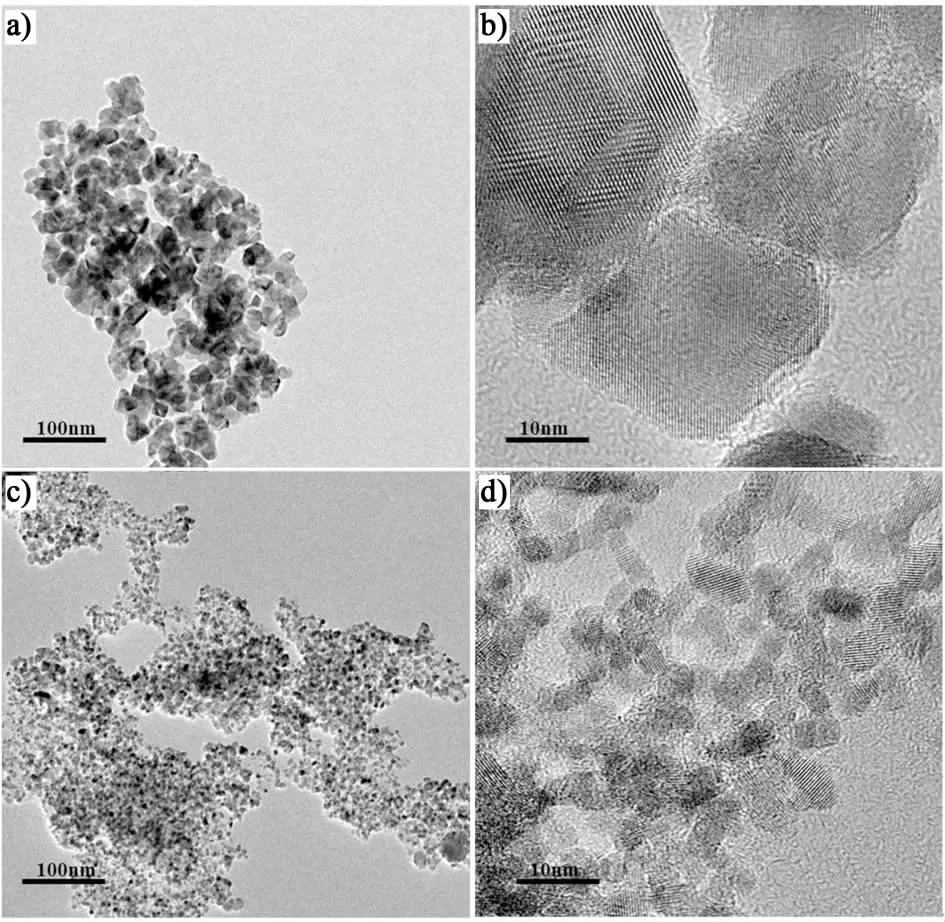
圖5 催化劑樣品的TEM圖片Fig.5 TEM images of catalysts SnO2 (a, b) and nano-SnO2 (c, d)
2.4 催化劑氧化還原能力分析
圖6為催化劑的H2-TPR圖,200~500 ℃的還原峰可被歸屬為表面4價Sn4+到Sn2+的還原,而高溫的還原峰為體相4價Sn4+到Sn2+的還原以及表面的2價Sn2+到Sn0的還原[20]。
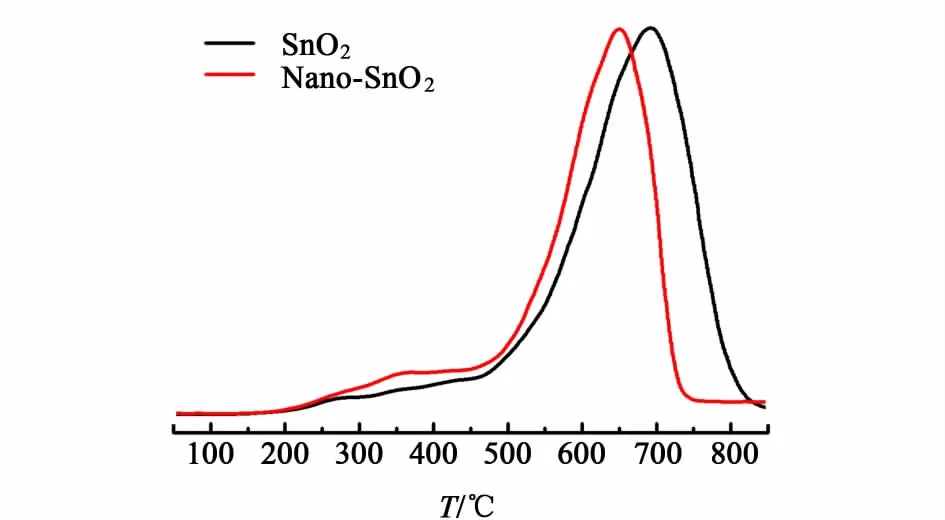
圖6 催化劑樣品的H2-TPR譜圖Fig.6 H2-TPR profiles of the catalysts
從圖6中可以看出,水熱制備的Nano-SnO2催化劑和沉淀法制備的SnO2催化劑的起始還原溫度相同,但低溫峰面積更大,即Nano-SnO2催化劑的表面Sn4+濃度高于SnO2催化劑,原因是前者具有更大的比表面積。Nano-SnO2催化劑高溫的還原峰向低溫方向偏移,可能是由于晶粒尺寸更小,有利于顆粒的還原。
2.5 催化劑CO氧化活性
圖7為催化劑隨反應溫度變化的CO轉化率曲線,由圖7可知兩者T10相差5 ℃,T50相差15 ℃,T90相差35 ℃。由此可以看出相比于沉淀法制備的SnO2催化劑,Nano-SnO2催化劑具有高的表觀催化活性。
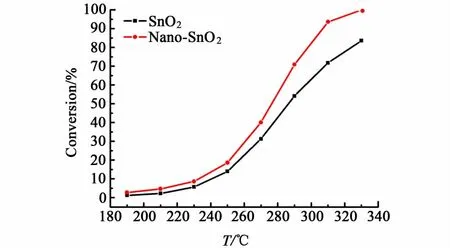
圖7 催化劑樣品的CO轉化率曲線Fig.7 Conversion curves of the CO oxidation via the different catalysts
圖8給出了催化劑的阿倫尼烏斯曲線,并將其表觀活化能(Ea)和指前因子(A)列于表2。如表2所示,相比于傳統SnO2材料,納米SnO2催化劑的活化能從61.3下降到54.2 kJ·mol-1,同時指前因子(A)也由23.2下降到19.4。活化能與催化反應的能壘相關,Ea降低表明在納米SnO2催化劑上CO更加容易發生氧化反應。指前因子(A)和活性位的數量緊密相關[4],之前曾有報道顯示SnO2催化劑的活性晶面是(001)面[21],可能本文所制備的納米顆粒暴露的(001)面比例下降,導致指前因子(A)下降,從而使其單位比表面積的反應速率變小。本研究所報道的納米尺寸SnO2在CO催化氧化過程中活化能降低這一結果,能為其作為催化劑載體材料以及摻雜型復合金屬氧化物催化劑的設計提供重要的理論參考。

表2 表觀活化能和指前因子Table 2 Apparent activation energies (Ea) and pre-exponential factors (A) of the catalysts
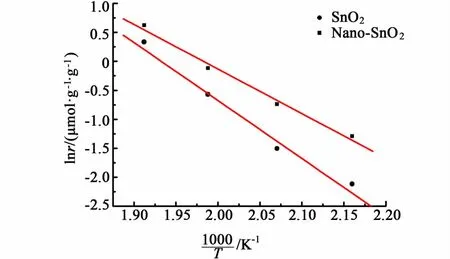
圖8 CO催化氧化的阿侖尼烏斯圖Fig.8 Arrhenius plots of the catalysts upon the CO oxidation
表3比較了文獻報道的SnO2基催化劑的CO催化氧化活性。可以看出,經過摻雜后的SnO2基催化劑的活性較高。而作為單一組分的SnO2催化劑,本研究的實驗結果不低于文獻報道,納米樣品的反應速率甚至接近于Sn-Ce復合金屬氧化物催化劑。
3 結論
以CTAB為模板,SnCl4為錫源,采用水熱法成功合成了粒徑為5 nm的SnO2納米顆粒。所合成的Nano-SnO2催化劑具有高比表面積、均一粒徑、分布均勻等特點。在氧化還原能力方面,低溫峰面積更大,表面Sn4+濃度高于SnO2催化劑,這有利于CO的氧化消除。在隨后的CO氧化性能測試中,Nano-SnO2催化劑的反應活化能比傳統SnO2材料有所下降,表明在納米SnO2催化劑上CO更加容易發生氧化反應。同時指前因子(A)也由23.2下降到19.4,表明納米顆粒暴露的(001)面比例下降。本研究所報道的納米尺寸SnO2在CO催化氧化過程中活化能降低這一結果,能為其作為催化劑載體材料以及摻雜型復合金屬氧化物催化劑的設計提供重要的理論參考。

表3 催化劑的反應速率Table 3 Rates of the catalysts
a反應速率為250 ℃下催化劑的速率;b反應速率為140 ℃下催化劑的速率。
參考文獻:
[1]Raub J A, Benignus V A. Carbon monoxide and the nervous system[J]. Neuroscience & Biobehavioral Reviews, 2002, 26(8): 925-940
[2]Blumenthal I. Carbon monoxide poisoning[J]. Journal of the Royal Society of Medicine, 2001, 94(6): 270-272
[3]Green I X, Tang W, Neurock M,etal. Spectroscopic observation of dual catalytic sites during oxidation of CO on a Au/TiO2catalyst[J]. Science, 2011, 333(6 043): 736-739
[4]Xie X, Li Y, Liu Z,etal. Low-Temperature oxidation of CO catalysed by Co3O4nanorods[J]. Nature, 2009, 458(7 239): 746-749
[5]Lopez N, Janssens T V W, Clausen B S,etal. On the origin of the catalytic activity of gold nanoparticles for low-temperature CO oxidation[J]. Journal of Catalysis, 2004, 223(1): 232-235
[6]Ackermann M D, Pedersen T M, Hendriksen B L M,etal. Structure and reactivity of surface oxides on Pt (110) during catalytic CO oxidation[J]. Physical Review Letters, 2005, 95(25): 255 505.1-255 505.4
[7]Zhang C, Hu P. CO oxidation on Pd (100) and Pd (111): A comparative study of reaction pathways and reactivity at low and medium coverages[J]. Journal of the American Chemical Society, 2001, 123(6): 1 166-1 172
[8]Blume R, H?vecker M, Zafeiratos S,etal. Catalytically active states of Ru (0001) catalyst in CO oxidation reaction[J]. Journal of Catalysis, 2006, 239(2): 354-361
[9]Liu X, Liu J, Chang Z,etal. Crystal plane effect of Fe2O3with various morphologies on CO catalytic oxidation[J]. Catalysis Communications, 2011, 12(6): 530-534
[10]Pan C, Zhang D, Shi L,etal. Template-Free synthesis, controlled conversion, and CO oxidation properties of CeO2nanorods, nanotubes, nanowires, and nanocubes[J]. European Journal of Inorganic Chemistry, 2008, 2008(15): 2 429-2 436
[11]Zhou K, Wang R, Xu B,etal. Synthesis, characterization and catalytic properties of CuO nanocrystals with various shapes[J]. Nanotechnology, 2006, 17(15): 3 939-3 943
[12]Bao H, Zhang W, Hua Q,etal. Crystal-Plane-Controlled surface restructuring and catalytic performance of oxide nanocrystals[J]. Angewandte Chemie International Edition, 2011, 50(51): 12 294-12 298
[13]Kida T, Fujiyama S, Suematsu K,etal. Pore and particle size control of gas sensing films using SnO2nanoparticles synthesized by seed-mediated growth: Design of highly sensitive gas sensors[J]. The Journal of Physical Chemistry C, 2013, 117(34): 17 574-17 582
[14]Chen J, Lou X. SnO2-Based nanomaterials: Synthesis and application in lithium-ion batteries[J]. Small, 2013, 9(11): 1 877-1 893
[15]Hossain M A, Jennings J R, Koh Z Y,etal. Carrier generation and collection in CdS/CdSe-sensitized SnO2solar cells exhibiting unprecedented photocurrent densities[J]. ACS Nano, 2011, 5(4): 3 172-3 181
[16]Wang S, Huang J, Zhao Y,etal. Preparation, characterization and catalytic behavior of SnO2supported Au catalysts for low-temperature CO oxidation[J]. Journal of Molecular Catalysis A: Chemical, 2006, 259(1): 245-252
[17]Roller J M, Yu H, Zhang L,etal. Evaluation of phase segregation in ternary Pt-Rh-SnO2catalysts prepared from the vapor phase[J]. Microscopy and Microanalysis, 2014, 20(S3): 462-463
[18]Baidya T, Gupta A, Deshpandey P A,etal. High oxygen storage capacity and high rates of CO oxidation and NO reduction catalytic properties of Ce1-xSnxO2and Ce0.78Sn0.2Pd0.02O2-δ[J]. The Journal of Physical Chemistry C, 2009, 113(10): 4 059-4 068
[19]Li Y, Peng H, Xu X,etal. Facile preparation of mesoporous Cu-Sn solid solutions as active catalysts for CO oxidation[J]. RSC Advances, 2015, 5(33): 25 755-25 764
[20]Liu C, Xian H, Jiang Z,etal. Insight into the improvement effect of the Ce doping into the SnO2catalyst for the catalytic combustion of methane[J]. Applied Catalysis B: Environmental, 2015, 176: 542-552
[21]Sun Y, Lei F, Gao S,etal. Atomically thin tin dioxide sheets for efficient catalytic oxidation of carbon monoxide[J]. Angewandte Chemie International Edition, 2013, 125(40): 10 763-10 766
[22]Xu X, Liu F, Han X,etal. Elucidating the promotional effects of niobia on SnO2for CO oxidation: developing an XRD extrapolation method to measure the lattice capacity of solid solutions[J]. Catalysis Science & Technology, 2016. DOI: 10.1039/C5CY01870F
[23]Zhang R, Shang J, Zeng X,etal. SnO2promoted by praseodymia: Novel catalysts for CO oxidation[J]. Zeitschrift für Physikalische Chemie International Journal of Research in Physical Chemistry and Chemical Physics, 2012, 226(4): 275-290
[24]Wang X, Tian J, Zheng Y,etal. Tuning Al2O3surface with SnO2to prepare improved supports for Pd for CO oxidation[J]. Chem Cat Chem, 2014, 6(6): 1 604-1 611

