基于SH片段的中國腮腺炎病毒疫苗株與野毒株鑒別方法的建立
肖芳,施勇,李健雄,龔甜,劉師文,熊英
(江西省疾病預防控制中心,江西南昌330029)
·論著·
基于SH片段的中國腮腺炎病毒疫苗株與野毒株鑒別方法的建立
肖芳,施勇,李健雄,龔甜,劉師文,熊英
(江西省疾病預防控制中心,江西南昌330029)
目的研究建立一種簡便快速的鑒別中國腮腺炎病毒疫苗株與野毒株方法。方法在已擴增出的小疏水蛋白基因(small hydrophobic gene)(SH基因)上,尋找能將中國腮腺炎病毒疫苗株區別于野毒株的限制性內切酶酶切位點,并對逆轉錄-聚合酶鏈反應(Reverse Transcription-Polymerase Chain Reaction,RT-PCR)的方法進行特異性實驗證明。結果非腮腺病毒RT-PCR結果均未見陽性條帶,說明RT-PCR方法特異。PCR產物經BclI酶切作用后,腮腺炎野毒株將會被酶切為170bp和340bp兩個片段,而疫苗株則被酶切為270bp和240bp兩個片段。結論新建立的RT-PCR-RFLP是一種快速、簡便的鑒別中國腮腺炎病毒疫苗株與野毒株的方法。
腮腺炎病毒;疫苗株;野毒株;逆轉錄聚合酶鏈反應;限制性片段長度多態性分析
腮腺炎病毒是一種不分節段、單負鏈的RNA病毒,它屬于副粘病毒科腮腺炎病毒屬。腮腺炎病毒基因組結構為:3’N-P-M-F-SH-HN-L-5’,分別編碼以下蛋白:核殼蛋白(N),磷酸化蛋白(P),膜蛋白(M),融合蛋白(F),小疏水蛋白(SH),血凝素神經氨酸酶蛋白(HN)及大蛋白(L)。其中SH基因是整個腮腺炎病毒基因組中變異最大的部分,它常常被用作腮腺炎毒株型別及毒株間同源性分析[1]。2008年,我國將腮腺炎減毒活疫苗納入國家免疫規劃,18~24月齡接種1劑麻疹-腮腺炎-風疹聯合減毒活疫苗或麻疹-腮腺炎聯合減毒活疫苗。2009年江西省將腮腺炎納入擴大免疫規劃項目[2]。現階段,中國使用的腮腺炎疫苗均為減毒活疫苗,且為A基因型,主要是S79株和Jeryl-lynn株[3]。目前,全球發現的腮腺炎病毒有12個基因型,但只有一個血清型[4]。通過血清學檢測無法鑒定腮腺炎病毒的基因型別,也無法區分是疫苗株還是野毒株感染。江西省目前腮腺炎病毒流行株的基因型為F基因型[5],這與中國目前的優勢基因型是一致的[6~9]。大多數國家都是依靠測序后序列分析的方法來鑒定腮腺炎病毒的基因型別及區分疫苗株還是野毒株[10]。但序列分析的方法受條件限制很難廣泛開展,因此建立一種快速簡便易操作的鑒別腮腺炎疫苗株與野毒株的方法非常必要。逆轉錄-聚合酶鏈反應-限制性片段長度多態性分析(Reverse Transcription-Polymerase Chain Reaction-Restriction FragmentLength Polymorphism,RT-PCRRFLP)技術具有簡便、可操作性強、容易推廣的優勢。
1 材料與方法
1.1 材料實驗所使用的流行性腮腺炎(腮腺炎)病毒、麻疹病毒、風疹病毒、流感病毒、水痘病毒均分離于江西省疾病預防控制中心病毒實驗室,麻疹-腮腺炎-風疹聯合減毒活疫苗(Measles,Mumps,Rubella Combined Attenuated Live Vaccine;MMR)(上海生物制品有限公司)為現在江西省預防接種所使用。
1.2 試劑QIAGEN RNeasy Mini Kit(生產批號:151042932);QIAGEN One Step RT-PCR Kit試劑盒(生產批號:151046825);BclI限制性內切酶(New England Biolabs公司,生產批號:6121305)。
1.3 方法
1.3.1 腮腺炎毒株的分離將抗生素處理過的腮腺炎病人咽拭子標本接種于已長成單層的Vero-Slam細胞上,每天觀察細胞病變(CPE),連續觀察7d,當>75%的細胞出現CPE時,凍融后-80℃冰箱保存。未產生CPE的細胞培養物反復凍融,如前培養盲傳3代。
1.3.2 病毒核酸的提取提取所獲得的出現CPE的細胞培養物核酸。取病毒細胞培養液200μl,采用德國QIAGEN公司的RNeasy Mini Kit提取,具體步驟參考產品說明書。
1.3.3 腮腺炎SH基因序列的擴增與測定
1.3.3.1 RT-PCR擴增SH基因及序列測定采用QIAGEN One Step RT-PCR Kit試劑盒對提取的培養物核酸進行MuV SH基因RT-PCR擴增。所用引物序列為[11]:SH 5-1 AATATCAAGTAGTGTCGATGA,SH 5-2 AGGTGCAAAGGTGGCATTGTC。反應條件為:60℃1min,42℃10min,50℃30mim,95℃15min,逆轉錄;94℃變性45s,55℃退火40s,72℃延伸1min,35個循環后,72℃延伸10min[12]。擴增后的PCR產物(約長500bp),經1.5%瓊脂糖凝膠電泳鑒定后,PCR產物送至生工生物工程(上海)股份有限公司測定。
1.3.3.2 序列整理及分子生物學信息分析已測序的序列用DNAStar 5.0的Seqman進行序列的拼接,從GenBank基因數據庫下載MuV各基因型的參考序列進行序列比對分析。采用Mega 4.0軟件進行核苷酸和氨基酸同源性分析、系統進化樹的構建及遺傳距離的分析。
1.3.4 腮腺炎病毒野毒株與疫苗株鑒別RT-PCRRFLP方法
1.3.4.1 酶切反應的條件取上述PCR產物3μl、BclI限制性內切酶(New England Biolabs公司)0.45 μl、10×NEB緩沖液1μl、H2O 5.55μl。對照管為10μl PCR產物。將酶切管與對照管同時置于50℃水浴2h,腮腺炎野毒株將會被酶切為170bp和340bp兩個片段,而疫苗株則被酶切為270bp和240bp兩個片段。見圖1。

圖1 酶切圖譜分析
1.3.4.2 電泳One-step RT-PCR擴增產物及RFLP酶切產物用2%的瓊脂糖凝膠進行電泳檢測后觀察結果。
2 結果
2.1 病毒分離與鑒定咽拭子標本接種到Vero-Slam細胞上經盲傳3代后,90%細胞出現融合病變,經RT-PCR方法鑒定為腮腺炎病毒,分離的腮腺炎毒株在約500bp處有一條清晰的條帶,見圖2。

圖2 RT-PCR結果
2.2 SH基因片段的序列測定結果將所獲得的腮腺炎毒株SH基因的316個核苷酸片段與WHO提供的12個基因型的17株參考株相對應的核苷酸片段構建系統進化樹,結果顯示所分離的腮腺炎毒株與WHO提供的MuV F基因型參考株Z77160-WSH1-CNA96-F、Z77158-WLZ1-CNA95-F最為接近,并形成獨立的分支,故分離株為F基因型。見圖3。
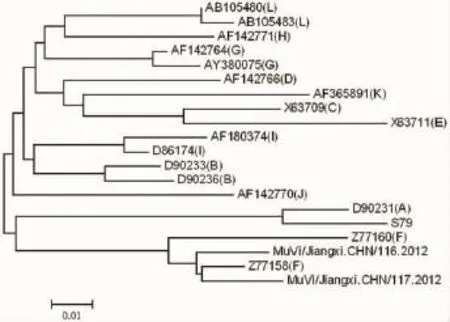
圖3 系統進化樹分析
2.3 腮腺炎病毒特異性檢驗對腮腺炎病毒、麻疹病毒、風疹病毒、流感病毒、水痘病毒進行RNA或DNA提取,經RT-PCR或PCR擴增,腮腺炎病毒核酸擴增為陽性,在500bp處呈現陽性電泳條帶;非腮腺炎病毒的病毒核酸擴增為陰性,與之前預期的結果一致。見圖4。

圖4 腮腺炎病毒特異性檢驗結果
2.4 RFLP方法鑒別腮腺炎野毒株與疫苗株的結果經BclI限制性內切酶酶切后,分離到的腮腺炎病毒野毒株能被該酶切成170bp和340bp兩個片段,而疫苗株則被酶切為270bp和240bp兩個片段,由此來提示該毒株為腮腺炎野毒株。見圖5。

圖5 BclI酶切前后的電泳圖
3 討論
兒童腮腺炎疫苗常規免疫在2008年以麻風腮三聯苗的形式引入中國。如今使用的麻風腮疫苗中的腮腺炎疫苗株為S79株和Jeryl-lynn株。腮腺炎疫苗的使用大大降低了我國腮腺炎病毒的發病率,但也有研究顯示,Jeryl-lynn疫苗株可引起與腮腺炎野毒株類似的中樞神經系統反應[13]。目前中國對MuV未形成系統的監測體系,國內還沒有文獻報道由于接種腮腺炎疫苗導致的腦膜炎,但在國外已有相關的報道[14,15]。因此,在接種腮腺炎疫苗后證明腮腺炎感染是疫苗株還是野毒株導致尤為重要。本研究中,根據我國現有腮腺炎野病毒基因型分布情況,建立了適用于我國的對腮腺炎病毒野毒株與疫苗株RT-PCR-RFLP快速鑒別方法。
小疏水蛋白SH基因在整個腮腺炎病毒的基因組蛋白中變異最大,全長316bp,編碼57個氨基酸,功能尚不清楚,對病毒的復制是一種非必須蛋白,是腮腺炎病毒分型的依據[16]。有一項最新的研究認為SH蛋白可以作為一種信號途徑特異性的阻斷由腫瘤壞死因子-(TNF-)介導的細胞凋亡,是一種涉及逃逸宿主抗病毒反應的膜內蛋白[17]。目前,除了遼寧、福建、陜西在2011年發現了G基因型的腮腺炎病毒外,其余有文獻報道的省份腮腺炎病毒的優勢基因型仍是F基因型[18,19]。所以我們要區別腮腺炎野毒株和疫苗株主要是要區別F基因型與A基因型。許多作者都報道過Urabe株或Jeryl Lynn株的P、F、SH和HN基因處的核苷酸序列與野毒株不同[20-23]。我們在SH基因片段處用RFLP,一種簡單、靈敏的方法從野毒株中區分疫苗株。腮腺炎病毒SH基因的核苷酸變異比較大,為316bp,本研究所利用的一步法RT-PCR具有較好特異性。利用所建立的RFLP方法對分離的MuV株與腮腺炎疫苗株SH片段PCR產物進行BclI酶切作用后,分離到的MuV毒株能被該酶切成170bp和340bp兩個片段,而疫苗株則被酶切為270bp和240bp兩個片段。腮腺炎病毒疫苗株與野毒株鑒別方法的建立,對腮腺炎疫苗納入免疫規劃后腮腺炎樣病例的監測具有實際意義,對科學區分由接種MuV疫苗引起的相關病例和MuV野病毒感染引起的腮腺炎病例具有指導意義。本研究所建立的RT-PCR-RFLP方法是一種快速、簡便,又經濟實用的鑒別MuV株與腮腺炎野病毒株的方法,容易推廣和普及。
[1]Jin L,Beard S,Brown DWG.Genetic heterogeneity of mumps virus in the United Kingdom:identification of two new genotypes[J].J Infect Dis,1999,180(3):829-833.
[2]毛向群,涂秋鳳.2008-2012年江西省流行性腮腺炎監測疫情分析[J].首都公共衛生,2013,7(6):251-253.
[3]崔愛利,金俐,許文波.F基因型腮腺炎病毒全基因組基因特征分析[J].病毒學報,2013,29(6):602-607.
[4]崔愛利.流行性腮腺炎病毒的分子流行病學研究[J].中國計劃免疫,2006,12(6):521-526.
[5]肖芳,施勇,龔甜,等.江西省流行性腮腺炎病毒基因特征分析[J].中國衛生檢驗雜志,2016,26(16):2288-2290.
[6]鄧秀英,馬福寶,陸培善,等.江蘇省流行性腮腺炎病毒的基因特征分析[J].中國衛生檢驗雜志,2015,25(2):229-232.
[7]李平,李月玲,高建中,等.陜西省流行性腮腺炎病毒基因及抗體水平分析[J].中國公共衛生,2010,26(10):1300-1301.
[8]司源,馬鈺,李平,等.2011年陜西省流行性腮腺炎病毒株基因型別分析[J].中華疾病控制雜志,2014,18(2):176-177.
[9]王艷,馬艷,韓悅,等.遼寧省2008~2011年流行性腮腺炎野病毒SH蛋白基因特征分析[J].病毒學報,2012,28(5):506-510.
[10]Forsey T,Mawn JA,Yates PJ,et al.Differentiation of vaccine and wild mumps viruses using the polymerase chain reaction and dideoxynucleotide sequencing[J].J Gen Virol,1990,71(Pt 4):987-990.
[11]崔愛利,朱貞,王常銀,等.中國2006~2008年流行性腮腺炎病毒的基因特征分析[J].中國疫苗和免疫,2009,15(1):8-13.
[12]肖芳,李健雄,周珺,等.2013年-2014年江西省乙型流感病毒HA1基因特性分析[J].中國衛生檢驗雜志,2015,25(17):2943-2946.
[13]Nalin DR.Mumps,measles,and rubella vaccination and encephalitis[J].BMJ,1989,299(6709):1219.
[14]Gray JA,Burns SM.Mumps meningitis following measles,mumps,and rubella immunisation[J].Lancet,1989,2(8654):98.
[15]Murray MW,Lewis MJ.Mumps meningitis after measles,mumps,and rubella vaccination[J].Lancet,1989,2(8664):677.
[16]Jin L,Rima B,Brown D,et al.Proposal for genetic characterisation of wild-type mumps strains:preliminary standardisation of the nomenclature[J].Arch Virol,2005,150(9):1903-1909.
[17]Wilson RL,Fuentes SM,Wang P,et al.Function of small hydrophobic proteins of paramyxovirus[J].J Virol,2006,80(4):1700-1709.
[18]楊秀惠,管輝日,嚴延生,等.福建省一起流行性腮腺炎爆發的病毒分離及基因特征分析[J].中國疫苗及免疫,2013,19(1):43-46.
[19]王艷,馬艷,郝爽,等.遼寧省2008~2014年流行腮腺炎病毒SH和HN基因特征分析[J].病毒學報,2016,32(2):179-184.
[20]Brown EG,Furesz J,Dimock K,et al.Nucleotide sequence analysis of Urabe mumps vaccine strain that caused meningitis in vaccine recipients[J].Vaccine,1991,9(11):840-842.
[21]Forsey T,Mawn JA,Yates PJ,et al.Differentiation of vaccine and wild mumps viruses using the polymerase chain reaction and dideoxynucleotide sequencing[J].J Gen Virol,1990,71(Pt 4):987-990.
[22]Katayama K,Oya A,TanabayashiK,etal.Differentiationof mumps vaccine strains from wild viruses by single-strand conformation polymorphism of the P gene[J].Vaccine,1993,11(6):621-623.
[23]Sugiura A,Yamada A.Aseptic meningitis as a complication of mumps vaccination[J].Pediatr Infect Dis J,1991,10(3):209-213.
The establishment of method for identifying China vaccine strains and wild strains of Mumps virus based on the SH fragment
XIAO Fang,SHI Yong,LI Jianxiong,GONG Tian,LIU Shiwen,XIONG Ying.
Jiangxi Provincial Center for Disease Control and Prevention,Nanchang 330029,China.
Objective To establish a simple and quick method for identifying China vaccine strains and wild strains of Mumps Virus.Methods To search the enzyme site in Small Hydrophobic gene of mumps virus for different domestic vaccine strains and wild strains of mumps virus and then to confirm the specificity of the RT-PCR method,and then to identify the RT-PCR product by RFLP.Results No positive bands can be found in the non-mumps virus strains,it means that the RT-PCR method has good specificity,the PCR products of China mumps vaccine strains of S79 and Jeryl-lynn were all cut into two fragments(270bp and 240bp)by BclI,but mumps wild virus strains were all cut into two fragments(170bp and 340bp)by BclI.Conclusion The RTPCR-RFLP method we established is a rapid and simple method for identifying China vaccine strain and wild strain of mumps virus.
∶Mumps virus;Mumps vaccine virus strain;Mumps wild virus strain;Reverse transcription-polymerase chain reaction;Restriction fragment length polymorphism
R373.1+6,R446.62
A
1674-1129(2017)03-0297-04
2016-10-31;
2017-04-20)
10.3969/j.issn.1674-1129.2017.03.002
江西省衛生廳科技計劃(20111522)
肖芳,女,1984年生,碩士研究生,主管技師,從事病毒檢驗工作,E-mail:181272013@qq.com。
熊英,女,1968年生,碩士研究生,主任技師,研究方向為分子病毒檢測,E-mail:18079125868@163.com。

