兩種麻疹病毒和風疹病毒三重實時熒光RT-PCR檢測試劑應用比較的研究
龔甜,施勇,李健雄,張艷妮,徐剛
(江西省疾病預防控制中心,江西南昌330029)
·實驗研究·
兩種麻疹病毒和風疹病毒三重實時熒光RT-PCR檢測試劑應用比較的研究
龔甜,施勇,李健雄,張艷妮,徐剛
(江西省疾病預防控制中心,江西南昌330029)
目的比較評價兩種含內質控三重實時熒光RT-PCR檢測試劑檢測麻疹病毒和風疹病毒結果的差異。方法對江西省市級麻疹風疹實驗室上送的麻疹病毒或風疹病毒核酸陽性咽拭子標本進行復核,同時用兩種含內質控的麻疹病毒和風疹病毒三重熒光RT-PCR試劑盒檢測,并對檢測結果進行比較分析。結果麻疹病毒和風疹病毒核酸陽性咽拭子標本符合率分別為95.12%和100.00%;兩種試劑檢測麻疹病毒特異度和靈敏度均較好;試劑A和試劑B檢測風疹病毒特異度較好,靈敏度分別為71.43%和100%;試劑A和試劑B檢測人RNase P核酸靈敏度分別為100%和92.73%。結論試劑A在對麻疹病毒核酸檢測方面具有較高的敏感度及特異度,有較高應用和推廣價值。
麻疹病毒;風疹病毒;三重熒光RT-PCR
2013年江西省麻疹風疹實驗室網絡在原血清學診斷網絡基礎上[1],引進了麻疹病毒和風疹病毒熒光RT-PCR檢測技術,并在全省進行推廣,與全國麻疹風疹實驗室網絡同步,建立了麻疹病毒(Measles virus,MV)和風疹病毒(Rubella virus,RV)核酸快速診斷實驗室網絡[2]。本研究使用麻疹病毒和風疹病毒雙重實時熒光RT-PCR商品化檢測試劑對江西省市級麻疹風疹實驗室上送的MV或RV核酸陽性咽拭子標本進行復核,同時為了更有效的監控臨床標本的采樣質量及因操作失誤等所致的假陰性結果出現,本研究還引進余蓓蓓[3]等人關于含使用人RNase P作為內質控的麻疹病毒和風疹病毒三重實時熒光RT-PCR檢測方法,并與國內1種含內質控人RNase P核酸麻疹病毒和風疹病毒三重熒光RT-PCR商品化試劑,同時對上述咽拭子標本進行復核檢測,進行試劑比較研究。現將研究情況分析如下。
1 材料與方法
1.1 標本來源標本主要來自于江西省市級麻疹風疹實驗室根據《全國麻疹監測方案》[4,5]對麻疹風疹疑似病例咽拭子標本進行MV和RV核酸檢測的MV或RV核酸陽性咽拭子標本。其中:MV核酸陽性標本41份,RV核酸陽性標本14份。
1.2 MV和RV核酸檢測
1.2.1 病毒RNA提取取咽拭子標本200μl,采用Qiagen公司的Reansy Mini kit(lot no:145046864)提取病毒RNA,具體操作步驟參照試劑盒說明書。1.2.2 MV和RV雙重熒光RT-PCR商品化檢測試劑麻疹病毒/風疹病毒雙通道核酸檢測試劑盒(PCR-熒光探針法)購自達安基因公司(Lot No:2014003)。相關操作和反應條件按照試劑盒說明書進行。反應在美國ABI熒光PCR儀7500進行。
1.2.3 含內質控MV和RV三重熒光RT-PCR檢測方法
1.2.3.1 本實驗室引進的含內質控MV和RV三重熒光RT-PCR檢測方法引物和探針于上海生工生物工程技術服務有限公司合成,具體序列[3]見表1。

表1 含內質控麻疹病毒和風疹病毒三重熒光RT-PCR檢測引物具體序列表
采用ABI公司生產的AgPath-ID(TM)Onestep RT-PCR Kit(lot no:1407156)進行反應體系配制,命名為試劑A,總體積為25μl,相關操作按照試劑盒說明書進行。反應條件:45℃10min,95℃預變性10min,95℃變性15s,60℃延伸1min,(收集熒光信號),共45個循環。反應在美國ABI熒光PCR儀7500進行。
1.2.3.2 含內質控MV和RV三重熒光RT-PCR商品化檢測試劑麻疹和風疹病毒核酸檢測試劑盒(熒光定量PCR方法)購自國內目前較為常見的公司,命名為試劑B(lot no:20141201)。相關操作和反應條件按照試劑盒說明書進行。反應在美國ABI熒光PCR儀7500進行。
1.3 檢測結果判定根據相關試劑盒說明書判定標準對檢測結果進行判定。
1.4 統計學分析運用SPSS 19.0軟件對研究數據進行分析。
2 結果
2.1 MV和RV雙重熒光RT-PCR檢測方法41份MV核酸陽性標本,檢出39份陽性,陽性符合率均95.12%。RV核酸陽性標本標本14份均為陽性,陽性符合率為100%。
2.2 含內質控MV和RV三重熒光RT-PCR檢測方法
2.2.1 MV核酸檢測結果比較41份MV核酸陽性標本,兩種試劑均檢出39份MV核酸陽性,陽性符合率均為95.12%,兩種試劑檢測結果與MV和RV雙重熒光RT-PCR商品化檢測試劑一致。見表2。

表2 兩種方法檢測MV比較
2.2.2 RV核酸檢測結果比較試劑A均檢出10份RV核酸陽性,陽性符合率均為71.43%;試劑B檢出14份RV核酸陽性,陽性符合率為100%。試劑B檢測結果與MV和RV雙重熒光RT-PCR商品化檢測試劑一致。見表3。

表3 兩種方法檢測RV比較
2.2 人RNase P核酸檢測結果比較試劑A均檢出55份人RNase P核酸陽性,陽性率為100.00%;試劑B檢出51份人RNase P核酸陽性,陽性率為92.73%。見表4。
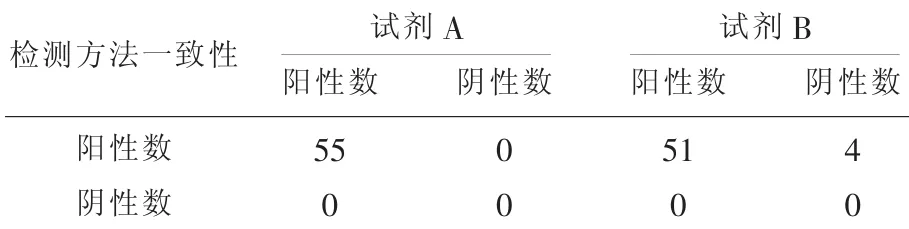
表4 兩種方法檢測RNase P比較
3 討論
MV和RV均可引起急性全身性出疹性呼吸道傳染病[6],二者在臨床癥狀上較難以區分,因此,MV和RV的鑒別主要依賴于特異性的實驗室診斷,尤其是在消除麻疹階段和達到麻疹消除目標期間,由風疹引起的出疹樣病例會更加的凸顯。及時、敏感和特異的病原檢測方法對于麻疹甚至風疹的消除極為重要的。實時熒光RT-PCR是近年發展起來的一項快速、高靈敏度和高特異性的核酸檢測技術,目前,廣泛用于病毒等病原微生物核酸的快速檢測[7-12]。應用實時熒光RT-PCR法能夠及時發現和診斷麻疹,降低麻疹的漏診率,尤其在麻疹疫情處置中能夠在幾個小時內即可得到實驗室確診,為麻疹疫情的處理和控制贏取寶貴的時間[13-15]。
通過上述檢測發現,江西省麻疹風疹實驗室網絡MV和RV核酸陽性咽拭子標本符合率分別為95.12%和100.00%;3份MV核酸陽性咽拭子標本經復核為陰性,可能與原始咽拭子標本核酸量少,經過凍融在進行復核,核酸量降至檢出限有關。由于江西省麻疹病毒和風疹病毒核酸快速診斷實驗室網絡于2013年新建立,因此需要加強對標本采集質量和實驗室網絡質量控制等,為消除麻疹階段病例的早期診斷提供可靠的實驗室證據。
為了避免因人為操作失誤而導致產生假陰性檢測結果[16],本研究引進含使用人RNase P作為內質控的麻疹病毒和風疹病毒多重熒光RT-PCR檢測方法,發現所有標本的人RNase P檢測均為陽性,有效的監控了樣本中的PCR抑制因素以及由操作誤差所造成的假陰性結果;本方法在對麻疹病毒和以人RNase P作為內質控的核酸檢測靈敏度和特異度較好,但在風疹病毒檢測方面靈敏度低于商品化試劑B,而商品化試劑B在對以人RNase P作為內質控核酸檢測方面靈敏度低于本研究引進的方法。另外,本研究引進的方法為實驗室自行合成引物和探針,因此,在檢測費用方面也僅為商品化試劑的一半。
綜上所述,本研究引進的含使用人RNase P作為內質控的麻疹病毒和風疹病毒三重實時熒光RT-PCR檢測方法檢測費用低,在對麻疹病毒和人RNase P核酸檢測具有較高的靈敏度和特異度,具有較高的應用和推廣價值。但是還需要進一步改進提高風疹病毒的核酸檢測靈敏度。
[1]許松濤,張燕,王慧玲,等.中國2012年麻疹/風疹實驗室網絡運轉情況分析[J].中國疫苗和免疫,2014,20(1):62-66.
[2]龔甜,熊英,張艷妮,等.2013年江西省麻疹/風疹實驗室網絡運轉分析[J].現代預防醫學,2015,42(5):841-843.
[3]余蓓蓓,馮燕,徐昌平,等.含內質控多重熒光RT-PCR同時檢測麻疹病毒和風疹病毒的研究[J].病毒學報,2010,26(2):109-114.
[4]中國疾病預防控制中心.全國麻疹監測方案[S].2009.
[5]中國疾病預防控制中心.全國麻疹監測方案[S].2014.
[6]Xiong Y,Wang D,Lin W,et al.Age-related changes in serological susceptibility patterns to measles:results from a seroepidemiological study in Dongguan,China[J].Hum Vaccin Immunother,2014,10(4):1097-2003.
[7]楊鵬飛,燕清麗,張麗萍,等.漢坦病毒通用型實時熒光定量RTPCR方法的建立及應用[J].現代預防醫學,2016,43(2):321-324. [8]許聯紅,岳玉林,王永仿,等.雙重實時熒光RT-PCR法檢測腸道病毒方法的建立及應用[J].重慶醫學,2016,45(33):4688-4690.
[9]唐海淑,杜相品,甫爾哈提·吾守爾,等.脊髓灰質炎病毒實時熒光定量RT-PCR方法的應用與發展[J].國際檢驗醫學雜志,2016,37(18):2603-2605.
[10]周其偉,高秀潔,陳華云,等.H7N9禽流感病毒實時熒光RTPCR檢測方法的建立與評價[J].熱帶醫學雜志,2015,15(1):36-39.
[11]呂莉琨,楊東靖,李力,等.手足口病柯薩奇病毒A2、A4和A5型SYBR GreenⅠ實時熒光定量RT-PCR檢測方法的建立[J].中國病原生物學雜志,2017,12(1):15-19.
[12]劉婷婷,謝芝勛,宋德貴,等.H3N8亞型禽流感病毒實時熒光定量RT-PCR檢測方法的建立及應用[J].畜牧與獸醫,2015,49 (12):84-89.
[13]Michel Y,Saloum K,Tournier C,et al.Rapid molecular diagnosis of measles virus infection in an epidemic setting[J].J Med Virol,2013,85(4):723-730.
[14]高丹,張國斌,賈妮娜.實時熒光RT-PCR法快速檢測麻疹病毒核酸[J].中國衛生檢驗雜志,2015,25(11):1815-1819.
[15]陳玲霞,姬莉莉,孫建飛.麻疹實驗室診斷中ELISA法和實時熒光定量RT-PCR法的比較[J].實用預防醫學,2016,23(1):106-108.
[16]Hwang S,Kang B,Hong J,et al.Development of duplex real-time RT-PCR based on Taqman technology for detecting simultaneously the genome of pan-enterovirus and enterovirus 71[J].J Med Virol,2013,85(7):1274-1279.
Study on the Comparative of two types of triplex real-time RT-PCR detection reagent for measles virus and rubella virus
GONG Tian,SHI Yong,LI Jianxiong,ZHANG Yanni,XU Gang.
Jiangxi Provincial Center for Disease Control and Prevention,Nanchang 330029,China.
Objective A comparative evaluation of two kinds of triplex real-time RT-PCR detection reagents containing internal control for the detection of measles virus and rubella virus.Methods Provincial Measles Laboratory Network measles virus and rubella virus nucleic acid positive throat swab specimens were checked,and two kinds of triplex fluorescence quantitative PCR kits(reagent A and B)were compared.Results Measles and rubella virus nucleic acid positive throat swab specimens coincidence rate were 95.12%and 100.00%;the specificity and sensitivity of both reagents were good;the specificity of reagent A and B for detection of rubella virus were good,and their sensitivity were 71.43%and 100%;the sensitivity of reagent A and B for measuring human RNase P RNA were 92.73%and 100%respectively.Conclusions The reagent A has high sensitivity and specificity in the detection of measles virus nucleic acid,and has high application value.
∶Measles virus;Rubella virus;Three realtime RT-PCR
R446.62,R373.1
A
1674-1129(2017)03-0315-03
2016-08-17;
2017-03-10)
10.3969/j.issn.1674-1129.2017.03.007
龔甜,女,1982年生,碩士,病原生物學,主要從事麻疹病毒等傳染性病毒分子生物學研究。

