采用極差檢驗對比方案評估兩種生化檢測系統檢測結果的可比性
胡志清,徐翠紅
(鄭州大學附屬洛陽中心醫院,河南洛陽471009)
·質量控制·
采用極差檢驗對比方案評估兩種生化檢測系統檢測結果的可比性
胡志清,徐翠紅
(鄭州大學附屬洛陽中心醫院,河南洛陽471009)
目的評估兩種生化檢測系統檢測血清谷丙轉氨酶(ALT)、谷草轉氨酶(AST)、尿素氮(UREA)、肌酐(CREA)、葡萄糖(GLU)的可比性。方法應用極差檢驗比對方案,選取患者血清樣本,分別在Hitachi 7600生化檢測系統、Olympus AU640生化檢測系統進行ALT、AST、UREA、CREA、GLU測定,計算極差(%),以1/3個體生物學變異作為臨界差值可接受標準,判斷兩種檢測系統檢測結果之間的可比性。結果⑴同一質控水平,兩種生化檢測系統測定各項目的變異系數(CV)較大值與較小值之比均<2,符合極差法要求。⑵ALT比對樣本范圍分別為29.6~44.4U/L、106.1~159.1U/L,AST比對樣本范圍分別為29.0~43. 4U/L、119.4~179.0U/L,UREA比對樣本范圍分別為5.9~8.9mmol/L、15.4~23.0mmol/L,CREA比對樣本范圍分別為100.0~150. 0μmol/L、292.1~438.1μmol/L,GLU比對樣本范圍分別為5.6~8.4mmol/L、12.2~18.4mmol/L。⑶血清ALT、AST、UREA、CREA、GLU在低值水平、高值水平的極差(%)均<臨界差值可接受標準。結論兩種生化檢測系統測定血清ALT、AST、UREA、CREA、GLU具有一致性。
極差檢驗;生化檢測系統;可比性;不精密度
目前,大型醫療機構往往存在著多種不同的生化檢測系統,如何保證不同生化檢測系統之間檢測結果的可比性已成為臨床實驗室主任最關心的問題。傳統方法比對試驗采用美國臨床和實驗室標準化研究院(CLSI)的EP9或EP15文件進行,但這兩種方法的試驗設計、數據處理較為復雜,其臨床常規應用受到一定程度的限制。本實驗室以CLSI的C54-A極差檢驗比對方法[1,2]對兩種不同生化檢測系統檢測結果進行了可比性驗證,現報告如下。
1 材料與方法
1.1 儀器和試劑Hitachi 7600全自動生化分析儀和Olympus AU640全自動生化分析儀,使用試劑均為美康生物公司產品。質控品由RANDOX公司購買,低值、高值質控批號分別為1047UN和849UE。
1.2 方法
1.2.1 不精密度估計根據兩種檢測系統近6個月的室內質控變異系數(CV)分別計算兩個質控水平的合成CV,合成CV=[(CVH2+CVO2)/2]1/2,其中CVH代表Hitachi 7600檢測系統近6個月的室內質控
CV
,CVO代表Olympus AU640檢測系統近6個月的室內質控CV。將同一質控水平CVH和CVO進行比較,較大值與較小值之比<2即可以采用極差檢驗比對方案,否則應采用CLSI EP9或EP15文件進行可比性驗證。
1.2.2 確定可接受標準以及樣本重復檢測次數采用1/3個體內生物學變異作為比對試驗臨界差值可接受標準[3],ALT、AST、UREA、CREA、GLU的臨界差值可接受標準分別為6.47%、4.10%、4.03%、1.98%、1.87%。再通過查閱極差檢驗臨界差值(%)表確定樣本重復檢測次數[4]。
1.2.3 確定比對樣本濃度以各水平質控物總均值±20%計算樣本范圍,每個檢測項目在低值和高值水平各選擇1個樣本。
1.2.4 可比性評價按照已確定的重復檢測次數檢測樣本,分別計算總均值、極差、極差(%),極差(%)≤臨界差值可接受標準認為兩種檢測系統的檢測結果具有可比性。
2 結果
2.1 兩種檢測系統不精密度估計以及確定比對實驗重復檢測次數同一質控水平,兩種生化檢測系統測定各項目的CV較大值與較小值之比均<2,符合極差法要求。再查閱極差檢驗臨界差值(%)表,確定極差比對實驗的重復檢測次數。結果見表1。
2.2 確定比對樣本濃度范圍ALT比對樣本范圍分別為29.6~44.4U/L、106.1~159.1U/L,AST比對樣本范圍分別為29.0~43.4U/L、119.4~179.0U/L,UREA比對樣本范圍分別為5.9~8.9mmol/L、15.4~23.0mmol/L,CREA比對樣本范圍分別為100.0~150.0μmol/L、292.1~438.1μmol/L,GLU比對樣本范圍分別為5.6~8.4mmol/L、12.2~18.4mmol/L。結果見表2。
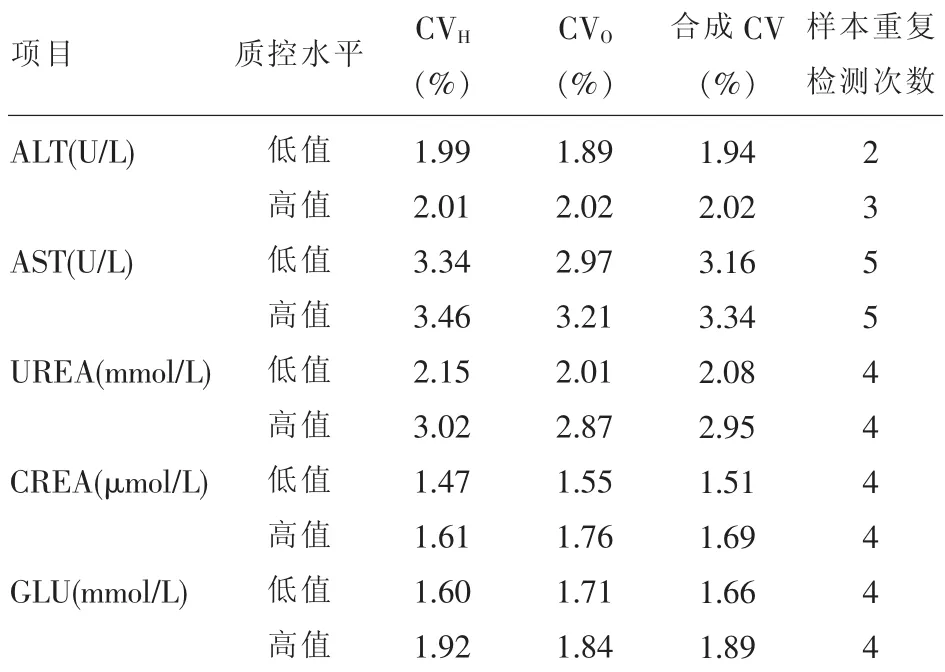
表1 兩種檢測系統不精密度估計以及確定比對實驗重復檢測次數

表2 確定比對樣本濃度范圍
2.3 兩種檢測系統檢測結果的可比性評價血清ALT、AST、UREA、CREA、GLU在低值水平、高值水平的極差(%)均<臨界差值可接受標準。結果見表3。
3 討論
常規生化項目是醫學檢驗最基本的檢驗項目,目前主要由生化檢測系統來完成。隨著醫療機構工作量的增大,很多醫院同時擁有多種生化檢測系統。值得注意的是,不同生化檢測系統的檢測原理、測量程序以及所用檢測試劑可能不同,從而影響同一患者樣本在不同生化檢測系統上的檢測結果的可比性。目前實驗室內不同檢測系統之間的比對方案主要參照EP9指南文件,但是EP9文件在樣本數量要求、濃度水平選擇、數據剔除規則上十分嚴格,且比對過程、數據處理較為繁瑣,不適宜頻繁地開展比對試驗。C54-A指南文件和《臨床檢驗方法確認與性能驗證》一書提出了極差檢驗比對方案,其既可以滿足工作要求,又簡單易行。
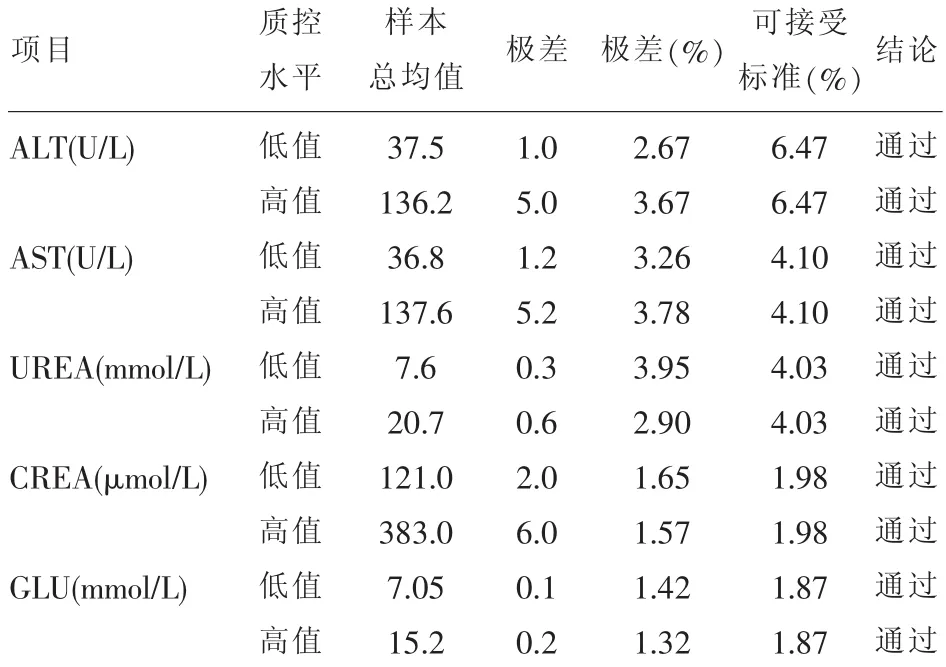
表3 兩種檢測系統檢測結果的可比性評價
極差檢驗比對方案最多可同時進行10種檢測系統之間的比對,且對于每個待評項目,只需分析2個或以上分析物濃度水平,重復檢測次數不超過5次,該方案目前已經在臨床上廣泛使用[5-7]。值得注意的是,極差檢驗比對方案也是有條件的,該方案要求所比對的檢測系統必須通過全面的性能驗證,而且不同檢測系統間同一質控水平CV較大值與較小值之比必須<2。對于極差檢驗比對方案,可接受標準的選擇按優先順序依次為基于臨床結果可比性、基于臨床問卷可比性、基于生物學變異可比性、基于已發表專業推薦的分析性能、基于認可機構設定目標的分析性能和基于一般能力分析性能。不同的實驗室和比對項目可根據實際情況選擇不同級別的接受標準[8-10]。
本實驗室所使用的Hitachi 7600和Olympus AU640全自動生化分析儀每年均由儀器生產商技術人員進行校準、維護和性能驗證,同時,由本實驗室工作人員做好日保養、周保養和月保養,保證機器狀態良好。為保證同一實驗室內檢測結果的一致性,我們按照極差檢驗比對方案對兩種生化檢測系統檢測結果進行了可比性驗證,在沒有基于臨床結果研究和關鍵臨床醫生建議的情況下,優先選擇1/3個體生物學變異作為臨界差值可接受標準。比對結果顯示,ALT、AST、UREA、CREA和GLU在低值水平和髙值水平的極差(%)均小于臨界差值可接受標準,所比對項目在低值、高值兩個水平上檢測結果具有一致性。
[1]CLSI C54-A.Verification of comparability of patient results within one health care system;Approved Guideline[S].CLSI document. Wayne,PA:NCCLS,2008.
[2]王治國.臨床檢驗方法確認與性能驗證[M].北京:人民衛生出版社,2009:319-334.
[3]Bartlett WA,Braga F,Carobene A,et al.A checklist for critical appraisal of studies of biological variation[J].Clin Chem Lab Med,2015,53(6):879-885.
[4]王治國.臨床檢驗方法確認與性能驗證[M].北京,人民衛生出版社,2009:402-403.
[5]吳際,鄭衛東,李廣華,等.不同檢測系統凝血四項結果的可比性驗證[J].臨床輸血與檢驗,2015,17(1):26-29.
[6]趙海建,王萌,張傳寶,等.同一醫院內血清葡萄糖在兩臺不同檢測系統土可比性驗證[J].現代檢驗醫學雜志,2013,13(8):158-159.
[7]羅欲承,陳燕,孫巧蘭.Beckman Coulter LH750與Sysmex XS-1000i血液分析儀檢驗結果的可比性驗證[J].實驗與檢驗醫學,2016,34(5):605-607.
[8]萬臘根,羅東,張才成,等.不同生化分析儀檢驗結查可比性驗證[J].實驗與檢驗醫學,2016,34(3):339-344.
[9]王薇,陸學軍,李少男,等.同一醫院內兩臺凝血分析儀血漿凝血酶原時間的可比性驗證[J].現代檢驗醫學雜志,2011,26(4):114-115.
[10]楊葉子,李俊立.用極差檢驗方案驗證3臺血細胞分析系統血小板計數的可比性[J].國際檢驗醫學雜志,2013,34(20):2741-2742.
R446.11+2
A
1674-1129(2017)03-0354-02
2017-02-28;
2017-04-17)
10.3969/j.issn.1674-1129.2017.03.018

