水中壬基酚殘留檢測方法的研究及其應用
賈林賢++姜蕾++林勇++劉迎++潘波
摘要:建立了固相萃取-高效液相色譜和濁點萃取-高效液相色譜2種方法檢測水溶液中壬基酚,分析了2種方法對水溶液中壬基酚回收率的影響。固相萃取以C18小柱作為固相萃取小柱,5 mL甲醇作為洗脫液進行固相萃取,后經HPLC檢測,回收率可以達到80.28%~82.38%,相對標準偏差為0.40%~4.57%,檢出限為0.9 μg/L。濁點萃取以非離子表面活性劑聚乙二醇-6000(PEG-6000)作為萃取劑,在33 g/L的PEG-6000,溶液pH值為2.0,160 g/L Na2SO4,45 ℃水浴15 min條件下進行濁點萃取,用HPLC檢測。壬基酚的質量濃度在0.02~2.0 mg/L時,其質量濃度與HPLC檢測峰面積呈現良好的線性關系,相關系數為0.999 4,檢出限為0.4 μg/L;壬基酚的萃取率為84.97%~101.64%,相對標準偏差為0.03%~4.40%,符合有機污染物檢出方法要求。通過斑馬魚急性毒性試驗,檢測水中壬基酚含量,證明濁點萃取-高效液相色譜法用于檢測水中壬基酚殘留的方法可行。對比固相萃取,濁點萃取更具發展前景。
關鍵詞:壬基酚;濁點萃取;固相萃取;高效液相色譜法;水
中圖分類號: S481+.8;TQ450.2+64文獻標志碼: A
文章編號:1002-1302(2017)09-0147-04
壬基酚(nonylphenol,簡稱NP)是一種用于合成非離子表面活性劑-壬基酚聚氧乙烯醚(NPEOs)的主要原料,也是其降解產物,廣泛存在于環境介質(水體、土壤、沉積物及大氣)中[1-2];NPEOs作為一種農藥助劑,還廣泛應用于各種農藥制劑中。2001年聯合國環境規劃署已經將NP確定為27種優先控制的持久性有毒污染物之一,歐盟于2013年7月通過了《關于統一各成員國有關限制銷售和使用某些危害物質及制品的法律法規和管理條例》(2003/53/EC),該法規禁止在歐洲地區銷售和使用含量超過0.1%的NPEOs或者NP的產品及其配方產品[3]。我國也在初步探討禁止在農藥制劑中添加或少添加NPEOs[4]。與NPEOs相比,壬基酚較難繼續降解,毒性、親脂性強,易富集,且有促癌作用和內分泌干擾效應[5-8]。壬基酚在水中的溶解度較低,在分析檢測時往往需要進行前處理將其富集。主要的前處理技術有液-液萃取、固相萃取、微波溶出、加速溶劑萃取及超臨界流體萃取等方法[9],檢測方法主要為液相色譜、氣相色譜或者氣-質聯用。
固相萃取(solid phase extraction,SPE)是指使用固體吸附劑將待測組分選擇性吸附或選擇性洗脫達到富集、分離、凈化的一種前處理技術。吸附劑種類、用量、保留體積、流速、洗脫溶劑均是影響固相萃取效率的主要因素。除了傳統的固相萃取技術以外還出現了全自動固相萃取、固相微萃取、磁力攪拌棒吸附萃取、基質分散固相萃取和分子印跡固相萃取等固相萃取技術[10]。固相萃取技術在環境樣品分析檢測中應用廣泛,特別是針對水樣的預處理。固相萃取技術與色譜和質譜等檢測手段的聯用是有機污染物殘留檢測分析的一種重要手段。
濁點萃取法(cloud point extraction,CPE)是一種環境友好型液-液萃取技術,利用表面活性劑作為萃取劑,避免使用揮發性有機溶劑,成本較低且對環境幾乎無危害,可以達到令人滿意的回收提取率和富集效率[11-13]。表面活性劑的分子由非極性基團——疏水基和極性基團或離子基團——親水基組成。水溶液中表面活性劑質量濃度的增加使得疏水基聚集成核,親水基向外張開,從而形成膠束[14]。表面活性劑的溶解度隨著溶液溫度的升高逐漸降低,升至一定溫度后,整個溶液變渾濁,此時的溫度被稱為表面活性劑的濁點(cloud point,CP)。表面活性劑的水溶液在靜置或離心后可以得到2個分離的透明液相:表面活性劑相(或束膠相)和水相。表面活性劑溶液分層時,疏水性物質隨著疏水基進入表面活性劑相,而親水性物質留在水相中,這種通過提升溫度使溶液產生濁點現象,并將樣品中對水具有不同親合性的物質進行分離的方法被稱為濁點萃取法[14]。濁點萃取技術最早應用于金屬離子的檢測[15],近年來濁點萃取技術作為一種前處理技術在有機污染物殘留檢測分析中應用也十分廣泛[16]。
本研究通過建立固相萃取和濁點萃取2種萃取方法回收水中壬基酚,利用高效液相色譜進行檢測,分析2種萃取方法對水中壬基酚回收率的影響,并通過斑馬魚急性毒性試驗驗證濁點萃取-高效液相色譜法的可行性。
1材料與方法
1.1試劑與儀器
壬基酚(異構體混合物)(上海子起生物科技有限公司);甲醇(色譜純)、丙酮(分析純)、乙腈(色譜純)、超純水(18.2 MΩ/cm);曲拉通X-100(Triton X-100)、曲拉通-114(Triton X-114)、聚乙二醇-6000(PEG-6000)、C18小柱、石墨碳黑小柱和石墨碳黑/氨基小柱。
試驗用儀器有Water高效液相色譜儀、菲利普爾超純水儀、超聲儀、固相萃取儀、雷磁pH計。
1.2試驗方法
1.2.1色譜方法
1.2.1.1固相萃取-高效液相色譜法
配制0.02、0.20、2.00 mg/L 的壬基酚水溶液待用。取一固相萃取小柱,用 5 mL 甲醇和5 mL超純水進行預淋洗,加壓抽干,將配制好的壬基酚水溶液5 mL過柱,棄流,再用5 mL甲醇分2次進行洗脫,收集洗脫液,待HPLC檢測。
選擇C18小柱、石墨碳黑小柱和石墨碳黑/氨基小柱3種小柱作為固相萃取小柱,試驗濃度選擇0.02、0.20、2.00 mg/L 的丙酮、甲醇、乙腈作為洗脫液,洗脫液體積為 5 mL,按上述方法進行固相萃取,而后經HPLC檢測。
1.2.1.2濁點萃取-高效液相色譜法
取20 mL水樣于 50 mL 離心管中,加入6.4 g Na2SO4和4.4 mL體積分數為30%的PEG-6000。用90% H2SO4調節溶液pH值至2.0;用水定容至40 mL,振蕩至Na2SO4完全溶解;將離心管放入45 ℃水浴鍋中平衡15 min,3 000 r/min,25 ℃離心5 min;冰水浴5 min,用吸管將表面活性劑相吸出,置于10 mL試管中,用超純水定容至10 mL,待HPLC檢測。
1.2.2色譜條件
色譜柱為Waters-Symmetry C18液相色譜柱,4.6×150 mm,5 μm。流動相水、甲醇、乙腈體積比為 22 ∶70 ∶8。流速0.7 mL/min,進樣量20 μL,發射波長 275 nm,檢測波長308 nm,柱溫25 ℃。
1.2.3不同處理對萃取效果影響
本試驗設計了21~42 g/L PEG-6000;0.5~12 pH值;100、120、140、160、180、200 g/L的Na2SO4;30、40、45、50、55 ℃的平衡溫度,來研究不同處理對水中壬基酚萃取效率的影響。
1.2.4壬基酚對斑馬魚的急性毒性及水中壬基酚含量的檢測
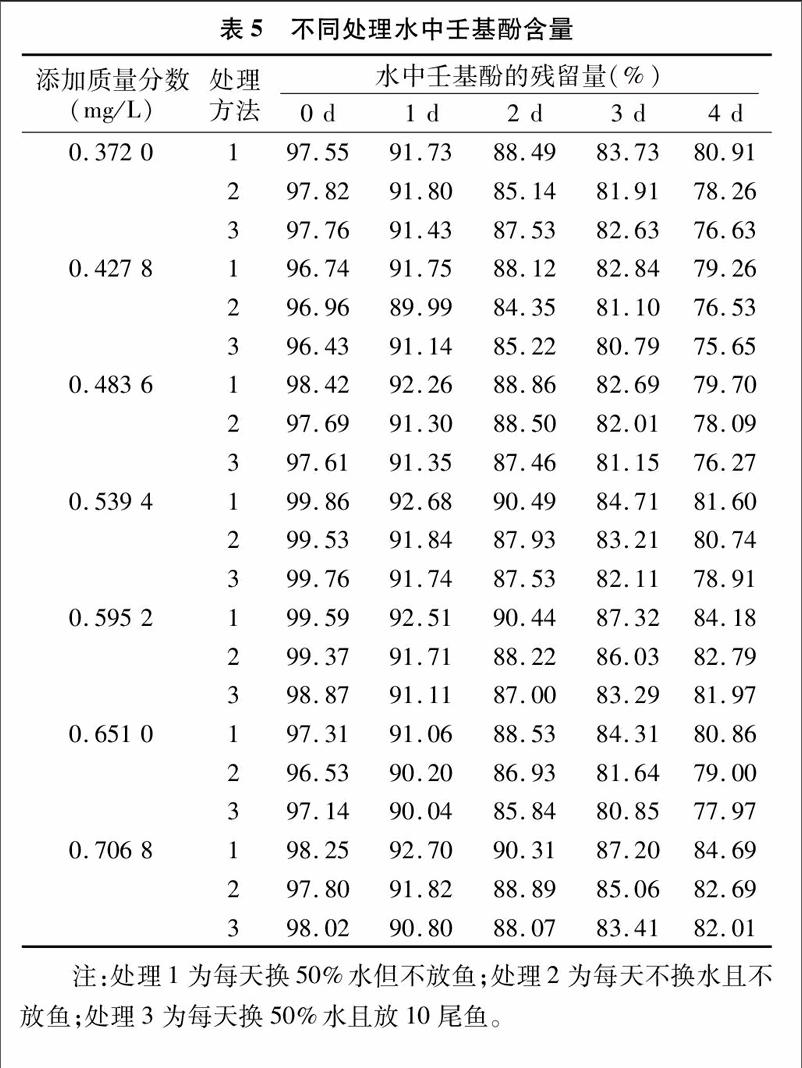
參照《化學農藥環境安全評價試驗準則(征求意見稿)》中斑馬魚急性毒性試驗方法,設置0.372 0、0.427 8、0.492 0、0.565 8、0.650 7、0.748 3、0.860 5 mg/L等7個濃度。另設每天換50%的水但不放魚;每天不換水且不放魚;每天換50%的水放10尾魚3個處理,測定不同壬基酚添加量下,0、1、2、3、4 d壬基酚殘留量。
2結果與分析
2.1洗脫液種類和萃取小柱對固相萃取-高效液相色譜法萃取效果的影響
選擇C18小柱、石墨碳黑小柱和石墨碳黑/氨基小柱3種小柱,使用C18小柱作為固相萃取小柱,5 mL甲醇作為洗脫液進行固相萃取,后經HPLC檢測,回收率達到80.28%~82.38%,相對標準偏差為0.40%~4.57%(表1)。
2.2濁點萃取-高效液相色譜法
根據文獻報道,Triton X-n在紫外區域有較強的吸收,對高效液相色譜-紫外檢測會形成干擾[12,17]。Tween-80濁點較高,在進行濁點萃取時,所需溫度較高,且回收率較低[18]。
而PEG-6000 則不會對高效液相色譜-紫外檢測產生影響,并且其可以作為非離子表面活性劑在一定的條件下完成濁點萃取分相[19]。故本試驗選擇PEG-6000作為濁點萃取的萃取劑按照“1.2.2.2”節的試驗方法對壬基酚進行濁點萃取。
2.2.1不同質量濃度的PEG-6000對萃取效率的影響
表面活性劑的添加量影響富集相體積大小,關系到萃取分離的效果。試驗中隨著萃取體系中PEG-6000質量濃度的增加,壬基酚的回收率呈現先升高后降低的趨勢(圖1)。在21~33 g/L之間,壬基酚的回收率逐漸升高。在33 g/L時,壬基酚的回收率達到最高,為93.10%。隨著PEG-6000濃度的繼續增加,壬基酚的回收率出現下降。引起這種現象的原因可能是由于在21~33 g/L之間,PEG-6000對壬基酚的萃取還未達到飽和。而PEG-6000的質量濃度超過33 g/L時,因其用量過大而對壬基酚有所稀釋,從而降低了壬基酚的回收率。綜上所述,試驗選擇33 g/L的PEG-6000做為萃取濃度。
2.2.2不同pH值對萃取效率的影響
由于被萃取物及所使用的表面活性劑的性質各異,為達到較好的萃取效率,故所需體系pH值也不盡相同。被萃取物與非離子表面活性膠束以疏水分配為主要方式,故調節pH值使得被萃取物保持分子態能取得較好的萃取效率[20]。萃取體系不同pH值對壬基酚[CM(25]的萃取回收效率影響較大(圖2)。試驗結果顯示在溶液pH值2.0時,壬基酚的萃取回收效率最高。這可能是由于溶液處于不同的pH值,壬基酚的電離程度不一樣引起的[14]。
2.2.3鹽濃度對萃取效率的影響
將無機鹽電解質添加到非離子表面活性劑溶液中,可以使得膠束中氫鍵斷裂,進而引起疏水基從水相中脫離,致使濁點降低,并且可以使得目標化合物易于收集[21-22]。Na2SO4的加入會對壬基酚的萃取效果產生顯著影響(圖3)。隨著溶液中Na2SO4質量濃度增加,壬基酚的回收率呈現先上升后下降的趨勢,在160 g/L時達到最大,故本試驗選擇以質量濃度為160 g/L的Na2SO4作為壬基酚濁點萃取的無機鹽添加濃度。
2.2.4不同平衡溫度對萃取效率的影響
不同的平衡溫度對萃取效率影響較大,適當地提高平衡溫度可以通過破壞非離子表面活性劑與水之間的氫鍵作用力,使其發生脫水現象減少萃取相體積[23],增加萃取溶質的分配系數從而提高萃取效率[22]。試驗結果表明,平衡溫度在30~45 ℃之間萃取效率逐漸升高,在45 ℃時達到最高,超過45 ℃后萃取效率逐漸降低(圖4)。故本試驗選擇45 ℃作為壬基酚濁點萃取的平衡溫度。
2.2.5其他條件
膠束與目標提取物的作用需要一定的時間(一般為10~30 min),但時間過長(超過30 min)對萃取效率的影響不大[24-25],故本試驗選擇15 min作為平衡時間。離心的目的是為了讓表面活性劑相和水相進行分離,有研究表明3 000 r/min,15 min即可使得分離達到較好的效果[26-27]。
2.3壬基酚標準曲線及檢出限
將質量濃度系列的壬基酚標準溶液,在“1.2.1”節色譜操作條件下進行HPLC檢測(圖5),繪制出壬基酚水溶液的標準曲線。其線性方程、線性范圍及相關性系數見表2,在002~2.0 mg/L范圍內呈現良好的線性關系(r=0.999 2)。
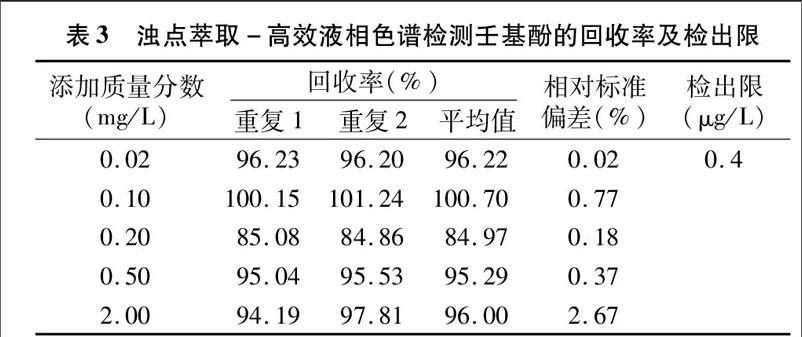
對濃度系列的壬基酚標準樣品進行“1.2.2.2”節濁點萃取操作后,以“1.2.1”節色譜操作條件下測定,檢測回收率、相對標準偏差及檢出限見表3,繪制標準曲線。以信噪比(S/N)=3時所檢測出的壬基酚濃度為儀器檢測限,為 0.4 μg/L。線性方程、范圍及相關系數見表2。
2.4方法評價
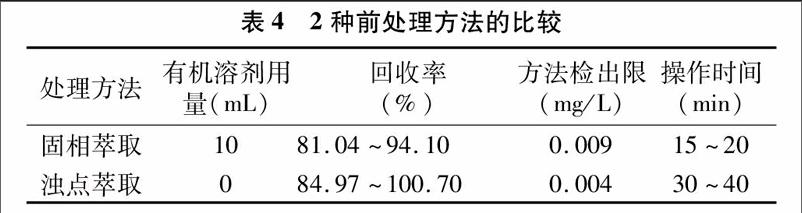
本研究建立了固相萃取法和濁點萃取法2種前處理方法回[CM(25]收水體中壬基酚并使用高效液相色譜進行檢測分析,2種前處理方法的特點、準確度、操作時間及靈敏度比較見表4。
2.5壬基酚對斑馬魚的急性毒性及水中壬基酚含量的檢測
壬基酚對斑馬魚的24、48、72、96 h半數致死濃度分別為0.844 6、0.666 0、0.612 5、0.560 6 mg/L,95%置信區間分別為0.768 6~0.928 1、0.600 4~0.738 3、0.547 3~0.685 4、0.503 5~0.624 1 mg/L,與戴媛媛等的報道結果[28]相近。
按照“1.2.2.2”節的方法,檢測水中壬基酚每天的殘留量。結果顯示水中壬基酚在加藥當天的的回收率為 96.43%~99.85%,證明濁點萃取-高效液相色譜法用于檢測水中壬基酚殘留的方法可行性。同時,隨著時間的推移,水中壬基酚的殘留量逐漸減少,且殘留量的大小關系為每天換50%水放10尾魚(半靜態法)<每天不換水且不放魚<每天換50%水但不放魚(表5),其原因可能為壬基酚在水中會發生降解,且壬基酚富集于沉積物[29]。
3結論
固相萃取-高效液相色譜和濁點萃取-高效液相色譜2種方法都能滿足有機污染物殘留檢測的要求。濁點萃取前處理技術在整個處理過程中不使用揮發性有機溶劑,使用的萃取劑-表面活性劑易于進行后續處理,同時在回收率和檢出限方面也具有比固相萃取前處理技術更好的效果,但是操作時間比固相萃取長。濁點萃取作為一種環境樣品有機污染物殘留檢測的前處理技術有較好的推廣前景。
參考文獻:
[1]Cheng C Y,Wu C Y,Wang C H,et al. Determination and distribution characteristics of degradation products of nonylphenol polyethoxylates in the rivers of Taiwan[J]. Chemosphere,2007,65(11):2275-2281.
[2]張婷瑜,張福金,何江,等. 壬基酚的土壤殘留及其行為研究進展[J]. 農業資源與環境學報,2014,31(2):118-125.
[3]The European Union.Regulation concerning the registration, evaluation,authorization and restriction of chemicals[S]. 2006.
[4]農業部農藥檢定所.農藥助劑禁限用名單[JP3](征求意見稿)[Z]. 2015.
[5]Naylor C G,Staples C A,Klecka G M,et al. Biodegradation of [14C] Ring-Labeled nonylphenol ethoxylate[J]. Archives of Environmental Contamination and Toxicology,2006,51(1):11-20.
[6]夏繼剛,牛翠娟,高穎,等. 壬基酚長期暴露對斑馬魚雄魚第二性征、精子活力的影響[J]. 生態毒理學報,2010,5(1):44-49.
[7]范奇元,金泰,將學之,等. 我國部分地區環境中壬基酚的檢測[J]. 中國公共衛生,2002,18(11):1372-1373.
[8]吳偉,瞿建宏,陳家長,等. 壬基酚聚氧乙烯醚及其降解產物對[JP3]水生生物的毒理效應[J]. 湛江海洋大學學報,2003,23(6):39-44.
[9]張諾,賈瑞寶,孫韶華,等. 壬基酚的檢測及毒理學研究進展[J]. 環境與健康雜志,2013,30(4):362-365.
[10]吳芳華. 固相萃取新技術研究進展[J]. 分析測試技術與儀器,2012,18(2):114-120.
[11]丁昱文. 濁點萃取用于有機磷農藥殘留的檢測[J]. 清華大學學報(自然科學版),2009(3):407-410.
[12]楊遠高,周光明,陳君,等. 濁點萃取石高效液相色譜法測定小兒瀉速停顆粒中多酚類化合物[J]. 分析試驗室,2013,32(3):10-13.
[13]Yildiz Z,Arslan G,Tor A. Preconcentrative separation of chromium(Ⅲ) species from chromium(Ⅵ) by cloud point extraction and determination by flame atomic absorption spectrometry[J]. Microchimica Acta,2011,174(3):399-405.
[14]張慧,許曉菁,楊一青,等. 濁點萃取技術及其應用研究進展[J]. 化工進展,2012,31(S1):441-445.
[15]Watanabe H,Tanaka H. A non-ionic surfactant as a new solvent [JP3]for liquid-liquid extraction of zinc(Ⅱ) with 1-(2-pyridylazo)-2-naphthol[J]. Talanta,1978,25(10):585-589.
[16]李竺,郜洪文,陳玲,等. 固相萃取萃取技術在環境中農藥殘留分析的研究進展[J]. 世界科技研究與發展,2005,27(5):64-71.
[17]王曉中,楊慶鳳. 濁點萃取HPLC法測定穿心蓮中兩種內酯含量[J]. 遼東學院學報(自然科學版),2015,22(3):157-160.
[18]李健華,廖林波. 濁點萃取-氣相色譜法測定水中鄰苯二甲酸酯類化合物[J]. 海峽藥學,2016,28(1):45-48.
[19]姚炳佳. 基于非離子型表面活性劑的新型濁點萃取的研究[D]. 上海:上海交通大學,2008:8-9.
[20]余益軍,孫兆海,鮮放鳴,等. 濁點萃取在環境有機分析中的影響因素及應用[J]. 理化檢驗:化學分冊,2008,44(7):696-700.
[21]孫梅,劉桂建,吳強華. 濁點萃取技術在環境樣品痕量元素分析中的應用研究進展[J]. 環境化學,2013(6):1016-1024.
[22]姜蕾,賈林賢,林靖凌,等. 濁點萃取-超高效液相色譜法檢測水中戊菌唑殘留量[J]. 分析實驗室,2015,34(2):155-158.
[23]Paleologos E K,Giokas D L,Karayannis M I. Micelle-mediated separation and cloud-point extraction[J]. Trac Trends in Analytical Chemistry,2005,24(5):426-436.
[24]馬岳,黃駿雄. 濁點萃取在環境化學方面的應用[J]. 上海環境科學,2000,1(7):319-324.
[25]李燕,張新艷,張曉霞. 濁點萃取-原子吸收光譜法測定水和花粉中痕量銅、鉛、鎘[J]. 環境監測管理與技術,2016,28(3):37-40.
[26]黃海霞,譚雪晴. TritonX-100對廢水中Cd2+、Co2+的濁點萃取研究[J]. 綿陽師范學院學報,2015(2):47-50.
[27]姜蕾,賈林賢,林靖凌,等. 土壤中戊菌唑殘留的分析方法[J]. 農藥,2015,54(3):197-200.
[28]戴媛媛,牛海鳳,董玉波,等. 壬基酚對水生生物的毒性研究進展[J]. 環境與健康雜志,2012,29(10):948-951.
[29]李艷霞,段曉勇,李先國,等. 水中壬基酚光降解機理研究[J]. 化學學報,2012,70(17):1819-1826.

