腎移植術后患者西羅莫司血藥濃度的測定
鄒 靜,肖洪濤,李晉奇,師健友,王 婷
(四川省醫(yī)學科學院·四川省人民醫(yī)院藥學部,四川 成都 610072)
腎移植術后患者西羅莫司血藥濃度的測定
鄒 靜,肖洪濤,李晉奇,師健友,王 婷
(四川省醫(yī)學科學院·四川省人民醫(yī)院藥學部,四川 成都 610072)
目的 建立腎移植術后患者西羅莫司血藥濃度的液相色譜-質譜聯(lián)用(HPLC-MS)測定方法。方法選取服用FK506/CsA+西羅莫司+糖皮質激素三聯(lián)免疫治療的腎移植術后患者20例,采集西羅莫司谷濃度全血樣本,以達那唑為內標,經(jīng)沉淀蛋白及液液萃取處理后,經(jīng)液相色譜分離,采用ESI離子源,以SIR正離子方式進行檢測,檢測離子為m/z 936.76(西羅莫司),m/z 338.26(內標)。同時將所建立的HPLC-MS法和微粒子酶免疫法(MEIA)分別測定腎移植患者全血西羅莫司濃度,評價兩種分析方法測定結果的一致性。結果西羅莫司在0.2~100 μg/L范圍內線性關系良好(r=0.9992),最低定量限為0.2 μg/L。日內、日間精密度均小于6%,方法學回收率為92.93%~102.98%。兩種方法測得的數(shù)據(jù)相關系數(shù)為0.979(P<0.05),兩組數(shù)據(jù)間存在相關性(n=20)。當西羅莫司濃度在1.9~11.1 μg/L時,兩種方法測定的平均偏差為1.4 μg/L。結論本文建立的HPLC-MS測定方法快速、準確、靈敏、選擇性高,適用于臨床對西羅莫司的血藥濃度監(jiān)測;HPLC-MS法和MEIA法測定西羅莫司全血濃度存在相關性,同一份樣本用MEIA測定的濃度均值比HPLC-MS法測定的值高。
西羅莫司;達那唑;高效液相色譜法-質譜聯(lián)用;血藥濃度監(jiān)測;微粒子酶免疫法
西羅莫司(雷帕霉素)是由鏈霉菌屬產(chǎn)生的大環(huán)內酯類抗生素,是一種療效好、低毒、尚未發(fā)現(xiàn)有明顯腎毒性的免疫抑制劑[1],因西羅莫司引起的可逆性副作用,如高脂血癥、白細胞及血小板減少癥、肺炎增加傾向等,在血藥濃度由30 μg/L降至15 μg/L后均有好轉[2],因此當器官移植后出現(xiàn)肝腎功能不全或他克莫司(FK506)、環(huán)孢霉素(CsA)不能達到理想的藥物濃度時,西羅莫司是作為替換治療或輔助治療的最佳選擇之一。
西羅莫司有效血藥濃度范圍窄,其口服生物利用度僅為14%~15%[3],且由于患者疾病狀態(tài)、器官移植類型、年齡、劑量等因素在藥物吸收和代謝上都可能存在個體差異,因此不易估計給藥后的血藥濃度。此外,治療過程中的合并用藥、影響細胞色素P4503 A酶系的藥物都能引起血藥濃度的改變。對大部分患者而言,藥物的療效、毒副作用與血藥濃度成正相關,因此測定個體血藥濃度以調整用藥的劑量和次數(shù)、制定個體化治療方案在臨床上有著至關重要的意義。HPLC法測定西羅莫司濃度的方法已有文獻報道[4~6]。但這些方法中有的采用較為昂貴的LC-MS/MS,有些尚需難以獲得的特殊內標。本文建立用LC-MS法測定SRL的全血藥物濃度,以滿足醫(yī)院對其進行血藥濃度監(jiān)測的日常需求。
1 資料與方法
1.1 一般資料
1.1.1 腎移植術后患者血藥采集 2011年5月~7月選取服用FK506/CsA+西羅莫司+糖皮質激素三聯(lián)免疫治療的腎移植術后患者20例,年齡20~65周歲,處于腎移植穩(wěn)定狀態(tài)。患者口服西羅莫司劑量為1~2 mg/天,1次/天,西羅莫司血藥濃度首次測定可在術后第7~10天后的谷值血藥濃度,第1個月內每周測定1~2次,第2個月每周測定1次,之后每個月測定1次,采血時間為即將服西羅莫司前抽血。
1.1.2 試劑與儀器 西羅莫司測定試劑盒與西羅莫司質控及校準品系列,均為美國Abbott公司提供。Waters 2695高效液相色譜儀(美國 Waters公司),含系統(tǒng)控制器,四元低壓梯度輸液泵,全自動進樣器,柱恒溫箱,MassLynx4.0色譜數(shù)據(jù)工作站;色譜柱為Agilent Zorbax SB-C18(100×2.1 mm,3.5 μm);BP211D電子分析天平(德國沙多利斯公司);IMx分析儀(美國Abbott公司)。甲醇(色譜純,美國Fisher公司),乙腈(色譜純,美國Fisher公司);水為超純水;對照品:西羅莫司對照品(批號:0709022P,純度:99.5%,浙江省藥品檢驗所);內標達那唑(I.S.)對照品(批號:100126-200402,供含量測定用,中國藥品生物制品檢定所)。
1.2 方法
1.2.1 色譜條件 流動相:H2O-乙腈-甲醇 (27:45:28,v/v);流速:0.2 ml/min,柱溫:60 ℃。
1.2.2 質譜條件 電噴霧電離源(ESI+),采用選擇離子監(jiān)測模式同時測定西羅莫司([M+Na]+,m/z 936.76),內標達那唑([M+H]+,m/z 338.26);毛細管電壓3.4 kV;椎孔電壓(西羅莫司72 V,達那唑28 V);二級椎孔電壓2 V;六級桿透鏡電壓0.2 V;源溫度120℃;脫溶劑氣溫度350℃;脫溶劑氣流量700 L/h;錐孔氣流量50 L/h。
1.2.3 溶液、標準曲線和質控樣品的配制 ① 對照品溶液:精密稱取西羅莫司對照品5.03 mg(相當于西羅莫司 5.005 mg),以甲醇溶解,并定容于25 ml容量瓶中,混勻即成西羅莫司儲備液(200.19 mg/L)。取西羅莫司儲備液2.5 ml,以50%甲醇定容于50 ml容量瓶中,即得西羅莫司工作液(10.01 mg/L),置-30℃冰箱儲存?zhèn)溆谩"趦葮巳芤?精密稱取達那唑標準品5 mg,以50%甲醇水溶液溶解,并定容于25 ml容量瓶中,即得內標儲備液(200 mg/L)。取內標儲備液1 ml,以50%甲醇水溶液定容于50 ml容量瓶中,即得內標工作液(4 mg/L),置4℃冰箱儲存?zhèn)溆谩"蹣藴是€的制備:取西羅莫司工作液(10.01 mg/L)0.1 ml,置于10 ml容量瓶中,以空白人全血定容,混勻即得西羅莫司全血濃度100.1 μg/L,再以空白人全血按對倍稀釋,配成各含50.05、20.02、10.01、5.005、2.002、1.001、0.5005、0.2002 μg/L西羅莫司的全血樣品,置-30℃冰箱儲存?zhèn)溆谩"苜|控樣品的配制。精密稱取西羅莫司對照品4.97 mg(相當于西羅莫司4.945 mg),以甲醇溶解,并定容于25 ml容量瓶中,混勻即成西羅莫司儲備液(197.81 mg/L)。取西羅莫司儲備液2.5 ml,以50%甲醇定容于50 ml容量瓶中,即得西羅莫司溶液(9.89 mg/L),取9.89 mg/L的西羅莫司溶液0.08 ml,置于10 ml容量瓶中,以空白人全血定容,混勻即得西羅莫司全血高質控樣品,濃度79.12 μg/L,再按此法配制得西羅莫司中質控樣品(19.78 μg/L),低質控樣品(0.495 μg/L),置-30 ℃ 冰箱儲存?zhèn)溆谩?/p>
1.2.4 樣品預處理 取全血樣品0.1 ml,加入25 μl內標工作液,漩渦混勻,加入5%ZnSO4、丙酮各150 μl,漩渦混勻 6 分鐘后,12000 rpm,6 ℃離心 6 min,轉移上清液于另一潔凈圓底玻璃試管,加入4 ml叔丁基甲醚,漩渦萃取8 min,3000 rpm,6℃離心8 min,轉移上層有機相于另一尖底試管;于(45±5)℃水浴通氮氣流吹干。殘渣加入80%甲醇120 μl旋渦混合1 min,加入環(huán)己烷2 ml旋渦萃取4 min,2200 rpm,6℃離心4 min,吸棄上層有機相,取下層水相10 μl進樣。記錄西羅莫司和內標離子流色譜圖的色譜峰面積,計算西羅莫司和內標的峰面積比,從標準曲線求算樣品中西羅莫司濃度。
1.2.5 方法學考察 ①標準曲線和線性范圍:取標準曲線全血樣品0.1 ml,加入25 μl內標工作液,按照“1.2.4樣品預處理”進行操作,記錄西羅莫司和內標離子流色譜圖的色譜峰面積,以西羅莫司和內標峰面積比對應其濃度進行線性回歸,考察線性。②精密度與回收率試驗:取高、中、低質控樣品各0.1 ml,于同批內連續(xù)測定5次,將記錄峰面積比代入當日線性回歸方程,計算西羅莫司濃度,以測得值與理論加入值之比計算方法學回收率,得到批內精密度與回收率;在不同天連續(xù)分3批每濃度各測定5次,計算批間精密度與回收率。③萃取回收率試驗:按標準曲線方法配制并測定 100.1、10.01、0.495 μg/L三個濃度血樣,每個濃度平行測定3份,所得峰面積與對照品溶液直接進樣所得峰面積進行比較,計算萃取回收率。④基質效應:將高、中、低(79.12、19.78、0.495 μg/L)質控樣品,按“1.2.4樣品處理”操作,進樣得峰面積A1,用相同體積的純水代替空白全血,按“1.2.4樣品處理”操作,記錄色譜圖峰面積A2,將A1與A2相除,即得絕對基質效應。⑤穩(wěn)定性考察:根據(jù)樣品測定過程中可能遇到的不穩(wěn)定因素,實驗先后考察了工作液-20℃保存的穩(wěn)定性;全血樣品在4℃放置7天的穩(wěn)定性,和在-30℃保存0、8、14及30天的穩(wěn)定性;全血樣品反復凍融0、1、2次的穩(wěn)定性;測定樣品處理完后立即進樣與室溫放置4 h后進樣的結果差異。
1.2.6 LC-MS法與MEIA法測定比較 目前,測定西羅莫司血藥濃度的方法主要為免疫法和LC-MS法,因此將所建立的LC-MS法與微粒子酶免疫分析法(MEIA法)對同一樣品的測定結果進行比較,考察兩種測量方法的一致性。對于之前選擇的20例腎移植術后患者,在采集谷濃度血樣時,取其靜脈血樣2~3 ml,立即移入經(jīng)EDTA處理的試管中,充分混勻,平均分為兩份,分別采用LC-MS法和MEIA法進行測定。
MEIA法測定的主要步驟為:精確吸取樣本全血150 μl加入離心管中,精確加入150 μl沉淀劑,振搖10秒,離心5分鐘,轉速10000轉/分,取上清液150 μl置雅培IMx分析儀內,IMX分析儀將自動檢測并打印結果。
1.3 統(tǒng)計學方法采用SPSS 19.0統(tǒng)計軟件,以MEIA法所測的值為X變量,LC-MS法所測的值為Y變量,進行雙變量相關分析,考察測定結果相關性。采用 MedCalc 17.4.4統(tǒng)計軟件,進行 Bland-Altman分析,考察兩個測量方法的一致性。
2 結果
2.1 方法專屬性在選定測定條件下,根據(jù)質譜分析結果,進行SIR監(jiān)測,西羅莫司和內標的m/z分別為936.76和338.26。空白血漿、西羅莫司和內標加空白血漿及血漿樣品色譜圖見圖1~3。空白血漿中內源性雜質和代謝物不干擾西羅莫司及內標物的測定,保留時間分別為3.07 min和7.52 min。
2.2 方法學考察結果西羅莫司全血標準曲線回歸方程:Y=7.63×10-3X+1.55×10-4(r=0.9992,weighting=1/X2)。表明西羅莫司在0.2002~100.1 μg/L范圍內線性良好,最低定量限為0.2002 μg/L,其RSD為6.58%。萃取回收率試驗結果顯示,SRL萃取回收率為53.6%~58.9%。經(jīng)試驗測定計算高、中、低質控樣品中基質效應分別為(97.01±6.52)%、(103.01±5.64)%及(93.0±8.25)%,RSD分別為9.3%、7.7%、11.1%。高、中、低質控樣品精密度與回收率試驗結果見表1。
穩(wěn)定性考察結果顯示,工作液-20℃冷凍保存29 d均能保持穩(wěn)定,滿足測定要求。西羅莫司全血樣品在-30℃保存30 d,西羅莫司濃度結果穩(wěn)定。對比測定凍融0、1、2次的全血樣品以及4℃放置7 d的全血樣品,測定結果表明,在凍融和4℃放置條件下西羅莫司濃度結果穩(wěn)定。對比測定樣品處理完后立即進樣與室溫放置4 h后進樣,測定結果表明,預處理后殘留物復溶后放置4 h西羅莫司測定結果穩(wěn)定。

圖1 LC-MS色譜圖-空白全血 a:總離子色譜圖;b:m/z 338.26色譜圖;c:m/z 936.76色譜圖;1:內標,2:西羅莫司

圖2 LC-MS色譜圖-空白全血加標液 a:總離子色譜圖;b:m/z 338.26色譜圖;c:m/z 936.76色譜圖;1:內標,2:西羅莫司
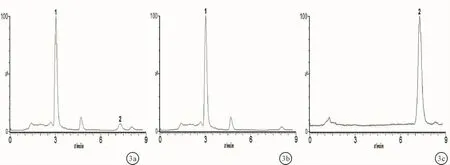
圖3 LC-MS色譜圖-腎移植術后患者口服西羅莫司后全血樣品 a:總離子色譜圖;b:m/z 338.26色譜圖;c:m/z 936.76色譜圖;1:內標,2:西羅莫司

表1 SRL在人全血中的方法學回收率與批內、批間精密度 (n=5)
2.3 統(tǒng)計分析結果雙變量相關分析得出,r=0.979(P<0.05),提示兩組數(shù)據(jù)間存在相關性,回歸方程為Y=0.729X+0.1021。收集的20份樣本濃度在 1.9~11.1 μg/L,相對于 LC-MS,MEIA 的平均百分偏差為32.3%,平均偏差為1.43 μg/L。對兩組數(shù)據(jù)進行Bland-Altman偏差分析,見圖4。結果顯示,同一份樣本用 MEIA測定的濃度均值比HPLC-MS法測定的值高。

圖4 兩種方法測定數(shù)據(jù)的絕對平均偏差
3 討論
因SRL的有效治療濃度范圍較低4~10 μg/L,因此SRL的測定方法必須考慮到檢測靈敏度與分離效果的問題。目前微粒免疫測定法(MEIA)和高效液相色譜-串聯(lián)質譜聯(lián)用法(HPLC-MS/MS)常用來測定西羅莫司血藥濃度,盡管HPLC-MS/MS分離能力好、高靈敏度且快速的儀器優(yōu)勢,但儀器昂貴的價格亦限制了其應用的普遍性,而在進行有效的樣品預處理后,選擇HPLC-MS進行檢測,同樣可以達到HPLC-MS/MS的檢測靈敏度。故本文選擇HPLC-MS法對西羅莫司的血藥濃度進行了測定。
西羅莫司吸收入血后,95%分布于紅細胞內,少部分與血漿脂蛋白結合[7],因此測定西羅莫司 的血藥濃度需用全血。血樣的預處理先必須充分破壞紅細胞,并沉淀蛋白,使西羅莫司從中分離出來,便于提取,隨后還須將全血中的各種內源性雜質進行去除,以避免干擾西羅莫司的測定。固相萃取辦法雖高效、可靠,但成本過高;而直接沉淀蛋白法雖然簡便,但提取物中內源性物質較多,基質效應較高,因此在樣品預處理方法的建立階段,作者參考國內外同行的已報道方法[6,8],并根據(jù)實驗室現(xiàn)有條件,決定采用液液萃取方式處理樣品,同時選擇較易獲取的達那唑作為內標,以提高本方法的通用性。作者對流動性的配比、色譜條件、質譜條件也進行了不斷優(yōu)化,最終確定的流動相、樣品處理方法與質譜條件,進一步提高了本方法的靈敏度。
本研究還比較分析了MEIA與HPLC-MS兩種方法測定結果的差異,并給出兩種方法之間轉換的定量關系,方便臨床醫(yī)生對TDM的結果解讀;同時建立測定全血西羅莫司濃度的LC-MS法,可用于臨床西羅莫司的濃度監(jiān)測。體內西羅莫司主要經(jīng)肝微粒體細胞色素P450酶系代謝為具有結構相似的去甲基化、羥基化成無免疫抑制活性的產(chǎn)物,而臨床藥理學活性主要由西羅莫司母藥產(chǎn)生[9]。MEIA法是非特異性的,可與代謝產(chǎn)物發(fā)生交叉反應,與專門針對母體分子的LC-MS檢測法相比,交叉干擾能夠導致測定結果產(chǎn)生固定的正偏差[10]。本研究結果顯示,MEIA法測定相對于LC-MS測定值明顯偏高,與西羅莫司體內代謝特征及兩種測定方法的原理相符合。
因此本文建立的LC-MS法測定腎移植術后患者西羅莫司血藥濃度快速、準確、靈敏、選擇性高,與Abbott IMx測定西羅莫司的免疫分析法比較均有較好的相關性,但LC-MS法能避免免疫分析方法中交叉免疫所造成的測定值偏高,更適用于臨床對西羅莫司的血藥濃度監(jiān)測,尤其適用于腎移植術后以西羅莫司作為輔助用藥時,西羅莫司血藥濃度較低者的含量測定。
[1]Stepkowski SM,Chen H,Daloze P,et al.Rapamycin,a potent immunosuppressive drug for vascularized heart,kidney,and small bowel transplantation in the rat[J].Transplantation,1991,51(1):22-26.
[2]Hong JC,Kahan BD.Sirolimus induced thrombocytopenia and leukopenia in renal transplant recipients:Risk factors,incidence,progression,and management[J].Transplantation,2000,69:2085-2098.
[3]Kahan BD,Wong RL,Carter C,et al.A phase I study of a 42 week course of SDZ-RAD(RAD)quiescent cyclosporine-prednisone-treated renal transplant recipients[J].Transplantation,1999,68(8):1100-1106.
[4]Panos H,Dietrich AV.Evaluation of a cyano stationary phase for the determination of tacrolimus,sirolimus and cyclosporin A in whole blood by high-performance liquid chromatography-tandem mass spectrometry[J].J Chromatogr B,809(2004):287-294.
[5]時穎華,李中東,施孝金,等.HPLC法測定人全血中西羅莫司的濃度[J].中國臨床藥學雜志,2004,13(2):76-78.
[6]黃明珠,胡興江,陳俊春,等.西羅莫司全血濃度測定方法及臨床應用[J].中國臨床藥理學雜志,2014,30(5):445-447.
[7]Yatscoff RW,Wang P,Chan K,et al.Rapamycin:distribution,pharmacokinetics,and therapeutic range investigations [J].Ther Drug Monit,1995,17(6):666-671.
[8]徐紅冰,胡道德,陳桂良,等.HPLC法檢測腎移植患者全血中西羅莫司的藥物濃度[J].藥學服務與研究,2004,4(2):152-154.
[9]Leung LY,Lim HK,Abell MW,et al.Pharmacokinetics and metabolic disposition of sirolimus in healthy male volunteers after a single oral dose[J].Ther Drug Monit,2006,28:51-61.
[10]Schmid RW,Lotz J,Schweigert R,et al.Multi-site analytical evaluation of a chemiluminescent magnetic microparticle immunoassay(CMIA)for sirolimus on the Abbott ARCHITECT analyzer[J].Clin Biochem,2009,42:1543-1548.
Determination of blood concentrations of sirolimus in patients after renal transplantation
ZOU Jing,XIAO Hong-tao,LI Jin-qi,SHI Jian-you,WANG Ting (Department of Pharmacy,Sichuan Academy of Medical Science & Sichuan Provincial People's Hospital,Chengdu 610072,China)
Objective To develop a HPLC-MS method for determination of blood sirolimus(SRL)concentrations in patients after renal transplantation.MethodsWe selected 20 patients who
a triple immunotherapy of FK506/CsA+Sirolimus+glucocorticoids after rental transplantation.The whole blood samples were collected.To determine the concentrations of SRL,danazol was used as the internal standard(IS),and SRL and IS were separated on a Zorbax SB-C18 Narrow Bore RR(100 × 2.1 mm,3.5 μm)with a mobile phase containing H2O-acetonitrile-methanol(27:45:28,v/v)at a flow rate of 0.2 ml/min and temperature of the column is 60 ℃following protein precipitation and a simple two-step liquid-liquid extraction procedure.The mass spectrometer was operated in the positive ion mode,and selective ion monitors(SIM)were at m/z 936.76([M+Na]+)for SRL and 338.26([M+H]+)for internal stand-ard,respectively.At the same time,a microparticle enzyme immunoassay(MEIA)was also used to determine blood SRL concentrations.The consistency of results by the HPLC-MS method MEIA was analyzed.ResultsCalibration curves were linear(r=0.9992)between 0.2 and 100 μg/L of SRL and the sensitivity was 0.2 μg/L.Intraday and inter-day precision was less than 6%.Analytical recovery ranged from 92.93%to 102.98%.The correlation coefficient of the two methods was 0.979(P<0.05)suggesting a close correlation between the two methods(n=20) .An average deviation of the two methods was 1.4 μg/L when blood SRL concentrations ranging from 1.9 to 11.1 μg/L.ConclusionThe HPLC-MS method described herein had been successfully applied for TDM in adult renal transplant recipients due to its low limits of quantification and stability.There is a correlation between the HPLC-MS and MEIA in determination of blood RSL concentrations.However,the average concentration values of the same sample are higher using MEIA when compared to HPLC-MS method.
Sirolimus;Danazol;HPLC-MS;TDM;MEIA
R965
A
1672-6170(2017)04-0036-05
2017-02-03;
2017-04-03)
2015年四川省人民醫(yī)院青年基金立項資助項目(編號:2015QN05)

