TNF-α多肽抑制劑的合成及初步活性篩選
曹穎男
廣州市中山大學新華學院,廣東廣州 510520
TNF-α多肽抑制劑的合成及初步活性篩選
曹穎男
廣州市中山大學新華學院,廣東廣州 510520
目的 初步探究TNF-R1的胞外區第四功能域CRD4衍生多肽對TNF-α與受體TNF-R1結合過程的影響。方法 以CRD4的部分序列為模板設計衍生小肽片段,采用生物活性酶聯免疫吸附測定法 (BioLISA)觀察所合成的小肽對于TNF-α與其受體TNF-R1結合情況的影響。結果 小肽Pep 3在濃度分別為20,40,60,80,100,120 μM可劑量依賴性抑制TNF-α與其受體TNF-R1的結合;然而肽段Pep 1和Pep 2均未表現明顯的抑制效果。結論 TNF-R1的CRD4的A1模塊衍生小肽Pep 3能夠有效抑制TNF-α與其受體TNF-R1結合,提示該序列所在區域是影響TNF-α與其受體TNF-R1結合的關鍵部位。
TNF-α;TNF-R1;CRD4;短肽;BioLISA
腫瘤壞死因子(Tumor necrosis factor-α,TNF-α)是一種主要由單核細胞/巨噬細胞產生的、具有廣泛生物學活性的細胞因子。在類風濕關節炎,腸炎和感染性休克等疾病的發生、發展中占有很重要的地位[1-2]。TNF-α主要通過與其位于細胞膜上的I型受體(TNF-R1)的細胞外區域結合之后,來啟動其信號通路。TNF-R1的細胞外區域包含四個亞功能域,分別是CRD1(residues15-53),CRD2(residues 54-97),CRD3(residues 98-138)和 CRD4(residues 139-166)。其中CRD1,CRD2和CRD3分別由一個A型模塊和一個B型模塊構成,CRD4不同于其他3個亞功能域,它是由一個A模塊(residues 139-150)和一個結構不規則的C模塊(residues 153-172)構成[3-4]。顯然對于各個亞功能域來說,A模塊是相對保守的結構,極有可能在TNF-α和TNF-R1的結合過程中發揮重要作用,但目前國內外對于CRD4的A模塊在TNF-R1與TNF-α相互識別的過程中所起到的作用鮮有報道。本研究針對于TNF-R1的CRD4區域A模塊設計衍生小肽,檢測其對于TNF-α和TNF-R1的結合的影響。
1 實驗材料
1.1 主要試劑
2-Chlorotrityl chloride樹脂和Fmoc保護氨基酸等購自吉爾生化(上海)公司。人TNF-α和人TNF-α BioLISAkit試劑盒購自奧地利Bender Medsystems公司。短肽S11K和WP9QY由中山大學藥學院卜憲章教授友情饋贈。
1.2 實驗儀器
固相多肽合成反應器,電子分析天平,酶標儀。
2 實驗方法
2.1 多肽的合成及質譜表征
采用Fmoc/tBu法[5]逐步合成小肽。所得肽分子量經ESI-MS質譜分析。
2.2 TNF-αbinding測試
TNF-α以PBS緩沖液稀釋至濃度為20 ng/mL,與等體積的肽溶液混合,配成200 μL反應體系,25℃孵育1 h。以等量的PBS緩沖液及DMSO與TNF-α孵育,分別作為空白對照和溶劑對照。S11K肽和WP9QY肽分別為陰性對照和陽性對照。洗板2次。加100 μL/孔樣品稀釋液至所有的標準品孔內,將孵育后的反應體系50 μL/孔轉移至ELISA板。向各孔內加50μL樣本稀釋液,50 μL Biotin-Conjugate(1:100稀釋),4℃過夜。次日洗板5次。加Strepavidin-HRP(1:100稀釋),25℃孵育1 h。 洗板5次。加入 TMB 底物 100 μL/孔,25℃避光反應 15~20 min。450 nm測吸光度。
3 實驗結果
3.1 衍生小肽的氨基酸序列信息和ESI-MS質譜表征
成功合成3條衍生小肽,樣品的測量值與計算值相符合,表征正確。見表1。
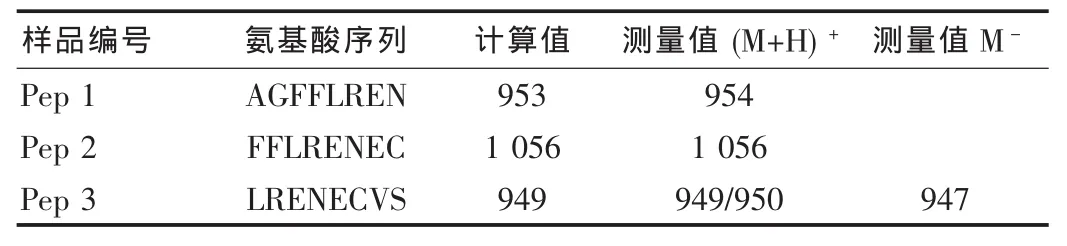
表1 TNF-R1第四區衍生小肽的ESI-MS質譜分析
3.2 衍生小肽的活性篩選
小肽Pep 3顯著抑制TNF-α與TNF-R1的結合,且呈劑量依賴性關系;而Pep 1和Pep 2均未表現出抑制作用。見圖1。
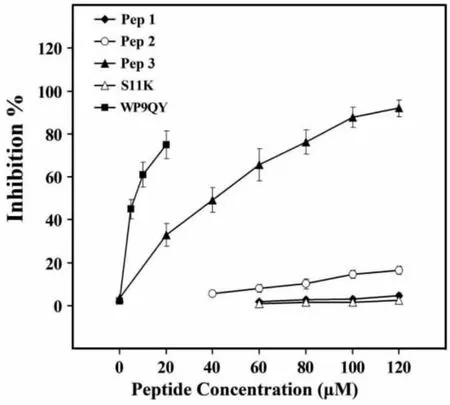
圖1 衍生小肽對TNF-α與TNF-R1結合過程的影響
4 討論
該研究發現TNF-R1的CRD4區域衍生小肽Pep 3(residues145-152)能夠顯著抑制TNF-α和TNF-R1的結合。提示TNF-R1的CRD4的A1模塊區域內能夠影響TNF-α與其受體TNF-R1結合的關鍵作用區域位于Leu145至Ser152之間。有學者發現在TNF-R1上連接CRD3和CRD4的一段區域(residues 130-149)以及CRD4上的一段區域(residues 146-165)都參與了TNF-α和 TNF-R1的結合[6]。這一點與目前的研究結果在部分程度上是一致的。雖然目前尚缺乏關于Pep 3與TNF-α或TNF-R1的作用模式方面的數據,但這并不影響所推測出的結論,那就是:TNF-R1的CRD4區能夠直接參與TNF-α與TNF-R1的結合,從而影響了二者的相互作用。
[1]Kim EY,Moudgil KD.Immunomodulation of autoimmune arthritisbypro-inflammatorycytokines[J].Cytokine,2017(4):12.
[2]Hirano T,Mori Y.Anti-atherogenic and anti-inflammatory properties of glucagon-like peptide-1,glucose-dependent insulinotropic polypepide,and dipeptidyl peptidase-4 inhibitors in experimental animals[J].J Diabetes Investig,2016,Suppl 1:80-86.
[3]Naismith JH,Devine TQ,Kohno T,et al.Structures of theextracellular domain of the type I tumor necrosis factor receptor[J].Structure,1996(4):1251-1262.
[4]Takasaki W,Kajino Y,Kajino K,et al.Structure-based design and characterization of exocyclic peptidomimetics that inhibit TNF alpha binding to its receptor[J].Nat Biotechnol,1997(15):1266-1270.
[5]Merrifield B.Solid phase synthesis[J].Science,1986(232):341-347.
[6]Naismith JH,Devine TQ,Brandhuber BJ,et al.Crystallographic evidence for dimerization of unliganded tumor necrosis factor receptor[J].J Biol Chem,1995(270):13303-13307.
Synthesis and Preliminary Activity Screening of TNF-α Polypeptide Inhibitors
CAO Ying-nan
Xinhua College of Zhongshan University,Guangzhou,Guangdong Province,510520 China
Objective To preliminarily study the effect of fourth functional domain CRD4-derived tripetides in extracellular region of TNF-R1 on the combination course of TNF-α and receptor TNF-R1.Methods The derived tripetide segments were designed by taking some sequences of CRD4 as models and the effect of small peptides on the combination course of TNF-α and receptor TNF-R1 was observed by the BioLISA.Results The concentrations of small peptide Pep 3 were respectively 20,40,60,80,100,and 120 μM,which could inhibit the combination of TNF-α and receptor TNF-R1,but the Pep 1 and Pep 2 had no obvious inhabitation effect.Conclusion The A1 module-derived-small peptide Pep 3 of CRD4 of TNF-R1 can effectively inhabit the combination of TNF-α and receptor TNF-R1,which reminds that the region in which the sequence is located is the key site that can influence the combination of TNF-α and receptor TNF-R1.
TNF-α;TNF-R1;CRD4;Small peptide;BioLISA
R96
A
1672-5654(2017)07(a)-0097-03
2017-04-06)
10.16659/j.cnki.1672-5654.2017.19.097
曹穎男(1983-),女,山東煙臺人,博士,講師,研究方向:藥理學。

