不同醫學營養治療對老年2型糖尿病患者胰島素抵抗的影響
王瑞萍 楊 莉 劉軍平 胡亦偉 婁 建
(延安醫院老年醫學科,云南 昆明 650051)
不同醫學營養治療對老年2型糖尿病患者胰島素抵抗的影響
王瑞萍 楊 莉 劉軍平 胡亦偉1婁 建2
(延安醫院老年醫學科,云南 昆明 650051)
目的探討不同醫學營養治療方法對老年2型糖尿病(T2DM)患者胰島素抵抗的影響。方法將85例T2DM患者按完全隨機分組法分為三組,對照組29例、低血糖生成指數膳食組27例、水溶性膳食纖維組29例,三組均參照中國糖尿病醫學營養治療指南編制糖尿病(DM)膳食食譜,并給予口服降糖藥,低血糖生成指數膳食組早晚餐完全用低血糖生成指數膳食替代,水溶性膳食纖維組在早、晚餐時各添加水溶性膳食纖維10 g。干預期1個月,干預前后觀察各組患者血糖、血脂、腎功能及胰島素抵抗情況。結果與干預前比較,各組干預后血糖均有不同程度下降(P<0.05),低血糖生成指數膳食組及水溶性膳食纖維組干預后胰島素抵抗指標下降(P<0.05)。與對照組比較,干預后低血糖生成指數膳食組和水溶性膳食纖維組胰島素抵抗明顯低于對照組(P<0.05)。結論老年T2DM患者在DM膳食譜及口服藥物治療基礎上,給予低血糖生成指數膳食替代治療或添加水溶性膳食纖維,能有效控制血糖水平,降低胰島素抵抗。
2型糖尿病;醫學營養治療;血糖;胰島素抵抗
研究表明〔1〕,胰島素抵抗在糖尿病(DM)的發生發展中起著極其重要的作用,胰島素抵抗易導致糖脂代謝紊亂。因胰島素介導的葡萄糖利用率降低,一部分老年2型DM(T2DM)患者胰島素敏感性下降,血液中的胰島素增高來補償胰島素抵抗,但胰島素的分泌仍然不足〔2,3〕,藥物治療對血糖水平的控制仍然不佳。為了尋求有效控制老年T2DM患者血糖水平及改善胰島素抵抗同時又安全、易施行的方法,本研究以老年T2DM患者為研究對象,在醫學營養治療指南和口服降糖藥物的基礎上,采用低血糖生成指數(GI,GI值≤45)膳食替代或補充水溶性膳食纖維等方法,觀察血糖控制情況及胰島素抵抗情況。
1 資料與方法
1.1一般資料 選擇2014年1~8月在延安醫院老年病科住院的85例60~80歲老年T2DM患者為研究對象,均符合DM診斷標準并且病程在1年以上,使用口服降糖藥2 w以上近期無藥物調整。排除標準:甲亢、惡性腫瘤、伴糖尿病嚴重并發癥、有嚴重的肝腎功能不全、近期有感染、服用糖皮質激素、依從性差的患者以及不能保證完成治療及觀察時限的患者。所有入選患者均簽署知情同意書。85例患者隨機分為對照組、低GI膳食組、水溶性膳食纖維組。三組患者在年齡、性別、體重、體重指數(BMI)等一般臨床資料比較無統計學差異(P>0.05)。見表1。
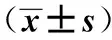
表1 各組一般臨床情況比較
1.2實驗分組與干預 三組均參照中國DM醫學營養治療指南(2011版)編制DM膳食食譜,聯合口服降糖藥,且三組患者在使用口服降糖藥的種類上無差異。在此基礎上,低GI膳食組給予低GI膳食完全替代早、晚餐,水溶性膳食纖維組于早、晚餐各添加水溶性膳食纖維10 g。觀察期為1個月。低GI膳食和水溶性膳食纖維均為購入成品,低GI膳食成品主要成分為抗性淀粉,每100 g所含能量為394 kCal,蛋白質含量18.2 g,脂肪含量5 g,碳水化合物含量69 g,膳食纖維含量8 g。水溶性膳食纖維由低聚木糖、低聚果糖、低聚葡萄糖和膳食纖維組成,含量各占25%。
1.3觀察指標及檢測 入選85例患者干預前后均測量身高、體重,并計算BMI。生化指標包括空腹血糖(FPG)、餐后2 h血糖(2 h-PG)、糖化血紅蛋白(HbA1c)、血清總膽固醇(TC)、血清甘油三酯(TG)、高密度脂蛋白(HDL)、低密度脂蛋白(LDL)、尿素氮(BUN)、肌酐(Cr)、尿酸(UA)。由我院檢驗科采用美國產的AU5421全自動生化分析儀進行檢測。
1.4放免指標檢測 放免指標包括空腹胰島素(FINS)水平。我院放免室采用日本東曹株式會社的試劑盒,采用直接化學發光技術的兩點夾層免疫法檢測。利用FPG和FINS計算內穩態模型評價指數(HOMA-IR)反映胰島素抵抗程度,其計算公式為:HOMA-IR=FPG(mmol/L)×FINS(mIU/L)/22.5。數值越大,胰島素抵抗越大。
1.5統計學方法 采用SPSS17.0統計軟件進行χ2及t檢驗。
2 結 果
2.1三組患者服用不同口服降糖藥的構成情況 各組患者根據病情的不同使用不同口服降糖藥物,其構成比無統計學差異(χ2=0.174,P=1.000)。見表2。
2.2不同醫學營養治療對血糖、血脂、腎功的影響 干預前三組各指標組間比較無顯著差異(P>0.05)。干預1個月后,對照組及水溶性膳食纖維組患者2 h-PG、TG較干預前有改善(P<0.05),而FPG、HbA1c、TC、LDL、HDL干預前后無統計學差異(P>0.05)。低GI膳食組患者FPG、2 h-PG、TC、TG、LDL、HDL均較干預前明顯改善(P<0.05),HbA1c干預前后無統計學差異(P>0.05),與對照組及水溶性膳食纖維組比較,低GI膳食組在干預后FPG、2 h-PG、TC、TG、LDL明顯下降,HDL增高(P<0.05)。三組間干預后HbA1c、BUN、Cr、UA比較無顯著差異(P>0.05)。見表3。
2.3不同醫學營養治療對胰島素抵抗的影響 干預前三組各指標比較無顯著差異(P>0.05)。三組患者中服用胰島素增敏劑+促泌劑及雙胍類藥物的患者,干預后FINS、HOMA-IR較干預前均有下降(P<0.05)。對照組中服用其他藥物患者干預前后FINS、HOMA-IR無明顯變化(P>0.05),而低GI膳食組和水溶性膳食纖維組中服用其他類藥物患者在干預后FINS、HOMA-IR較干預前均有下降(P<0.05)。與對照組比較,低GI膳食組和水溶性膳食纖維組干預后FINS、HOMA-IR下降明顯(P<0.05)。見表4。

表2 各組服用不同口服降糖藥的構成情況(n)
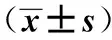
表3 不同醫學營養治療對血糖、血脂、腎功的影響
與本組干預前比較:1)P<0.05;與對照組及水溶性膳食纖維組干預后比較:2)P<0.05
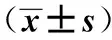
表4 不同醫學營養治療對胰島素抵抗的影響
與本組干預前比較:1)P<0.05;與對照組干預后比較:2)P<0.05
3 討 論
本研究結果表明給糖尿病患者制定膳食譜有助于2 h PG及TG的控制,雙胍類藥物及胰島素增敏劑能改善胰島素抵抗,結論與國內的一些研究報道吻合〔4~6〕。低GI膳食不僅有明顯的降糖協同作用,還能夠降低T2DM患者的血漿纖溶酶原活化抑制因子1的水平,改善纖溶功能〔7〕,有效控制患者脂代謝水平和體重。同時還能增加胰島素敏感性,改善胰島素的抵抗。本研究提示糖尿病患者膳食中添加膳食纖維有助于餐后血糖、血脂的控制,提示改善胰島素抵抗。由于存在胰島素抵抗,肝臟的正常生理活動受到影響,游離脂肪酸和甘油三酯的合成增多從而導致脂代謝紊亂。本研究中低GI膳食的主要成分為抗性淀粉,其在胃腸道內停留的時間長、吸收率低、能抵抗淀粉酶的消化,葡萄糖釋放比較緩慢,因其通過小腸進入大腸后,在結腸微生物作用下發酵釋放出有代謝活性短鏈脂肪酸(乙酸、丙酸、丁酸)〔8〕。短鏈脂肪酸可影響脂肪組織中的脂肪分解,游離脂肪酸的釋放和反調節效應將受到抑制,使血中游離脂肪酸減少,因此攝入低GI膳食可調節脂代謝,使血糖下降,胰島素抵抗得到改善〔9~11〕。水溶性膳食纖維因進入胃腸道后遇水及葡萄糖后,以黏膠形式存在,黏膠對葡萄糖的吸收較為緩慢,避免了進食后血糖的迅速升高,間接起到了控制血糖的作用,水溶性膳食纖維還可以通過吸附腸腔內的膽汁酸來達到降低膽固醇的作用。同時膳食纖維在腸腔內增加了腸內容物的黏稠度,使得油脂的吸收率降低。一些文獻報道,水溶性膳食纖維攝入量的增加可改善DM患者的血脂水平〔12,13〕。因血糖上升緩慢,脂代謝的改善,從而提高了胰島素的利用率,改善胰島素抵抗〔14~16〕。成品低GI膳食替代或者添加水溶性膳食纖維能協助降糖藥物發揮良好的降糖效應,改善胰島素抵抗,且應用低GI膳食替代或者添加水溶性膳食纖維容易施行,使用安全,在控制T2DM血糖、降低胰島素抵抗方面具有很好前景。
1Goldstein BJ.Insunlin resistance as the core defect in type 2 diabetes mellitus〔J〕.Am J Cardiol,2002;90(4):3G-10G.
2潘長玉.糖尿病學〔M〕.第14版.北京:人民衛生出版社,2007:722-3.
3史軼蘩.協和內分泌和代謝學〔M〕.北京:科學出版社,2000:1-311.
4Zenari L,Marangoni A.What are the preferred strategies for control of glycaemic variability in patients with type 2 diabetes mellitus〔J〕?Diabetes Obes Metab,2013;9(2):17-25.
5陳漢輝,盧燕金.二甲雙胍對2型糖尿病胰島素抵抗的療效分析〔J〕.世界最新醫學信息文摘,2014;14(1):187-8.
6韋俊杰.二甲雙胍改善2型糖尿病胰島素抵抗的臨床研究〔J〕.中外醫學研究,2014;12(9):28-9.
7龐曉瑜,郭 卉.胰島素增敏劑與ACEI類藥物治療胰島素抵抗的研究進展〔J〕.中國醫藥科學,2013;3(6):34-6.
8梁 珊.低血糖指數膳食對2型糖尿病患者糖脂代謝的研究〔J〕.糖尿病臨床,2013;5(7):215-7.
9張文青,張月明.抗性淀粉對糖尿病大鼠胰島素抵抗的影響〔J〕.營養學報,2008;30(3):257-61.
10陳開寧,高勇義,黎 藝,等.低血糖指數膳食聯合運動干預對初診2型糖尿病胰島素抵抗的影響〔J〕.重慶醫學,2010;39(5):581-3.
11Janine AH.Resistant starch:metabolic effects and potential health benefit〔J〕.J AOAC Int,2014;87:761-8.
12Linda CT.Diet and metabolic syndrome:where does resistant starch fiftin〔J〕?J AOAC Int,2014;87:756-60.
13Weickert MO,Pfeiffer AF.Metabolic effects of dietary fiber consumption and prevention of diabetes〔J〕.J Nutr,2008;138(3):439-42.
14Chutkan R,Fahey G,Wright WL,etal.Viscous versus nonviscous soluble fiber supplements:mechanisms and evidence for fiber-specific health benefits〔J〕.J Am Acade Nurs Pract,2012;24(8):476-87.
15Yu K,Ke MY,Li WH,etal.The impact of soluble dietary fibre on gastric emptying,postprandial blood glucose and insulin in patients with type 2 diabetes〔J〕.Asia Pacific J Clin Nutr,2014;23(2):210-8.
16Hindy G,Sonestedt E,Ericson U,etal.Role of TCF7L2 risk variant and dietary fibre intake on incident type 2 diabetes〔J〕.Diabetologia,2012;55(10):2646-54.
〔2016-07-16修回〕
(編輯 苑云杰/曹夢園)
R459.3;R587.1
A
1005-9202(2017)18-4518-03;doi:10.3969/j.issn.1005-9202.2017.18.038
1 延安醫院檢驗科 2 延安醫院營養科
王瑞萍(1973-),女,碩士,副主任醫師,主要從事老年病研究。

