子宮內膜癌組織中miRNA-302c的表達變化及其意義
杜寧寧,譚文舉,李洪言,付娟娟
(1安徽省亳州市人民醫院,安徽亳州 236800;2安徽醫科大學第一附屬醫院;3安徽醫科大學第二附屬醫院)
子宮內膜癌組織中miRNA-302c的表達變化及其意義
杜寧寧1,譚文舉1,李洪言2,付娟娟3
(1安徽省亳州市人民醫院,安徽亳州236800;2安徽醫科大學第一附屬醫院;3安徽醫科大學第二附屬醫院)
目的觀察子宮內膜癌組織中miRNA-302c的表達變化,并探討其臨床意義。方法選擇2012年1月~2013年12月收治的51例子宮內膜癌患者的手術切除腫瘤組織標本為觀察組,同期因子宮肌瘤行全子宮切除術的40例患者的正常子宮內膜組織標本為對照組。采用實時熒光定量PCR法檢測兩組標本中的miRNA-302c。分析51例子宮內膜癌患者腫瘤組織標本miRNA-302c相對表達量與臨床病理參數的關系。采用受試者工作曲線和最大約登指數法確定用子宮內膜癌組織標本miRNA-302c表達量預測患者死亡和復發的截斷值,將其用截斷值分為高miRNA-302c表達組和低miRNA-302c表達組,采用Kaplan-Meier法計算并比較高、低miRNA-302c表達組的3年累計生存率和復發率。結果觀察組、對照組miRNA-302c表達量分別為1.721±2.804、4.024±6.518,兩組相比P<0.05。51例子宮內膜癌患者子宮內膜癌組織標本miRNA-302c表達量與臨床分期、分化程度、淋巴結轉移有關(P均<0.05)。用腫瘤組織標本miRNA-302c表達量預測患者死亡的截斷值為1.568,用其將51例子宮內膜癌患者分為高miRNA-302c表達組(miRNA-302c表達量<1.568)30例和低miRNA-302c表達組(miRNA-302c表達量≥1.568)21例,其3年累計生存率分別為96.67%(29/30)、90.47%(19/21),P<0.05。用腫瘤組織標本miRNA-302c表達量預測患者復發的截斷值為1.803,用其將51例子宮內膜癌患者分為高miRNA-302c表達組(miRNA-302c表達量<1.803)24例和低miRNA-302c表達組(miRNA-302c表達量≥1.803)27例,其復發率分別為16.67%(4/24)、29.63%(8/27),P<0.05。結論子宮內膜癌組織miRNA-302c表達降低。檢測子宮內膜癌組織miRNA-302c表達有助于判斷子宮內膜癌的臨床分期、分化程度、淋巴結轉移及預測預后、復發。
子宮內膜癌;微小RNA;微小RNA-302c
子宮內膜癌是臨床上較為常見的女性生殖道腫瘤之一,主要是指原發于子宮內膜的一組上皮性惡性腫瘤[1]。有研究報道顯示,子宮內膜癌為女性生殖道的三大惡性腫瘤之一,其發病率在所有女性腫瘤中位居第四,僅低于大腸癌、肺癌以及乳腺癌[2]。因此,對患者進行早期有效的診斷及治療顯得尤為重要。而明確其具體的發病機制是臨床有效治療的必經途徑[3]。近年來研究報道,在子宮內膜癌的發生、發展過程中,微小RNA(miRNA)表達譜具有顯著的異常[4]。miRNA-302c參與了卵巢癌的發生發展過程[5]。但是目前子宮內膜癌組織中miRNA-302c表達的變化及其臨床意義尚未見研究報道。我們對此進行了研究。
1 資料與方法
1.1 臨床資料 選擇2012年1月~2013年12月收治的51例子宮內膜癌患者的手術切除腫瘤組織標本為觀察組。患者年齡51~74(61.2±4.2)歲。均根據2009年國際婦產科聯盟所制定的子宮內膜癌診斷及分期標準確診,臨床分期Ⅰ期37例,Ⅱ期4例,Ⅲ期5例,Ⅳ期5例;分化程度低分化5例,中分化18例,高分化28例;有淋巴結轉移6例,無淋巴結轉移45例;有肌層浸潤4例,無肌層浸潤47例。患者手術前均未行激素治療及放化療。隨訪3年,臨床及隨訪資料齊全。另取同期因子宮肌瘤行全子宮切除術的40例患者的正常子宮內膜組織標本為對照組,患者年齡53~73(61.3±4.3)歲。兩組患者年齡相比P>0.05。本研究已經醫院倫理委員會批準,入組者均已簽署知情同意書。
1.2 miRNA-302c檢測方法 采用實時熒光定量PCR法。先參照RNAiso Plus試劑盒說明書操作提取總RNA,然后采用Takara公司生產的miRNA專用逆轉錄試劑盒行逆轉錄,反應體系(10 μL)為mRQ Buffer(2×)5 μL,RNA Sample 3.75 μL,mRQ Enzyme 1.25 μL。反應條件為37 ℃ 1 h,85 ℃ 5 min。然后行實時熒光定量PCR。反應體系(20 μL)為SUBR Premix Ex Taq Ⅱ(2×)10 μL,PCR For-ward Primer(10 μmol/L)0.8 μL,PCR Reverse Primer(10 μmol/L)0.8 μL,R0X Reference Dye Ⅱ(50×)0.4 μL,DNA2.0 μL,ddH2O 6.0 μL。反應條件:95 ℃ 30 s,95 ℃ 3 s,61 ℃ 30 s,重復40個循環。以U6為內參照,采用2-△△Ct表示miRNA-302c表達量。
1.3 子宮內膜癌組織miRNA-302c表達與子宮內膜癌預后和復發的關系分析方法 繪制用子宮內膜癌組織標本miRNA-302c表達量預測患者死亡和復發的受試者工作曲線,用最大約登指數法確定截斷值,據此將子宮內膜癌患者分為高、低miRNA-302c表達組,比較3年累計生存率和復發率。
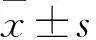
2 結果
2.1 兩組miRNA-302c表達量比較 觀察組、對照組miRNA-302c相對表達量分別為1.721±2.804、4.024±6.518,兩組相比P<0.05。
2.2 子宮內膜癌組織miRNA-302c表達與子宮內膜癌臨床病理參數的關系 見表1。子宮內膜癌患者子宮內膜癌組織標本miRNA-302c表達量與臨床分期、分化程度、淋巴結轉移有關(P均<0.05),與肌層浸潤無關(P>0.05)。
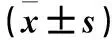
表1 子宮內膜癌組織miRNA-302c表達與子宮內膜癌臨床病理參數的關系
2.3 子宮內膜癌組織miRNA-302c表達與子宮內膜癌預后和復發的關系 用子宮內膜癌組織標本miRNA-302c表達量預測患者死亡的截斷值為1.568,用其將51例子宮內膜癌患者分為高miRNA-302c表達組(miRNA-302c表達量<1.568)30例和低miRNA-302c表達組(miRNA-302c表達量≥1.568)21例,其3年累計生存率分別為96.67%(29/30)、90.47%(19/21),P<0.05。用子宮內膜癌組織標本miRNA-302c表達量預測患者復發的截斷值為1.803,用其將51例子宮內膜癌患者分為高miRNA-302c表達組(miRNA-302c表達量≥1.803)24例和低miRNA-302c表達組(miRNA-302c表達量<1.803)27例,其復發率分別為16.67%(4/24)、29.63%(8/27),P<0.05。
3 討論
子宮內膜癌占所有女性生殖道惡性腫瘤的20%~30%,且隨著我國人們生活水平的不斷改變以及生活習慣的逐漸變化,該病發病率正呈逐年上升趨勢,甚至開始趨于年輕化,嚴重影響了我國婦女的身心健康[6,7]。雖然大部分子宮內膜患者均存在顯著的臨床癥狀,可得到早期有效的診斷以及治療,但仍有部分患者在就診時便已是晚期。由此,子宮內膜癌的早期發現以及治療對改善疾病預后以及延長患者生存時間具有極其重要的意義[8]。近年來隨著人們對miRNA分子的作用以及機制了解的逐漸深入,其已成為臨床研究腫瘤發生、發展的熱點[9,10]。miRNA是由22~25個核苷酸組成的一種非編碼單鏈小RNA,其主要作用是通過和靶基因mRNA產生作用,從而使得其在轉錄后的翻譯過程中受到抑制或被降解,進一步降低了其蛋白表達水平,最終在多項生命過程中發揮至關重要的作用[11,12]。有研究報道顯示,miRNA-302c會對細胞周期產生一定影響,同時在染色體結構的形成以及p63基因的蛋白、mRNA表達方面均具有一定的作用[13,14]。國內外已有研究報道顯示,miRNA-302c在多種惡性腫瘤中具有抑制腫瘤細胞增長殖的作用。
本研究結果顯示子宮內膜癌組織中miRNA-302c表達低于正常子宮內膜組織。這提示miRNA-302c表達下調與子宮內膜癌有關。安琪等[15,16]研究顯示,miRNA-302c在肝癌細胞中發揮的作用是通過抑制異黏蛋白的表達,從而對內皮-間充質轉化產生一定的抑制作用,進一步對肝癌細胞的生長繁殖產生明顯的抑制作用。周胤健等[17,18]研究證實,乳腺癌細胞中miRNA-302c可有效抑制下游基因ERα表達。結合本研究結果,筆者認為在子宮內膜癌組織中,miRNA-302c也可能是通過與靶基因的結合,從而達到抑制腫瘤生長繁殖的目的。
本研究結果顯示,臨床分期Ⅰ期者子宮內膜癌組織miRNA-302c表達量高于Ⅱ~Ⅳ期者,低分化子宮內膜癌組織miRNA-302c表達量低于中、高分化患者,有淋巴結轉移的子宮內膜癌組織miRNA-302c表達量低于無淋巴結轉移者。表明miRNA-302c與子宮內膜癌的臨床分期、分化程度及淋巴結轉移有關,且miRNA-302c可能發揮類似抑癌基因的作用。王穎等[19,20]認為,腫瘤細胞中miRNA-302c可直接或間接發揮抑癌基因的作用,并以此對腫瘤細胞的增殖、分化以及凋亡進行調節,參與了腫瘤的發生、發展、侵襲以及轉移。本研究結果與其相似。這提示我們檢測子宮內膜癌組織miRNA-302c表達有助于判斷子宮內膜癌的臨床分期、分化程度、淋巴結轉移。目前對于miRNA-302c如何調控細胞的增殖、分化以及凋亡仍不清楚,可以確定的是miRNA-302c可以通過與多種癌基因的3′非編碼區片段結合,從而阻斷基因的表達,但哪些基因是miRNA-302c的作用靶點仍不清楚,而研究其作用機制將是我們今后研究的重點,這有利于為子宮內膜癌的早期診斷以及有效治療。
本研究結果顯示,子宮內膜癌組織miRNA-302c表達與患者預后和復發有關,miRNA-302c表達相對較低者復發較多,預后不佳。這進一步證明miRNA-302c在子宮內膜癌組織中具有類似抑癌基因的功能。檢測子宮內膜癌組織miRNA-302c有助于判斷子宮內膜癌組織的預后和復發情況,具有重要的臨床意義。
[1] 張鳳仙,張建,陳素蕓,等.18F-FDG PET/CT顯像SUVmax對子宮內膜癌術前浸潤及轉移的評估價值[J].中華核醫學與分子影像雜志,2017,37(2):75-80.
[2] 孔祥怡.微小RNA與子宮內膜癌關系的研究進展[J].現代婦產科進展,2013,22(10):843-845.
[3] Wilczynski M, Danielska J, Dzieniecka M, et al. Prognostic and clinical significance of miRNA-205 in endometrioid endometrial cancer[J]. PLoS One, 2016,11(10):164687-164688.
[4] Alowayed N, Salker MS, Zeng N, et al. LEFTY2 controls migration of human endometrial cancer cells via focal adhesion kinase activity (FAK) and miRNA-200a[J]. Cell Physiol Biochem, 2016,39(3):815-826.
[5] Dong P, Ihira K, Xiong Y, et al. Reactivation of epigenetically silenced miR-124 reverses the epithelial-to-mesenchymal transition and inhibits invasion in endometrial cancer cells via the direct repression of IQGAP1 expression[J]. Oncotarget, 2016,7(15):20260-20270.
[6] 饒云霞.子宮內膜癌患者血清 HE4、CP2、HCgp-39含量與腫瘤惡性程度的關系探究[J].海南醫學院學報,2017,23(4):444-447.
[7] 葉文蔚,鄭飛云,程愛花,等.miR-205對Ⅱ型子宮內膜癌細胞生物學行為的調空作用研究[J].醫學研究雜志,2016,45(7):47-51.
[8] 張金霞,林明燕,林亞,等.miR-34c抑制人子宮內膜癌的機制分析[J].中華全科醫學,2016,14(8):1282-1285.
[9] 李飄飄,包珊.子宮內膜癌中miRNA與自噬的研究進展[J].海南醫學,2014,25(21):3201-3203.
[10] 王淑芳,馮玉珍,霍新龍,等.MicroRNA在子宮內膜癌發生、發展及臨床診治中的研究[J].中國醫藥導報,2013,10(6):30-32.
[11] 楊艷.食管癌相關微RNA研究進展[J].腫瘤研究與臨床,2017,29(2):129-133.
[12] 孔祥怡,周懷君.miRNA-30c及其靶基因MTA-1在子宮內膜癌裸鼠皮下移植瘤中的作用[J].東南大學學報(醫學版),2016,35(3):364-370.
[13] 李華偉,張哲.miR-302a在胃癌中表達及其對胃癌細胞凋亡與細胞周期影響[J].臨床軍醫雜志,2017,45(1):42-45.
[14] Gui J, Yan F, Yu B, et al. MicroRNA miR-302?inhibits the tumorigenicity of endometrial cancer cells by suppression of Cyclin D1 and CDK1[J]. Cancer Lett, 2014,345(01):39-47.
[15] 安琪,馬曉欣.miRNA-302 c在子宮內膜癌組織中的表達及其與臨床病理資料的關系[J].現代腫瘤醫學,2017,25(1):127-130.
[16] 李寶恒,宋巖峰.microRNA在婦科疾病中的作用[J].中華臨床醫師雜志(電子版),2016,10(6):844-848.
[17] 周胤健,杜英,梅麗娜,等.子宮內膜癌microRNA表達譜的初步研究[J].中華實驗和臨床病毒學雜志,2014,28(4):280-282.
[18] Zhou C, Gu HF, Rong T, et al. MicroRNA 302/367 cluster effectively facilitates direct reprogramming from human fibroblasts into functional neurons[J]. Stem Cells Dev, 2015,24(23):2746-2755.
[19] 王穎,阿迪拉·斯依提,張曉明,等.子宮內膜癌微小RNA的表達特點及其臨床意義[J].中華病理學雜志,2014,43(2):88-94.
[20] 劉霞,夏偉,邵寧生,等.微小RNA-200b對子宮內膜癌細胞中TIMP2基因表達的影響[J].中華婦產科雜志,2013,48(11):867-869.
10.3969/j.issn.1002-266X.2017.35.015
R737.35
B
1002-266X(2017)35-0047-03
2017-05-23)
安徽省科技廳科技攻關項目(1604a0802098) 。

