抗腫瘤血管形成藥物的臨床療效研究
周文靜
【摘要】 目的 研究人參皂甙2Rg3、姜黃素、青蒿琥酯、熊果酸4種中藥對抗腫瘤血管形成的臨床療效。方法 132例腫瘤患者, 隨機分為Ⅰ組、Ⅱ組、Ⅲ組、Ⅳ組, 每組33例。Ⅰ組使用人參皂甙2Rg3治療, Ⅱ組使用姜黃素治療, Ⅲ組使用青蒿琥酯治療, Ⅳ組使用熊果酸治療, 分別觀察四組的抗腫瘤血管形成的臨床療效。結果 Ⅰ組(人參皂甙2Rg3)的有效率為88%, Ⅱ組(姜黃素)的有效率為91%, Ⅲ組(青蒿琥酯)的有效率為85%, Ⅳ組(熊果酸)的有效率為82%;四組有效率比較差異無統計學意義(P=0.9989>0.05)。結論 人參皂甙2Rg3、姜黃素、青蒿琥酯、熊果酸對抗腫瘤血管形成都有較好的臨床療效。
【關鍵詞】 抗腫瘤血管形成;人參皂甙2Rg3;姜黃素;青蒿琥酯;熊果酸
DOI:10.14163/j.cnki.11-5547/r.2017.32.059
1971年Folkman在新英格蘭醫學雜志上首次提出腫瘤的生長和轉移依賴于血管生成, 為腫瘤研究開辟了新天地, 通過對腫瘤血管生成進行治療成為一項重要的治療策略。通過對抑制腫瘤血管生成分子機制的研究[1, 2], 在尋找抗腫瘤血管形成藥物方面取得了較大的進展, 在美國就已有20余種腫瘤血管生成抑制劑進入臨床。另一方面, 近些年的熱點之一是從植物中提取抗腫瘤血管形成藥物, 如人參皂甙2Rg3、姜黃素、青蒿琥酯、熊果酸等, 也表現出較好的療效性。因此, 研究中藥對抗腫瘤血管形成的臨床療效有重要的研究意義。本文對本院進行治療的腫瘤患者分別使用人參皂甙2Rg3、姜黃素、青蒿琥酯、熊果酸這4種抗腫瘤血管形成的中藥進行治療, 觀察其對抗腫瘤血管形成的臨床療效。報告如下。
1 資料與方法
1. 1 一般資料 選取2016年1月~2017年7月在院治療的132例腫瘤患者, 隨機分為Ⅰ、Ⅱ、Ⅲ、Ⅳ組, 每組33例。Ⅰ組中男18例, 女15例, 年齡50~76歲, 中位年齡62歲, 其中肺癌12例, 胃癌7例, 乳腺癌6例, 肝癌4例, 食管癌4例。
Ⅱ組中男17例, 女16例, 年齡52~74歲, 中位年齡60歲, 其中肺癌9例, 胃癌13例, 乳腺癌4例, 肝癌5例, 食管癌2例。
Ⅲ組中男14例, 女19例, 年齡55~80歲, 中位年齡67歲, 其中肺癌5例, 胃癌10例, 乳腺癌7例, 肝癌4例, 食管癌7例。
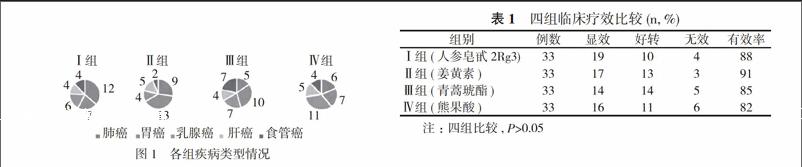
Ⅳ組中男15例, 女18例, 年齡51~77歲, 中位年齡63歲, 其中肺癌6例, 胃癌7例;乳腺癌11例, 肝癌5例, 食管癌4例。四組患者一般資料比較, 差異無統計學意義(P>0.05), 具有可比性。全部病例均經組織學或細胞學確診。卡氏評分(KPS評分)均≥80分。各組疾病類型見圖1。
1. 2 方法 Ⅰ組使用人參皂甙2Rg3作為抗腫瘤血管形成的中藥進行治療, 其主要機制經中國中醫研究院廣安門醫院的研究證實[3], 是作用于血管內皮生長因子(VEGF)和堿性成纖維細胞生長因子(bFGF)兩個腫瘤血管生長基因的位點, 抑制其蛋白質合成和基因的表達, 從而阻斷腫瘤吸收養分和播散細胞的通道, 起到抗腫瘤轉移的作用。Ⅱ組使用姜黃素作為抗腫瘤血管形成的中藥進行治療, 其主要機制是通過抑制人臍靜脈內皮細胞(HUVEC)的增殖進而抵抗腫瘤血管的形成 [4]。而HUVEC在遷移、增殖和分化過程中易導致血管形成, 從而容易誘導和促進腫瘤發生。Ⅲ組使用青蒿琥酯作為抗腫瘤血管形成的中藥進行治療, 其主要機制經免疫組化結果表明, 具有抑制VEGF和KDR/ flk21在腫瘤組織中的表達作用[5]。Ⅳ組使用熊果酸作為抗腫瘤血管形成的中藥進行治療, 其主要機制推測可能通過與糖皮質激素受體或類似的核受體結合發揮作用。
1. 3 療效判定標準 觀察比較四組抗腫瘤血管形成的臨床療效。參照文獻[4]制定療效判定標準, 分為顯效、好轉、無效;有效率=(顯效+好轉)/總例數×100%。
1. 4 統計學方法 所有數據分析采用Matlab進行, 計量Ⅰ~Ⅳ組所使用的人參皂甙2Rg3、姜黃素、青蒿琥酯、熊果酸這4種抗腫瘤血管形成的有效率, 四組數據運用Kruskal-Wallis秩和檢驗。P<0.05 為差異有統計學意義。
2 結果
Ⅰ組(人參皂甙2Rg3)的有效率為88%, Ⅱ組(姜黃素)的有效率為91%, Ⅲ組(青蒿琥酯)的有效率為85%, Ⅳ組(熊果酸)的有效率為82%。四組有效率比較, 差異無統計學意義(P=0.9989>0.05)。見表1。
3 討論
近年來研究證明, 新血管生成是腫瘤生長和轉移的必要條件之一, 而斷絕或減少腫瘤血管供應, 抑制腫瘤血管生成是控制腫瘤生長和轉移的重要途徑[6-8]。抑制腫瘤血管生成的關鍵在于條件血管生成因子或其受體, 包括VEGF和血管內皮生長因子受體(VEGFRs)。VEGF具有誘導血管通透性的能力, 通透性增強導致纖維蛋白沉積在細胞外基質, 作為血管內皮細胞遷移的一個支架, 而VEGFRs可與VRGF結合并激活導致血管通透性增強。內皮抑素(ES)是一種強烈抑制血管形成的因子, 能與VEGF競爭性結合, 通過抑制內皮細胞增值、促進內皮細胞凋亡等作用最終達到抑制腫瘤血管生成的作用[9, 10]。
研究表明, 人參皂甙2Rg3、姜黃素、青蒿琥酯、熊果酸等許多中藥成分可以抑制VEGF, 增高ES, 從而抑制血管腫瘤血管生長。這為腫瘤的治療提供了新的契機, 與傳統的腫瘤治療相比其具有特異性強、正常組織不易受損、不易發生耐藥、抗瘤譜廣等優勢。除了本文中的4種中藥外, 還可以使用鯊魚軟骨、紅素、昆布硫酸多糖、苦參堿、參麥注射液等藥物來抗腫瘤血管的生成[7]。當然, 目前抗腫瘤血管生成藥物的臨床應用, 多以扶正為主, 對其療效評價無統一標準。相信, 隨著科學技術的進步, 其在癌癥治療中將會起著越來越重要的作用。
參考文獻
[1] Turner HE, Nagy Z, Gatter KC, et al. Angiogenesis in pituitary adenomas-relationship to endocrine function, treatment and outcome. Journal of Endocrinology, 2000, 165(2):475-481.
[2] 高文, 何彥津, 梁鳳鳴. 姜黃素抗腫瘤血管生成分子機制研究進展. 國際眼科雜志, 2016, 16(3):466-468.
[3] 周逢倉, 金明. 腫瘤的分子診斷及其研究進展(綜述). 安徽衛生職業技術學院學報, 2003, 2(1):54-56.
[4] Aggarwal BB, Sung B. Pharmacological basis for the role of curcumin in chronic diseases: an age-old spice with modern targets. Trends in Pharmacological Sciences, 2009, 30(2):85.
[5] 陳歡歡, 周慧君. 青蒿琥酯的抗血管生成作用. 藥學學報, 2004, 39(1):29-33.
[6] 林洪生. 惡性腫瘤中醫診療指南. 北京:人民衛生出版社, 2014.
[7] 張芷旋, 周清華. 中藥抗肺癌血管生成藥物的研究進展. 中國肺癌雜志, 2006, 9(1):96-99.
[8] 李湘洲, 欒芳菲, 張勝, 等. 黃酮類化合物的抗腫瘤和抗血管生成作用研究進展. 食品與機械, 2016(1):199-201.
[9] 張俊利, 李宜放. 中醫藥抗腫瘤血管生成研究現狀. 醫學綜述, 2015, 21(8):1394-1395.
[10] 吳軍, 王婧, 曹邦偉. 抗腫瘤血管生成藥物不良反應的發生機制及處理. 醫學綜述, 2016, 22(16):3154-3157.
[收稿日期:2017-09-07]endprint

