砷角化癥伴多發性基底細胞癌一例
汪其鳳 王建民 董舒炳 段香艷 王德技 樊 潔 馬 英
砷角化癥(arsenical keratoses)是患者常年飲用砷污染井水,服用含砷的藥物,或者職業接觸砷劑后,掌跖部出現點狀或疣狀角化過度的表現,持續數年后皮膚可出現癌變,現報道一例砷角化癥伴多發性基底細胞癌并進行文獻復習。
臨床資料患者,男,70歲。雙手足部皮疹20年,頭面部、軀干、四肢皮疹10年。20年前患者雙手掌、足底部出現角化性皮疹,逐漸增多,并融合成斑塊。10年前胸部出現甲蓋大褐色斑片,皮損逐漸擴展至軀干、四肢,1年前左側額部亦出現類似皮損,無明顯癢痛感,類似皮損累積有20余處。
體檢:系統檢查未見異常,淺表淋巴結未及腫大。皮膚科檢查:雙手掌、手指側緣,足底部角化性丘疹,部分融合成斑片,質硬,去除表面角質,可見淺窩樣凹陷(圖1)。額部、軀干、四肢散在分布褐色或黑褐色扁平或高出皮面的斑片、斑塊,直徑最小為0.5 cm×0.5 cm,最大為5 cm×8 cm,邊界清晰,部分皮損邊緣堤狀隆起,部分呈環形,皮損表面粗糙干燥,期間色素不均(圖2)。胸背部可見多處大小不一手術瘢痕。左側前臂部見一環形色素沉著斑,中央見色素減退(圖3)。

圖1 足底部角化性丘疹,部分融合成斑片,質硬,去除表面角質,可見淺窩樣凹陷圖2 軀干散在分布褐色或黑褐色扁平或高出皮面的斑片、斑塊,部分皮損邊緣堤狀隆起,部分呈環形,皮損表面粗糙干燥,期間色素不均(箭頭所指為右下角放大圖)圖3 左側前臂部見一環形色素沉著斑,中央見色素減退
既往史:近年無明顯體重下降,無高血壓,無糖尿病,家族中無類似皮膚病史。患者30年前在鐵礦從事采礦工作,患者工作的礦場位于中國的云南騰沖,主要開采的是火山石。
實驗室檢查:血常規、肝腎功能、血糖、血脂檢測均在正常范圍;尿常規:尿膽原(+),余未見異常;尿砷:30 μg/L(40~100 μg/L);TB/NK細胞:CD4+ T細胞31%,CD8+ T細胞36%,CD4+/CD8+ 0.86↓(0.9-3.60);
腫瘤標記物:癌胚抗原CEA 0.85 μg/L,甲胎蛋白AFP 8.04 μg/L(0~10),糖類抗原CA125 9.74 U/mL,糖類抗原CA199 8.72 U/mL,糖類抗原CA153 37.20 U/mL↑(0~35),前列腺特異抗原PSA 0.24 ng/mL,游離前列腺特異抗原FPSA 0.13 ng/mL;免疫學檢查:抗核抗體1∶100,ENA抗體譜均陰性,補體C3片段1.02 g/L,補體C4 0.2150 g/L,類風濕因子9.75 IU/mL,C反應蛋白3.28 mg/L,抗鏈球菌溶血素O 55.30 IU/mL。B超:肝囊腫,膽囊、胰腺、脾臟未見異常,后腹膜淋巴結未見異常;肺部CT:兩肺紋理增多。皮損病理檢查:(胸壁)基底細胞癌伴真皮淺層慢性炎細胞浸潤,局部鱗狀上皮中度非典型增生,建議臨床隨訪(圖4)。
診斷:砷角化癥伴多發性基底細胞癌。
治療:予口服阿維A膠囊10 mg日2次,配合外用他扎羅汀軟膏治療掌跖部角化性皮損。腫瘤皮損部分手術切除,其余外用5%咪喹莫特軟膏日1次。2個月后患者角化性皮損略有改善,腫瘤皮損部分有消退,中央色素減少甚至部分只遺留色素沉著斑伴色素減退。目前患者繼續治療隨訪中。
討論砷常被用來治療銀屑病、梅毒、特應性皮炎、哮喘、白血病等。但同時砷劑是一種公認致癌物,由于飲水、藥物、職業等因素長期接觸砷,通過人體皮膚、消化道、呼吸道等途徑接觸和攝入砷化物,可引起
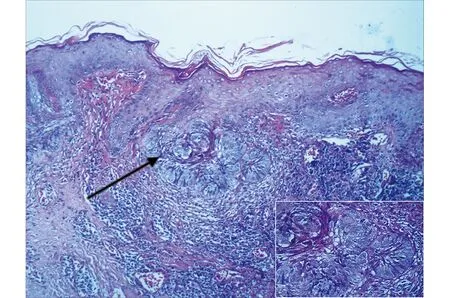
圖4 基底細胞癌伴真皮淺層慢性炎細胞浸潤,局部鱗狀上皮中度非典型增生(HE,×100,箭頭所指為右下角放大圖HE,×400)
皮膚、肺和膀胱等組織器官的腫瘤發生[1],尤其在皮膚的蓄積,可出現色素沉著、皮膚角化等相關皮膚病。砷角化癥可累及手掌、跖部,有時也可發生在耳部,皮損表現為手掌部角化過度,當用指甲挖去損害時,可以見到淺窩樣凹陷。本病持續數年后可以癌變,常見如鮑溫病、基底細胞癌、鱗癌等。通過接觸砷劑的患者,發生基底細胞癌更為常見,其潛伏期可達20余年,皮損好發于頭皮和軀干非暴露部位[2]。砷角化癥的發病機制尚不清楚,一系列表現與體內砷含量的過度吸收和累積有關。砷相關皮膚病與患者的淋巴細胞免疫功能異常也有關,砷劑可以下調淋巴細胞以及分泌的細胞因子水平[3]。Cooper等認為砷劑能刺激角質形成細胞p38和細胞外信號調節激酶(ERK)的活化,從而刺激角質形成細胞增殖,促進DNA的合成增加,而增殖的角質形成細胞分泌轉化生長因子-6(TGF-6)、表皮生長因子(EGF)等細胞因子,增強激活子蛋白-1(AP-1)、核轉錄因子-κB(NF-κB)活性,在炎癥和皮膚癌的發病中發揮重要作用[4]。砷劑的致癌作用仍不清楚,多數認為與細胞增殖異常、氧化應激、DNA修復異常有關[5]。Tchounwou等表明,砷是一種癌基因誘導劑,被誘導的基因復制、重組、擴增并為病毒所激活,從而引起皮膚和內臟的良、惡性腫瘤[6]。
維A酸類藥物對砷劑相關性皮膚病有良好療效,它能誘導細胞分化,抑制細胞異常增殖,抑制過度角化,從而起到治療作用[7]。對于腫瘤病灶,手術切除是治療本病的主要方法,小的皮疹可用液氮冷凍或CO2激光治療。Lonergan等在一例銀屑病患者使用砷劑治療后全身出現40余處非黑素瘤性皮膚腫瘤,使用5%咪喹莫特軟膏,日1次,6周后腫瘤性皮損均有消退,隨訪3年未見復發[8]。咪喹莫特(imiquimod)屬于非核苷類異環胺類藥物,是一種新的免疫調節藥物,它是一種TLR-7促進劑,誘導合成Thl類細胞因子,包括IFN-α,TNF-α及IL-6等,增強獲得性免疫。Sauder已證明,咪喹莫特能激活朗格漢斯細胞從皮膚遷移至局部引流的淋巴結,引起朗格漢斯細胞形態學的改變;通過誘發細胞因子如IL-12,IFN等增強細胞免疫[9]。咪喹莫特處理的腫瘤細胞模型顯示細胞增殖活性下降以及金屬蛋白酶組織抑制劑1(TIMP-1)表達增加,后者可抑制血管產生和細胞增殖[10]。Schiessl等用5%咪喹莫特治療47例基底細胞癌患者,日1次,每周5次,連續6周,有效率達到95.7%,經過隨訪17個月,復發率只有6.6%[11]。因此對于多發的基底細胞癌或者無法進行手術治療的患者,外用咪喹莫特軟膏是一種安全有效的治療方法。
根據本例患者有明確的砷劑接觸史,典型的臨床表現以及組織病理檢查,砷劑角化伴多發基底細胞癌診斷成立,雖然尿砷在正常范圍,但由于砷劑的長期接觸,刺激免疫系統可誘導產生一系列的臨床表現。本例患者掌跖部的角化皮損需與點狀掌跖角皮癥進行鑒別,而基底細胞癌需要與皮膚Bowen病,黑色素瘤及鱗狀細胞癌作鑒別,病理診斷可以支持[12]。針對該患者角化性皮損我們予以維甲酸治療。多發性基底細胞癌,較大的皮損予以手術切除,余予以咪喹莫特軟膏外用治療,部分有消退,目前該患者還在隨訪中。因此,對于長期接觸砷劑的人群需要加強防護,及時診斷,盡早治療。
[1] Lee L, Bebb G. A case of Bowen’s disease and small-cell lung carcinoma: long-term consequences of chronic arsenic exposure in Chinese traditional medicine[J]. Environ Health Perspect,2005,113(2):207-210.
[2] 趙辨.中國臨床皮膚病學[M].南京:江蘇科學技術出版社,2009.1092.
[3] Soto-Pena GA, Luna AL, Acosta-Saavedra L, et al. Assessment of lymphocyte subpopulations and cytokine secretion in children exposed to arsenic[J]. FASEB J,2006,20(6):779-781.
[4] Cooper KL, Myers TA, Rosenberg M, et al. Roles of mitogen activated protein kinases and EGF receptor in arsenite-stimulated matrix metalloproteinase-9 production[J]. Toxicol Appl Pharmacol,2004,200(3):177-185.
[5] Liu J, Xie Y, Ducharme DM, et al. Global gene expression associated with hepatocarcinogenesis in adult male mice induced by in utero arsenic exposure[J]. Environ Health Perspect,2006,114(3):404-411.
[6] Tchounwou PB, Patlolla AK, Centeno JA. Carcinogenic and systemic health effects associated with arsenic exposure--a critical review[J]. Toxicol Pathol,2003,31(6):575-588.
[7] Khandpur S, Sharma VK. Successful treatment of multiple premalignant and malignant lesions in arsenical keratosis with a combination of acitretin and intralesional 5-fluorouracil[J]. J Dermatol,2003,30(10):730-734.
[8] Lonergan CL, Mcnamara EK, Cordoro KM, et al. Imiquimod cream 5% for the treatment of arsenic-induced cutaneous neoplasms[J]. Cutis,2010,85(4):199-202.
[9] Sauder DN. Immunomodulatory and pharmacologic properties of imiquimod[J]. J Am Acad Dermatol,2000,43(1 Pt 2):S6-S11.
[10] Sidbury R, Neuschler N, Neuschler E, et al. Topically applied imiquimod inhibits vascular tumor growth in vivo[J]. J Invest Dermatol,2003,121(5):1205-1209.
[11] Schiessl C, Wolber C, Tauber M, et al. Treatment of all basal cell carcinoma variants including large and high-risk lesions with 5% imiquimod cream: histological and clinical changes, outcome, and follow-up[J]. J Drugs Dermatol,2007,6(5):507-513.
[12] Pimparkar BD, Bhave A. Arsenicosis: review of recent advances[J]. J Assoc Physicians India,2010,58:617-624,629.

