咔唑及其衍生物的合成方法研究
李 璐
(寶雞職業技術學院,陜西 寶雞 721000)
咔唑是一種重要的含氮雜原子化合物,它作為精細化學品的中間體,在有機發光材料[1-3]、偶氮染料[4-5]、醫藥[6]等領域有著廣泛的應用。咔唑類化合物不僅是一類很好的給電子基團并且還具有良好的空穴導電功能和有機電致發光的特性。研究發現咔唑及其衍生物自身也能發生氧化偶聯反應[7],這不僅擴大了咔唑類化合物的研究范圍,也賦予了咔唑類化合物新的用途和研究前景。近年來,結構新穎性能優越的咔唑類衍生物的合成和設計備受科研工作者的青睞,因此,尋求高效、簡潔的合成方法有助于發揮咔唑類化合物的應用價值。本文對咔唑及其衍生物的合成方法進行了概括。
1 咔唑及其衍生物的合成
構建咔唑環的方式很多[8],目前比較常見的主要有過渡金屬催化的環化反應、Diels-Alder反應,DDQ氧化脫氫、重氮化反應以及Buchwald-Hartwig偶聯反應等。
(1)以過渡金屬釕和鈀催化構建咔唑環:
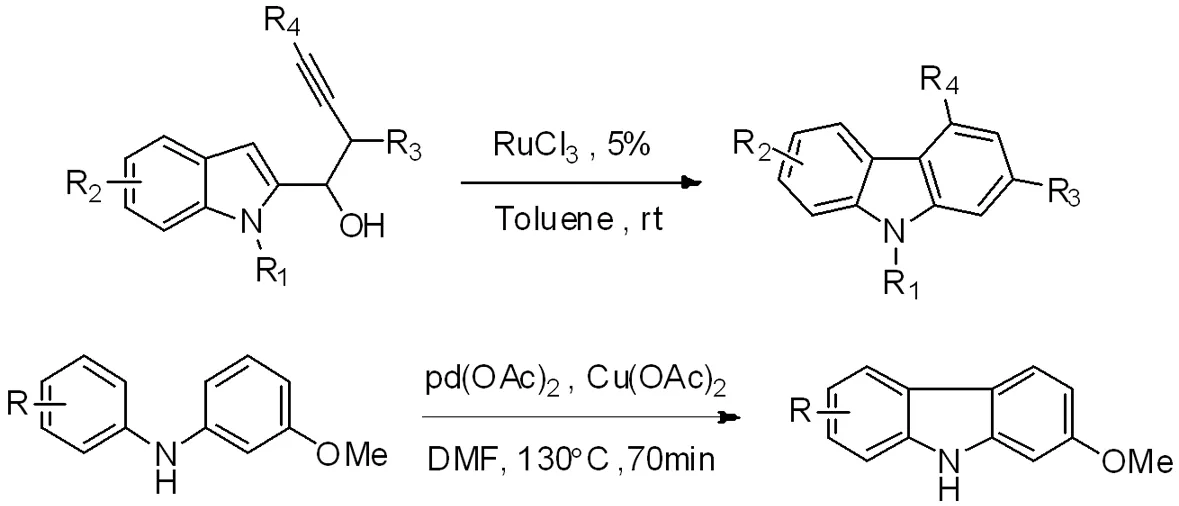
(2)通過Diels-Alder環加成反應得到中間體,中間體伴隨脫羧反應得到咔唑環:
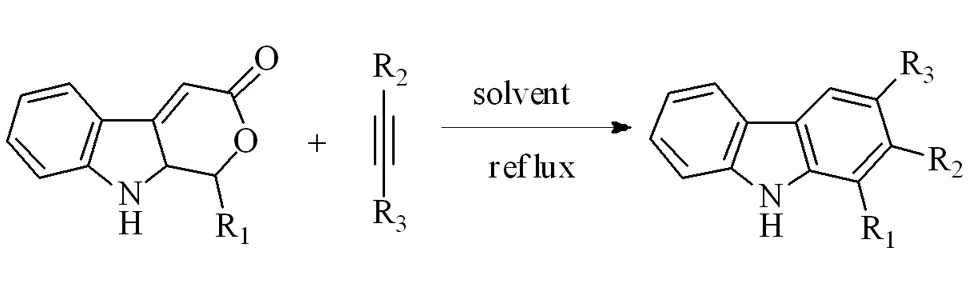
(3)DDQ氧化脫氫芳構化[9]或鈀碳催化的芳構化:

(4)通過重氮化反應得到不穩定的重氮鹽中間體,經加熱使重氮鹽釋放氮氣時發生重排得到了咔唑環:
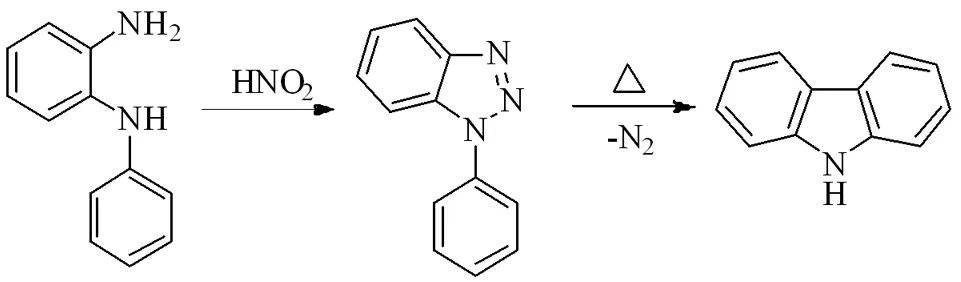
(5)通過鄰二鹵苯在鈀催化下發生兩Buchwald-Hartwig偶聯反應得到咔唑環[10]:

(6)其它方式合成咔唑類衍生物:
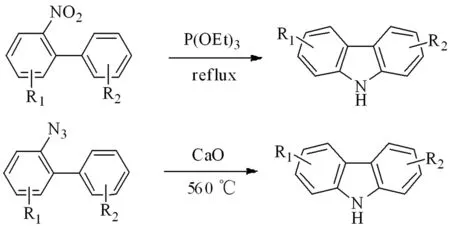
(7)咔唑類衍生物的合成:9-取代的咔唑類烷基化合物主要是通過親電取代得到的。咔唑9位上的二級胺具有弱酸性,通過強堿的作用使得氮原子變成氮負離子,烷基鏈上靠近鹵素的α碳因受鹵原子吸電子作用的影響,缺電子性增強,這樣形成的碳原子很容易發生親電取代反應,形成9-取代的咔唑類化合物。

目前合成中利用鹵代烴與咔唑的9位發生取代反應,得到的衍生物既是一類小分子熒光材料,也是活化咔唑環上的3,6 兩個位置的策略,同時也是防止了一些活潑基團與9 位的氫原子發生副反應的方法。
(8)3,6位鏈接的咔唑類衍生物的合成:在咔唑環的3,6 位是電子云較為富集的地方,很容易發生磺化、硝化、傅克、鹵代、氧化偶聯、甲酰化等反應,這些反應的反生為官能團的轉化與特定位置的修飾提供了便利的條件。
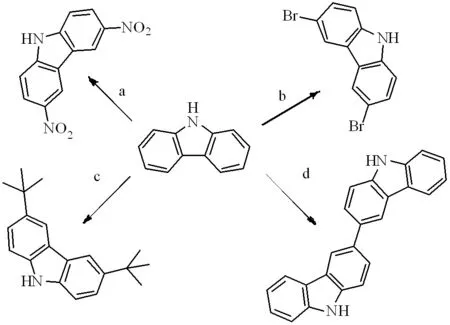
Condition: (a) Cu(NO3)2,acetic anhydride,acetic acid (90℃); (b) NBS,DCM (c) t-BuCl,AlCl3,DCM; (d) FeCl3,CHCl3
目前大多數咔唑環的結構修飾主要表現在咔唑環的3,6位上,3,6位鏈接的咔唑類芳香衍生物通常先發生鹵代反應,然后再利用Suzuki-Miyaura偶聯反應得到。通常是先將咔唑環上9位的二級胺保護起來(可以鍵聯烷基或者芳香基團),再進行3,6-位上的鹵代(Br、I)反應,最后通過鈀催化的偶聯反應得到3,6位鏈接的咔唑類芳香衍生物。

Conditions: (a) KI,KIO3,HOAc; (b) carbazole,Cu2O,K2CO3
2 結語與展望
咔唑及其衍生物在有機合成領域中是一類用途廣泛、實用價值高、自身能發出藍色熒光的含氮雜環類化合物。在有機共價多孔材料領域里是一類重要的合成中間體,在所涉及到的很多研究領域都占有舉足輕重的地位。相信在已有合成咔唑類化合物的基礎上,后續會報道出有更多結構新穎、性質獨特的咔唑類化合物。
[1]K?nig B,Pelka M,Zieg H,et al.Photoinduced electron transfer in a phenothiazine-riboflavin dyad assembled by zinc-imide coordination in water[J].J Am Chem Soc,1999,121(8):1681-1687.
[2]Boyde S,Strouse G F,Jones W E J,et al.Intramolecular energy transfer in a chromophore-quencher complex[J].J Am Chem Soc,1989,111(19): 7448-7454.
[3]Tamai N,Yamazaki T,Yamazaki I.Two-dimensional excitation energy transfer between chromophoric carbazole and anthracene in langmuir-blodgett monolayer films[J]. J Phys Chem,1987,91(4):841-845.
[4]Crosby G A,Demas J N.Measurement of photoluminescence quantum yields. a review[J]. J Phys Chem,1971,75(8):991-1024.
[5]Ren Y,Yu X Q,Zhang D J,et al.Synthesis,structure and properties of a new two-photon photopolymerization initiator[J].J Mater Chem,2002,12(12):3431-3437.
[6]Kim D,Lee J K,Kang S O,et al.Molecular engineering of organic dyes containing N-aryl carbazole moiety for solar cell[J].Tetrahedron,2007,63(9):1913-1922.
[7]萬有志,范 慧,張小強.單偶氮及雙偶氮苯咔唑類化合物的合成與表征[J].精細化工,2005,22(8):569-571.
[8]Schmidt A W,Reddy K R,Kn?lker H J. Occurrence,biogenesis,and synthesis of biologically active carbazole alkaloids[J]. Chem Rev,2012,112(6):3193-3328.
[9]李 璐.多環芳烴類化合物的合成研究進展[J].廣州化工,2017,45(5):1-3,6.
[10]Tokito S,Iijima T,Suzuri Y,et al.Confinement of triplet energy on phosphorescent molecules for highly-efficient organic blue-light-emitting devices[J].Appl Phys Lett,2003,83(3):569-571.

