自研糖化血紅蛋白床旁檢測分析儀的性能評估*
李新華,趙 珂,魏 芳,馬凱惠,張憲黨△
(1.山東省內分泌與代謝病研究所,濟南 250062;2.山東中醫藥大學附屬醫院普外科,濟南 250000)
糖化血紅蛋白(HbA1c)是機體血液中血糖與血紅蛋白結合的產物,兩者結合呈不可逆,其結合速率與平均120 d壽命的紅細胞糖化量呈正相關,臨床HbA1c水平可反映患者近8~12周的血糖控制情況,作為糖尿病篩查、診斷、長期血糖控制、療效評估的重要指標[1-3]。本課題組研發一款HbA1c床旁檢測分析儀,基本原理是采用顯色型親和層析法,在3~5 min內實現HbA1c定量檢測,更加方便、快捷、準確[4]。本研究對自研HbA1c床旁檢測分析系統進行方法學評價,與美國Bio-Rad公司D10型HbA1c分析儀進行對比分析,為該儀器的臨床應用提供實驗數據。
1 資料與方法
1.1一般資料 選取該院及社區糖尿病篩查患者82例,年齡35~75歲。健康對照組為104例健康體檢者,男56例,女48例,年齡22~66歲。所有研究對象分別抽取2 mL靜脈血,置于乙二胺四乙酸二鉀(EDTA-K2)試管中,充分混勻,2~8 ℃保存。同一標本分別由2種儀器檢測1次,1周內完成。
1.2儀器與試劑 D10型HbA1c分析儀及其配套試劑(試劑批號R1:AA50235,R2:20236)、質控品(批號:33910,L1:5.4%;L2:9.9%)、校準樣品(低值樣品(level 1,批號AA50119,標定值為5.4%)、高值樣品(level 2,批號AA50120,標定值為10.1%),中值樣品(level 3,低值和高值等量混合,標定值為7.75%)。自研HbA1c床旁檢測分析儀及其配套試劑(試劑批號160318)和質控品(Bio-Rad批號:33910,L1:5.4%;L2:9.9%)[4]。
1.3方法
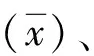
1.3.2相關性試驗 選取82例新鮮抗凝全血分別在2種儀器上檢測HbA1c并進行比較。以自研儀器檢測結果(Y)對Bio-Rad D10檢測結果(X)的直線回歸方程:Y=bX+a,b可接受范圍為0.095~1.05,相關系數R2>0.95,偏差符合率大于或等于90%(允許偏差:±3.5%)。
1.3.3參考值范圍試驗 選取104例健康體檢者,納入標準:血糖、血脂、血常規、肝功能等檢查均正常;心電圖、胸透、彩超無異常;排除標準:6個月內手術史、4個月內輸血/獻血史、妊娠者。采用自研儀器檢測健康者HbA1c水平。
1.3.4干擾試驗 每組取3例全血標本,分別收集高中低3個水平的果糖胺、葡萄糖、維生素C、總膽紅素、血紅蛋白F(HbF)、三酰甘油進行檢測。干擾物質分別為:(1)果糖胺:20、10、5 mmol/L。(2)葡萄糖:100、50、25 mmol/L。(3)維生素C:40、20、10 mg/dL。(4)總膽紅素:120、60、30 μmol/L。(5)HbF:20、10、5 mg/dL。(6)三酰甘油:20、10、5 mmol/L。
1.3.5校準品試驗 全部校準品分裝后于4 ℃保存,各水平標本每天取1管,檢測之前充分混勻。儀器校準、質控測定,結果在控后進行常規操作。依照EP10-A文件[5],各標本每天按照中、高、低、中、中、低、低、高、高、中的順序進行檢測,檢測5 d。第1個中值為檢測起始用,不作統計,其余9個數據中的任何1個不合格都會使該批標本的全部數據作廢,須重新檢測。
1.4統計學處理 采用SPSS13.0統計軟件及實驗室專業評價軟件1.82版對數據進行分析。P<0.05位為差異有統計學意義。
2 結 果
2.1離群點分析 橫坐標為靶值濃度,縱坐標為測定值與靶值濃度偏差,每天校準品的測定值均標于圖上,進行離群點觀察,精密度初評。結果顯示:無離群點、精密度良好。見圖1。
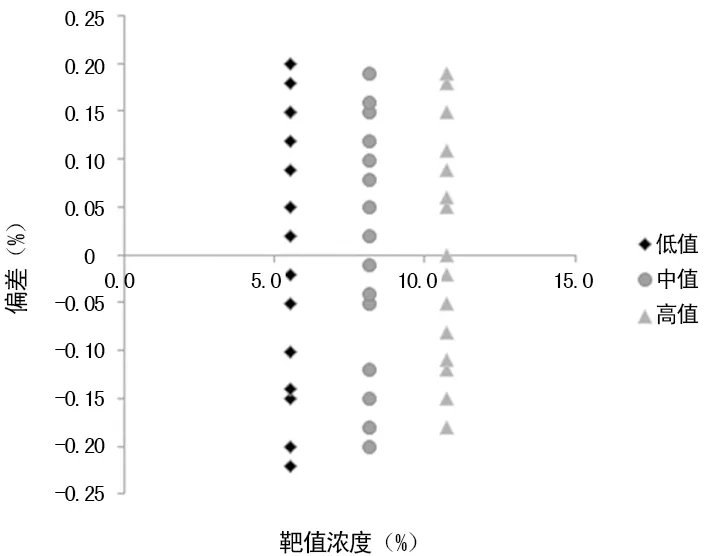
圖1 HbA1c離群散點圖
2.2線性評價 橫坐標(X)為靶值,縱坐標(Y)為測定值,將低、中、高3個校準品靶值以X=Y繪制參考線,低、中、高3個校準品連續檢測5 d的結果均值繪制測定線,與參考線比較,對線性、偏差進行初評。結果顯示:線性良好、偏差小。見圖2。
2.3偏差分析 偏差以校準品各濃度連續檢測5 d的結果均值與其對應靶值之差計算,均未超過設定的范圍,判斷臨床均可以接受。結果顯示:高、中、低3個濃度校準品的絕對偏差分別為―0.05%、―0.03%、―0.01%,遠低于允許偏差,均可接受。見表1。
2.4多元回歸分析 根據5 d所有數據計算截距、斜率、非線性、漂移,作回歸分析和t檢驗。HbA1c測定截距差異有統計學意義(P<0.01),與靶值有恒定誤差(t>4.6,P<0.01);斜率、非線性、漂移差異均無統計學意義(―4.6
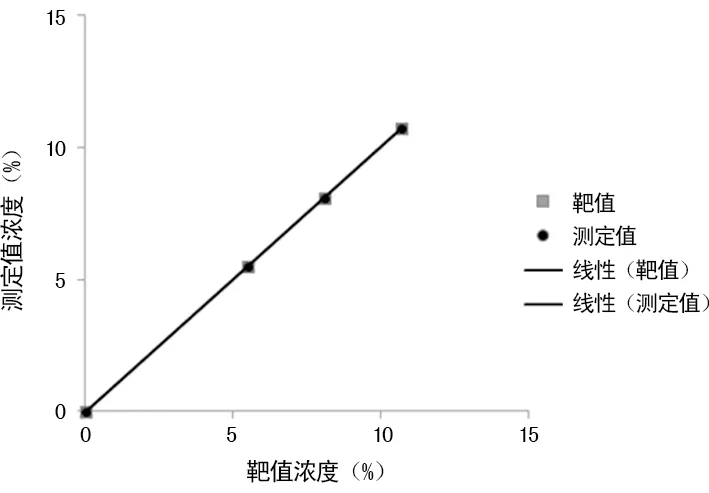
圖2 HbA1c線性圖
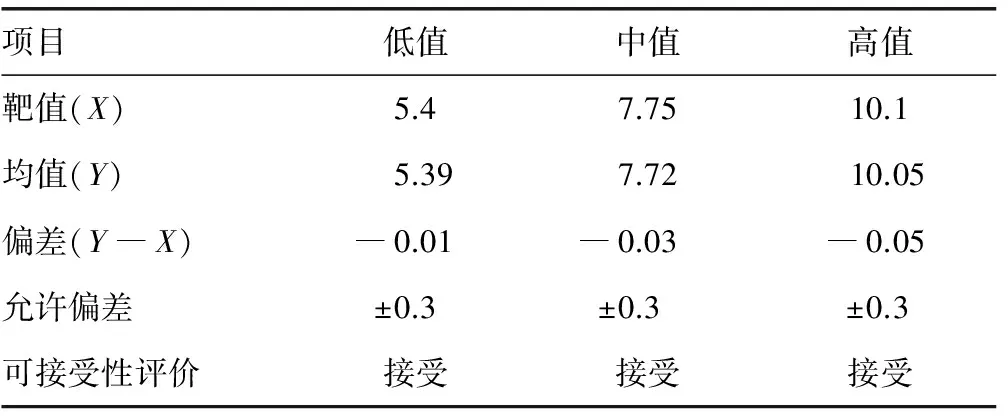
表1 偏差分析(%)
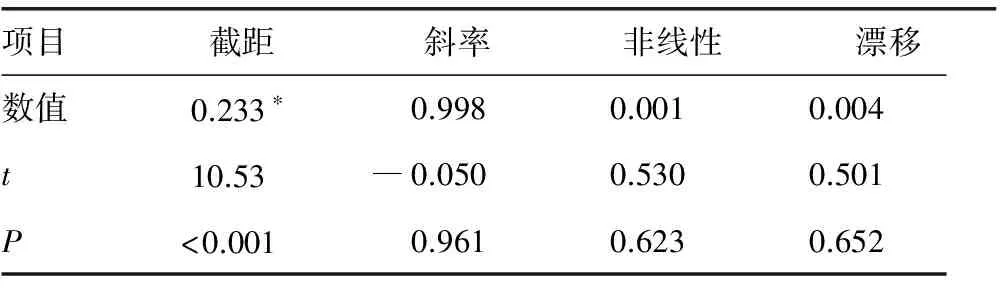
表2 HbA1c多元回歸分析
注:與靶值回歸分析截距比較,*P<0.01
2.5總不精密度分析 HbA1c低、中、高3個校準品的總不精密度(CV)分別為1.298%、0.906%、1.014%,遠小于美國糖尿病協會規定的5%允許誤差范圍,臨床均可接受。見表3。
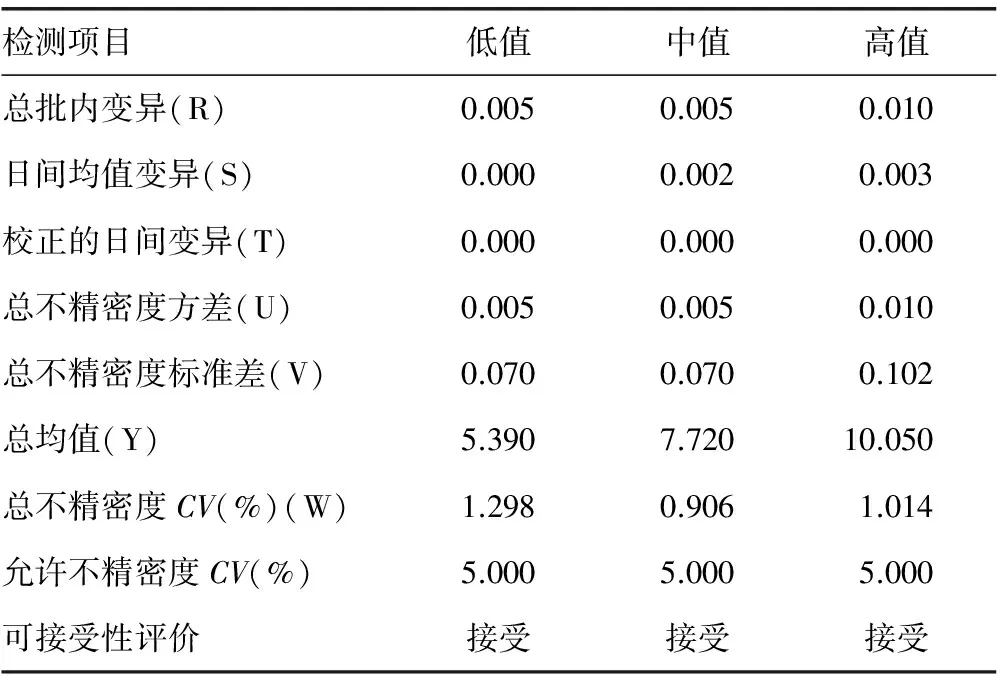
表3 HbA1c總不精密度分析
2.6精密度試驗 自研儀器檢測高值與低值全血標本和質控品,批內與批間不精密度均可接受。見表4。
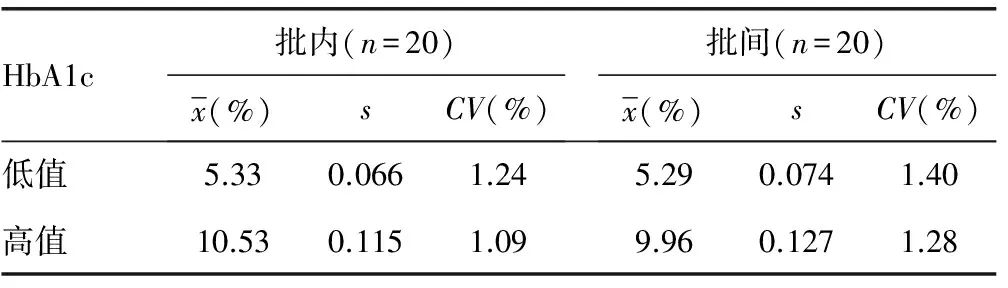
表4 精密度試驗結果
2.7相關性試驗 2種儀器檢測HbA1c的結果高度相關。自研儀器(Y)對Bio-Rad D10(X)的直線回歸方程:Y=1.004 9X―0.041 1(R2=0.998 2,P<0.001),預期偏倚0.06,相對偏倚0.83%,偏差符合率100%,自研儀器與Bio-Rad D10的對比試驗達可接受范圍。見圖3。
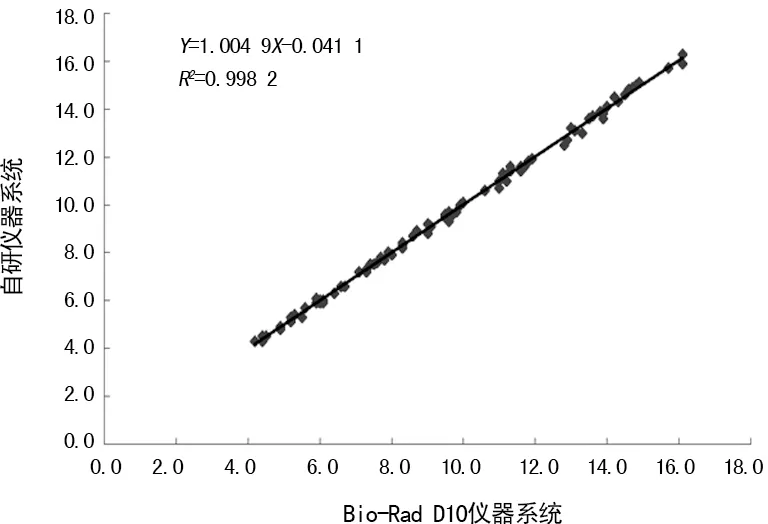
圖3 2種儀器檢測HbA1c結果的相關性
2.8參考值范圍 自研儀器檢測104例健康體檢者,HbA1c平均值為5.3%(95%CI:4.7%~6.3%),檢測范圍3%~18%。健康體檢者以每10歲為年齡段分為5組,即20~29歲、30~39歲、40~49歲、50~59歲、60~69歲,各組HbA1c平均值分別為5.1%、5.2%、5.3%、5.4%、5.4%。見表5。
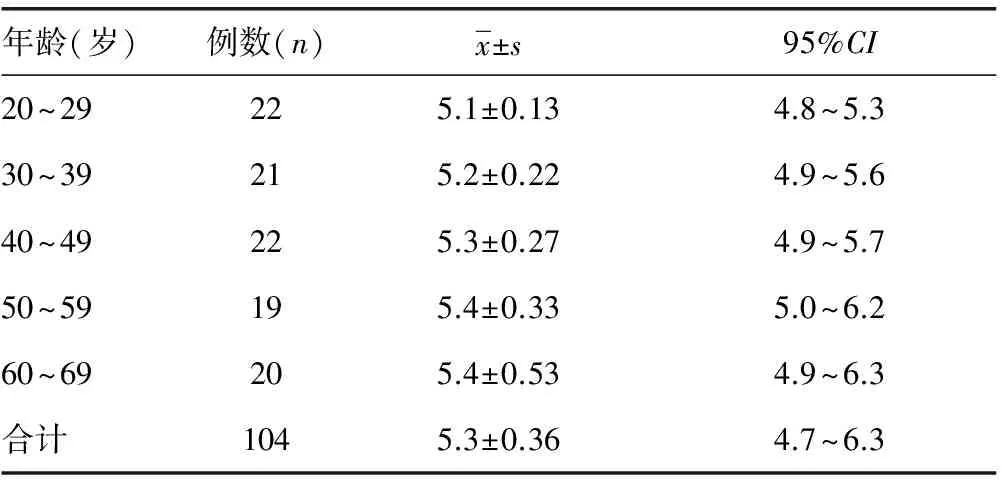
表5 自研儀器檢測健康體檢者的HbA1c值
2.9干擾試驗 分別在全血標本中添加不同濃度的果糖胺、葡萄糖、維生素C、總膽紅素、HbF、三酰甘油進行檢測,各干擾物對HbA1c的變異系數分別為:果糖胺小于或等于1.60%、葡萄糖小于或等于0.90%、維生素C小于或等于0.40%、總膽紅素小于或等于1.50%、HbF小于或等于1.80%、三酰甘油小于或等于1.10%。見表6。
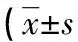
表6 不同干擾物對 HbA1c檢測的結果或%)
3 討 論
自研糖化血紅蛋白床旁檢測分析儀采用顯色型親和層析法,檢測總HbA1c和總的非HbA1c,經過系統校正后獲得HbA1c檢測結果,不受血紅蛋白變異體影響[6]。該方法是目前檢測HbA1c的常用方法之一,曾經應用于美國糖尿病控制與并發癥研究[7]。
本研究根據《糖化血紅蛋白實驗室檢測指南》、美國臨床和實驗室標準協會(CLSI)、美國臨床實驗室標準化委員會(NCCLS)頒布的部分文件,對自研HbA1c床旁檢測系統進行性能評估[2,5,8-10]。
本研究結果顯示,自研儀器檢測HbA1c的高值、中值、低值偏差與總不精密度均在允許范圍,多元回歸分析中斜率、非線性、漂移差異均無統計學意義(P>0.05),表明該儀器檢測HbA1c的精密度和準確度良好,而截距差異有統計學意義(P<0.01),表明與靶值有恒定誤差(t>4.6,P<0.01)。精密度試驗顯示自研儀器檢測HbA1c批內與批間不精密度均可接受(均CV<1.50%),重復性較好,結果穩定。相關性試驗證實2種儀器檢測 HbA1c的結果顯著相關(R2=0.998 2,P<0.01),預期偏倚0.06,相對偏倚0.83%,偏差符合率100%,處于可接受范圍。果糖胺、葡萄糖、維生素C、總膽紅素、HbF、三酰甘油等常見干擾物對檢測結果影響小(均CV<1.80%)。HbA1c水平主要與血糖相關,但也受年齡、性別、藥物、異常血紅蛋白、貧血、紅細胞增多等因素的影響[11]。該儀器參考值范圍驗證在選取健康體檢者時也考慮上述影響因素,HbA1c參考值范圍為4.7%~6.3%。
綜上所述,自研糖化血紅蛋白床旁檢測分析儀檢測HbA1c的線性、準確度、精密度等各項指標性能均符合臨床要求。同時該儀器操作方便、準確度高、重復性好,且每例標本可獨立操作,不產生攜帶污染,適合于急診及床旁檢測。
參考文獻
[1]于秀娟,歐超偉.糖化血紅蛋白檢測的影響因素及臨床意義[J].中國老年學雜志,2013,33(19):4930-4933.
[2]衛生部臨床檢驗中心,北京市醫療器械檢驗所,北京大學人民醫院.糖化血紅蛋白實驗室檢測指南[J].中國糖尿病雜志,2013,21(8):673-678.
[3]ADA.Executive summary:Standards of medical care in diabetes——2013[J].Diabetes Care,2013,36(Suppl 1):S4-S10.
[4]李新華,趙珂,魏芳,等.顯色型親和層析法檢測糖化血紅蛋白的建立及性能評估[J].中國糖尿病雜志,2016,24(10):882-886.
[5]National Committee for Laboratory Standards.Preliminary evaluation of quantitative clinical laboratory methods:EP10-A[S].Wayne,PA,USA:NCCLS,1998.
[6]宋智心,徐國賓,馬懷安,等.糖化血紅蛋白測定的標準化現狀[J].中華檢驗醫學雜志,2012,35(6):497-500.
[7]JOHN W G.Haemoglobin a(1c):analysis and standardisation[J].Clin Chem Lab Med,2003,41(9):1199-1212.
[8]National Committee for Laboratory Standards.Evaluation of precision performance of quantitative measurement methods;approved guideline-second edition:EP5-A2[S].Wayne,PA,USA:NCCLSI,2004.
[9]National Committee for Laboratory Standards.Method comparison and bias estimation using patient samples;approved guideline-second edition:EP9-A2[S].Wayne,PA,USA,NCCLSI,2002.
[10]National Committee for Laboratory Standards.Evaluation of the linearity of quantitative measurement procedures;a statistical approach;approved guideline:EP6-A[S].Wayne,PA,USA:NCCLSI,2003.
[11]費小薔,蔣伏松,陸志強.糖化血紅蛋白的基礎與臨床應用[J/CD].中華臨床醫師雜志(電子版),2012,6(19):5966-5969.

