Al改性檸條生物炭對P的吸附特性及其機制
王彤彤,崔慶亮,王麗麗,譚連帥,孫層層,鄭紀勇,* (.西北農林科技大學資源環境學院,陜西 楊凌 7200;2.中國科學院水利部水土保持研究所,黃土高原土壤侵蝕與旱地農業國家重點試驗室,陜西 楊凌7200;3.中國科學院大學,北京 00049;4.長江水利委員會長江科學院,重慶分院,重慶 400026)
在大多數生態系統中,磷(主要是磷酸鹽)是動植物體生長必不可少的營養元素之一[1],然而,磷是大多數湖泊和淡水體系富營養化的控制因子[2],富集會導致水體富營養化加劇,致使水質惡化,危害人類和動植物的健康[3],降低了水資源價值并增加治理成本,成為世界范圍內嚴重的環境問題[1,4].目前去除水體中磷的主要技術[5-7]中吸附法因高效快捷、設備簡單、運行可靠[8-10]、成本較低[3]、能回收利用磷資源而備受關注[11],Ma等[12]認為其是最有效的除磷方法.吸附材料的選擇是吸附法的關鍵[6],利用原料廣泛、比表面積大、多孔結構、富含官能團、具有較高環境穩定性的生物炭吸附污染物已受到了廣大學者的青睞[13-14].
生物炭(biochar)是指生物質在缺氧或無氧條件下經中高溫熱裂解得到的一類富含碳素的、穩定的、高度芳香化的固體產物[15].Li等[16],Han等[17],Mohan等[18]和Mukherjee等[19]均報道了生物炭表面主要是凈負電荷,在廢水處理中,對常見的陰離子污染物(PO43-)去除很有限,僅是依靠較大比表面積的物理吸附.Namasivayam 等[20]用椰殼纖維與堅果殼為原料制備的活性炭吸附除磷,但除磷效果不穩定且容易洗出.Yao等[21]報道了由13種不同類型生物質制得的生物炭去除水中磷的效果,發現其對磷的吸附能力有限,與常規吸附材料相比沒有顯著的優越性.為了拓展生物炭在含磷污水領域的應用,有學者嘗試對生物炭進行改性來提高磷吸附能力[16,22].化學改性可利用炭材料表面特性引入對磷有吸附固定能力的鐵、鋁、鎂等羥基氧化物,從而強化炭材料磷吸附作用,賦予其特定功能[16,22-24].目前國內外對生物炭的改性方法主要集中在鐵改性和鎂改性, Wang等[25],Chen等[26]和Zhang等[27]報道過用鐵、鎂鹽對生物炭改性表現出優良磷吸附性能,且改性方法簡便易行、成本可控.余國文等[22]以氯化鋁為改性劑,采用水解共沉淀法對竹炭改性,改性后竹炭對P的吸附量為10.0mg/g,是改性前的1.3倍;其認為針對不同除磷要求開發新型低廉高效磷吸附生物炭材料正成為關注的焦點.目前,國內對鋁改性生物炭的相關研究還較少.
檸條(Caragana korshinski)作為先鋒樹種,在我國北方干旱半干旱區防風固沙、涵養水分、水土保持中發揮顯著作用[28].然而,檸條資源的利用率還不到 40%,很多處于荒蕪狀態[28].探索檸條資源的高效利用途徑有助于促進我國北方生態文明的建設.因此,本試驗以檸條為原料,采用限氧升溫法制備生物炭,通過Al直接修飾法改性生物炭,確定最佳改性比例.開展 Al改性生物炭對P的批量吸附試驗,同時利用SEM,BET比表面積和孔徑分析,元素分析,XRD,FTIR等技術對樣品進行表征分析,探究其對水溶液中P的吸附特性和機制.以等溫吸附模型和吸附動力學模型對試驗數據進行擬合,反映吸附特性,分析添加量和pH值對吸附量的影響,闡明其吸附機制,以期為廢棄物檸條的資源化和高效利用,水體富營養化治理,發展生態循環經濟提供理論依據.
1 材料與方法
1.1 生物炭材料與制備
本文選取的原料包括:檸條采自寧夏回族自治區固原市上黃村,20年限.
(1) 檸條生物炭的制備
參考文獻[13]的炭化工藝,將足量檸條原料切成指節大小長度,用蒸餾水沖洗若干次后烘干.填滿于帶蓋的鐵盒中,加蓋密閉,放入南京博蘊通GF11Q-B箱式氣氛爐中熱解,設置熱解溫度為650℃,恒溫時間為3h,恒定升溫速率為10℃/min,通入氮氣保護塑造厭氧環境.采用三段式程序升溫熱裂解法,統一升溫時長為 1h,降溫時長為 1h,之后冷卻至室溫.將生物炭材料用粉碎機破碎成粉末.注意,制備的生物炭不經過蒸餾水淋洗過程.為敘述方便,檸條生物炭簡寫為 NB.表 1列舉出NB的主要化學組成成分.
(2) 直接修飾法制備Al改性檸條生物炭
每次取足量生物炭粉末,過 1mm 篩子,加入100mL的三角瓶,設計7個梯度的AlCl3溶液(以 Al元素計,鋁炭比為 0:1,即未改性生物炭),鋁炭比為 0:1、0.0135:1、0.027:1、0.054:1、0.1:1、0.2:1、0.27:1,分別將檸條生物炭浸泡在相應濃度梯度的 AlCl3溶液中,超聲振動 6h,然后靜置30min,過濾,用蒸餾水清洗一次,倒入玉坩堝,在 95℃干燥箱中直至完全烘干,呈干燥固體狀態,冷卻至室溫備用,即可得到7種不同鋁炭比的 Al改性生物炭.為敘述方便,Al改性檸條生物炭簡寫為Al-NB.

表1 檸條生物炭化學性質Table 1 Chemical property of NB
1.2 生物炭表征
微觀形貌表征:采用日本電子 JSM-6510LV型SEM,額定掃描電壓為20kV.
生物炭樣品比表面積、孔體積、孔徑表征:采用國家標準方法GB/T 19587-2004,“氣體吸附BET法”測定,吸附氣體采用氮氣,儀器為北京金埃譜公司V-Sorb 2800P型比表面積及孔徑分析儀.表2列舉出NB和檸條的表面特征測試結果.

表2 檸條生物炭和檸條的表面特征測試結果Table 2 Surface characteristics of the biochar and Caragana korshinskii
元素含量表征:采用美國賽默飛世爾科技公司(Thermo Scientific) Flash 2000型元素分析儀測定BC的C、H、O、N、S元素含量.采用美國Agilent公司 720型 ICP-OES儀器測定 NB和Al-NB的Al和P元素含量.本部分樣品被送往上海薈銘檢測設備有限公司進行測定分析及數據處理.
物相結構表征:采用美國 RIGAKU公司D/max 2400轉耙全自動X射線粉末衍射儀分析(XRD)測定.掃描步長為 0.02,掃描速度為2deg/min,電壓為 30~40kV,電流為 30~40mA,接受狹縫寬度為0.15,測定結果使用Jade6.0軟件分析.
官能團定性表征:將樣品烘干 3d,研磨過1mm 篩,用 KBr壓片法在美國 Bruker公司的Vertex70紅外光譜儀上進行測定,波數范圍為 4 000~400cm-1,分辨率 2cm-1,掃描次數為 16.
1.3 吸附試驗
選擇KH2PO4來配置不同濃度的標準P溶液.配置方法參考[29],溶液中主要存在的離子是H2PO4-、HPO42-和 PO43-.
(1)最佳改性比例Al-NB生物炭的確定
準確稱取 0.1000g上述 7種不同比例的Al-NB于 250mL錐形瓶,分別加入到體積為50ml的50mg/L的P溶液,將錐形瓶用塑料膜封口放入 25℃±1℃的氣浴恒溫振蕩器中,以150r/min的轉速振蕩 24h,然后過 0.45μm 濾膜,取上清液稀釋后,用于分析吸附后溶液的濃度.每個處理設3個平行,和空白處理(生物炭+H2O),應用統計學方法取均值進行分析.采用鉬酸銨分光光度法(GB11893-89)測定濾液中總 P的濃度,儀器為美國PE公司LAMBDA 25紫外可見分光光度計.并根據吸附試驗前后 P濃度的差值計算吸附量和去除率:
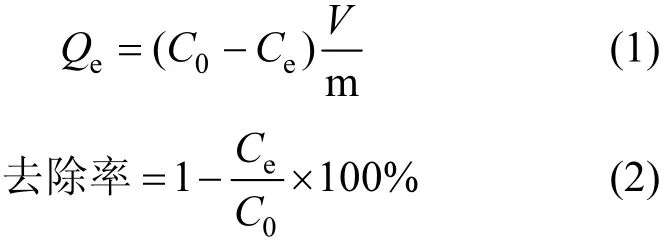
式中:Qe為吸附平衡的吸附量,mg/g;C0為初始溶液濃度,mg/L;Ce為吸附平衡時溶液濃度,mg/L;V為溶液體積,L;m為生物炭用量,g.
(2)等溫吸附試驗
P溶液的初始質量濃度分別設為1,2,5,10,20,50,80,120,200mg/L,稱取最佳改性比例的 Al-NB 0.1000g,吸附時間為 24h.溫度為 25℃.其余方法同上.
(3)吸附動力學試驗
吸附時間設置為 1,3,5,7,10,15,20,24,48h.稱取最佳改性比例的Al-NB 0.1000g,P溶液的初始質量濃度為50mg/L,溫度為25℃.其余方法同上.
(4)不同添加量對重金屬吸附的影響
分別取0.04,0.08,0.12,0.16,0.2,0.3g的最佳改性比例的Al-NB,設置P溶液的初始質量濃度為50mg/L,吸附時間為 24h.溫度為 25℃.其余方法同上.
(5)溶液初始pH的影響
采用1%HNO3和1%NaOH溶液,調節P溶液的初始 pH值,調節溶液初始pH值為1~12,稱取備選NB0.1000g,P溶液的初始質量濃度為100mg/L,吸附時間為24h,溫度為25℃.其余方法同上.
(6)吸附機理探索
將原始檸條生物炭,Al改性檸條生物炭,吸附 P的 Al改性檸條生物炭,三種樣品分別測試FTIR,表征生物炭的吸附點位和吸附P的機理.
化學試劑 HNO3、NaOH、AlCl3、KH2PO4、四水合鉬酸銨、酒石酸銻鉀、濃硫酸、抗壞血酸等均為分析純(北京化工廠),試驗用水均為二次去離子水.
1.4 模型分析
1.4.1 等溫吸附模型 吸附劑的吸附量隨著被吸附物濃度的增大而增大,最后達到吸附平衡.為了更好的研究吸附劑的吸附行為,常見的等溫吸附模型[13,30]有:
(1)Langmuir吸附方程

式中:Qe為吸附平衡的吸附量,mg/g;Qm為最大吸附量,mg/g;Ce為吸附平衡時溶液濃度,mg/L;a代表Langmuir吸附平衡常數.
通過Langmuir方程可進一步計算出吸附反應的平衡常數 RL,即 RL=1/(1+a×C0).無量綱參數分離因子RL可用來進一步表述吸附劑的吸附性能[31].若 RL值在 0~1范圍內,說明該吸附過程為有益吸附,RL=1表示線性吸附,RL=1表示不可逆吸附[13].
(2)Freundlich吸附方程

式中,KF和n是Freundlich常數,分別代表吸附劑的吸附能力和吸附強度.
(3)Temkim吸附方程

式中,A為平衡結合常數,mg/L;B是Temkim方程系數,與吸附熱有關.
(4)Dubinin-Radushkevich (D-R)吸附方程
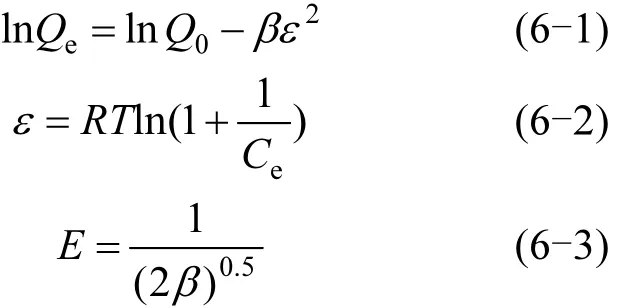
式中:β是D-R方程系數,mol2/J2;Q0是最大單位吸附量,mmol/g1;ε是Polanyi吸附勢;R為理想氣體常數8.314J/(mol·K);T為絕對溫度;E是吸附自由能,J/mol.
1.4.2 吸附動力學模型 吸附劑的吸附量隨著被吸附物時間的增大而增大,最后達到吸附平衡.為了明確吸附過程的反應級數和吸附機制,采用的吸附動力學模型[13,30]如下:
(1)準一級動力學方程
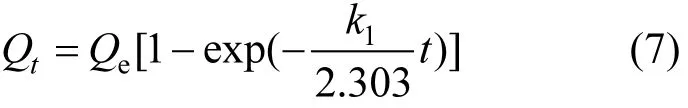
式中:Qt為t時的吸附量,mg/g;Qe為吸附平衡的吸附量,mg/g;k1為準一級吸附速率常數,min-1.
(2)準二級動力學方程
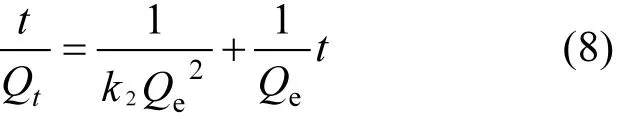
利用準二級動力學參數可以計算初始吸附速率
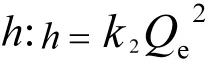
式中:k2為準二級吸附速率常數g/(mg·min).
(3)Elovich model
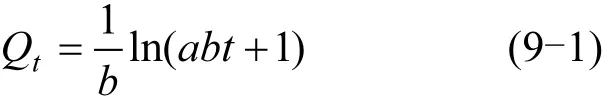
當abt>>1時,上述方程可以簡化為:

式中:a、b為Elovich方程常數,分別表示初始吸附速率(g/(mg·min) )及解吸常數(g/mg).
(4)顆粒內擴散模型

式中:ki為顆粒內擴散速率常數,mg/(g·min0.5);C為常數,表示吸附劑的邊界層數,對生物炭來說,C會隨生物炭表面異質性和親水性基團的增加而降低,C值越大說明邊界層對吸附的影響越大.
1.5 數據處理
本試驗數據采用Excel和SPSS 18.0統計分析,等溫吸附和吸附動力學曲線用Origin Pro 8.5擬合并作圖.
2 結果與分析
2.1 Al-NB生物炭的表征
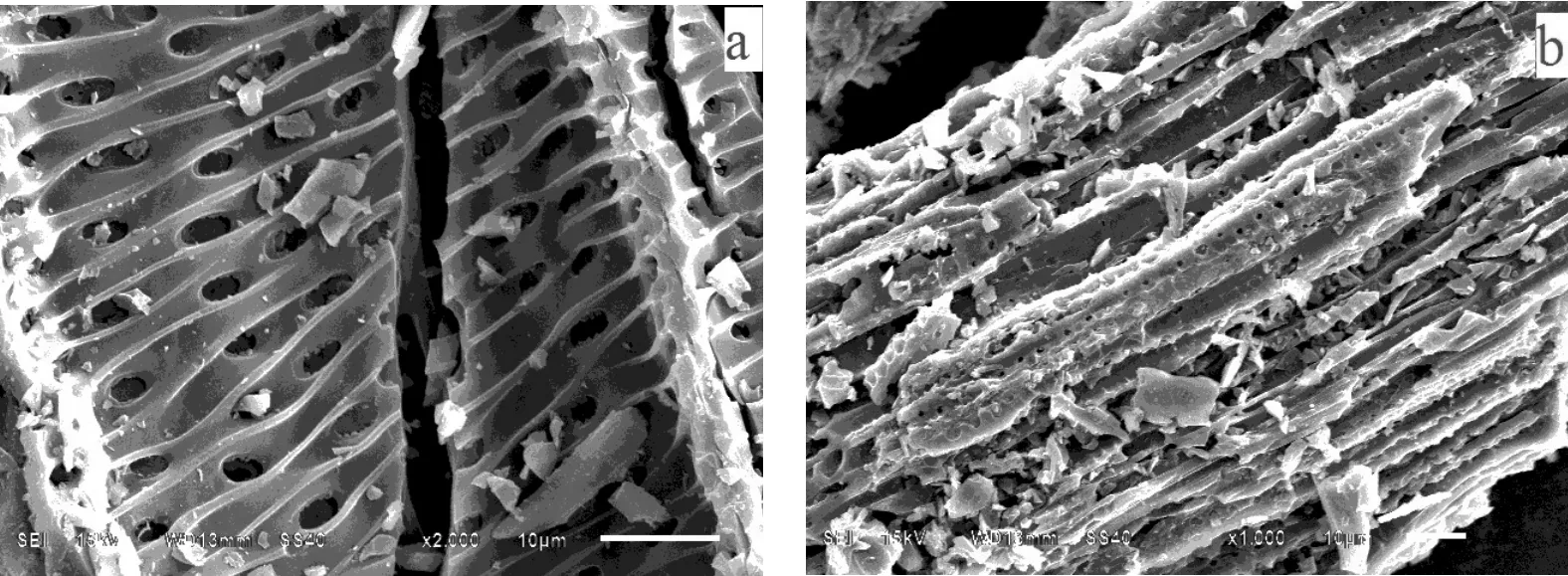

圖1 不同改性比例Al-NB的SEMFig.1 SEM images of different modified ratio on Al-NB
2.1.1 SEM分析 由圖1(a)可見,Al-NB(0:1)即未改性生物炭有纖維管狀結構的薄片,清晰的多孔結構,表面富含顆粒,因為是 650℃高溫下熱裂解的,有明顯的斷層.對比圖1(b、c)和1(a)可以發現Al-NB表面泛著刺眼的白色光斑,而這種光斑很有可能是 Al3+產生的金屬光澤,因為在相同熱解溫度和時間條件下制備的生物炭,除了Al改性修飾處理外,其余處理均相同,這間接證明Al3+被修飾到NB表層.圖1(d)是圖1(b)的放大處理,清楚的看到Al-NB的部分孔隙被某種物質填充,而這種填充物質,很可能是 Al3+.綜上可觀察到Al-NB的表面顆粒帶金屬光澤,許多孔隙和顆粒被包裹,均勻一體,且保留NB多孔的特性.很可能是因Al3+被修飾到NB表面所引起的.
2.1.2 元素分析 NB和Al-NB的元素分析結果見表3.可以明顯看出,Al-NB生物炭的Al元素含量增加,增長了63.4倍,證明Al3+被修飾到檸條生物炭.此外,Al改性前后,P元素含量變化不大,差異可能是由Al修飾劑中含有部分雜質所致.
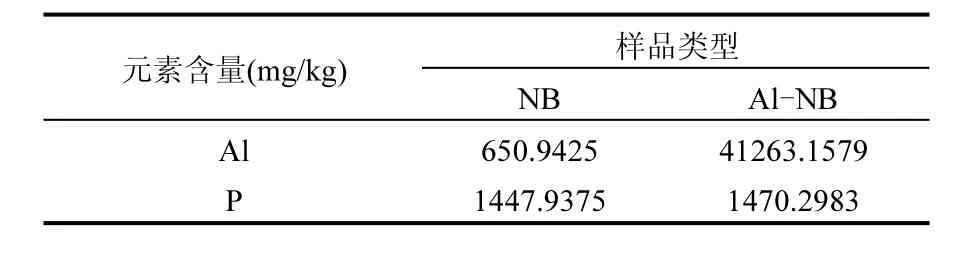
表3 Al-NB生物炭的ICP元素組成Table 3 Al modified NB elementary compositions by ICP
2.1.3 XRD分析 Al改性檸條生物炭前后的XRD如圖2所示,從XRD圖譜中可以明顯看出,標豎線的峰為氫氧化鋁特征峰,表面負載在檸條生物炭上的鋁主要以氫氧化鋁形式存在.這與余國文等[22]研究鋁改性竹炭結果一致,結晶程度最高的是氫氧化鋁.Li等[16]研究Mg/Al-LDHs雙金屬氫氧化物改性甘蔗生物炭與本研究的XRD出峰位置和峰形極其相似,表明Al以氫氧化物的形式被成功負載在檸條生物炭炭基骨架上.結合元素分析與SEM圖,可以確定Al被修飾到NB上.
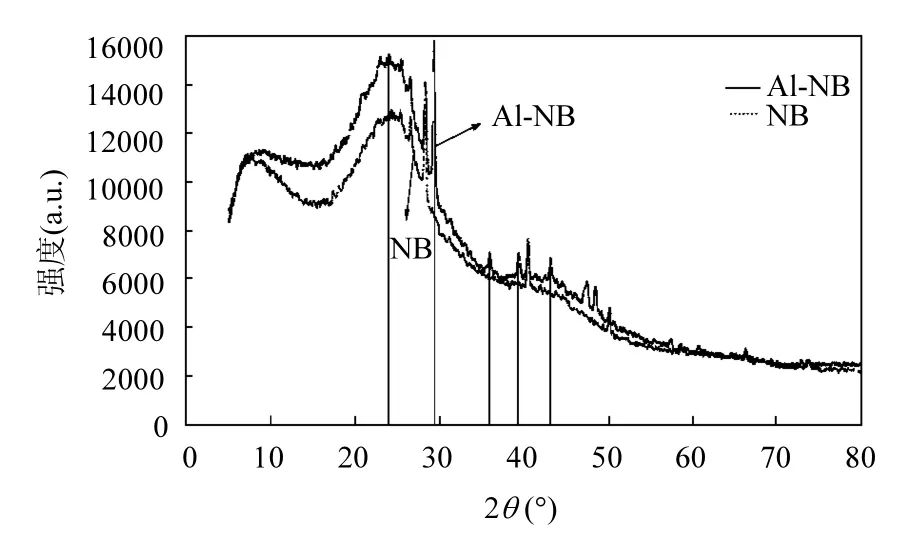
圖2 Al改性檸條生物炭前后的XRDFig.2 XRD patterns of NB and Al-NB
2.2 最佳改性比例的Al-NB生物炭的確定
由圖3可見,原始NB(即Al-NB 0:1)對P的吸附最大為1.38mg/g,而Al改性處理的檸條生物炭,無論何種改性比例,吸附量均明顯高于未改性的原始 NB.6種 Al-NB對 P的平均吸附量為10.84mg/g,是未改性NB的7.86倍,且隨著鋁炭比的增大,Al-NB對P的吸附量呈增大趨勢,直到鋁炭比為0.2:1時,吸附量達到最大,此時對 P的吸附量為 11.52mg/g,是未改性 NB的8.35倍.當鋁炭比繼續增大(Al-NB 0.27:1)時,吸附量下降,這意味著過高的 Al3+改性比例不利于吸附,主要因為高濃度的 Al3+會在表面吸附和液膜擴散完之后,在顆粒內擴散,占據了吸附點位,與P產生了競爭吸附;此外,進入顆粒內的Al3+對于生物炭表面改性正電荷吸附P作用不大.因此Al-NB生物炭最佳改性比例為0.2:1.

圖3 不同改性比例的Al-NB對P吸附量的影響Fig.3 Effect of Al-NB with different modification ratio on the adsorption capacity of P
2.3 Al-NB生物炭對P的等溫吸附過程
由圖4可見,Al-NB隨著P濃度的增加,吸附量也隨之增加.在低初始P濃度為1~20mg/L范圍時,吸附平衡的濃度范圍在 0.07~4.82mg/L之間,吸附曲線陡峭,P吸附量呈直線快速增加趨勢,由0.46mg/g增加到7.59mg/g.當初始P濃度范圍為50~200mg/L時,平衡液中P濃度從26.82mg/L增長到 160.11mg/L,而吸附量從 11.59mg/g緩慢增加到 19.94mg/g,最后吸附趨于穩定,達到吸附平衡.吸附曲線呈現先快后慢,這主要是因為吸附點位和吸附過程的進行所影響[13].
利用四種等溫吸附模型進行數據擬合,擬合曲線及相關參數由圖4和表4所示.Langmuir和Freundlich方程的擬合優度R2均大于0.9,明顯優于Temkin和D-R模型.Langmuir和Freundlich方程的R2極其接近,雖然Freundlich方程的R2稍大 0.005,但由 Langmuir模型計算的理論最大吸附量(19.97)與試驗所得數據(19.94)相差不大,說明Al-NB對P的吸附更符合Langmuir模型,這意味著吸附過程近似單分子層吸附.進一步研究發現,Li等[16]在研究Mg/Al改性生物炭吸附P時得出 Langmuir模型是最符合的等溫模型,此外,Chen等[26]和 Wang等[32]也得出相似的結果;其研究中對比多種方法改性生物炭,發現改性生物炭對P的吸附幾乎都更符合Langmuir模型的擬合.這可能是因為 Al3+被先吸附固定在原始生物炭表面,將生物炭表面負電荷改性為正電荷;然后P以單分子層方式被吸附在Al-NB表面,主要是由Al3+異性電荷吸附所致.
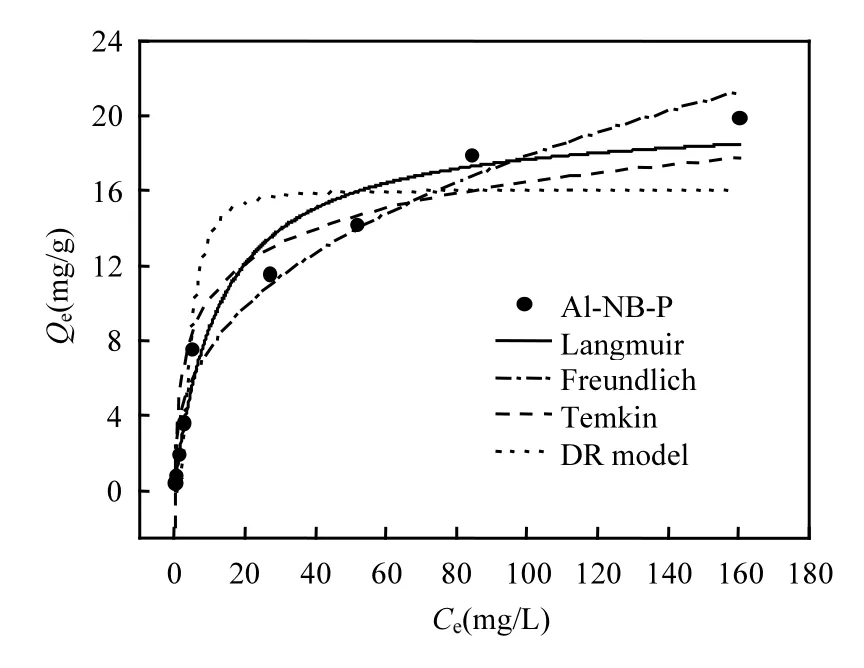
圖4 Al-NB對P等溫吸附曲線Fig.4 Isotherm adsorption of Al-NB biochar for P
在 Langmuir模型中,Qm為理論最大吸附量為19.97mg/g,比真實最大吸附量19.34mg/g稍大;由表 4中參數 a,和初始濃度 C0值計算得出 RL為0.06~0.86,表明P在Al-NB生物炭上的吸附為有益吸附.在Freundlich吸附模型中,n等于2.68大于2,說明Al-NB對P吸附強度較高.本試驗中Temkin模型擬合優度R2較高,說明Al-NB對P的吸附主要是化學吸附.由表3看出,Al-NB對P吸附能 E為 8.42kJ/mol,說明吸附行為以化學吸附為主,這與上文Temkin模型相互印證.Q0為單位最大吸附量,這與Langmuir方程中Qm有相似含義,兩者之間變化不大.
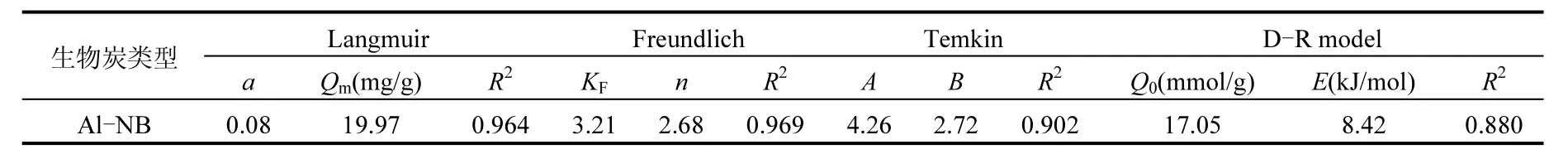
表4 Al-NB對P等溫吸附模型擬合參數Table 4 Isothermal adsorption fitting parameters of Al-NB for P
2.4 Al-NB生物炭對P的吸附動力學過程
吸附P的動力學過程如圖5所示.隨著吸附時間的增加,Al-NB生物炭對P的吸附大致表現為開始時吸附速率很快,大量吸附,然后曲線慢慢變緩,接著再快速吸附-緩慢吸附,最后達到吸附平衡,在48h時出現部分解吸現象,吸附量稍微降低.可以明顯看出,Al-NB生物炭對P的吸附較緩慢,吸附5h時,吸附量僅達飽和吸附量的49%,隨著吸附時間的增長,吸附量持續增加,吸附10h時,吸附量才到飽和吸附量的 89.7%,直到 24h時才達到飽和吸附,逐漸趨于吸附平衡.
利用四種吸附動力學方程擬合的模型參數由表5列出.可知,準一級動力學方程、準二級吸附動力學方程和Elovich模型的擬合優度R2均大于 0.9,而準一級動力學方程計算出的平衡濃度(12.06mg/g)與試驗值(11.96mg/g)基本相似,且 R2也相對較高,說明該模型適合用于描述Al-NB對P的吸附動力學過程.準一級動力學方程基于假定吸附受擴散步驟的控制,吸附速率正比于平衡吸附量與 t時刻吸附量的差值,用于描述主要通過邊界擴散完成的單層吸附,這與Langmuir模型解釋的單分子層吸附類似,可見 P以單分子層方式被吸附在Al-NB表面,主要是由Al3+異性電荷吸附所致.這與 Wang等[32]報道 La2O3改性修飾橡木生物炭對P的吸附結果一致.Ren等[33]研究生物炭吸附P時也得到類似.
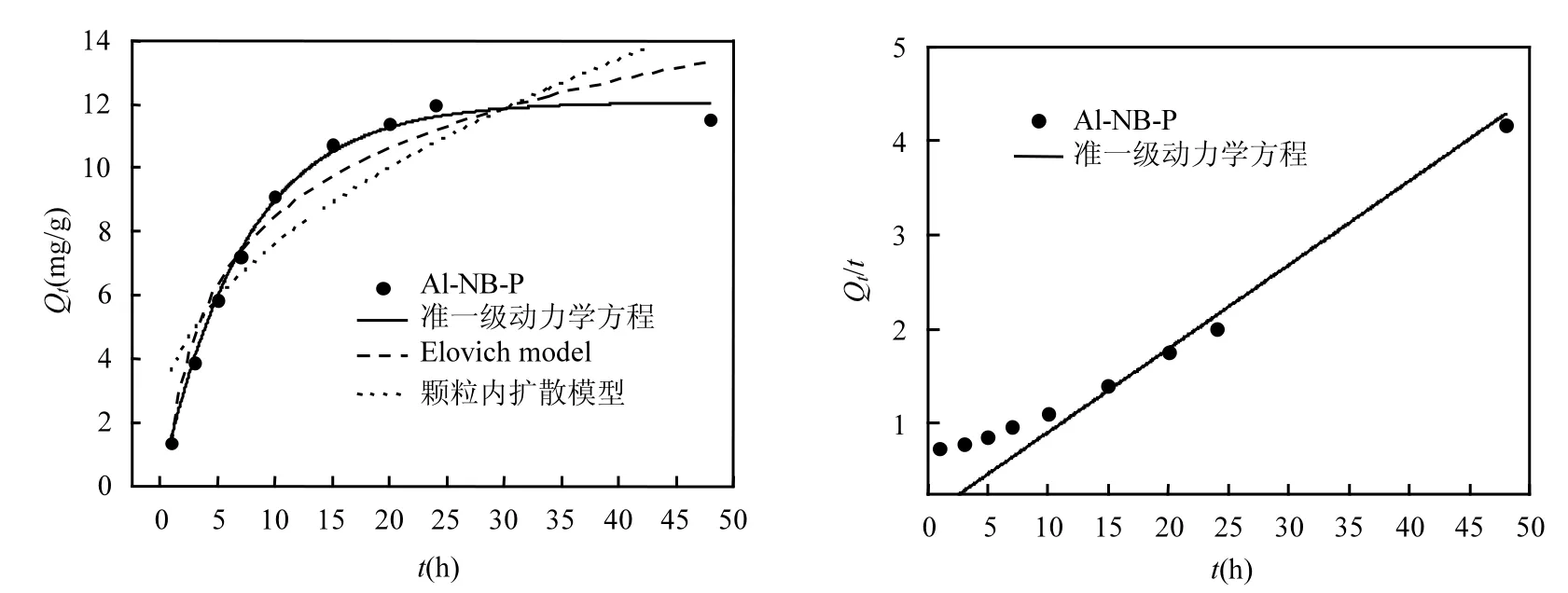
圖5 Al-NB生物炭對P吸附動力學曲線Fig.5 Adsorption Kinetics of Al-NB for P

表5 Al-NB生物炭對P等溫吸附模型擬合參數Table 5 Adsorption Kinetics fitting parameters of Al-NB for P
根據準二級動力學方程擬合參數,計算吸附速率h,得到h為0.008mg/(g·min),約每小時吸附0.5mg/g的P. Elovich模型的擬合優度R2較高,說明 Al-NB在整個吸附過程中具有均勻分布的表面吸附能,這很可能導致Al3+被均勻吸附在生物炭表面,然后 P被均勻的吸附在 Al-NB表面.b值為解吸常數,Al-NB對P的解吸常數為0.32較小,說明Al-NB對P的吸附較穩定,不容易解吸.對于顆粒內擴散模型,擬合直線沒有過原點,則說明顆粒擴散不是唯一限速因素,還有表面吸附和液膜擴散共同控制吸附反應速率.C值為 1.79,說明Al-NB的邊界層對P的吸附影響較小,這是因為 P的吸附影響因素很單一,主要是NB較大的比表面積和Al3+;表現為均勻的表面單分子層吸附.
2.5 添加量對Al-NB吸附P的影響

圖6 添加量對Al-NB吸附P的影響Fig.6 Effects of adsorbent dose on Al-NB adsorption of P
由圖 6可以看出,隨著檸條生物炭添加量的增大,對 P的吸附量不斷減小,去除率逐漸增加.當添加量在0.04~0.2g時,去除率從45%快速增加,增幅高達24%,添加量快速降低,直到0.2g時開始平緩.當添加量為 0.3g時,去除率達到 85%最高,吸附量也達到最低.這主要是由于吸附劑投加量的增加,總官能團數和有效的吸附點位增加,因此去除率也隨之增加[34];而吸附量隨著吸附劑投加量的增加而減小,可能與吸附劑的溶解性、結合位點之間的靜電感應和排斥作用有關[6].此外,根據公式(1)和(2)推算,去除率=m×C0×Qe/V,當溶液體積V和初始溶液濃度C0一定時,若生物炭添加質量m增加,(去除率/Qe)也相應增加;此時去除率增加則吸附量必然會減小.綜上,確定 Al-NB吸附P的最佳添加量為 0.125g/50mL,即為 2.5g/L;即圖6中,兩條曲線的交匯處所對應的橫坐標值.
2.6 pH對Al-NB吸附P的影響
由圖7可見,在pH=1~4時,隨著pH值的升高,Al-NB對P的吸附量增加.當pH=4~10時,Al-NB對P的吸附量呈穩定狀態,其中pH=7時,吸附量達到最大值 22.90mg/g.當pH=10~12時,隨著 pH值的升高,Al-NB對 P的吸附量呈現減小趨勢.這與馬鋒鋒等[6]和唐登勇等[35]研究初始pH對生物炭吸附P的變化一致.根據H3PO4的酸解離平衡式和平衡解離常數可知,pH為 6~8時,PO43-主要以H2PO4-和HPO42-陰離子形式存在[36],可與負載在檸條生物炭上的 Al3+發生吸附,隨 pH 值的升高,檸條生物炭表面有機官能團的酸離解度增加,且pH 值的升高更有利于重金屬離子水解,更容易吸附陰離子[35].馬鋒鋒等[6]認為隨 pH 值的升高,HPO42-含量以數量級的倍數增加,膠體界面的電量增強,也是吸附量增加的原因.隨著 pH增大超過10時,溶液中OH-濃度增加,與PO43-產生了競爭,由于總的吸附位點是一定的,不利于吸附的進行,且溶液中的 Al3+發生沉淀作用,導致水溶液中Al3+平衡濃度降低,Al-NB生物炭表面正電荷減弱,P的吸附量逐漸降低[6].該吸附適應的pH范圍較寬,這有利于檸條生物炭的實際應用.
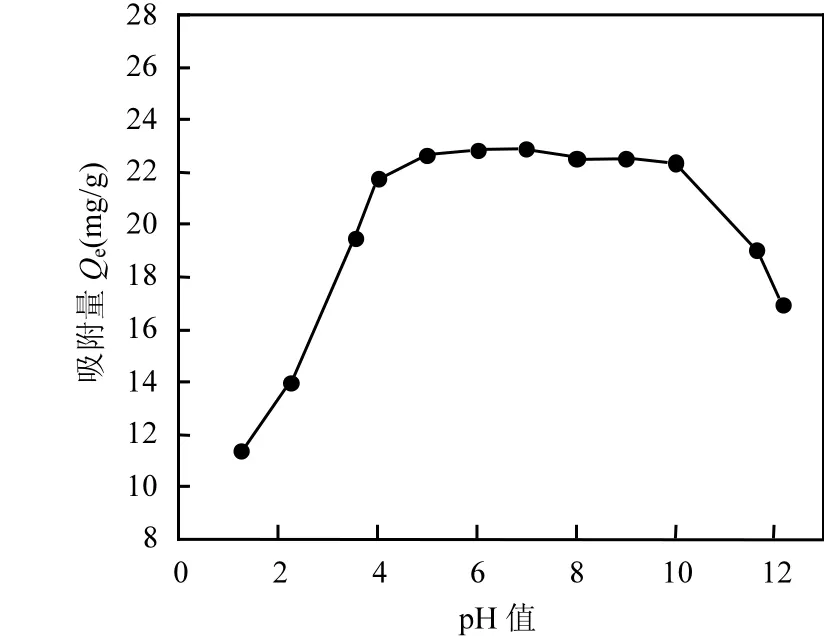
圖7 初始pH對Al-NB吸附P的影響Fig.7 Effects of initial pH on NB adsorption of P
由圖8可以看出,在酸性范圍時,平衡pH大于初始初始 pH值,點在對角線之上,這說明添加了Al-NB吸附P后,溶液的pH值升高了.在堿性范圍內,平衡pH小于初始初始pH值,點在對角線之下,這說明添加了Al-NB吸附P后,溶液的pH值降低了.可以判斷出,添加了 Al改性檸條生物炭后,吸附P時,溶液的pH值有向中性范圍傾靠的趨勢,起到一定的緩沖作用.筆者認為這很可能是因為 Al是兩性物質,在酸堿平衡中十分活躍,起到了酸堿緩沖劑的作用,而Al-NB在結構上存在Al3+,在性質上保留了Al的兩性.
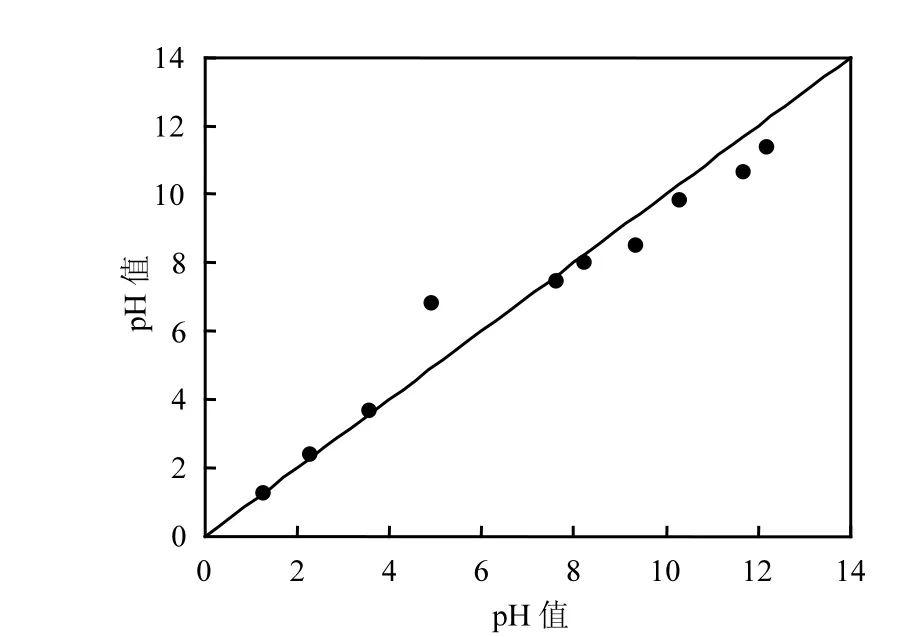
圖8 Al-NB吸附P前后pH值對比Fig.8 Effect of solution initial pH on equilibrium solution pH
3 討論
3.1 Al-NB對P的吸附機制探討
Al-NB吸附P前后的FTIR譜圖如圖9所示,經過基線校正處理.可以看出,3418cm-1處的—OH基共振峰明顯減弱,說明—OH基被P占據,分子內—OH中的分子氫鍵作用力減弱;因為羥基在吸附劑上是以共價鍵存在,并不是離子,所以羥基交換一般認為是配體交換過程,可見配體交換存在于生物炭吸附 P過程中[16];557cm-1處和630cm-1處的 Al—O 吸收共振峰也明顯減弱,說明Al—O基參與了P的吸附過程,Li等[16]也有此處官能團吸附 P的報道.加之,Al-NB吸附 P后717cm-1處的峰向 730cm-1處偏移轉化,973cm-1處的峰完全消失,903cm-1處的峰開始減弱;在1053cm-1處出現了一個很強的不對稱峰,這個峰是 P—O 基(PO43-、HPO42-和H2PO4-均有可能存在),這意味著P通過潛在的單原子螯合配位和雙齒顆粒內表面絡合作用,被強烈的吸附在重金屬氧化物表面(Al—O),Nero等[37],Li等[38],Novillo等[39]和 Li等[16]均有類似的報道.另一方面,在1053cm-1處的旁邊,可以清晰的看到1130cm-1的肩峰,Nero等[37]和 Li等[38]認為出現這種現象主要是因為球外(顆粒外)表面絡合作用的產生所致,例如 HPO42-或 H2PO4-被Al-NB表面正電荷吸引.1384cm-1處的N—O伸縮峰發生改變,這說明Al-NB表面的一些陰離子(NO3-)被釋放出來,與HPO42-或H2PO4-等陰離子進行交換,所以Al-NB吸附P之后此處峰強烈顯示出來.
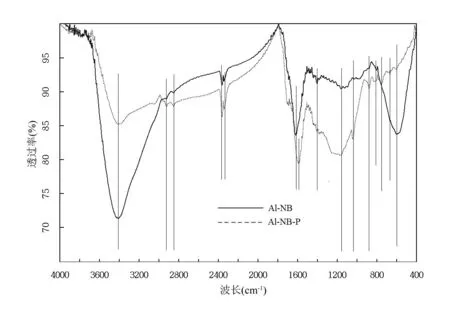
圖9 Al-NB生物炭吸附P前后FTIR譜圖對比Fig.9 FTIR spectrograms of Al-NB before and after the absorption for P
其次,在1396cm-1處的NH4+因為異性電荷吸引作用,可以吸附P,所以此處的峰發生右移,且此處的峰變的更高,更為明顯.2280cm-1左右的脂肪類C—H和C=O基和2900cm-1左右的甲基峰增強,這可能是因為在Al-NB表面此處結合的Al3+與P發生吸附,濃度降低,檸條生物炭自身的官能團被重新釋放所致.基于以上分析,P被Al-NB吸附的機制主要包括:靜電吸附作用(主要是帶正電荷的金屬氧化物與含P陰離子吸附,NH4+的電荷吸附作用),配體交換(羥基),P與陰離子交換,顆粒內表面絡合作用等.
3.2 不同改性方法制備的生物炭對P的吸附能力差異
統計不同改性方法制備的各類生物炭對 P吸附的相關報道,整理出表6.通過對比發現,本文研究的Al改性檸條生物炭對P的吸附效果普遍高于未改性的生物炭(各類不同源材料制備),Fe改性生物炭和Mg改性蘆葦/互花米草生物炭,低于其他 Mg或者化學方法改性制備的生物炭.結合表2可以發現,檸條制備成生物炭后,多點BET比表面積增大了69.6倍,吸附總孔體積也相應的增加,呈介孔狀態[40].綜合平衡時間,制備溫度,改性方法難易程度及成本等因素來看,Al-NB有一定的應用價值.
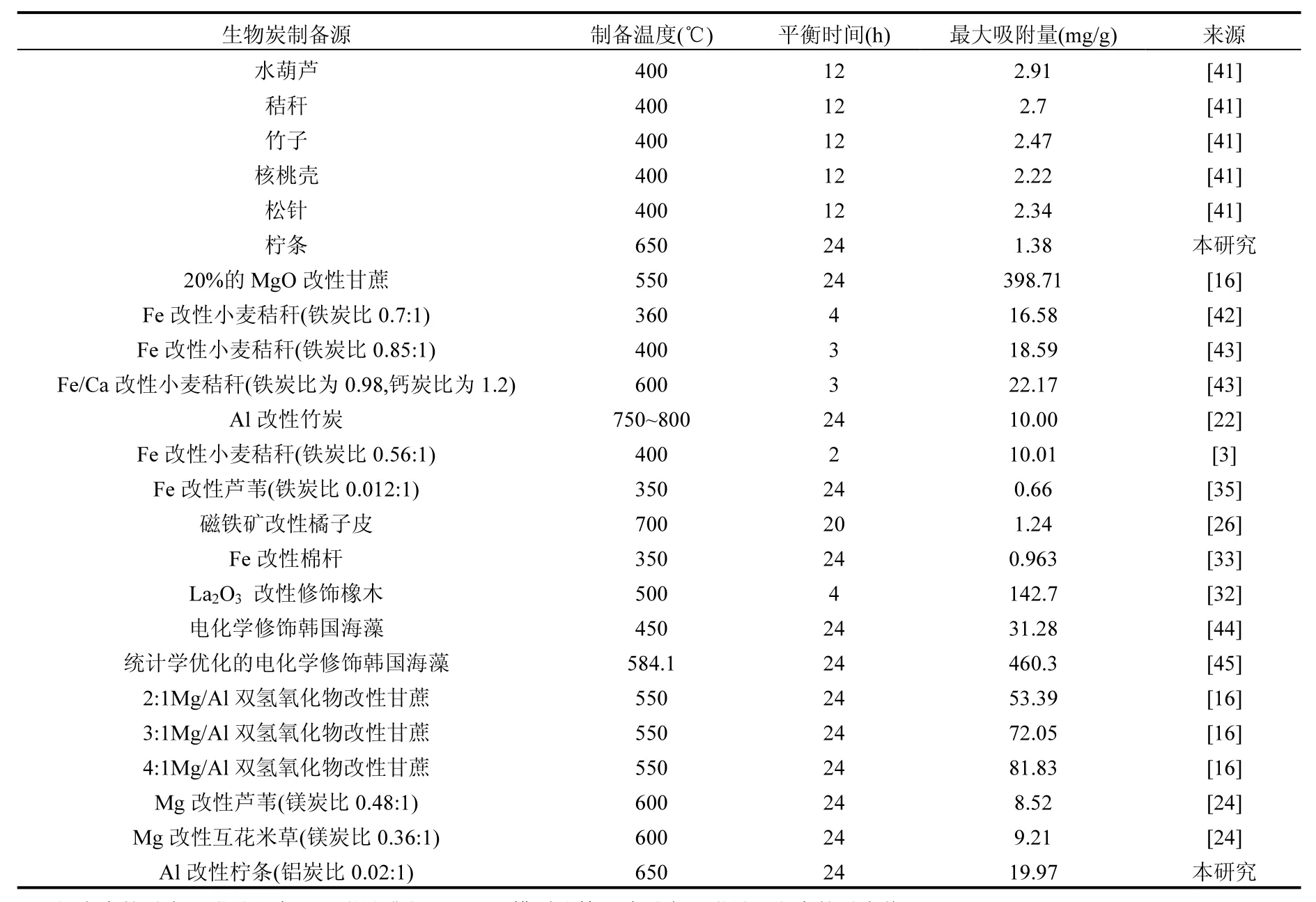
表6 不同改性生方法制備的生物炭對P的吸附性能力比較Table 6 Comparison of sorption capacity of Al-NB with selected biochars derived from different materials and modified method for P
4 結論
4.1 Al-NB生物炭最佳改性比例為 0.2:1,是未改性NB的8.35倍.Langmuir模型能夠很好的描述檸Al-NB對P的等溫吸附過程,這說明吸附過程主要是近似單分子層的吸附,且為有益吸附;Al-NB對P的吸附動力學符合準一級動力學模型,說明其吸附通過邊界擴散完成的單層吸附,結合其他模型來看,顆粒內擴散與表面吸附和液膜擴散等共同控制吸附反應速率.
4.2 Al-NB對P的理論最大吸附量為19.97mg/g,平衡時間為 24h.隨著添加量的增大,Al-NB對P的吸附量不斷減小,去除率逐漸增加,2.5g/L為最佳添加量.pH在4~10時Al-NB對P的吸附效果良好,當 pH=7時,達到最佳;吸附 P后,溶液的pH值有向中性范圍傾靠的趨勢,Al-NB起到一定的緩沖作用.
4.3 P被Al-NB吸附的機制主要包括:靜電作用(主要是帶正電荷的金屬氧化物與含P陰離子吸附,NH4+的電荷吸附作用),配體交換(羥基),與陰離子(NO3-)交換,顆粒內表面絡合作用等.
4.4 Al改性檸條生物炭對P的吸附效果普遍高于未改性的生物炭和Fe改性生物炭,低于Mg或者其他方法改性制備的生物炭,具有一定的應用價值.
[1]Yao Y, Gao B, Chen J J, et al. Engineered biochar reclaiming phosphate from aqueous solutions: mechanisms and potential application as a slow-release fertilizer [J]. Environmental science& technology, 2013,47(15):8700-8708.
[2]吳慧芳,胡文華.聚合氯化鋁污泥吸附除磷的改性研究 [J]. 中國環境科學, 2011,31(8):1289-1294.
[3]蔣旭濤,遲 杰.鐵改性生物炭對磷的吸附及磷形態的變化特征[J]. 農業環境科學學報, 2014,33(9):1817-1822.
[4]Smith V H. Eutrophication of freshwater and coastal marine ecosystems a global problem [J]. Environmental Science and Pollution Research, 2003,10(2):126-139.
[5]Boujelben N, Bouzid J, Elouear Z, et al. Phosphorus removal from aqueous solution using iron coated natural and engineered sorbents [J]. Journal of Hazardous Materials, 2008,151(1):103-110.
[6]馬鋒鋒,趙保衛,鐘金魁,等.牛糞生物炭對磷的吸附特性及其影響因素研究 [J]. 中國環境科學, 2015,35(4):1156-1163.
[7]孫海軍,馮彥房,曹學鴻,等. Al/Zn 改性竹炭去除水體中PO43-離子及影響因素的研究 [J]. 水處理技術, 2017,43(8):40-43.
[8]Altmann J, Rehfeld D, Tr?der K, et al. Combination of granular activated carbon adsorption and deep-bed filtration as a single advanced wastewater treatment step for organic micropollutant and phosphorus removal [J]. Water research, 2016,92:131-139.
[9]Chen T H, Wang J Z, Wang J, et al. Phosphorus removal from aqueous solutions containing low concentration of phosphate using pyrite calcinate sorbent [J]. International Journal of Environmental Science and Technology, 2015,12(3):885-892.
[10]萬 霞,梅昌艮,何俐臻,等.磁性生物炭的制備,表征及對磷的吸附特性 [J]. 安全與環境學報, 2017,17(3):1069-1075.
[11]胡菲菲,何丕文.不同熱解溫度制備的雞糞生物炭對廢水中磷的吸附 [J]. 湖北農業科學, 2014,53(8):1774-1778.
[12]Ma Z H, Li Q, Yue Q Y, et al. Adsorption removal of ammonium and phosphate from water by fertilizer controlled release agent prepared from wheat straw [J]. Chemical Engineering Journal,2011,171(3):1209-1217.
[13]王彤彤,馬江波,曲 東,等.兩種木材生物炭對銅離子的吸附特性及其機理研究 [J]. 環境科學, 2017,38(5):2161-2171.
[14]Ok Y S, Chang S X, Gao B, et al. SMART biochar technology—a shifting paradigm towards advanced materials and healthcare research [J]. Environmental Technology & Innovation, 2015,4:206-209.
[15]Wang T T, Stewart C E, Ma J B, et al. Applicability of five models to simulate water infiltration into soil with added biochar[J]. Journal of Arid Land, 2017,9(5):701-711.
[16]Li R, Wang J J, Zhou B, et al. Enhancing phosphate adsorption by Mg/Al layered double hydroxide functionalized biochar with different Mg/Al ratios [J]. Science of the Total Environment,2016,559:121-129.
[17]Han Y T, Cao X, Ouyang X, et al. Adsorption kinetics of magnetic biochar derived from peanut hull on removal of Cr (VI)from aqueous solution: effects of production conditions and particle size [J]. Chemosphere, 2016,145:336-341.
[18]Mohan D, Sarswat A, Ok Y S, et al. Organic and inorganic contaminants removal from water with biochar, a renewable, low cost and sustainable adsorbent—a critical review [J]. Bioresource technology, 2014,160:191-202.
[19]Mukherjee A, Zimmerman A R, Harris W. Surface chemistry variations among a series of laboratory-produced biochars [J].Geoderma, 2011,163(3/4):247-255.
[20]Namasivayam C, Sangeetha D. Equilibrium and kinetic studies of adsorption of phosphate onto ZnCl2, activated coir pith carbon [J].Journal of Colloid & Interface Science, 2004,280(2):359-365.
[21]Yao Y, Gao B, Zhang M, et al. Effect of biochar amendment on sorption and leaching of nitrate, ammonium, and phosphate in a sandy soil [J]. Chemosphere, 2012,89(11):1467-1471.
[22]余國文,章北平,丁興輝.鋁改性竹炭的磷吸附性能研究 [J]. 華中科技大學學報(自然科學版), 2015,43(10):117-122.
[23]Yaghi N, Hartikainen H. Enhancement of phosphorus sorption onto light expanded clay aggregates by means of aluminum and iron oxide coatings [J]. Chemosphere, 2013,93(9):1879-1886.
[24]孟慶瑞,崔心紅,朱 義,等.載氧化鎂水生植物生物炭的特性表征及對水中磷的吸 [J]. 環境科學學報, 2017,37(8):2960-2967.
[25]Wang C H, Gao S J, Wang T X, et al. Effectiveness of sequential thermal and acid activation on phosphorus removal by ferric and alum water treatment residuals [J]. Chemical Engineering Journal,2011,172(2):885-891.
[26]Chen B, Chen Z, Lv S. A novel magnetic biochar efficiently sorbs organic pollutants and phosphate [J]. Bioresource technology,2011,102(2):716-723.
[27]Zhang M, Gao B, Yao Y, et al. Synthesis of porous MgO-biochar nanocomposites for removal of phosphate and nitrate from aqueous solutions [J]. Chemical Engineering Journal, 2012,210:26-32.
[28]公丕濤.檸條生物炭生產及其對半干旱地區土壤微生態環境的影響 [D]. 北京:中國林業科學研究院, 2014.
[29]鮑士旦.土壤農化分析(第三版) [M]. 北京:中國農業出版社,2003.
[30]常 春,王勝利,郭景陽,等.不同熱解條件下合成生物炭對銅離子的吸附動力學研究 [J]. 環境科學學報, 2016,36(7):2491-2502.
[31]Mohan D, Sarswat A, Ok Y S, et al. Organic and inorganic contaminants removal from water with biochar, a renewable, low cost and sustainable adsorbent—a critical review [J]. Bioresource technology, 2014,160(5):191-202.
[32]Wang Z, Guo H, Shen F, et al. Biochar produced from oak sawdust by Lanthanum (La)-involved pyrolysis for adsorption of ammonium (NH4+), nitrate (NO3?), and phosphate (PO43?) [J].Chemosphere, 2015,119:646-653.
[33]Ren J, Li N, Li L, et al. Granulation and ferric oxides loading enable biochar derived from cotton stalk to remove phosphate from water [J]. Bioresource technology, 2015,178:119-125.
[34]Pellera F M, Giannis A, Kalderis D, et al. Adsorption of Cu(II)ions from aqueous solutions on biochars prepared from agricultural by-products [J]. Journal of Environmental Management, 2012,96(1):35-42.
[35]唐登勇,黃 越,胥瑞晨,等.改性蘆葦生物炭對水中低濃度磷的吸附特征 [J]. 環境科學, 2016,37(6):2195-2201.
[36]Chen N, Feng C, Zhang Z, et al. Preparation and characterization of lanthanum(III) loaded granular ceramic for phosphorus adsorption from aqueous solution [J]. Journal of the Taiwan Institute of Chemical Engineers, 2012,43(5):783-789.
[37]Nero M D, Galindo C, Barillon R, et al. Surface reactivity of α-Al2O3, and mechanisms of phosphate sorption: In situ, ATRFTIR spectroscopy and ζ, potential studies [J]. Journal of Colloid& Interface Science, 2010,342(2):437—444.
[38]Li W, Pierre-Louis A M, Kwon K D, et al. Molecular level investigations of phosphate sorption on corundum (α-Al2O3) by 31P solid state NMR, ATR-FTIR and quantum chemical calculation [J]. Geochimica et Cosmochimica Acta, 2013,107:252-266.
[39]Novillo C, Guaya D, Avenda?o A A P, et al. Evaluation of phosphate removal capacity of Mg/Al layered double hydroxides from aqueous solutions [J]. Fuel, 2014,138:72-79.
[40]Hverett D H. IUPAC manual of symbols and terminology for physicochemical quantities and units [J]. Pure and applied chemistry, 1972,31(4):579-638.
[41]代銀分,李永梅,范茂攀,等.不同原料生物炭對磷的吸附-解吸能力及其對土壤磷吸附解析的影響 [J]. 山西農業大學學報:自然科學版, 2016,36(5):345-351.
[42]李際會.改性生物炭吸附硝酸鹽和磷酸鹽研究 [D]. 北京:中國農業科學院, 2012.
[43]李際會.小麥秸稈炭改性活化及其氮磷吸附效應研究 [D]. 北京:中國農業科學院, 2015.
[44]Jung K W, Hwang M J, Jeong T U, et al. A novel approach for preparation of modified-biochar derived from marine macroalgae:dual purpose electro-modification for improvement of surface area and metal impregnation [J]. Bioresource technology, 2015,191:342-345.
[45]Jung K W, Jeong T U, Kang H J, et al. Preparation of modifiedbiochar from Laminaria japonica: Simultaneous optimization of aluminum electrode-based electro-modification and pyrolysis processes and its application for phosphate removal [J].Bioresource technology, 2016,214:548-557.

