白酒中揮發性苦澀味物質的提取和分離
王尹葉,范文來,徐巖
(江南大學 生物工程學院,釀造微生物與應用酶學研究室,教育部工業生物技術重點實驗室,江蘇 無錫,214122)
苦味和澀味是白酒中常見的異味[1],直接影響著白酒的品質。我國各香型白酒都不同程度地存在苦、澀味問題。早期有學者推測白酒中呈苦味化合物可能是正丙醇、1-丁醇、異丁醇、異戊醇、糠醛、丙烯醛、單寧、硫化物、氨基酸等;呈澀味的化合物主要是乳酸、乳酸乙酯、異丁醇、異戊醇、糠醛和單寧等[2-3]。應用現代味覺研究技術即味覺稀釋分析(taste dilution analysis,TDA)[4]研究發現,乳酸、2-糠酸、2-羥基-3-甲基丁酸、2,3-二羥基丙酸、富馬酸、馬來酸、3-苯基乳酸、檸檬酸和琥珀酸在白酒中呈澀味[5]。然而,到目前為止,鮮見白酒中揮發性呈味物質的研究報道。
TDA技術是國際上研究食品味覺的常用方法[4],即用感官評價與儀器分析結合的方法在食品中分離和鑒定不揮發的味覺活性物質。如運用TDA研究發現羥基苯甲酸乙酯和羥基肉桂酸乙酯是葡萄酒的重要苦味化合物;羥基苯甲酸、羥基肉桂酸、黃酮-3-醇糖苷和二氫黃酮-3-醇鼠李糖苷被確定為葡萄酒的關鍵澀味化合物[6]。TDA技術還用于糖/氨基酸混合物發生美拉德反應的產物[4]、咖啡[7]、燕麥[8]、胡蘿卜[9]、啤酒[10]、榛子[11]和奶酪[12]中呈苦味化合物研究;黑茶[13]、紅醋栗[14]、菠菜[15]中呈澀味物質研究。但是,目前尚未有對揮發性呈味物質的研究報道。
本研究運用TDA的思路,擬建立一種白酒中揮發性苦味和澀味化合物提取、分離和鑒定的方法,以期確定白酒中呈苦味和澀味的揮發性物質,為消減白酒苦澀味,提升白酒品質提供理論指導。
1 材料與方法
1.1 材料與試劑
白酒樣品:芝麻香型原酒(64%vol)。
標準品與試劑: 乙醇、正丙醇、1-丁醇、2-甲基丙醇、3-甲基丁醇、糠醛、乳酸乙酯、乳酸、蔗糖、鹽酸奎寧、NaCl、谷氨酸鈉、單寧酸、磷酸和戊烷均為色譜級,購自美國Sigma-Aldrich公司;無水乙醚為分析純,購自國藥集團,使用前進行重蒸。進行感官分析所用水為娃哈哈純凈水(購自杭州娃哈哈集團有限公司),使用前用1 mol/L磷酸(GRAS列為食品和藥物中的添加劑[16])將pH值調節至3.8。
1.2 儀器與設備
旋轉蒸發儀R-300,瑞士Buchi公司;便攜式密度計DM 35,奧地利Anton Paar 公司;GC-6890N-MSD 5975,美國Agilent 公司;Waters半制備液相色譜(配有Waters 2627自動進樣器、Waters 2489紫外/可見光檢測器、Waters 2535 四元泵洗脫系統),美國Waters 公司; N-EVAP111 氮吹儀,美國Organomation 公司。
1.3 試驗方法
1.3.1 味覺品評訓練
味覺品評小組由從事白酒風味研究的10名學生和1 名具有12 年以上感官分析經驗的教師組成,所有成員均沒有味覺障礙史,且定期參加味覺培訓(至少每周1次,持續2年)[4]。為盡可能減少任何有毒化合物的攝入,采用吞-吐法[13]進行感官分析,即試驗材料1 mL放入口腔中,在口腔中保持10 s后吐出。
1.3.2 真空旋轉蒸發
50 mL樣品在30 ℃水浴條件下進行真空(10 kPa)旋轉蒸發,得到揮發性組分和不揮發組分,揮發性組分直接用于品嘗,不揮發組分經真空冷凍干燥[6],并用純凈水復溶。采用0~5六點刻度法對2個組進行味覺品評。為防止嗅覺的干擾,味覺品評需要戴鼻夾。
1.3.3 梯度減壓蒸餾提取白酒中呈苦味和澀味的化合物
取100 mL酒樣置于250 mL旋轉蒸發瓶中,進行梯度減壓蒸餾(0.08、0.06、0.04、0.02 MPa),設置不同水浴加熱溫度(40、50、60、70、80、85、90 ℃),探索在最小真空度(0.08 MPa)能蒸餾出液體的最小加熱溫度,并在此溫度下進行減壓蒸餾,收集接收相。每1個梯度真空度條件蒸餾至5 min內沒有液體滴下記為蒸餾結束,記錄每1個梯度真空條件下蒸餾時間和餾出組分體積。共收集到4個餾出組分,標記為組分A、B、C和D,對餾出組分進行感官品評。
1.3.4 半制備分離
對梯度減壓蒸餾提取到的呈苦味和澀味的組分B進行半制備分離。分離條件:進樣量800 μL;流動相A:乙醇,流動相B:水;采用X Bridge?Pre C18色譜柱(10 mm×250 mm,1.8 μm,Waters公司),流速3 mL/min,檢測波長277 nm。洗脫條件:乙醇和水初始體積比5∶95,乙醇在8 min內上升至20%,20 min上升至50%,12 min升至100%,并維持25 min。按色譜峰收集到10 個亞組分,并標記為B-1~B-10,制備分離運行10 個回合,合并收集的相應組分,對所有組分進行溶劑萃取。
1.3.5 溶劑萃取
用密度計(DM 35)分別測量半制備組分B-1~B-10的酒精體積分數,并用純凈水稀釋至10%,每1個組分分別使用戊烷和乙醚進行萃取,每個溶劑萃取3次(萃取劑的使用體積是稀釋后組分總體積的50%)。收集到的有機相平均分成2份,1份氮吹濃縮至250 μL用于GC-MS進樣;另1份用4 mL純凈水水洗,恢復到原始體積,水洗相使用真空旋轉蒸發去除有機溶劑,用于味覺品評,選擇強度較大的亞組分進行TDA分析。其中戊烷萃取水洗相命名為“B-X-I” (X是指1~10),乙醚萃取水洗相命名為“B-X-II”,殘留相標記為“B-X-III”。
1.3.6 TDA
根據感官評價結果(表 3),對所有呈味亞組分(1~3 mL)分別用純凈水1∶1,1∶2,1∶4,……,稀釋,進行品評,計算TD值。其中苦味用三角試驗測定,澀味采用半舌測定[6]。
1.3.7 呈味化合物鑒定
對TD值較大的亞組分進行GC-MS分析,呈味化合物基于質譜庫檢索與標準品驗證比對以及對標準品感官驗證鑒定。
13.8 GC-MS條件
色譜柱:FFAP極性柱(60 m×0.25 mm×0.25 mm),進樣口溫度250 ℃;升溫程序:初溫50 ℃,保持2 min,以6 ℃/min 速率升溫至230 ℃,保持45 min;載氣(He),流速2 mL/min;進樣1 μL,不分流進樣。
質譜條件:離子源230 ℃,EI電離源,電子轟擊能量70 eV,掃描范圍為35~350 amu。
2 結果與討論
2.1 真空旋轉蒸發
通過真空旋轉蒸發,將白酒樣品分成揮發性組分和不揮發組分。感官品評結果表明,澀味、苦味和甜味主要集中在揮發性組分中(表 1),這與葡萄酒[6]和啤酒[10]中的苦味和澀味物質不同。
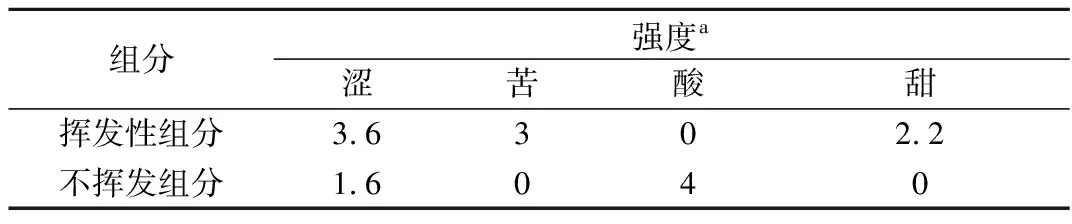
表1 真空旋轉蒸發分離白酒中揮發和不揮發物質的味覺評價Table 1 Sensory evaluation of the volatile and nonvolatile compounds in Baijiu separated by vacuum rotary evaporation
注:a:強度采用0~5六點強度法打分,0:沒有感覺到;5:感覺很強烈。
2.2 梯度減壓蒸餾
設置不同水浴加熱溫度(40、50、60、70、80、85、90℃),探索最小真空度0.08 MPa條件下能蒸餾出液體的最低溫度。實驗發現,只有水浴溫度達85 ℃之后,接收相才有液體餾出,故選取85 ℃作為水浴加熱條件,對樣品進行梯度減壓蒸餾。
通過減壓蒸餾分別接收到 A、B、C和D四個組分,對4個組分進行味覺品評(表 2)。組分A體積最大為61 mL,主要呈甜味,強度為3.0;組分 B體積最小,9 mL,但呈現了最強烈的澀味(4.6)和苦味(4.4);組分C表現出較低的澀味(2.1)和苦味(1.8)強度;組分D主要呈現酸味(4.8)和輕微收斂的澀味(2.0)。基于感官品嘗結果,重點研究組分B。
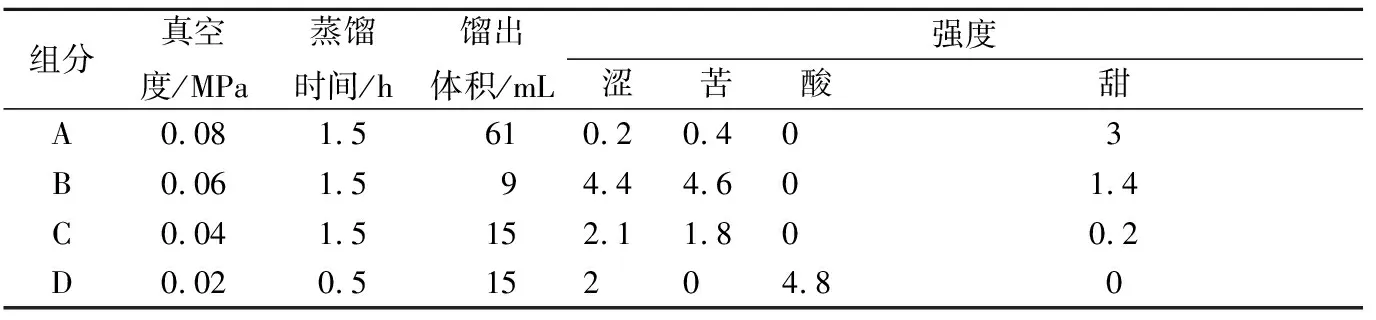
表2 梯度減壓蒸餾分離組分A-D的味覺品評Table 2 Sensorial evaluation of fractions A-D from gradient vacuum distillation
2.3 味覺活性物質分離
為了減少干擾,方便揮發性呈苦、澀味化合物的鑒定,對組分B進行半制備分離,根據色譜峰收集到10個亞組分B-1~B-10。由于分離出的呈苦味和澀味的化合物是揮發性的,因此選用戊烷和乙醚分別進行萃取,收集每個亞組分的有機相,平均分成2份,1份進行GC-MS分析,另1份水洗后真空旋轉蒸發除去溶劑進行味覺品評。
呈味化合物主要存在于乙醚萃取相中,即亞組分II中(表 3),且既呈澀味又呈苦味。其中亞組分 B-8-II的苦味和澀味強度最大,分別為4.6和4;其次是亞組分B-2-II,強度分別為3.4和3.2;再次是亞組分B-3-II,強度分別為3和2.6。戊烷萃取相(亞組分I)幾乎沒有味覺活性;萃取后殘留相(亞組分III)中的B-4-III、B-6-III和B-8-III呈現輕微的味覺特征。
運用三角試驗和半舌試驗對乙醚萃取相(亞組分II)進行TDA分析。TD值最大的是亞組分B-8-II(表 4),澀味TD值128,其次是亞組分B-2-II,為64;第3是亞組分B-3-II,稀釋32倍后仍能感受到澀味。此外,亞組分B-8-II也顯示了最強烈的苦味,其TD值為32(表 4),亞組分B-2-II和B-3-II的苦味TD值均為16,亞組分B-4-II的TD值為8。
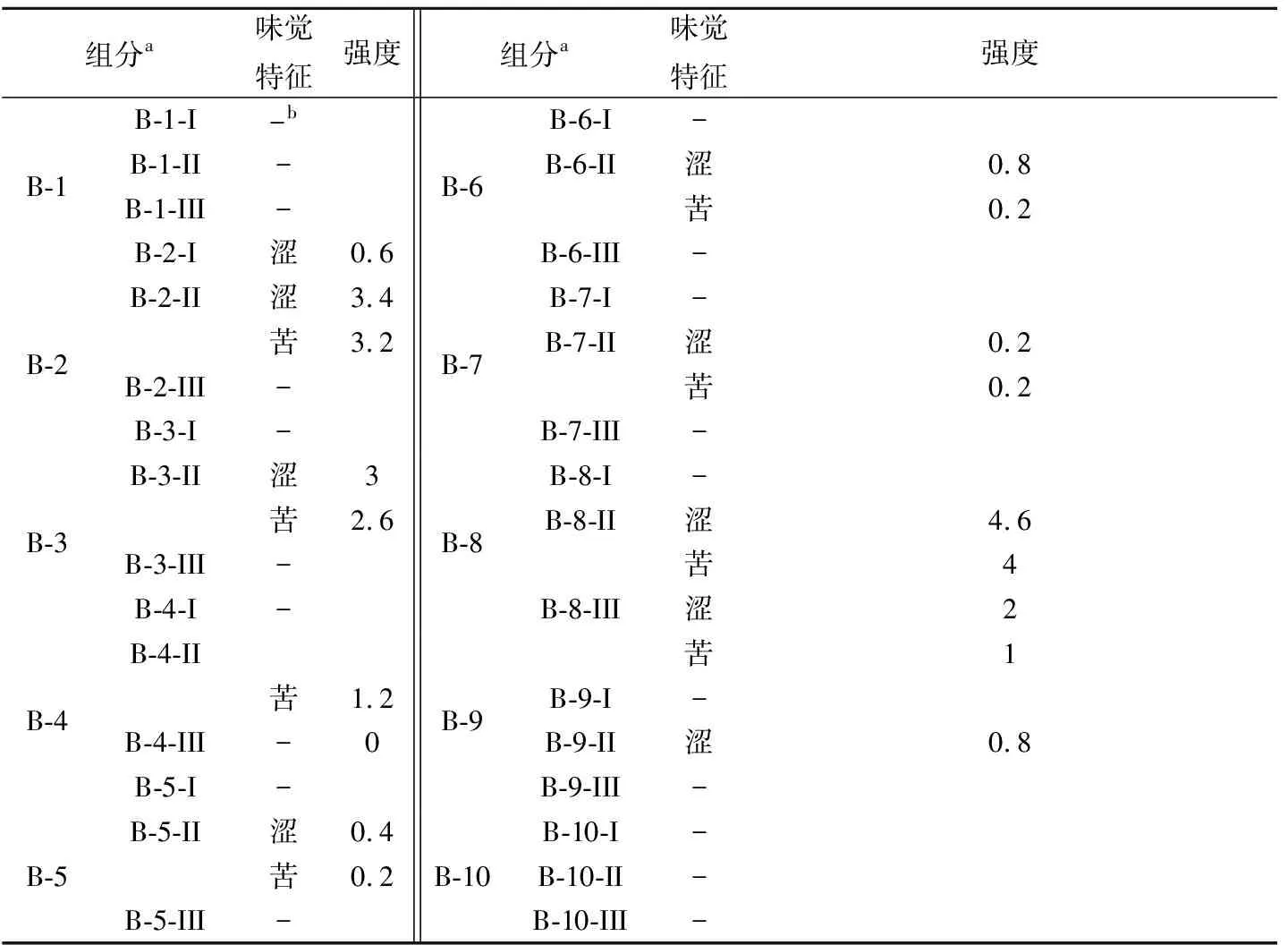
表3 戊烷三乙醚溶劑萃取組分的味覺特征及強度Table 3 Taste qualities and intensity of the fractions from pentane-diethyl ether solvent extraction
注:a組分B-1~B-10:指從半制備分離得到的10個亞組分; I是指半制備組分的戊烷萃取相;II是指半制備組分的乙醚萃取相;III是指半制備組分萃取后的殘留相。b表示沒有明顯味覺。
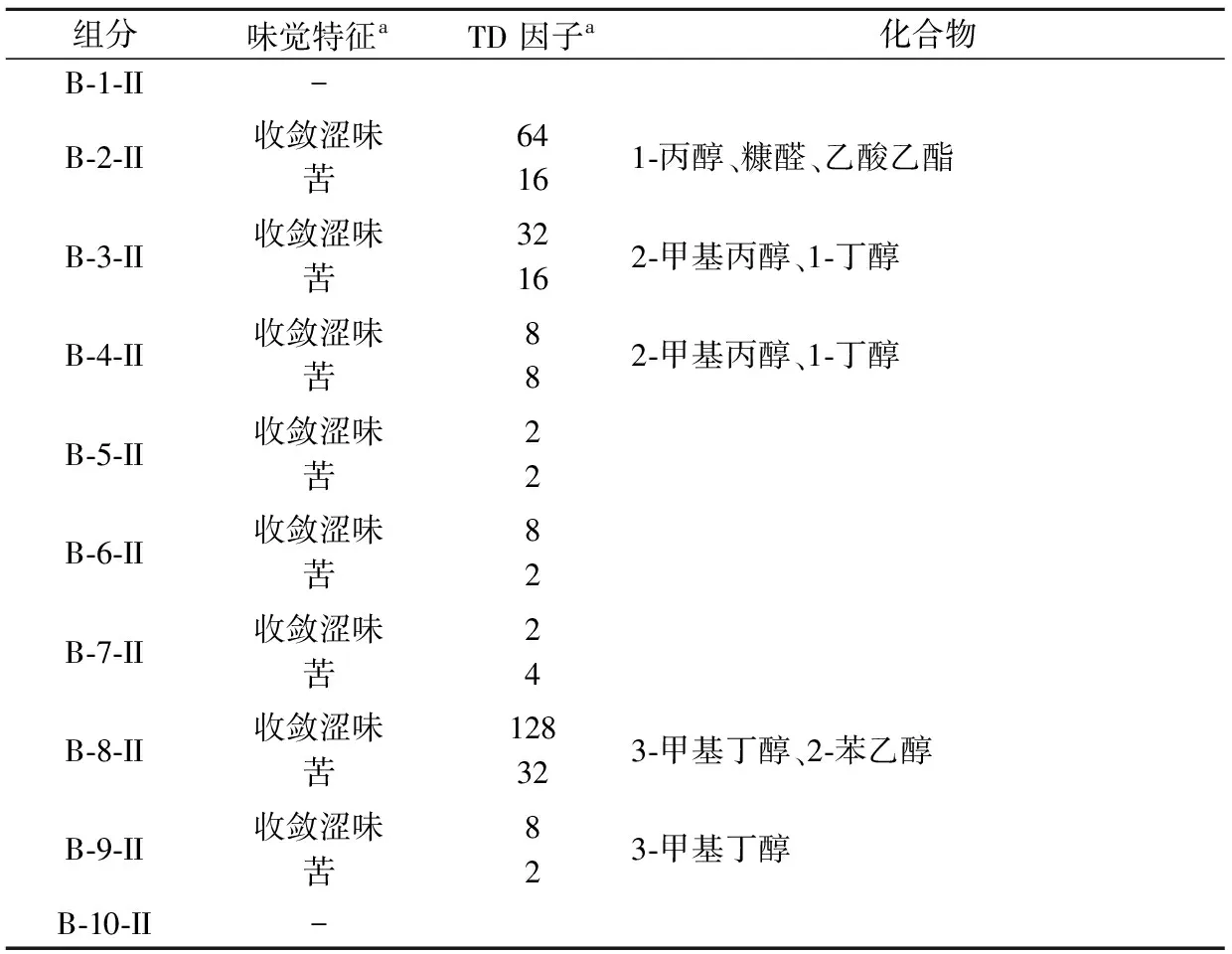
表4 乙醚萃取組分的味覺特征、味覺稀釋(TD)值及呈味化合物的鑒定Table 4 Taste qualities, taste dilution (TD) factors and identification of the compounds from diethyl ether extraction fractions
注:a測定TD因子時,澀味采用半舌試驗測定,苦味采用三角試驗測定。
為鑒定呈苦、澀味化合物,對相關組分進行GC-MS分析(表 4)。所有解析到的化合物均通過標準品驗證。在亞組分B-8-II中鑒定出3-甲基丁醇和2-苯乙醇。根據標準品味覺品嘗驗證,在水溶液中3-甲基丁醇既呈澀味又呈苦味,2-苯乙醇只呈澀味,2-苯乙醇的味覺特征是首次報道;亞組分B-2-II中鑒定出正丙醇、乳酸乙酯和糠醛,其中正丙醇、糠醛在水溶液中呈現苦味和澀味,乳酸乙酯只呈澀味;亞組分B-3-II和B-4-II都含相同的呈味化合物2-甲基丙醇和1-丁醇,它們都呈現苦味和澀味。這些化合物是白酒中常見的香氣化合物[17-18]。部分化合物如正丙醇、1-丁醇、乳酸乙酯、2-甲基丙醇、3-甲基丁醇和糠醛呈苦味和澀味特征與原先推測吻合[3, 19]。
3 結論
本研究以芝麻香型原酒為研究對象,首次建立了白酒中揮發性苦味和澀味化合物提取、分離、鑒定的方法。通過梯度減壓蒸餾、半制備分離、溶劑萃取、TDA結合GC-MS,鑒定白酒中揮發性的呈苦、澀味化合物。采用此方法發現2-苯乙醇和乳酸乙酯在白酒中呈現澀味,而糠醛、2-甲基丙醇、3-甲基丁醇、1-丁醇和正丙醇同時呈澀味和苦味,其中2-苯乙醇是首次報道了其味覺特征。下一步將進行這些化合物苦澀味閾值測定,以及pH等對苦、澀味的影響研究。

