溫腎固疏方干預絕經后骨質疏松藥理研究
沈蘊茹 郭海英
南京中醫藥大學第二臨床醫學院,江蘇 南京 210023
絕經后骨質疏松癥(post menopausal osteoporosis,PMOP)是一種受多種因素影響的代謝性疾病,婦女絕經后體內雌激素降低,骨質疏松癥常與脂代謝紊亂導致的心血管疾病伴隨發生。絕經后骨質疏松嚴重影響中老年婦女的日常生活甚至生命安全。近年來多項新研究闡明[1],載脂蛋白E(epolipoprotein E,ApoE)不僅作為重要角色參與脂代謝,也同時會影響骨代謝,雌激素水平也被證實對ApoE有影響[2]。國內外學者多將絕經后婦女骨質疏松與脂代謝異常的著重點放于ApoE,集中研究ApoE對骨代謝與脂代謝的調節作用。溫腎固疏方具有溫陽補骨、補腎健脾的功效,本研究通過建立大鼠骨質疏松模型,觀察溫腎固疏方對大鼠的以ApoE為連接點的骨質量、強度以及脂代謝指標的改變,尋找PMOP新的發病機制,并從此得到更加長期有效,易于推廣普及的PMOP防治手段。
1 實驗材料
1.1 實驗動物
健康9月齡未孕SPF級SD大鼠40只,雌性,體重(250±30)g,由南京中醫藥大學實驗中心提供,合格證號SYXK(蘇)2014-0001-201508662。
1.2 儀器、藥物及試劑
溫腎固疏方各藥物組成由南京中醫藥大學百草堂藥房提供,方藥組成: 熟地20 g、淫羊藿20 g、黨參10 g、丹參10 g、枸杞10 g、骨碎補10 g、補骨脂5 g,茯苓10 g,白術10 g,兩次煎液過濾合并濃縮。戊酸雌二醇(補佳樂,德國拜耳醫藥保健有限公司廣州分公司,180 A)。10%水合氯醛溶液(中國人民解放軍第一醫院,20130312)。青霉素(山東魯抗醫藥股份有限公司,B140808)。Elisa試劑盒購自于南京森貝伽生物,大鼠OT/BGP試劑盒(20161212),大鼠ApoE試劑盒(20161212),大鼠Lip試劑(20161212),大鼠sRANKL試劑盒(20161212),大鼠BMPs試劑盒(20161212),大鼠OPG試劑盒(20161212)。數字化雙能X線骨密度儀(MEDIX-90,法國MEDILINK公司)。CHD-1001 電子式雙柱萬能材料試驗機CHD-1001(東莞誠鼎)。全自動生化分析儀(日本東芝TBA-120FR)。
2 研究方法
2.1 去卵巢大鼠骨質疏松癥模型的建立
采用雙側性腺(卵巢)摘除法[3]制備絕經后骨質疏松模型。飼養環境:室溫(22±2)℃、濕度控制于50%,恒溫、恒濕、清潔、通風環境,自由飲食、飲水,飼養1 w后根據體重將SD大鼠隨機分為兩組:假手術組(Sham,n=6)、模型組(n=34)。模型組首先腹腔注射35 mg/kg的10%水合氯醛溶液麻醉,然后背部切口行去勢手術,剪除雙側卵巢,分層縫合。Sham組大鼠背部切口手術后,僅切除卵巢旁約1 g重的脂肪,不切除卵巢,最后每只大鼠經后肢肌肉注射80000 U青霉素,連續7 d觀察。
2.2 分組及干預
造模過程中無因感染等原因而不適合繼續干預的大鼠。將摘除雙側卵巢的模型組大鼠(n=34)隨機分組,分為:模型組(OVX,n=6),溫腎固疏方高劑量組(n=6)、中劑量組(n=6)、低劑量組(n=6)及雌激素組(n=6),剩余4只放血處死。大鼠于上述飼養環境中自由攝食、飲水,每周稱量體重一次。各組大鼠均于手術后3 w切口愈合后開始分組治療干預。用臨床擬用計量法(ACD法)擬定大鼠同類藥等效劑量,按成人6.30倍計算,給藥容積0.5 mL/100 g。溫腎固疏方治療組先計算出中劑量組計量,高劑量組為中劑量組2倍,低劑量組為中劑量組1/2。高劑量組:溫腎固疏方,21.21 g生藥/(kg·d);中劑量組:溫腎固疏方,10.605 g生藥/(kg·d);低劑量組:溫腎固疏方,5.3 025 g生藥/(kg·d)。雌激素組:戊酸雌二醇,10μg/(kg·d)。模型組:給予生理鹽水0.5 mL/100 g灌胃;假手術組給予生理鹽水0.5 mL/100 g灌胃。各組灌胃持續8 w。
2.3 標本釆集及測定
大鼠末次施治后,禁食24 h,次日取材。處死前稱量大鼠體質量,用10%水合氯醛溶液(35 mg/kg)腹腔注射麻醉,右心室抽血處死。血液收集后,4 ℃靜置3 h,3 000 r/min, 離心10 min,分離血清。酶聯免疫法(ELISA)測定OT/BGP、sRANKL、OPG、BMPs、ApoE、Lip。全自動生化儀測定血清高密度脂蛋白膽固醇(HDL-C)、低密度脂蛋白膽固醇(LDL-C)、TG、TC,計算AI(AI=LDL-C/HDL-C)。骨質量測定:取大鼠右側股骨、腰椎全段,放在有機玻璃盒支架上固定,以MEDIX-90骨密度測定儀掃描測定離體大鼠骨密度(bone mineral density,BMD)、骨礦含量(bone mineral content,BMC)。骨強度測定:取大鼠左側股骨,固定于電子式雙柱萬能材料試驗機上,測定股骨弾性模型、最大承載力、剛性、最大應力。
2.4 統計學方法
3 實驗結果
3.1 大鼠骨密度(BMD)、骨礦含量(BMC)變化
模型組與假手術組對比,模型組大鼠股骨、腰椎BMD、BMC明顯降低(P<0.05)。與模型組相比,雌激素組、高、中、低計量組大鼠股骨、腰椎BMD、BMC皆有增高,其中股骨BMD、BMC的雌激素組、低、高劑量組增高明顯(P<0.05)。腰椎BMD、BMC雌激素組增高明顯(P<0.05),BMC高劑量組增高明顯(P<0.05),雌激素組與溫腎固疏方各劑量組的股骨、腰椎BMD、BMC皆高于模型組。見表1。

表1 溫腎固疏方對不同組別去勢大鼠股骨骨密度的影響Table 1 Effects of WenShenGuShu formula on BMD and BMC of rat with osteoporosis
注:與假手術組相比,▲P<0.05。與模型組相比,*P<0.05,△P<0.01。
3.2 大鼠股骨生物力學的變化
模型組與假手術組相比,模型組彈性模量、最大承載力、剛性、最大應力皆顯著降低(P<0.05)。與模型組相比,雌激素組、低、中、高劑量彈性模量、最大承載力、剛性、最大應力皆高于模型組,其中,雌激素組、中劑量組弾性模型顯著增高(P<0.05),雌激素組、高劑量組最大承載力顯著增高(P<0.05),低劑量組與高劑量組剛性顯著增高(P<0.05),雌激素組、低劑量組與高劑量組最大應力顯著增高(P<0.05),高劑量組最為明顯(P<0.05)。見表2。
3.3 大鼠血清骨代謝的變化
模型組與假手術相比,模型組血清骨谷胺蛋白/骨鈣素(OT/BGP)、OPG、骨形成蛋白(bone morphogenetic protein,BMPs)下降,sRANKL上升。治療組與模型組相比,OT/BGP皆有上升,其中雌激素、中劑量組有統計學意義(P<0.05),高、低劑量組上升明顯(P<0.01);sRANKL皆下降,其中高、低劑量組具有統計學意義(P<0.05);OPG各組均上升,其中雌激素組、低劑量組具有統計學意義(P<0.05);BMPs各組均上升,雌激素組,高、低計量組有統計學意義(P<0.05)。溫腎固疏方高、低劑量灌胃對大鼠骨代謝作用明顯。見表3。

表2 大鼠股骨生物動力學變化Table 2 Effects of WenShenGuShu formula on biomechanics of femur in rats with osteoporosis
注:與假手術組相比,▲P<0.05。與模型組相比,*P<0.05,△P<0.01。

表3 溫腎固疏方對去勢大鼠骨代謝的影響Table 3 Effects of WenShenGuShu formula on bone metabolism of rats with osteoporosis
注:與假手術組相比,▲P<0.05。與模型組相比,*P<0.05,△P<0.01。
3.4 各組大鼠血清脂代謝的變化
模型組與假手術組對比,模型組Lipids、ApoE、LDL-C、TC均上升,HDL-C、TG均下降,Lipids、ApoE、LDL-C變化具有統計學意義(P<0.05),動脈硬化指數AI上升(P<0.05)。與模型組對比,雌激素組、低、中、高劑量組血清Lipids下降,低、中、高劑量組有統計學意義(P<0.05),低、高劑量組下降效果明顯(P<0.01),雌激素組、低、高劑量組ApoE下降,低劑量組具有統計學意(P<0.05)。低、高劑量組LDL-C下降明顯(P<0.05)。低劑量組TG下降明顯(P<0.05)。雌激素組、低、中、高劑量組AI均有下降,低、高劑量組有統計學意義(P<0.05),且溫腎固疏方低、高劑量組AI低于雌激素組。見表4。
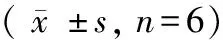
表4 溫腎固疏方對去勢大鼠脂代謝以及ApoE的影響
注:與假手術組相比,▲P<0.05。與模型組相比,*P<0.05,△P<0.01。
4 討論
前期研究表明[4],骨質疏松大鼠模型構建后大鼠雌激素水平迅速下降,光鏡下觀察模型組大鼠病理切片,可見骨松質骨小梁纖細明顯,數量減少,部分骨小梁斷裂呈典型骨質疏松模型,提示該實驗造模成功。本課題研究進一步探討絕經后骨質疏松的新發病機制以及治療方案,參照絕經后婦女骨質疏松導致骨折的多發部位,測定大鼠股骨、腰椎的BMD、BMC,溫腎固疏方高、中、低劑量組與模型組比較,低、高劑量組大鼠股骨BMD、BMC上升明顯(P<0.05),高劑量組大鼠腰椎BMC上升明顯(P<0.05)。測定股骨弾性模型、最大承載力、剛性、最大應力,中劑量組弾性模型顯著增高(P<0.05),高劑量組最大承載力顯著增高(P<0.05),低劑量組與高劑量組剛性顯著增高(P<0.05),低劑量組與高劑量組最大應力顯著增高(P<0.05)。上述實驗結果證明經溫腎固疏方治療后,去勢大鼠的骨質量與骨強度皆有提升,有防治絕經后骨質疏松癥的作用。
近年來研究發現,脂肪細胞與骨細胞兩者由骨髓間充質干細胞分化而來,基于雙向分化原理,骨髓間充質干細胞細胞會向脂肪細胞與骨細胞兩個方向分化。現階段研究證明[5],ApoE與Wnt信號通路的LRP受體結合,并能抑制PPARγ的活化,ApoE能夠通過調節Wnt通路與PPARγ從而影響β-catennin的表達,誘導骨髓間充質干細胞分化。OPG與sRANKL聯合說明Wnt信號通路的改變,sRANKL表達增高說明骨量流失。ApoE通過運輸脂溶性維生素K參與骨細胞的生成,維生素K大部分由飲食供給,去勢大鼠正常飲食,說明維生素K的結合受到影響,維生素K作為特別的脂溶性維生素只能與受體結合力較強的ApoE相結合運輸[6-8],維生素K能將骨鈣素中殘留的3谷氨酸羧化,該修飾過程對于維持γ-骨鈣素的完整性是必不可少的,骨鈣素水平下降會導致骨密度下降與骨脆性增加,OT/BGP下降說明去勢大鼠骨生成收到影響[9]。BMPs(骨形成蛋白)促進骨代謝作用與Smad 蛋白相偶聯,影響骨重建與骨吸收,參與骨髓間充質干細胞的雙向分化,抑制內源性BMP-4可以抑制PPARγ的表達,在前脂細胞分化中維持其狀態。本研究結果提示溫腎固疏方治療后模型大鼠各項骨代謝指標與上述理論相吻合,低、高劑量組血清OT/BGP上升(P<0.05);低、高劑量組sRANKL下降(P<0.05);低劑量組血清OPG上升(P<0.05);低、高劑量組BMPs上升(P<0.05);高、中、低劑量組血清Lip下降(P<0.05),低劑量組ApoE下降(P<0.05);低、高劑量組LDL-C下降;低劑量組TG下降(P<0.05)。低、高劑量組AI下降(P<0.05),且AI低于雌激素治療組。上述實驗結果提示溫腎固疏方通過調控ApoE,改善Wnt/PPAYγ的拮抗作用從而誘導β-catennin的表達,促使骨髓間充質干細胞向骨細胞分化,促進骨形成,防止脂細胞形成,改善脂代謝異常,并促進骨吸收,防止骨變異流失,進而改善絕經后骨質疏松情況。
在中醫理論中,“腎主骨”,腎與骨的關系密切,《內經》指出婦女在絕經前后,即“天癸衰”后會出現毛發枯黃,牙齒松動,骨質脆弱等表現。補腎一直以來作為中醫治療骨質疏松的主要方向。國內學者研究認為,ApoE在中醫理論中與痰證關系緊密,《仁齋直指方》中提出“肥人氣虛生痰,故多痰濕”,說明早于幾百年前就有臨床經驗研究指出脂代謝異常與痰濕體質、證候互相作用。痰濕證候會導致脂代謝異常,脂代謝異常也會反作用于痰濕證候,使痰淤體內,濕氣不排,進而導致濕濁在體內堆積,脾胃功能失調。脾胃與腎在藏象關系中聯系緊密,先天后天精微互相充養,脾胃功能失調,則后天之精運化失調,后天之精不能充養先天之精,故導致腎氣不充,腎臟功能失司,腎精與水谷精微不能充養骨骼,便會進一步引發骨枯、骨萎,也就是現代的骨質疏松癥。ApoE在脂代謝與骨代謝調節中起到至關重要的作用,中醫理論中也與痰濕證候相關[10-12],影響腎精充養骨的作用。大量臨床報告顯示絕經前后婦女常同時伴有骨質疏松和脂代謝異常導致的心血管系統疾病、阿爾茨海默病等,單一的他汀類藥物或雌激素替代療法都未能取得更好的療效,長期服用雌激素可能導致靜脈血栓和心血管疾病[13-15],長期服用雌激素的女性患有此類疾病的可能性要較一般女性高出2倍左右[6],并且會導致體重增加與明顯的情緒變化[16],故持續使用雌激素替代療法并非相對完善的治療PMOP手段。溫腎固疏方由熟地20 g、淫羊藿20 g、黨參10 g、丹參10 g、枸杞10 g、骨碎補10 g、補骨脂5 g,茯苓10 g,白術10 g按比例配伍制成。根據現代中藥研究,骨碎補[17]、熟地[18]、淫羊藿[19]皆有通過調節ApoE對骨髓間充質干細胞的雙向誘導分化作用,淫羊藿同時具有保護心血管的功能[20]。溫腎固疏方以溫腎健脾為治療原則,具有能夠長期服用、副作用小、能在一副湯藥中通過草藥配伍整體治療的優越點,并且具有中醫的整體治療觀念,能夠整體調節絕經后婦女的激素代謝。
本實驗通過對去勢大鼠骨質量、骨強度、骨代謝以及脂代謝指標的研究,證實溫腎固疏方通過調控ApoE從而改善骨代謝,防止骨流失,并能有效改善脂代謝,通過溫腎健脾法達到補骨的效果。但由于絕經后骨質疏松癥是一種機制復雜的綜合代謝性疾病,其機制尚不明確,且實驗依舊有改進空間,如大鼠與人類在生物形態學的不同導致部分結論不顯著、樣本量偏少、大鼠個體差異性等,對ApoE調控絕經后骨質疏松癥的機制依舊需要進一步探討,希望能從中尋找新的防治思路。

