米諾環素對慢性腦缺血大鼠腦內Notch信號通路的影響
陳毅 尤志珺 王傳玲 隨曉菲 蔡志友
米諾環素作為四環素類藥物中一種的有效的神經細胞保護劑,具有抗炎、抑制小膠質細胞、抑制基質金屬蛋白酶表達、氧化氮類產物的產生和細胞調亡過程等作用[1-6]。有研究發現米諾環素是一種有效的腦保護劑,并能降低血管性認知功能損害的癥狀[2-3]。有研究證實米諾環素可以有效促進VEGF的生物活性[7],而VEGF是腦缺血后血管新生的重要因子之一[8-10]。Notch信號通路是血管新生、內皮細胞形成的關鍵信號通路,激活Notch信號通路可增強內皮祖細胞的遷移、侵襲和血管形成的能力,而抑制Notch信號通路,則內皮祖細胞遷移、侵襲和血管形成的能力受到抑制。本實驗通過抑制Notch信號通路及米諾環素給藥后觀察大鼠的學習記憶能力以及觀察血管內皮生長因子VEGF和Notch信號通路下游蛋白Hes1的表達水平,以進一步探討米諾環素是否可以通過調節Notch信號通路進而影響腦組織血管修復能力,從而發揮腦保護作用。
1 材料與方法
1.1 材料
1.1.1 實驗動物 健康成年SD大鼠40只(雄性,260~300 g,由湖北醫藥學院實驗動物中心提供,使用許可證號 SYXK(鄂)2011-0031),按照隨機原則分為5組(n=8):假手術(Sham)組、缺血模型(Model)組、 DAPT(DAPT)組、米諾環素(Min)組、DAPT+米諾環素(DAPT+Min)組。
1.1.2 試劑及設備 鹽酸米諾環素膠囊(100 mg/粒),惠氏制藥有限公司,生產批號:M33265;DAPT抑制劑 (ab120633),Abcam公司;Anti-Hes1 antibody (ab108937),Abcam公司;Anti-VEGF antibody (ab1316),Abcam公司;MT-200 Morris水迷宮綜合跟蹤系統(由湖北醫藥學院基礎醫學研究所提供)。
1.2 方法
1.2.1 2-VO模型制備 參照文獻[11-12]制作大鼠慢性腦缺血模型:手術前12 h禁食水,用3.5%的水合氯醛,按1 mL/100 g體重對大鼠進行腹腔麻醉后仰臥固定,備皮,消毒,沿頸正中線切開皮膚,分離雙側頸總動脈,行雙側頸總動脈永久結扎術,術后注意保溫,常規飼養。假手術組除不結扎雙側頸總動脈外,余處理同缺血模型組大鼠。
1.2.2 給藥 將米諾環素用生理鹽水稀釋成5 mg/mL濃度備用,DAPT溶于DMSO中并在5%葡萄糖溶液中稀釋備用。假手術組、缺血模型組給予等量的生理鹽水灌胃;DAPT組予以Notch抑制劑DAPT(按10 μmol/kg腹腔注射,建模成功后給藥1次,以后每周給藥1次,其他處理同缺血模型組);米諾環素組以50 mg/kg米諾環素灌胃;DAPT+米諾環素組給藥:在DAPT組的基礎上同時給予50 mg/kg米諾環素灌胃。于建模成功正常飼養2 d后開始給藥,連續給藥4周。米諾環素的劑量選擇參考Stirling等[13]和Yrjanheikki等[14]的有關米諾環素神經保護作用機制的研究,DAPT使用方法參考Huang Man等[15]的有關DAPT作用神經細胞的研究。
1.2.3 行為學檢測 在給藥飼養4周后測試大鼠在Morris水迷宮(Morris water maze, MWM)實驗中逃避潛伏期的長短和跨越原平臺區位置的次數。(1) 定位航行實驗:水迷宮水深35 cm,水溫25 ℃,在固定象限設有安全島,高度33 cm,液面高于安全島2 cm;共歷時5 d,每組大鼠每天時間固定;大鼠入水點順序為第1 d,E-S-W-N;第2 d,S-W-N-E;第3 d,W-N-E-S;第4 d,N-E-W-S;第5 d,E-W-N-S;記錄每次找到平臺的時間(即逃避潛伏期,以秒為單位計時);如大鼠在60 s內找不到平臺,由實驗者將其引上平臺,潛伏期記為60 s,每次間隔5 min讓大鼠休息,再行下次實驗;(2) 空間探索實驗:定位航行實驗第5 d的最后1次結束時撤除平臺,將大鼠從任選的非平臺象限入水點面向池壁放入水中,記錄大鼠第1次到達平臺的時間以及2min內跨越原平臺的次數和大鼠在池中的游泳路徑,計算大鼠在平臺象限游泳路徑長度占總路徑長度的百分比。
1.2.4 免疫組化實驗 用3.5%水合氯醛麻醉大鼠,打開胸腔,經左心室快速灌注生理鹽水,直至右心房流出液清亮為止;然后用4%多聚甲醛灌注固定,斷頭取腦;冠狀切取視交叉后部腦組織,常規梯度酒精脫水,石蠟包埋;常規切片3~4 mm,70°烤片2 h;二甲苯脫蠟,梯度酒精洗滌, 3% H2O2室溫10 min滅活內源性酶;滴加羊血清封閉液10 min;不同切片分別加入適量的羊抗大鼠Hes1、小鼠抗大鼠VEGF,37 ℃ 60 min或4 ℃冰箱過夜;加反應增強劑,37 ℃恒溫孵育20 min;分別滴加辣根酶標兔抗羊IgG及兔抗小鼠IgG,37 ℃恒溫孵育30 min;除加入羊血清封閉液外,以上各步間均用0.01 mol/L PBS(pH 7.4)充分洗滌;最后DAB顯色,蘇木素復染,鹽酸酒精分化,中性樹膠封片。用已知陽性切片作為陽性對照,PBS替代一抗作為陰性對照。使用Image-Pro Plus 6.0軟件測定陽性細胞表達的面積,然后將假手術組定為1,換算其余各組相對值。
1.2.5 蛋白質免疫印跡法 各組腦組織加入細胞裂解液充分裂解,離心,BCA 方法行蛋白定量;取50 μg蛋白變性,經SDS/PAGE凝膠電泳,轉移至PVDF膜上,5%脫脂奶粉室溫封閉1 h,分別和羊抗大鼠Hes1多克隆抗體、小鼠抗大鼠VEGF單克隆抗體作用,4 ℃過夜;洗滌后分別加入辣根過氧化物酶結合的兔抗羊IgG(1∶5000)及兔抗小鼠IgG (1∶2000),室溫孵育1 h;于超高靈敏度化學成像發光儀照相,Image Lab 3.0軟件測定灰度值,與相應β-actin比較后將假手術組定為1,計算其余組相對值。所有蛋白質免疫印跡都在同組不同樣品上得到重復。

2 結 果
2.1 死亡率 假手術組大鼠無死亡,缺血模型組死亡1只,DAPT組死亡2只,米諾環素組無死亡,DAPT+米諾環素組死亡1只。以上大鼠均死于術后48 h內,不列入統計,另隨機選取大鼠補齊。各組大鼠死亡率比較無明顯差異(P>0.05)。
2.2 行為學實驗 與假手術組比較,缺血模型組的水迷宮定位航行逃避潛伏期延長(P<0.05),第1次跨越平臺時間延長(P<0.05),跨越平臺平均次數減少(P<0.05);DAPT組與缺血模型組比較、米諾環素組與DAPT組比較、DAPT+米諾環素組分別于DAPT組和米諾環素比較,逃避潛伏期、第1次跨越平臺時間及跨越平臺平均次數有顯著差異(P<0.05)(表1~2、圖1)。
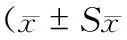
表1 水迷宮空間探索第1次跨越平臺時間及跨越平臺次數,n=8)
注:與Sham組比較,*P<0.05;與Model組比較,?P<0.05;與DAPT組比較,#P<0.05;與DAPT組和Min組比較,△P<0.05

圖1 各組大鼠行為學檢測組 A、B為各組大鼠逃避潛伏期;C為各組大鼠跨越平臺時間;D為各組跨越平臺次數;與假手術組比較,*P<0.05;與缺血模型組比較, ▲P<0.05;與DAPT組比較, #P<0.05;與DAPT抑制劑組和米諾環素組比較, ◆P<0.05
2.3 免疫組織化學染色法 與假手術組比較,缺血模型組Hes1和VEGF表達水平增高(P<0.05);與缺血模型組比較,DAPT組Hes1和VEGF表達水平顯著降低(P<0.05);與缺血模型組比較,米諾環素組Hes1和VEGF表達水平增高(P<0.05);與DAPT組比較,米諾環素組Hes1和VEGF表達水平顯著增高(P<0.01);與DAPT組比較,DAPT+米諾環素組Hes1和VEGF表達水平增高(P<0.05)(圖2)。
2.4 蛋白質印跡法 與缺血模型組比較,DAPT組Hes1和VEGF灰度值下降(P<0.05);與缺血模型組比較,米諾環素組Hes1和VEGF灰度值增高(P<0.05);與DAPT組比較,米諾環素組Hes1和VEGF灰度值增高(P<0.01);與DAPT組比較,DAPT+米諾環素組Hes1和VEGF灰度值增高(P<0.05)(圖3)。

表2 水迷宮定位航行逃避潛伏期,s,n=8)
注:與假手術組比較,*P<0.05;與缺血模型組比較,▲P<0.05;與DAPT組比較,#P<0.05;與DAPT組和米諾環素組比較,◆P<0.05

圖2 各組大鼠Hes1及VEGF免疫組化染色(海馬CA1區 SP ×400倍) A為各組大鼠Hes1的表達水平;B為各組大鼠VEGF表達水平;與假手術組比較,▲P<0.05;與缺血模型組比較,?P<0.05,#P<0.05;與DAPT組比較,△P<0.01,*P<0.05

圖3 各組大鼠Hes1及VEGF Western blot印跡檢測 A為各組大鼠Hes1表達水平;B為各組大鼠VEGF表達水平;與缺血模型組比較, ?P<0.05,#P<0.05;與DAPT組比較,△P<0.01,*P<0.05
3 討 論
腦缺血后血管增生修復能力受損。有研究證明腦缺血后微血管的密度與腦梗死的面積相關[16],微血管的新生為神經的再生創造了條件,這對神經功能的恢復產生了重要作用。由此可見,腦缺血后大腦微血管網的重建對受損部位的恢復是很重要的一個環節。
血管新生是指在原有血管的基礎上內皮細胞增殖、遷移和重塑,進而形成新血管的過程,涉及諸多的生長因子和信號通路分子[17],Notch信號通路就是其中比較重要的一個。眾所周知,血管內皮生長因子(Vascularendothelialgrowthfactor,VEGF)是血管生長因子中最重要的一員,可在體內誘導血管新生[18]。VEGF能直接刺激血管內皮細胞移動、增殖及分裂,并增加微血管通透性。VEGF與內皮細胞上的兩種受體KDR和Flt-1高親和力結合后直接刺激血管內皮細胞增殖,并誘導其遷移和形成管腔樣結構;同時還可增加微血管通透性,引起血漿蛋白(主要是纖維蛋白原)外滲,并通過誘導間質產生而促進體內新生血管生成[18]。Notch信號通路是一個在進化中高度保守的細胞間信號傳遞通路,由Notch受體、Notch配體(DSL蛋白)和轉錄因子CSL(一類DNA結合蛋白)等組成,Notch蛋白是一種細胞表面跨膜受體,Notch有4個Notch同源基(Notch1-4) 和5個配體(Jagged1,2;Delta1,2,3),Notch蛋白是一種細胞表面跨膜受體,其胞外段包含表皮生長因子樣重復受體,可與配體的Delta等相互作用。配體一旦與受體結合在早老蛋白-1(Presenilin-1)/γ-分泌酶作用下Notch發生兩次溶蛋白性裂解后Notch蛋白的胞內區域 (Notchintracellulardomain,NICD),NICD作為Notch的活化形式轉移進入細胞核,與DNA結合蛋白CSL(CBF-1/RBPJk-Su(H)-LAG1 )結合并使之活化,激活Hes家族,進而發揮一系列的生物學效應[19-20]。有研究證實Notch信號通路激活可增強內皮祖細胞的遷移、侵襲和血管形成的能力,促進腦外傷后神經血管的修復,而抑制Notch信號通路,內皮祖細胞遷移、侵襲和血管形成的能力受到抑制[8-10]。本實驗通過DAPT抑制劑抑制Notch信號通路,VEGF的表達水平明顯降低也說明了這一點。腦缺血后Notch信號通路被激活,本實驗中缺血模型組的Hes1表達水平較假手術組增高證實了這一點,同時缺血模型組的VEGF表達水平較假手術組也增高,也證實了Notch信號通路的激活可提高損傷腦組織的血管修復能力。
米諾環素作為一種有效的神經細胞保護劑,具有抗炎、抑制小膠質細胞、抑制基質金屬蛋白酶表達、氧化氮類產物的產生和細胞調亡過程等作用[1-6]。有研究證實米諾環素也可以有效促進VEGF的生物活性[7]。本實驗中米諾環素組的VEGF的表達水平明顯較缺血模型組增高,也進一步證實了米諾環素可以增強VEGF的活性。
本實驗中米諾環素組中的Hes1的表達水平較DAPT組和缺血模型組增高,DAPT+米諾環素組的Hes1的表達水平較DAPT組增高,表明米諾環素可以作用于Notch信號通路中。同時米諾環素組中的VEGF的表達水平較DAPT組和缺血模型組也同步增高,DAPT+米諾環素組的VEGF的表達水平較DAPT組也增高,則說明了米諾環素可以通過Notch信號通路來調節VEGF的表達水平,這也說明米諾環素可以通過Notch信號通路來增強腦缺血后大腦的血管修復能力。
本實驗證實了米諾環素可以通過Notch信號通路來提高損傷腦組織的血管修復能力,進而發揮了腦保護作用,這也為研究米諾環素發揮腦保護作用的機制向前邁進了一步,但同時也看到了本實驗的一些不足之處,比如Notch有4個Notch同源基(Notch1-4)和5個配體(Jagged1/2;Delta1/2/3),米諾環素是作用于哪一型還不清楚。另外,米諾環是否可以通過Notch信號通路來提高損傷腦組織的神經修復能力本研究沒有涉及,這些問題將在今后的研究中進一步的闡釋。

