重度阿爾茨海默病伴吞咽功能障礙患者行早期標準化腸內(nèi)營養(yǎng)對神經(jīng)功能和免疫系統(tǒng)指標的臨床療效
劉曉亮 魯利平 唐菊 李世芳 李小敏 楊景琦 李仲光 閆振 郭崢 秋軍峰 李建強 張冀燕
吞咽是機體最為復(fù)雜的反射之一,其需要至少6對以上的顱神經(jīng)和40多對頸面部肌肉參與,正常人每天會進行大約600余次的有效吞咽[1]。阿爾茲海默病作為一種進行性中樞神經(jīng)系統(tǒng)退行性疾病,吞咽障礙是其常見癥狀之一[2-3]。臨床癥狀主要是患者在吞咽時伴有梗阻、誤吸等。因此,為了避免患者因誤吸而引起相應(yīng)的并發(fā)癥,減少經(jīng)口進食,但這會進一步導(dǎo)致機體內(nèi)環(huán)境紊亂,增加致殘率,影響患者神經(jīng)功能康復(fù)和預(yù)后。腸內(nèi)營養(yǎng)是針對吞咽障礙的一種有效的替代措施,可以糾正和改善患者的內(nèi)環(huán)境平衡和營養(yǎng)狀況以及促進神經(jīng)功能的康復(fù)[4]。本研究旨在探討阿爾茲海默病伴吞咽功能障礙患者行早期腸內(nèi)營養(yǎng)支持治療后對神經(jīng)功能的改善作用。
1 資料與方法
1.1 一般資料
選擇2013年1月-2017年1月在本院接受診治的102例阿爾茲海默病伴吞咽功能障礙患者,其中男39例,女63例;年齡63~85歲,平均年齡(69.38±9.94)歲,患者平均病程為(5.38±3.10)年。根據(jù)數(shù)字表法隨機分為營養(yǎng)組和對照組,每組各51例,2組患者一般資料比較,無明顯差異(P>0.05)。
1.2 納入或排除標準
(1)符合美國精神病學會《精神障礙診斷與統(tǒng)計手冊》的診斷標準;(2)吞咽功能障礙經(jīng)過洼田氏飲水實驗≥3級的患者;(3)患者及其家屬簽署知情同意書;(4)經(jīng)過醫(yī)院倫理委員會批準;(5)排除患有嚴重免疫或消化系統(tǒng)疾病的患者;(6)排除患有顱腦惡性腫瘤的患者;(7)排除患有嚴重心、肝、腎等臟器功能不全的患者;(8)排除因腦卒中、腦出血等原因引起的吞咽障礙患者。
1.3 腸內(nèi)營養(yǎng)支持治療
營養(yǎng)組:患者入院24 h內(nèi)在進行病情評估完成后采用留置胃管鼻飼,腸內(nèi)營養(yǎng)支持治療(能全力、百普力,荷蘭紐迪希亞公司),熱量標準為20~30 kcal·kg-1·d-1。在支持治療的前3 d給予百普力,40 mL/h速度注入起調(diào),若無腹瀉等并發(fā)癥則以100~125 mL/h速度注入,在第4 d給予能全力制劑,營養(yǎng)液量為1000~1500 mL/d,營養(yǎng)支持治療時間14 d以上。對照組在入院早期給予靜脈營養(yǎng)支持,根據(jù)病情需要給予相應(yīng)的留置胃管,若給予留置胃管,則在營養(yǎng)師的指導(dǎo)下配置相應(yīng)的食物如稀飯、牛奶、蔬菜汁等。其他治療根據(jù)病情和治療指南采取一致的治療方法。
1.4 觀察指標
1.4.1 治療前后營養(yǎng)狀況比較 包括血清白蛋白(Serum albumin,ALB)、血紅蛋白(hemoglobin,Hb)、上臂三頭肌肌圍(arm muscle circumference,AMC)、三頭肌皮褶厚度(triceps skinfold,TSF)。
1.4.2 免疫功能情況 其中免疫功能指標包括總淋巴細胞計數(shù)(total lymphocyte count,TLC)、免疫球蛋白 G(Immunoglobulin G,IgG)、免疫球蛋白 M(Immunoglobulin M,IgM)、免疫球蛋白 A(Immunoglobulin A,IgA)。
1.4.3 治療前后神經(jīng)功能因子變化情況 包括神經(jīng)功能因子 S100B 蛋白(S-100B)、神經(jīng)元特異性烯醇化酶(neuron-specific enolase,NSE)、神經(jīng)膠質(zhì)纖維酸性蛋白(Recombinant Glial Fibrillary Acidic Protein,GFAP) 以及髓鞘堿性蛋白(myelin basic protein,MBP) 水平以及采用美國國立衛(wèi)生研究院卒中量表(National Institutes of Health Stroke Scale, NIHSS)對患者治療前后神經(jīng)功能缺損情況進行評定。
1.5 統(tǒng)計學處理
2 結(jié) 果
2.1 治療前后營養(yǎng)狀況比較
營養(yǎng)組患者在治療前后營養(yǎng)指標水平相對穩(wěn)定,治療后和對照組比較營養(yǎng)組各項營養(yǎng)指標水平顯著較高(P<0.05)(表1)。
2.2 免疫功能指標水平比較
治療前2組患者的免疫功能指標水平無明顯差異(P>0.05),治療后免疫功能指標水平均不同程度下降,但是營養(yǎng)組的免疫功能指標水平顯著高于對照組(P<0.05)(表2)。
2.3 神經(jīng)功能指標水平和NIHSS評分比較
治療前神經(jīng)功能指標(S-100、NSE、GFAP、MBP水平和NIHSS評分)比較2組無明顯差異(P>0.05),治療后2組患者神經(jīng)功能均一定程度上改善,其中和對照組比較營養(yǎng)組患者的S-100B 和NSE水平、NIHSS評分顯著較低(P<0.05),雖然營養(yǎng)組GFAP和MBP水平低于對照組,但無明顯差異(P>0.05)(表3)。
3 討 論
阿爾茲海默病是一種嚴重威脅人類健康的中樞神經(jīng)退行性疾病,臨床數(shù)據(jù)顯示其好發(fā)于老年人,尤其以女性多見[5]。隨著我國人口老齡化的加劇,阿爾茲海默病的發(fā)病率也在逐年遞增。陳淑玲等[6]學者認為阿爾茲海默病引起的吞咽障礙可能和吞咽反射和種樹調(diào)控機制有一定關(guān)系。目前存在的多數(shù)推測主要包括阿爾茲海默病引起的血管性病變和中樞膽堿能系統(tǒng)受損[6-7]。由于患者不能攝入正常的營養(yǎng)和熱量,且患者機體處于一種高分解代謝的狀態(tài),因而往往會引起營養(yǎng)不良和免疫功能下降的情況[6-7];這不僅嚴重地影響了患者的生活質(zhì)量,甚至會增加其病死率。因此,進行早期的腸內(nèi)營養(yǎng)支持治療對患者康復(fù)具有重要的臨床意義。
有研究顯示,營養(yǎng)支持分為腸內(nèi)和腸外營養(yǎng),但當患者的胃腸功能耐受的情況下腸內(nèi)營養(yǎng)在一定程度上有利于體內(nèi)內(nèi)環(huán)境的穩(wěn)定[8]。本研究結(jié)果顯示,治療后營養(yǎng)組患者的營養(yǎng)和免疫功能指標水平顯著高于對照組(P<0.05)。這說明在對患者實施早期標準的腸內(nèi)營養(yǎng)可以顯著促進和改善患者的營養(yǎng)攝入和減輕免疫系統(tǒng)損害。這和栗映泉等[9]研究結(jié)果一致。患者早期腸內(nèi)營養(yǎng)的供給有助于其內(nèi)環(huán)境和電解質(zhì)水平的平衡,從而促進腸粘膜生成,進而使腸道菌群得以穩(wěn)定。唐桂華等[10-11]學者認為患者機體腸道菌群的穩(wěn)定有助于增強免疫功能,而這間接地促進神經(jīng)功能的恢復(fù)。但是多數(shù)研究學者僅限于通過NIHSS評分對患者神經(jīng)缺損情況進行評估,而在蛋白或分子水平上卻鮮為少見。本研究發(fā)現(xiàn)治療后營養(yǎng)組患者的神經(jīng)功能均一定程度上改善,其中和對照組比較,營養(yǎng)組患者的S-100、NSE水平和NIHSS評分顯著較低(P<0.05),雖然營養(yǎng)組GFAP和MBP水平低于對照組,但無統(tǒng)計學意義(P>0.05),這可能和腸內(nèi)營養(yǎng)治療在對神經(jīng)功能恢復(fù)過程僅為輔助作用以及GFAP及MBP等指標對神經(jīng)功能缺損特異性不高等原因有關(guān)。反映神經(jīng)缺損的指標較多,其中,S-100是神經(jīng)膠質(zhì)細胞中一種營養(yǎng)蛋白,NSE則是神經(jīng)元細胞軸突胞質(zhì)中的可溶性胞漿蛋白,在神經(jīng)損傷后二者由于崩解進入血液而使其表達水平增高,因而臨床中常根據(jù)這二者的表達水平來判斷神經(jīng)損傷程度[12-13]。李宇輝等[14-15]學者表明患者在給予腸內(nèi)營養(yǎng)后NIHSS評分下降其可能和營養(yǎng)狀狀改善和肺部等感染控制程度有關(guān)。本研究早期腸內(nèi)營養(yǎng)治療對患者并發(fā)癥的控制作用未及時跟蹤記錄和檢查,這是本研究的不足之處。
綜上所述,阿爾茲海默病伴吞咽功能障礙患者行早期標準腸內(nèi)營養(yǎng)可以顯著改善患者的營養(yǎng)狀況和免疫功能,且在一定程度上改善神經(jīng)功能相關(guān)指標(S-100和NSE水平),保證了治療效果。

表1 治療前后患者營養(yǎng)情況比較)
注:與營養(yǎng)組比較,*P<0.05,△P>0.05
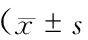
表2 免疫功能指標水平比較)
注:與營養(yǎng)組比較,*P<0.05
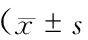
表3 治療前后神經(jīng)功能指標變化情況)
注:與營養(yǎng)組比較,*P<0.05

