大鼠羊水栓塞模型的法醫病理學檢驗分析
李連鵬 戴偉 李楨 王尚文 張桓
羊水栓塞(amniotic fluid embolism,AFE)是由于羊水進入母體血循環引起的一系列嚴重并發癥,臨床以突發性低血壓、低氧血癥及凝血功能障礙為主,AFE是一種發病率低,但是導致孕產婦死亡的重要原因,死亡率高達60%以上,是極其兇險且不可預料的產科并發癥,是孕產婦死亡的主要原因之一[1~3]。但查閱文獻和在法醫學實踐工作中發現,進入母體循環的羊水量至今無法計算,且多量羊水進入循環系統后發展變化規律不明確,故我們通過給母體注射不同劑量的自體羊水成分,將進入母體的羊水量進行限制,復制不同劑量的大鼠AFE模型和多量羊水入體的不同時間點AFE模型,并通過常規法醫學方法檢測和驗證,來研究AFE大鼠模型的發展變化規律。
1 材料與方法
1.1 實驗動物與分組 選取體重(395±30)g,孕齡20d左右的健康孕晚期SD大鼠80只(昆明醫科大學實驗動物研究中心和湖南斯萊克景達實驗動物有限公司提供),均為精選滿足實驗要求者。
分組:①健康孕晚期SD大鼠40只,隨機分成不同劑量的4組,即注入自體羊水1.25ml/kg組(低劑量組)8只、2.5ml/kg組(中劑量組)8只、4ml/kg組(大劑量組)8只以及注入所能采集到的最多無污染清亮的自體羊水組(約3ml/只,即極大劑量組)8只的大鼠模型和正常組大鼠8只做子宮次全切、下腔靜脈緩慢注射生理鹽水2ml/只后縫合;觀察60min后處殺。②健康孕晚期SD大鼠40只,隨機分成不同時間點的4組和正常組,后實驗組均注入4ml/kg羊水。實驗分組:分別為注入羊水后30min組8只、3h組8只、6h組8只、24h組8只和24h正常對照組8只。
1.2 實驗方法
1.2.1 制備實驗用羊水 羊水來自每只動物,實驗當天行子宮次全切,剪破離體子宮壁、羊膜腔后收集肉眼觀測清亮的羊水。
1.2.2 制備羊水栓塞動物模型 術前禁食6h,飲水不受限。10%水合氯醛腹腔注射麻醉動物,麻醉生效后固定于手術臺上剪去腹部體毛,使用含有效碘0.5%的碘伏消毒液消毒術區皮膚;使用消毒手術器械做腹部切口和子宮次全切術;使用無菌紗布覆蓋切口,并立即使用無菌生理鹽水漂洗離體子宮,擦干后行子宮內羊水收集,體外取羊水時速度要快,盡量避免胎糞浸染羊水,確保收集的羊水清亮;后按規定劑量從下腔靜脈緩慢注入自體羊水,實驗中注入羊水時速度盡量緩慢以貼近于臨床實際;注射完成后縫合腹壁各層組織并碘伏消毒。使用消毒過的鼠籠、墊料分籠單獨飼養實驗大鼠(以防止麻醉清醒早的大鼠利用體重壓迫麻醉清醒晚的大鼠)。上述各組到時間后拉頸處死動物,取肺、腦、肝組織,使用10%福爾馬林溶液固定后行石蠟包埋、采用相同組織的連續3張切片(厚度5μm),行常規組織HE染色,對無法檢出明確羊水成分組織的其余兩張切片,行抗角蛋白16染色法、APM雙重組化染色法染色,后行病理學檢查。正常對照組子宮次全切后從下腔靜脈緩慢注入生理鹽水后關腹。
1.2.3 查找羊水成分 由兩名從事十年以上法醫病理學鑒定的專家在顯微鏡下對大鼠肺、肝、腦組織病理切片進行羊水成分(鱗狀上皮細胞、毳毛、胎糞、粘液和羊水結晶等成分)的查找,如未發現羊水成分則行抗角蛋白16染色法、APM雙重組化染色法染色復查。
1.3 統計學方法 實驗定量資料(如:每張固定大小切片中檢出血管中有羊水成分的血管數量/該張切片中血管總數量)用均數±標準差(±s)表示,采用軟件SPSS 16.0進行統計分析,進行單因素方差分析及兩兩比較的q檢驗。P<0.05(或P<0.01)為組間差異有統計學意義。
2 結果
2.1 模型組孕鼠的臨床表現 對照組從腹主靜脈緩慢注入生理鹽水后出現短暫性呼吸加快,后恢復。AFE各組均有心率和呼吸頻率的改變:麻醉蘇醒后各組大鼠的心率均加快,且心率加快的持續時間隨著羊水劑量的增大而增大。麻醉蘇醒后各組大鼠的呼吸頻率均有加快,且呼吸頻率加快的持續時間隨著羊水劑量的增大而增大。在不同劑量的4組中,大劑量組和極大劑量組的心率和呼吸頻率加快時間是同步的,且各實驗動物從麻醉蘇醒至實驗結束均未恢復。在不同時間點的4組中,6h組和24h組持續時間分別為(4±1.75)h、(4±2.5)h,但差異無統計學意義;AFE各組均伴有局部抽搐、小便失禁等,差異無統計學意義。所有按無菌標準操作和術后單只分鼠籠單獨飼養的各組大鼠在處死前均無死亡。
2.2 染色結果
2.2.1 肺梗死和出血情況 極大劑量組3只(37.5%)檢見小灶狀的肺梗死、肺出血,大劑量組1只(12.5%)檢見小灶狀的肺梗死、肺出血;其余各組實驗大鼠肺、腦、肝中僅肺組織可以檢出羊水成分。在檢見小灶狀肺梗死的實驗大鼠的腦組織和肝組織中檢見毳毛(見圖1)、角化上皮、粘液和血栓等成分,分析認為毳毛和角化上皮等成分系肺梗死后進入肺靜脈通過體循環進入。
2.2.2 低劑量組存在未檢出羊水成分的情況 不同劑量的4組中,低劑量組3只(37.5%)肺組織中未檢出羊水成分。未檢出羊水成分實驗大鼠的肺、腦、肝組織均經過APM染色和抗角蛋白16染色亦未發現羊水成分。其余各組均檢出羊水成分。
2.2.3 各實驗組的相似性變化 各實驗組均有不同程度的肺水腫和炎性細胞浸潤,隨劑量增大而加重;不同劑量的4組中,大劑量組7只(87.5%)和極大劑量組8只(100%)的肺組織有重度肺水腫(見圖2)、肺出血及炎性反應。各實驗組的肺組織均可見不同程度的肺萎陷、肺泡腔變窄所致的肺泡大小不一(見圖3),間質血管擴張,出血,血管及支氣管周圍可見大量以中性粒細胞為主的炎性細胞浸潤,隨劑量增大而加重。各實驗組均可見腦水腫、神經細胞腫脹或固縮的缺氧性病變和肝細胞水樣變性的改變。各實驗組均可見溶血樣改變,部分管腔內可見腫脹的紅細胞(見圖4)。
2.2.4 羊水成分的重吸收和分解情況 不同時間點的4組中,24h組未檢見羊水成分中的毳毛、胎糞和粘液,同時該切片APM染色法能在支氣管中檢見分泌的粘液成分;檢見的角化上皮成分的量和大小均較前3組輕微,差異有統計學意義(P<0.05);炎性細胞浸潤程度略重。
2.2.5 HE染色下肺動脈分支及肺泡壁毛細血管內檢見紅色條索狀的角化上皮成分、淡紅色粘液、黃褐色的胎糞及紅色的微血栓,以及核藍色、胞漿紅色的合體樣細胞等羊水成分,均為非特異性著色(見圖 2)。
2.2.6 APM染色法下肺動脈分支及肺泡壁毛細血管內可見呈條索狀、桃紅色的鱗狀上皮細胞和毳毛等角化上皮成分以及藍色的酸性粘液和桃紅色的微血栓,肺上皮細胞的胞漿呈淡染的淺藍或無色,血管內皮細胞胞漿幾乎不著色(見圖5)。
2.2.7 Resist keratin-16免疫組化染色法下肺動脈分支及肺泡壁毛細血管內可見角化上皮呈褐色(見圖6)。

圖1 腦干HE染色,×200,示血管內檢見毳毛成分

圖2 肺HE染色,×400,示重度肺水腫

圖3 肺HE染色,×200,血管空虛、炎性細胞和肺泡大小不一

圖4 前額皮質HE染色,×400,血管內溶血
3 討論
一直認為,AFE的發生機理是由于羊水和羊水中的有形成分進入孕產婦血循環,但Clark等[4,5]觀察到胎兒的鱗狀上皮細胞進入孕婦血循環而不引起AFE癥狀,認為正常羊水進入孕產婦血循環可能并無危害。Hankins等[6]發現在所有輸注羊水的樣本中肺循環系統有升壓反應,且升壓反應程度在輸注羊水原液、被過濾的羊水、被過濾且被煮沸的羊水的標本是相同的。用羊水原液灌流離體肺[7],也未產生由于機械性栓塞而引起的肺動脈高壓和肺水腫,并且在鏡下檢查發現有胎兒毳毛及上皮細胞沉著在血管內,無明顯的血管痙攣發生;而用不含羊水有形成分的羊水栓塞樣血漿灌流離體肺,雖無機械性栓塞現象,但能立即使肺動脈壓升高,導致肺水腫產生。胡國英[8]等證實大鼠羊水入血后可引起中性粒細胞、巨噬細胞浸潤及一系列病理變化,由此引起肺損傷及臨床癥狀,但并無致死性動物。有報道稱AFE病例尸檢未在孕產婦血循環中發現胎兒鱗狀上皮碎屑,認為鱗狀上皮存在與否對AFE而言并非主要[9]。這些結果直接表明羊水栓塞致肺循環病變的原因不完全是羊水中有形成分引起的機械性栓塞,而羊水入血后引起一些血管活性物質的釋放導致機體出現嚴重的病理生理改變,或者是極少數的人對羊水中的抗原成分產生特殊的反應,使孕產婦出現嚴重的血液動力學變化,包括左心功能衰竭、肺血管損傷、凝血功能異常,這些是引發AFE的重要因素[10,11]。羊水進入孕產婦血循環是胎盤生理屏障存在破口之故,在正常妊娠中胎兒血細胞、胎兒上皮細胞或滋養層細胞在孕產婦血中可以見到。大多數情況下這些物質不引起臨床癥狀,但在某些孕婦中這種胎兒相關成分則可引起一系列嚴重的病理生理反應,極像在過敏性休克及感染性休克中所見[11~15]。現有部分觀點認為AFE發病機制可能是無抗體參加的過敏樣反應,在此反應中異體物質引起肥大細胞脫顆粒,異常的花生四烯酸代謝產物,包括白三烯、前列腺素、血栓素等進入孕產婦血循環引起一系列嚴重病理生理變化[12,13]。已有研究證實,這些遞質和凝血機制紊亂直接相關。可以說,羊水栓塞綜合征事實上是一種類過敏反應綜合征。隨著對變應原疾病發病機制認識的不斷深入,目前已從單純測定組胺、白三烯等介質延伸至檢測參與過敏性炎癥重要的生物活性物質,以評估炎癥的程度和判斷病情。具體機制尚需進一步研究。
我們的實驗也證實上述觀點,只有在羊水量極大的情況下,甚至是可以收集到的全部自體羊水成分通過下腔靜脈等進入右心室,才會有部分實驗大鼠通過栓塞引起肺組織小灶狀梗死,羊水成分才能通過梗死灶進入肺靜脈,且進入體循環的羊水量尚不足以引起臟器的梗死。但自體羊水大部分進入循環系統在臨床中是難以發生的,而且我們的實驗也證實羊水進入循環系統后存在吸收和分解的情況。且本次實驗的大鼠均未發生死亡,推測可能原因是致死性AFE發生率較低,實驗動物數量少,難以成功復制致死性AFE模型;在實驗中,收集的羊水保持清亮狀態,胎糞浸染少,致敏性強的胎糞成分少,也可能是無致死性AFE的原因之一;大鼠耐受性較強,對有創性手術和實驗抵御能力強,且無菌操作和大鼠飼養條件中環境的消毒是保證大鼠存活的必要條件;實驗觀測時間短,尚未達到溶血、出血等因素導致的多器官功能衰竭死亡,也可能是實驗中無致死性AFE的原因之一。從上述情況推測少量羊水成分進入孕鼠血循環后,單一因羊水成分中有形物質機械性栓塞尚不足以導致實驗動物死亡,且羊水成分存在重吸收和分解的情況。我們認為在實驗中羊水成分的檢出率應為100%,但本實驗結果卻顯示低劑量組3只孕鼠( 37.5% )肺組織中未檢出羊水成分,在黃神姣等[16]的實驗中,也證實通過病理學來診斷羊水栓塞可能是不可靠的。

圖5 肺APM染色,×400,示重度肺水腫
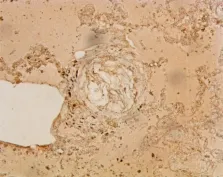
圖6 肺抗角蛋白16染色,×400,示重度肺水腫
綜上所述,羊水成分進入孕鼠血循環后,單一因羊水成分中有形物質機械性栓塞尚不足以導致實驗動物死亡,且羊水成分存在重吸收和分解的情況。羊水栓塞綜合征事實上是存在個體差異和種屬差異,是一種類過敏反應綜合征。隨著對變應原疾病發病機制認識的不斷深入,目前已從單純測定組胺、白三烯等介質延伸至檢測參與過敏性炎癥重要的生物活性物質,以評估炎癥的程度和判斷病情,而類過敏反應綜合征的發生和發展機制尚需進一步研究。

