自擬中藥方聯合西藥對類風濕關節炎患者相關細胞因子及骨代謝的影響
燕 妮
(河北省張家口市第二醫院,河北 張家口 075000)
類風濕關節炎(RA)是以對稱性關節炎為主要表現的自身免疫性疾病,其病理特點是滑膜增殖形成血管翳,骨及軟骨侵襲性破壞,最終導致關節強直、畸形與功能喪失[1]。RA屬祖國醫學“痹證”“尪痹”范疇,其病機為痰熱互結、寒濕內留、經絡阻滯、瘀血內停[2]。近年研究表明,中醫在RA治療方面取得滿意療效[3]。本研究采用自擬中藥方聯合西藥對RA患者進行治療,探討對相關細胞因子及骨代謝的影響,現報道如下。
1 臨床資料
1.1入選與剔除標準 入選標準:符合RA相關診斷標準[4],至少5個關節腫脹疼痛,并有滑膜炎證據;有典型的RA骨破壞改變;入院前1個月未服用過與治療相關的藥物及抗炎藥;患者及家屬知情并簽署同意書。剔除標準:心肝腎功能異常;合并骨性關節炎、痛風性關節炎、系統性紅斑狼瘡、胃腸道疾病、結締組織病、腫瘤及精神疾病等;妊娠或哺乳期女性;對治療相關藥物過敏及資料不全者。
1.2一般資料 選取2016年3月—2017年2月本院收治的符合上述標準的RA患者78例進行研究,將患者隨機分為2組:觀察組39例,男14例,女25例;年齡31~64(46.8±7.3)歲;病程2~11(5.6±1.7)年。對照組39例,男15例,女24例;年齡32~66(47.4±7.5)歲;病程2~10(5.7±1.8)年。2組年齡、性別、病程相比差異均無統計學意義(P均>0.05)。
1.3治療方法 對照組給予來氟米特膠囊(奧克魯,江蘇聯環藥業,國藥準字H20080215)口服,20 mg/次,1次/d;尼美舒利分散片(湖北舒邦藥業,國藥準字H20010730)口服,0.1 g/次,2次/d。觀察組在對照組治療基礎上服用自擬中藥方,方藥組成:制川烏10 g、制草烏10 g、海風藤20 g、青風藤15 g、地龍15 g、制沒藥10 g、雞血藤30 g、制乳香10 g、甘草10 g、桂枝15 g、白術15 g、白芍15 g、知母15 g、防風15 g,1劑/d,水煎分2次溫服。2組患者均治療3個月進行療效評價。
1.4觀察指標 采集2組患者治療前后清晨空腹靜脈血,魏氏法測定紅細胞沉降率(ESR),全自動免疫速率散射比濁法測定C反應蛋白(CRP)水平,膠乳凝集試驗測定類風濕因子(RF)水平,ELISA法測定血清白細胞介素-17(IL-17),IL-27,IL-32及腫瘤壞死因子-α(TNF-α)、Ⅰ型膠原氨基端前肽(PⅠNP)、骨特異性堿性磷酸酶(BAP)、血清骨鈣素(BGP)水平。
1.5統計學方法 數據采用SPSS 19.0軟件進行分析。計資料采用2檢驗;服從正態分布的計量資料以表示,組間比較采用獨立樣本t檢驗,治療前后比較采用配對t檢驗。P<0.05為差異有統計學意義。
2 結 果
2.1治療前后ESR、CRP、RF比較 2組患者治療后ESR、CRP、RF均較治療前明顯降低(P均<0.05),觀察組治療后ESR、CRP、RF均明顯低于對照組(P均<0.05)。見表1。
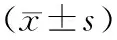
表1 2組治療前后ESR、CRP、RF比較
注:①與治療前比較,P<0.05。
2.2治療前后TNF-α、IL-17、IL-27、IL-32比較 2組患者治療后TNF-α、IL-17、IL-27、IL-32均較治療前明顯降低(P均<0.05),觀察組治療后TNF-α、IL-17、IL-27、IL-32均明顯低于對照組(P均<0.05)。見表2。
2.3治療前后PⅠNP、BAP、BGP比較 觀察組治療后PⅠNP、BAP均較治療前明顯降低(P均<0.05),BGP均較治療前明顯升高(P均<0.05);對照組治療后BAP較治療前明顯降低(P<0.05),BGP較治療前明顯升高(P<0.05)。觀察組治療后BAP、PⅠNP明顯低于對照組(P均<0.05),BGP明顯高于對照組(P<0.05)。見表3。
3 討 論
流行病學顯示,RA發病人群25~50歲者較多,其發病率在我國為0.32%~0.36%,其中未經治療者2年致殘率為50.0%,3年致殘率在70.0%以上,約一半患者因致殘而喪失勞動能力[5]。現代醫學認為,RA的發病同自身抗體、RF、感染因子、易感基因等致病抗體的產生密切相關[6]。
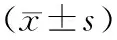
表2 2組治療前后TNF-α、IL-17、IL-27、IL-32比較
注:①與治療前比較,P<0.05。
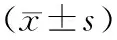
表3 2組治療前后PⅠNP、BAP、BGP比較
注:①與治療前比較,P<0.05。
RA患者西醫治療的原則是抗炎止痛、保持關節活動度與協調性、減緩或終止病情進展、維持正常生活與勞動能力,常用藥物包括非甾體類抗炎藥、免疫抑制劑、生物制劑、抗風濕藥、激素類等,但均缺乏選擇性,且長期大量應用易引起體質量增加、高血壓、股骨頭壞死等不良反應,因此臨床需結合其他藥物和方法進行治療,以最大可能減緩或終止RA病情進展[7]。中醫醫學認為,RA多因風、寒、濕、熱邪痹阻經絡、關節,導致氣滯、濕阻、痰凝、血瘀,治以祛風、散寒、活血、祛濕等為主[2]。有學者采用清熱除濕中藥聯合西藥治療活動期RA,結果關節疼痛、壓痛、腫脹、晨僵等指標改善情況明顯優于單純西藥治療[8]。本研究聯合自擬中藥對RA患者進行治療,方中制川烏、制草烏除濕通痹、散寒止痛;桂枝、白芍、甘草暢氣血、和營衛、解肌發表;防風勝濕、止痙、外散表寒;地龍善行走竄,通經活絡;制乳香、制沒藥行氣活血止痛;知母清熱瀉火、滋陰潤燥;海風藤、青風藤通經絡、祛風濕、止痹痛;白術健脾化濕;全方共奏祛風散寒、通絡止痛、化濕宣痹之功效。現代藥理學研究顯示[9-10],白芍中有效成分白芍總苷可從多個環個影響炎癥過程及體液免疫、細胞免疫過程,具有抗炎、止痛、保肝作用;川烏、草烏具有較好的鎮痛作用;知母可抑制急性炎性滲出、抑制毛細血管通透性、減輕組織水腫及抗炎作用;防風具有抗炎、鎮痛、消腫作用等。本研究結果顯示,2組患者治療后ESR、CRP、RF較治療前明顯降低,觀察組治療后ESR、CRP、RF明顯低于對照組,提示自擬中藥聯合西藥可進一步控制RA臨床癥狀,控制風濕活動。
研究認為,RA發病機制與遺傳易感個體自身免疫反應有關,免疫細胞及其相關細胞因子在RA發病、病情發展中起重要作用[6]。TNF-α被認為是滑膜炎癥反應的關鍵性因子,可誘導細胞因子促進白細胞聚集、激活內皮細胞、活化破骨細胞和破壞軟骨,在RA發病機制中發揮重要作用,是RA發病的啟動細胞因子[11]。IL-17是Th17細胞分泌的強大的促炎因子,可誘導核因子кB受體活化因子配體表達,破骨細胞祖細胞向成熟破骨細胞分化,使成骨減少及破骨增加,最終造成關節、軟骨的侵蝕破壞,IL-17還可促進TNF-α分泌,誘導滑膜液中IL-1、IL-6的表達,協同促進成骨細胞、軟骨細胞合成前列腺素E(PGE),刺激滑膜分泌炎癥因子,增加關節軟骨的損傷[9,12]。IL-27有免疫促進和免疫抑制效應,在活動性RA患者血清中其水平明顯升高,是反映疾病活動度的早期指標[13]。IL-32為促炎細胞因子,可誘導TNF-α、IL-1、IL-6等細胞因子的產生,參與關節的破壞[14]。本研究顯示,2組患者治療后TNF-α、IL-17、IL-27、IL-32均較治療前降低,觀察組治療后TNF-α、IL-17、IL-27、IL-32均低于對照組,提示自擬中藥聯合西藥具有明顯下調RA患者促炎因子的作用,從而有效保護關節,控制病情發展。
Ⅰ型膠原是機體最豐富的膠原類型,是礦化骨中唯一的膠原類型,是反映骨形成特異性和靈敏的指標;BAP是評價骨形成與骨轉換的重要酶,臨床測定其含量可準確反映早期骨改變情況;BGP是骨細胞合成的低分子蛋白,可直接反映成骨細胞活性[15-16]。本研究顯示,觀察組治療后PⅠNP、BAP低于對照組,BGP高于對照組,提示自擬中藥聯合西藥可有效拮抗RA患者的骨破壞,改善骨代謝。
綜上所述,自擬中藥方聯合西藥可有效控制RA的活動,下調促炎因子水平,改善骨代謝狀態,具有良好的臨床效果。

