化學反應原理核心考點測試題(A卷)
■河南省鄲城縣第一高級中學 王圓圓
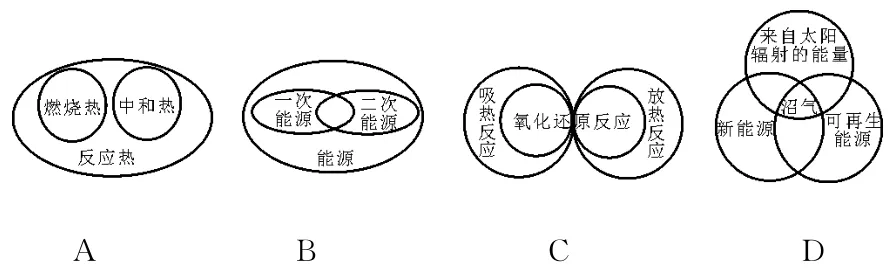
1.下列圖示關系不正確的是( )。 是( )。
2.自來水加工處理流程如下,下列有關說法不正確的是( )。
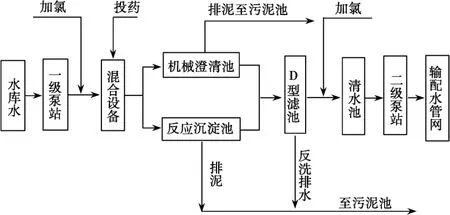
A.若用FeSO4作混凝劑,最終鐵將以Fe(OH)2形式進入反應沉淀池
C.自來水生產中,前面加氯起消毒殺菌作用,后面加氯是保持水中有效氯的含量,防止自來水二次污染
D.用ClO2消毒自來水,比等質量氯氣的消毒效率高
3.近幾年科學家發明的一種新型可控電池——鋰水電池,工作原理如圖1所示。下列有關說法正確的是( )。
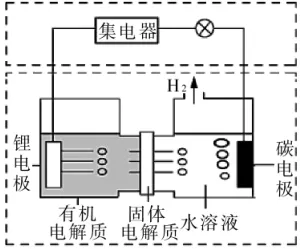
圖1
A.碳極發生氧化反應
B.有機電解質和水溶液不可以互換區域
C.Li電極的電極反應式為Li++e-==Li
D.若電源工作時產生標準狀況下1.12LH2,則有0.1mol電子通過有機電解質傳遞到正極
4.僅根據題中圖示得出的結論不合理的
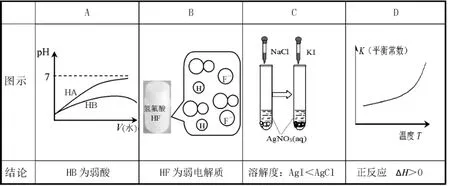
5.Ca(OH)2/CaO體系的能量循環如下所示。
下列說法正確的是( )。
A.ΔH5>0
B.ΔH1+ΔH2=0
C.ΔH3=ΔH4+ΔH5
D.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5=0
6.近年斯坦福大學研究人員研制出一種可在一分鐘內完成充放電的超常性能鋁離子電池,內部用AlCl-4和有機陽離子構成電解質溶液,其放電工作原理如圖2所示。下列說法不正確的是( )。

圖2
A.放電時,鋁為負極、石墨為正極
B.放電時,有機陽離子向鋁電極方向移動
7.葡萄酒中常加入亞硫酸鹽作為食品添加劑,為檢測某葡萄酒樣品中亞硫酸鹽的含量(通常以酒樣中SO2的量計),某研究小組設計了如下實驗(已知還原性:
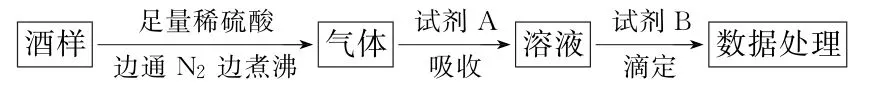
下列說法不正確的是( )。
A.葡萄酒中加亞硫酸鹽的主要目的是防止氧化,利用了亞硫酸鹽的還原性
B.通入N2和煮沸的目的是為了將產生的氣體從溶液中全部趕出
C.若試劑A選擇氯水,則試劑B可選擇NaOH標準液
D.若試劑A選擇堿液,調節吸收后溶液為中性,則試劑B可選擇I2標準液
8.向含1molNa2CO3的飽和溶液中緩緩通入CO2氣體,使之充分反應,下列圖像表示正確的是( )。
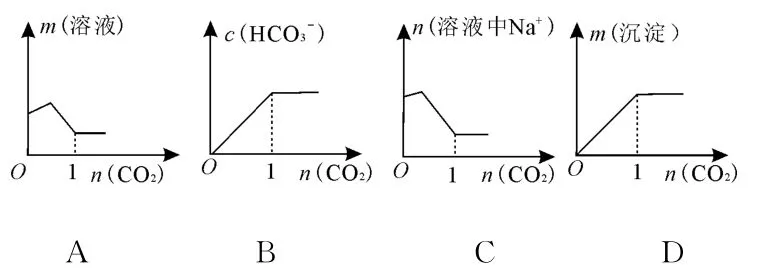
9.水玻璃(Na2SiO3溶液)廣泛應用于耐火材料、洗滌劑生產等領域,是一種重要的工業原料。用稻殼灰(SiO2:65%~70%,C:30%~35%)制取水玻璃的工藝流程如下。
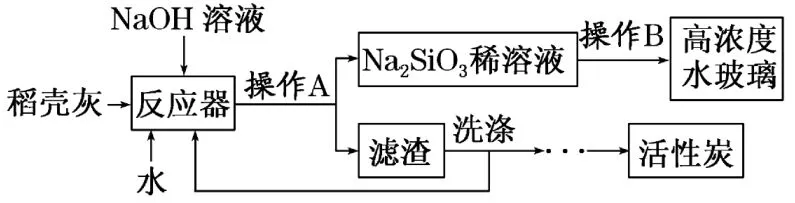
下列說法正確的是( )。
A.原材料稻殼灰價格低廉,且副產品活性炭有較高的經濟價值
B.操作A與操作B完全相同
C.該流程中硅元素的化合價發生改變
D.反應器中發生的復分解反應為SiO2+2NaOH==Na2SiO3+H2O
10.氯堿工業的尾氣——氯氣和氫氣,按照一定比例在合成爐內燃燒,可制備鹽酸。反應過程中的能量變化如下所示。
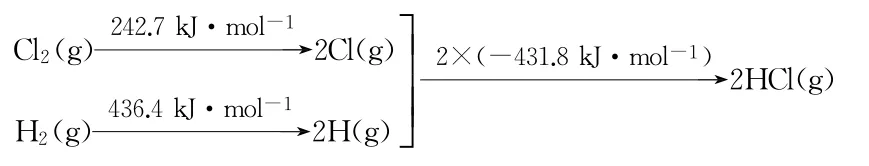
則 H2(g)+Cl2(g)==2HCl(g)的 ΔH為( )。
A.184.5kJ·mol-1
B.-184.5kJ·mol-1
C.1542.7kJ·mol-1
D.-1542.7kJ·mol-1
11.電石漿是氯堿工業中的一種廢棄物,其大致組成如表1所示。
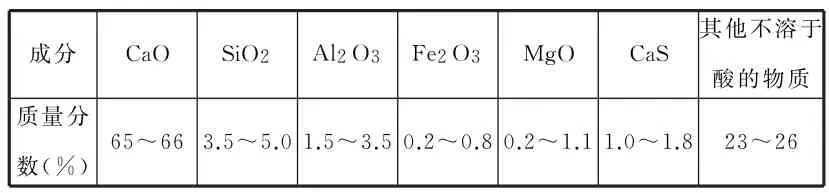
表1
用電石漿可生產無水CaCl2,某化工廠設計了以下工藝流程。
觀察組護士安全管理意識、安全防范完善性優于對照組,P<0.05,其中,觀察組護士安全管理意識、安全防范完善性96.55±2.89分、98.62±1.78分優于對照組82.50±3.13分、82.67±2.27分,P<0.05。
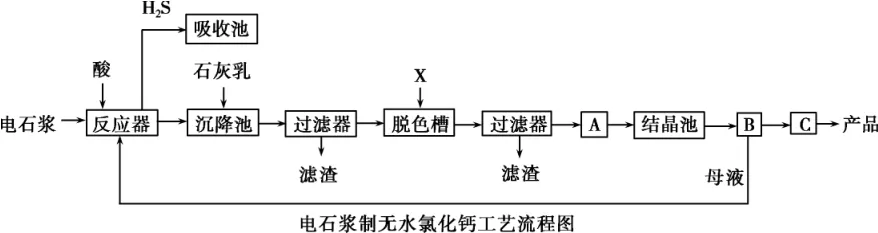
已知氯化鈣晶體的化學式是CaCl2·6H2O,H2S是一種酸性氣體,且具有還原性。下列說法錯誤的是( )。
A.反應器中加入的酸應選用硫酸
B.脫色槽中應加入的物質X是活性炭
C.設備A的作用是蒸發濃縮,設備C的作用是脫水干燥
D.將設備B中產生的母液重新引入反應器的目的是對母液回收利用,降低廢棄物排放量,提高經濟效益。
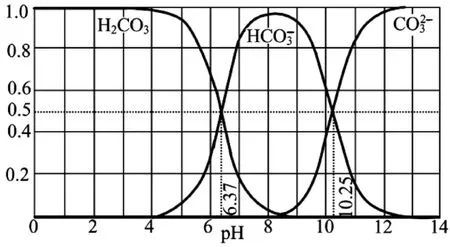
圖3
B.為獲得盡可能純的NaHCO3,宜控制溶液的pH為7~9
D.若是0.1molNaOH 反應后所得的1L溶液pH=10時,溶液中存在以下關系:
13.化學平衡常數K的數值大小是衡量化學反應進行程度的標志,在常溫下,下列反應的平衡常數的數值如下:
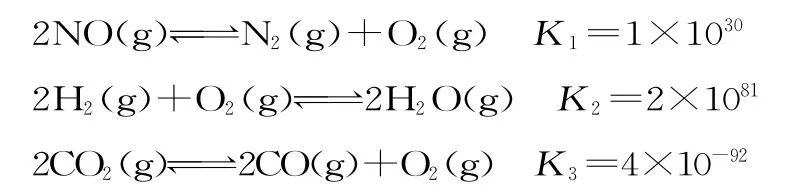
以下說法正確的是( )。
A.常溫下,NO分解產生O2的反應的平衡常數表達式為K1=c(N2)·c(O2)
B.常溫下,水分解產生O2,此時平衡常數的數值約為5×10-80
C.常溫下,NO、H2O、CO2三種化合物分解放出O2的傾向由大到小的順序為NO>H2O>CO2
D.以上說法都不正確
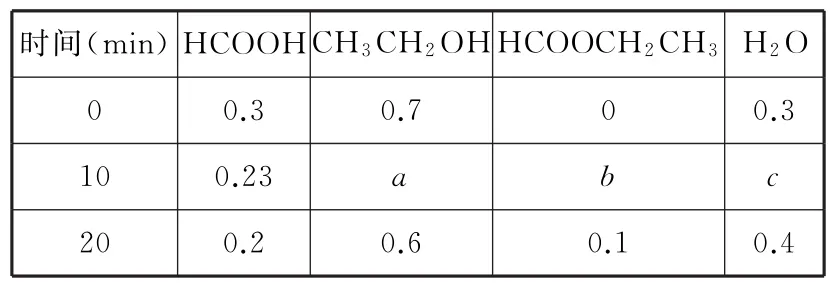
表2
有關物質在101.3kPa時沸點如表3。

表3
該反應的化學平衡常數表達為K=。有關下列敘述不正確的是( )。
A.由題給條件不能判斷出K值隨溫度變化是增大還是減小
B.表中a應該等于0.63mol·L-1
D.在起始濃度相同的情況下,要提高產率,可采取的措施是適當升高溫度,將甲酸乙酯蒸出
15.傳統的引爆炸藥由于其中含Pb,使用時將產生污染,同時其引爆后的剩余炸藥還嚴重危害接觸者的人身安全,美國UNC化學教授ThomasJ.Meyer等研發了環境友好、安全型的“綠色”引爆炸藥,其中一種可表示為Na2R,爆炸后不會產生危害性殘留物。已知10mLNa2R溶液含Na+的微粒數為N個,該Na2R溶液的物質的量濃度為( )。
A.N×10-2mol·L-1
16.研究CO2的利用對促進低碳社會的構建具有重要的意義。
(1)現有反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g) ΔH<0。在850℃時,K=1。
①如果上述反應的平衡常數K值變大,該反應____(填標號)。
a.一定向正反應方向移動
b.在平衡移動過程中正反應速率先增大后減小
c.一定向逆反應方向移動
d.在平衡移動過程中逆反應速率先減小后增大
②若反應的容器容積為2.0L,反應時間為4.0min,容器內氣體的物質的量減小了0.8mol,在這段時間內CO2的平均反應速率為____。
③在850℃時,若向1L的密閉容器中同時充入3.0molCO2(g)、1.0molH2(g)、1.0molCH3OH(g)和5molH2O(g),上述反應向____(填“正反應”或“逆反應”)方向進行。
(2)以二氧化鈦表面覆蓋Cu2Al2O4為催化劑,可以將CO2和CH4直接轉化成乙酸。
①在不同溫度下催化劑的催化效率與乙酸的生成速率如圖4所示。250~300℃時,溫度升高而乙酸的生成速率降低的原因是________。
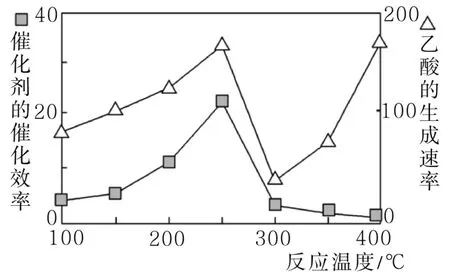
圖4
②為了提高該反應中CO2的轉化率,可以采取的措施是____。
17.氮元素在海洋中的循環,是整個海洋生態系統的基礎和關鍵。海洋中無機氮的循環過程可用圖5表示。
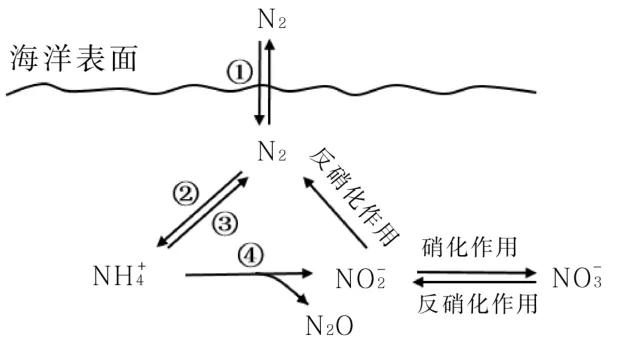
圖5
(1)海洋中的氮循環起始于氮的固定,其中屬于固氮作用的一步是____(填圖中數字序號)。
(2)下列關于海洋氮循環的說法正確的是____(填字母序號)。
a.海洋中存在游離態的氮
b.海洋中的氮循環起始于氮的氧化
c.海洋中的反硝化作用一定有氧氣的參與

(4)有人研究了溫度對海洋硝化細菌去除氨氮效果的影響,表4為對10L人工海水樣本的監測數據。
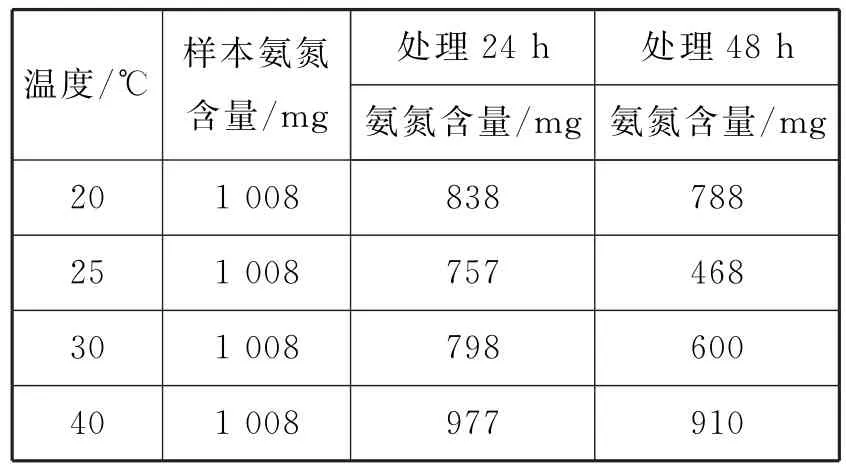
表4
硝化細菌去除氨氮的最佳反應溫度是____,在最佳反應溫度時,48h內去除氨氮反應的平均速率是____mg·L-1·h-1。
18.現代傳感信息技術在化學實驗中有廣泛的應用。某小組用傳感技術測定噴泉實驗中的壓強變化來認識噴泉實驗的原理(如圖6所示),并測定電離平衡常數Kb。
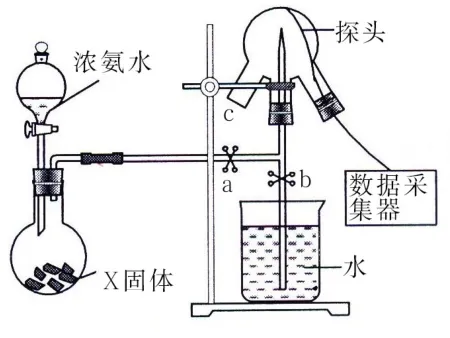
圖6
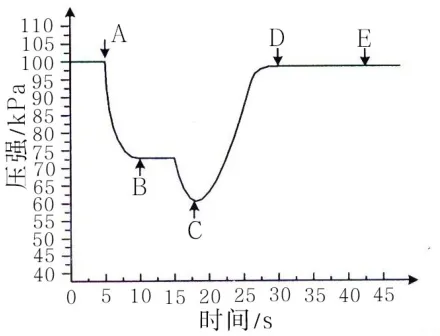
圖7
(1)實驗室可用濃氨水和X固體制取NH3,X固體可以是____。
A.生石灰 B.無水氯化鈣
C.五氧化二磷 D.堿石灰
(2)檢驗三頸瓶集滿NH3的方法是____。
(3)關閉a,將帶有裝滿水的膠頭滴管的橡皮塞塞緊c口,____,引發噴泉實驗,電腦繪制三頸瓶內氣壓變化曲線如圖7所示。圖7中____點時噴泉最劇烈。
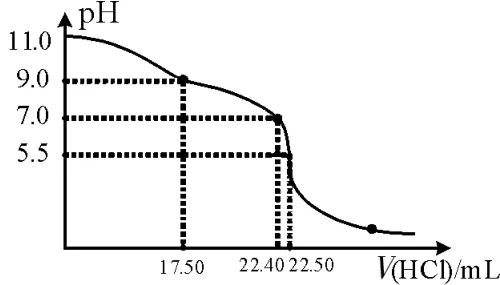
圖8
(4)從三頸瓶中用____(填儀器名稱)量取20.00mL氨水至錐形瓶中,用0.05000mol·L-1鹽酸滴定。用pH計采集數據,電腦繪制滴定曲線如圖8所示。
(5)據圖8計算,當pH=11.0時,NH3·H2O電離平衡常數Kb的近似值,Kb≈____。
19.某實驗小組同學依據資料深入探究Fe3+在水溶液中的行為。
資料:
ⅰ.Fe3+在水溶液中以水合鐵離子的形式存在,如[Fe(H2O)6]3+。
[Fe(H2O)6]3+發生如下水解反應:
[Fe(H2O)6]3+(幾乎無色)+nH2O?[Fe(H2O)6-n(OH)n]3-n(黃色)+nH3O+(n=0~6)
ⅱ.[FeCl4(H2O)2]-為黃色。
進行實驗:
【實驗Ⅰ】如圖9。

圖9
【實驗Ⅱ】
分別用試管①③中的試劑作為待測液,用色度計測定其透光率。透光率越小,溶液顏色越深;透光率越大,溶液顏色越淺。
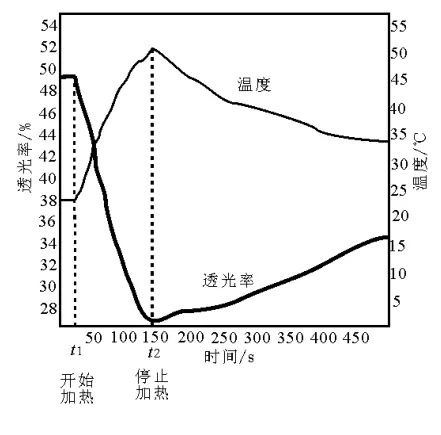
圖10 Fe(NO3)3溶液透光率隨溫度變化曲線
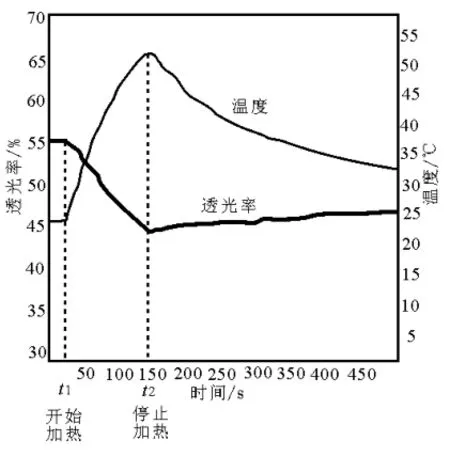
圖11 FeCl3溶液透光率 隨溫度變化曲線
(1)實驗Ⅰ中,試管②溶液變為無色的原因是____。
(2)實驗Ⅰ中,試管③溶液呈棕黃色與[FeCl4(H2O)2]-有關,支持此結論的實驗現象是____。
(3)由實驗Ⅱ圖10、圖11可知:加熱時,溶液顏色____(填“變淺”“變深”或“不變”)。
(4)由實驗Ⅱ,可以得出如下結論:
[結論一]FeCl3溶液中存在可逆反應:[FeCl4(H2O)2]-+4H2O?[Fe(H2O)6]3++4Cl-,得出此結論的理由是____。
[結論二]結論一中反應的ΔH____(填“>0”或“<0”)。
(5)實驗小組同學重新設計了一個實驗證明(4)中結論一。實驗方案:取試管①中溶液,___(請描述必要的實驗操作和現象)。
20.鎂及其化合物用途非常廣泛,目前世界上60%的鎂是從海水中提取的。從海水中提取鎂需先將海水淡化獲得淡水和濃海水,濃海水的主要成分如表5。
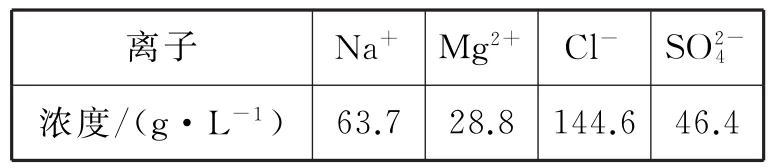
表5
利用濃海水提鎂的一段工藝流程如下。
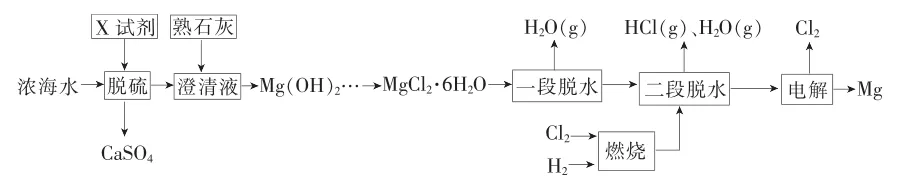
請回答下列問題:
(1)濃海水主要含有的四種離子中物質的量濃度最小的是____。在上述流程中,可以循環使用的物質是____。
(2)在該工藝過程中,X試劑的化學式為____。
(3)“一段脫水”的目的是制備MgCl2·2H2O;“二段脫水”的目的是制備電解原料,若將MgCl2·6H2O直接加熱脫水,則會生成Mg(OH)Cl。若電解原料中含有Mg(OH)Cl,電解時Mg(OH)Cl與陰極產生的Mg反應,使陰極表面產生MgO鈍化膜,降低電解效率。生成MgO的化學方程式為____。
(4)若制得Mg(OH)2的過程中濃海水的利用率為80%,由 Mg(OH)2至“二段脫水”制得電解原料的過程中鎂元素的利用率為90%,則1m3濃海水可得“二段脫水”后的電解原料質量為____g。
(5)以LiCl-KCl共熔鹽為電解質的Mg-V2O5電池是戰術導彈的常用電源,該電池的總反應為Mg+V2O5+2LiCl==MgCl2+V2O4·Li2O,該電池的正極反應式為____。
(6)Mg合金是重要的儲氫材料。2LiBH4/MgH2體系放氫焓變如下所示。
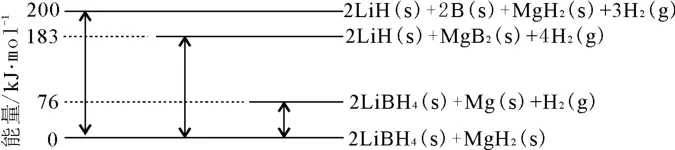
則:Mg(s)+2B(s)==MgB2(s) ΔH=____。

