化學反應原理核心考點測試題(B卷)參考答案
1.B 2.A 3.B 4.C 5.C 6.A 7.A 8.D
9.B 提示:a~b導電能力增強,是因為生成了鹽(強電解質),可以說明HR為弱酸,A項正確;b點溶液的pH=7,是因為生成的弱酸弱堿鹽中兩種離子的水解程度相同,B項錯誤;c點溶液是NH4R與NH3·H2O的混合溶液,溶液呈堿性,有c(OH-)>c(H+),根據電荷守恒有c(NH4)>c(R-),C項正確;溫度不變,Kw為常數,D項正確。
10.C 提示:VB2失電子發生氧化反應,則VB2極發生的電極反應為2VB2+22OH--22e-==V2O5+2B2O3+11H2O,A項錯誤;外電路中電子由VB2電極流向陰極c電極,B項錯誤;c電極表面先有紅色物質析出,后有氣泡產生,C項正確;當外電路中通過0.04mol電子時,B裝置內與氧氣相連的b為陽極,氫氧根失電子生成氧氣0.01mol,又共收集到0.448L氣體即0.02mol,則陰極也產生0.01mol的氫氣,所以溶液中的銅離子為0.01mol,則CuSO4溶液的物質的量濃度為0.1mol·L-1,D項錯誤。
11.B 提示:水蒸氣液化時放出熱量,放熱時焓變是負值,所以得CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(l) ΔH<-574kJ·mol-1,A項正確;等物質的量的甲烷分別參加反應①②時,碳元素的化合價變化相同,所以反應轉移的電子數相同,B項錯誤;由①+②得,2CH4(g)+4NO2(g)==2N2(g)+2CO2(g)+4H2O(g) ΔH=-1734kJ·mol-1,C項正確;整個過程中轉移電子的物質的量mol,D項正確。
12.D 提示:當V(NaOH)=20mL時,溶液發生反應H2A+NaOH==NaHA+H2O,結合圖像可知,在NaHA溶液中,HA-電離程度比HA-水解程度大,則有溶液中離子濃度大小關系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),A 項正確;由 A項可知,等體積等濃度的NaOH溶液與H2A溶液混合后,其溶液中水的電離程度比純水的小,B項正確;在NaHA溶液中,以HA-和H2O為基準微粒,由質子守恒得:c(OH-)+c(A2-)=c(H+)+c(H2A),C項正確;向Na2A溶液加入水的過程中,促進A2-水解,隨著水的量不斷增大,溶液的體積不斷增大,則溶液中OH-的濃度不斷減少,pH不斷減小,D項錯誤。
13.(1)增大E1-E2(2)ABD
提示:(1)根據圖像可知反應物的總能量低于生成物的總能量,因此反應Ⅰ是吸熱反應,ΔH1>0。升高溫度,平衡正向移動,平衡常數增大。將圖像中的反應物與生成物互換,即得到反應Ⅰ的逆反應的能量變化圖像,此時的反應物能量與過渡態的能量差E1-E2即為逆反應的活化能。(2)CO(g)+2H2(g)?CH3OH(g)是一個熵減小的反應,但能自發進行,因此必然是放熱反應,則降低溫度平衡正向移動,CO的轉化率增大,A項正確;將甲醇從反應體系中分離出來,生成物的濃度減小,平衡正向移動,B項正確;充入He但體積不變,反應體系中各組分的濃度不變,平衡不移動,C項錯誤。按原比例再充入CO和H2相當于增加了反應物的濃度,平衡正向移動,D正確。(3)當有3mol甲醇放電時,生成的3molCO2與4mol KOH發生反應,根據C元素和K元素守恒可求出溶液中生成了1molK2CO3和2mol KHCO3。由于水解一般都是很微弱的,且溶液呈堿性,因此有。(4)①根據圖示中電子的流向可知M電極是負極,N電極是正極。正極的電極反應式應為O2+4H++,用總反應式減去正極的電極反應式即得負極的電極反應式:CH3OH+H2O-②由于Al電極附近逐漸變渾濁并有氣泡逸出,因此Al作陽極,放電生成的Al3+與溶液中的發生雙水解反應,生成了Al(OH)3沉淀和CO2氣體。
14.(1)H2O2+2Fe2++2H+==2Fe3++2H2O
(2)3.6×104
(3)ZnO Fe3++3H2O==Fe(OH)3↓+3H+
(4)取最后一次洗滌液,加入硝酸鋇 坩堝
(5)在前期操作中添加了含鋅元素的物質
提示:(1)雙氧水與二價鐵離子反應的離子方程式為H2O2+2Fe2++2H+==2Fe3++2H2O。
(2)溶液的pH=6.4時,銅離子剛好沉淀完全:c(Fe2+)=所以
(3)三價鐵離子和鋁離子水解的離子方程式:Fe3++3H2O==Fe(OH)3+3H+,Al3++3H2O==Al(OH)3+3H+,要調節到3.7至5.2時除去三價鐵離子和鋁離子,但是不能引入新的雜質離子,可以選用ZnO,氧化鋅與氫離子反應,消耗氫離子,促進水解平衡向正方向移動,反應的離子方程式為Fe3++3H2O==Fe(OH)3↓+3H+。
(4)如果沉淀洗滌不干凈,則殘留硫酸根離子,取最后一次洗滌液,加入硝酸鋇,若產生白色沉淀則說明洗滌不干凈,反之洗滌干凈;在實驗室進行焙燒時,盛放沉淀丙的儀器為坩堝。
(5)在流程中調節pH時加入了氧化鋅,所以所得ZnO產品中鋅的含量遠超過鋅渣中鋅元素的含量。
15.(1)①作還原劑 ②0.05mol
(2)CaHPO4、Ca(H2PO4)2
(3)1.66
(4)114.87
(5)2.91
提示:(1)①根據圖11知焦炭的作用是還原P生成P4;②Cu元素的化合價由+2價降低到+1價,CuSO4是氧化劑,P4部分磷元素由0價降低到-3價,部分磷元素由0價升高到+5價,磷元素的化合價既升高又降低,所以P4既是氧化劑又是還原劑,若有11mol P4參加反應,其中5mol的P4作氧化劑,60 mol硫酸銅作氧化劑,只有6mol的P4作還原劑,則由電子守恒可知,有1mol的CuSO4參加反應,設被硫酸銅氧化的白磷分子的物質的量為n,則:n×4(5-0)=1mol×(2-1),解得n=0.05mol。
(2)磷酸為三元酸與氫氧化鈣反應,依據磷酸與氫氧化鈣量不同,得到的產物可能是Ca3(PO4)2、CaHPO4、Ca(H2PO4)2。
(5)mg磷灰石中Ca元素物質的量為mg×47.3%÷56g·mol-1=0.00845mmol,S元素物質的量為mg×3.5%÷80g·mol-1=0.00044mmol,P元素物質的量為31g·mol-1=0.004mmol,磷酸中P元素物質的量為 0.05L×0.5mol·L-1=0.025mol,硫酸中S元素質量為0.05L×0.1mol·L-1=0.005mol,由化學式可知,,故0.00845m=(0.00044m+0.005)+(0.004m,解得m=2.91。
16.Ⅰ.(1)Fe3+CCl4
(2)KI
Ⅱ.(1)藍色褪去,半分鐘內顏色不變化
(2)2CuCl2+4KI==2CuI↓+I2+4KCl
(3)85.5%
提示:Ⅰ.(1)根據步驟2中第①份試液中的實驗現象,加碘鹽中肯定含有Fe3+;根據下層為紫紅色知,X應為CCl4。(2)因為+5I-+6H+==3I2+3H2O,所以根據第②份試液中加入KIO3固體、淀粉無現象,證明碘鹽中一定不含KI。(3)由題干中所給信息,根據氧化劑的氧化性大于氧化產物的氧化性可知,氧化性:(4)由于在碘鹽中含有,所以加入足量KI固體后,發生的離子反應為
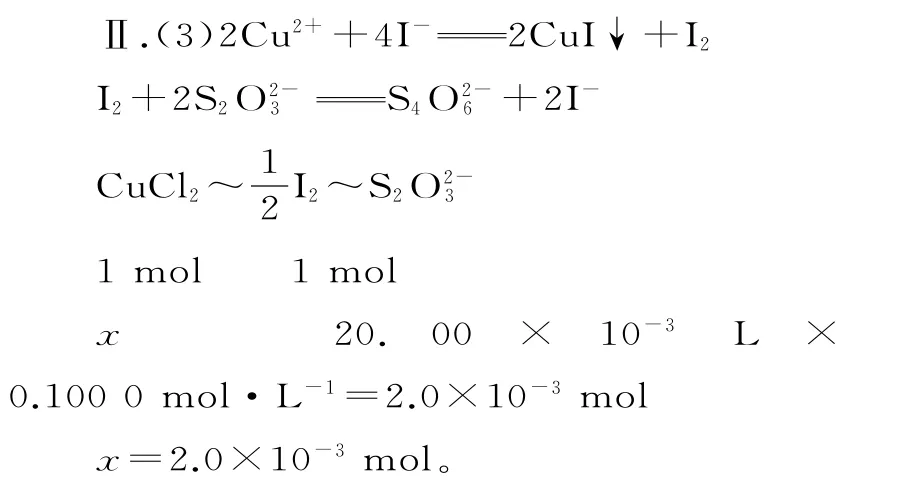
所以CuCl2·2H2O的質量分數為

