化學反應原理核心考點測試題(B卷)
■河南省鄲城縣第一高級中學 張亞濤
1.C-NaMO2電池是科學家正在研發的鈉離子電池,據悉該電池可以將傳統鋰電池的續航能力提升7倍,如圖1所示。該電池的電池反應式為NaMO2+nC?Na(1-x)MO2+NaxCn,下列有關該電池的說法正確的是( )。

圖1
A.電池放電時,溶液中鈉離子向負極移動
B.該電池負極的電極反應為NaMO2-xe-==Na(1-x)MO2+xNa+
C.消耗相同質量金屬時,用鋰作負極產生電子的物質的量比用鈉時少
D.電池充電時的陽極反應式為nC+xNa+-xe-==NaxCn

圖2
A.N2(g)+3H2(g)?2NH3(l) ΔH=2(a-b-c)kJ·mol-1
B.N2(g)+3H2(g)?2NH3(g) ΔH=2(b-a)kJ·mol-1
C.N2(g)+3H2(g)?2NH3(l) ΔH=(b+c-a)kJ·mol-1
D.N2(g)+3H2(g)?2NH3(g) ΔH=(a+b-c)kJ·mol-1
3.在298K時,實驗測得溶液中的反應H2O2+2HI?2H2O+I2在不同濃度時的化學反應速率(v)見表1。

表1
由此可推出當c(HI)=0.500mol·L-1、c(H2O2)=0.400mol·L-1時的反應速率為( )。
A.0.038mol·L-1·s-1
B.0.152mol·L-1·s-1
C.0.608mol·L-1·s-1
D.0.760mol·L-1·s-1
4.利用圖3所示裝置(電極均為惰性電極)可吸收SO2,并用陰極排出的溶液吸收NO2。下列說法正確的是( )。

圖3
A.a為直流電源的負極
D.電解時,H+由陰極室通過陽離子交換膜到陽極室
5.化學平衡狀態 Ⅰ、Ⅱ、Ⅲ的相關數據如表2。

表2
根據以上信息判斷,下列結論錯誤的是( )。
A.a>b
B.增大壓強,平衡狀態Ⅱ不移動
C.升高溫度平衡狀態Ⅲ向正反應方向移動
D.反應Ⅱ、Ⅲ均為放熱反應
6.假設圖4中原電池產生的電壓、電流均能滿足電解、電鍍要求,即為理想化。①~⑧為各裝置中的電極編號。下列說法錯誤的是( )。
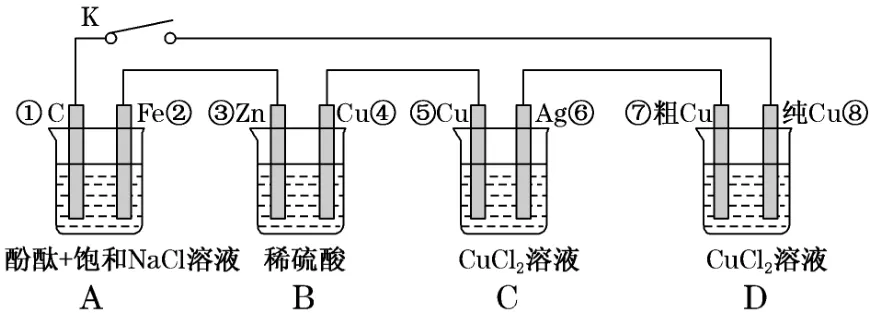
圖4
A.當K閉合時,A裝置發生吸氧腐蝕,在電路中作電源
B.當K斷開時,B裝置鋅片溶解,有氫氣產生
C.當K閉合后,整個電路中電子的流動方向為①→⑧;⑦→⑥;⑤→④;③→②
D.當K閉合后,A、B裝置中pH變大,C裝置中pH不變
7.白磷與氧可發生反應P4+5O2==P4O10。已知斷裂下列化學鍵需要吸收的能量:P—P為akJ·mol-1,P—O 為bkJ·mol-1,為dkJ·mol-1。根據圖5所示的分子結構和有關數據估算該反應的ΔH,其中正確的是( )。

圖5
A.(6a+5d-4c-12b)kJ·mol-1
B.(4c+12b-6a-5d)kJ·mol-1
C.4c+12b-4a-5d)kJ·mol-1
D.(4a+5d-4c-12b)kJ·mol-1
8.已知25℃時有關弱酸的電離平衡常數如表3。

表3
下列有關說法正確的是( )。
A.等物質的量濃度的各溶液pH關系為pH(Na2S)>pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)>pH(NaHCO3)
B.NaHCO3和Na2CO3混合溶液中,一定有
C.pH相等的NaF與CH3COOK溶液中:[c(Na+)-c(F-)]<[c(K+)-c(CH3COO-)]
D.等濃度的①CH3COONH4、②NH4F、③(NH4)2CO3、④NH4HCO3溶液中的③>②>①>④
9.常溫下,向10mL0.1mol·L-1的HR溶液中逐滴滴入0.1mol·L-1的NH3·H2O溶液,所得溶液pH及導電性變化如圖6。下列分析不正確的是( )。

圖6
A.a~b導電能力增強,說明HR為弱酸
B.b點溶液pH=7,說明NH4R沒有水解
C.c點溶液中存在c(NH4)>c(R-),c(OH-)>c(H+)
D.b~c任意點溶液均有c(H+)×c(OH-)=Kw=1.0×10-14
10.堿性硼化釩(VB2)—空氣電池工作時反應為4VB2+11O2==4B2O3+2V2O5。用該電池為電源,選用惰性電極電解硫酸銅溶液,實驗裝置如圖7所示。當外電路中通過0.04mol電子時,B裝置內共收集到0.448L氣體(標準狀況),則下列說法正確的是( )。
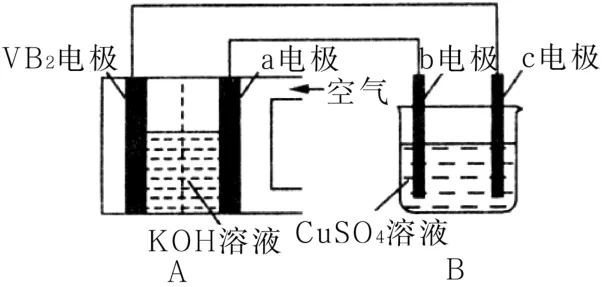
圖7
A.VB2電極發生的電極反應為2VB2+11H2O-22e-==V2O5+2B2O3+22H+
B.外電路中電子由c電極流向VB2電極
C.電解過程中,c電極表面先有紅色物質析出,后有氣泡產生
D.若B裝置內的液體體積為100mL,則CuSO4溶液的物質的量濃度為0.05mol·L-1
11.用CH4催化還原NOx可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ·mol-1
下列說法不正確的是( )。
A.由反應①可推知:CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(l) ΔH=-Q,Q>574kJ·mol-1
B.等物質的量的甲烷分別參加反應①②,反應轉移的電子數不同
C.若用標準狀況下4.48LCH4還原NO2至N2,則放出的熱量為173.4kJ
D.若用標準狀況下4.48LCH4還原NO2至N2,則整個過程中轉移的電子總物質的量為1.6mol
12.常溫下,向20mL0.2mol·L-1H2A溶液中滴加0.2mol·L-1NaOH溶液。有關微粒的物質的量變化如圖8(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。下列說法不正確的是( )。
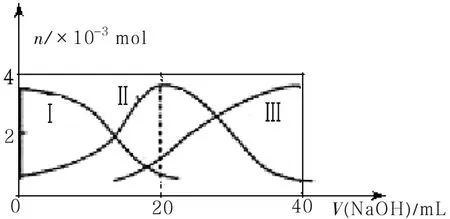
圖8
A.當V(NaOH)=20mL時,溶液中離子濃度大小關系:c(Na+)>c(HA?)>c(H+)>c(A2-)>c(OH?)
B.等體積等濃度的NaOH溶液與H2A溶液混合后,其溶液中水的電離程度比純水的小
C.NaHA溶液中:c(OH-)+c(A2-)=c(H+)+c(H2A)
D.向Na2A溶液加入水的過程中,pH可能增大也可能減小
13.甲醇是基礎有機化工原料和新型清潔燃料,廣泛用于制造各種燃料電池。工業上以甲烷和水蒸氣為原料制備甲醇,反應過程如下。
反應Ⅰ:CH4(g)+H2O(g)?CO(g)+3H2(g) ΔH1
反應 Ⅱ:CO(g)+2H2(g)?CH3OH(g) ΔH2
(1)圖9是反應Ⅰ進行過程中的能量變化示意圖。根據圖像判斷,升高溫度,反應Ⅰ的平衡常數將____(填“增大”“減小”或“不變”)。反應Ⅰ的逆反應的活化能為____(用含E1、E2的表達式表示)。
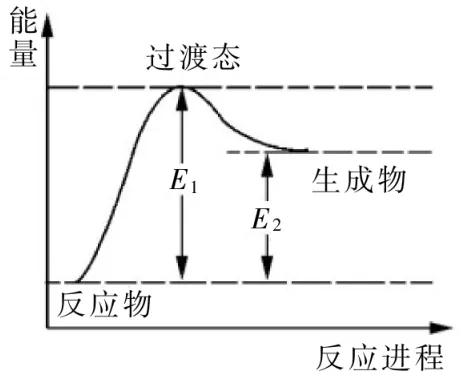
圖9
(2)已知在催化劑和一定壓強下,反應Ⅱ能自發進行。若保持容器容積不變,下列措施可增加該反應中CO轉化率的是____(填字母)。
A.適當降低溫度
B.將甲醇從反應體系中分離出來
C.充入He,使體系總壓強增大
D.按原比例再充入CO和H2
(3)一種甲醇燃料電池以多孔石墨為電極,一極通入甲醇蒸氣,另一極通入氧氣,電解質溶液為4L1mol·L-1的KOH溶液。當有3mol甲醇放電時,電解質溶液中各種離子的濃度由大到小的順序為____。
(4)圖10甲是一種甲醇燃料電池的結構示意圖,甲醇提供質子和電子,電子經外電路、質子經內電路到達另一極與氧氣反應,電池總反應為2CH3OH+3O2==2CO2+4H2O。
①M電極的電極反應式為____。
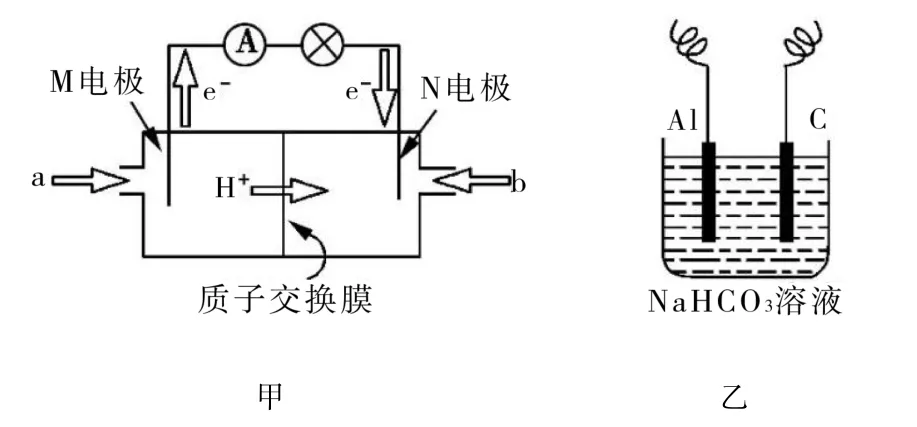
圖10
②以上述電池做電源,用圖10乙所示裝置,在實驗室中模擬鋁制品表面“鈍化”處理的過程,發現Al電極附近逐漸變渾濁并有氣泡逸出,原因是(用離子方程式表示)____。Al電極應接燃料電池的____(填“M”或“N”)極。
14.工業上可以從冶煉鋅、鋅制品加工企業回收的廢渣 (含有 ZnCO3、ZnO、FeO、Fe2O3、CuO、Al2O3)來提取氧化鋅和金屬銅等,其主要工藝流程如下所示。

有關氫氧化物開始沉淀和沉淀完全的pH如表4。

表4
(1)向酸浸液中加入的試劑A有多種選擇,若 A是 H2O2,反應的離子方程式是____。
(2)若試劑A為KOH稀溶液,當滴加至Cu2+恰好完全沉淀時,則濾液甲中
(已知:Ksp(Fe(OH)2)=8.0×10-16,Ksp(Cu(OH)2)=2.2×10-20)
(3)當酸浸液的pH用____(填試劑的化學式)調節到3.7至5.2時,可以使兩種離子完全沉淀,寫出其中任意一種沉淀反應的離子方程式:____。
(4)檢驗沉淀丙是否洗滌干凈,操作方法是____,在實驗室進行焙燒時,盛放沉淀丙的儀器名稱是____。
(5)上述流程中所得ZnO產品中鋅的含量遠超過鋅渣中鋅元素的含量,其原因是____。
15.磷灰石是生產磷肥的原料,它的組成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析結果如表5(各元素均以氧化物形式表示)。
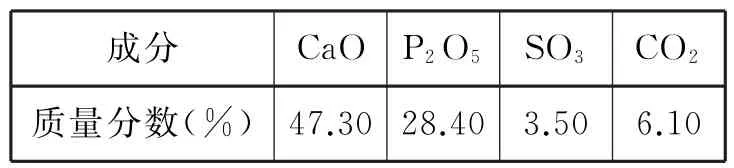
表5
磷及部分重要化合物的相互轉化如圖11所示。

圖11
(1)①步驟Ⅰ為白磷的工業生產方法之一,反應在1300℃的高溫爐中進行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是____。
②不慎將白磷沾到皮膚上,可用0.2mol·L-1CuSO4溶液沖洗,根據步驟Ⅱ可判斷,1molCuSO4所能氧化的白磷的物質的量為____。
(2)步驟Ⅲ中,反應物的比例不同可獲得不同的產物,除Ca3(PO4)2外可能的產物還有____。
(3)磷灰石中,碳元素的質量分數為____%(保留兩位小數)。
(4)取100g磷灰石粉末,加入足量的濃硫酸,并加熱,鈣元素全部以CaSO4的形式存在,可以得到(保留兩位小數)。
(5)取mg磷灰石粉末,用50.00mL混酸溶液(磷酸為0.5mol·L-1、硫酸為0.1mol·L-1)與其反應,結果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值:___。
Ⅰ.該小組為確定一份加碘鹽(可能含有KIO3、KI、Mg2+、Fe3+)的成分,設計定性實驗加以猜想和驗證。
(1)實驗過程如下。

表6
(2)該碘鹽中肯定不含的物質是____(用化學式或離子符號表達)。
(4)第③份試液中加入足量KI固體后,反應的離子方程式為____,____。
Ⅱ.用“間接碘量法”測定含有CuCl2·2H2O晶體的試樣(不含能與I-發生反應的氧化性雜質)的純度,過程如下:
取0.40g試樣溶于水,加入過量KI固體,充分反應,生成白色沉淀。加入淀粉作滴定指示劑,用0.1000mol·L-1Na2S2O3標準溶液滴定,到達滴定終點時,消耗Na2S2O3標準溶液20.00mL。
(1)滴定終點的現象是____。
(2)CuCl2溶液與KI反應的化學方程式為____。
(3)該試樣中CuCl2·2H2O的質量分數為____。的

