化學反應及能量轉化易錯問題剖析
■河南省鄲城縣第一高級中學 趙艷梅
化學反應與能量轉化是化學熱力學與動力學知識的綜合,是每年高考必考內容,既有基礎性試題,也有綜合性問題,基礎知識不扎實的同學在處理這類問題時,常常會出現一些不應有的錯誤。下面就其常見的一些易錯題型歸類分析如下,供學習時借鑒參考。
易錯點一:準確理解概念
例1 下列熱化學方程式中ΔH能正確表示物質的燃燒熱或中和熱的是( )。
B.KOH(aq)+HAc(aq)==KAc(aq)+H2O(l) ΔH=-57.3kJ·mol-1
C.C8H18(l)+12.5O2(g)==8CO2(g)+9H2O(l) ΔH=-5518kJ·mol-1
D.CH4(g)+2O2(g)==CO2(g)+2H2O(g) ΔH=-533kJ·mol-1
錯因分析:本題主要是考查燃燒熱、中和熱等概念,有的同學對這些概念理解不準確,對關鍵字詞把握不到位,導致錯選。
解析:反應熱化學方程式中生成的是2mol水,生成硫酸鋇沉淀也放熱,反應的中和熱不是57.3kJ·mol-1,故A項錯誤;HAc是弱酸,電離時要吸熱,反應的中和熱不是57.3kJ·mol-1,故B項錯誤;符合燃燒熱的概念,可燃物為1mol,產物為穩定氧化物,故C項正確;反應熱化學方程式中生成的水是氣體,不是穩定氧化物,故D項錯誤。
答案:C
誤區警示:準確理解概念是正確答題的基礎。像燃燒熱、中和熱、焓變、熱化學方程式等都是化學反應與能量變化知識考查中常遇到的基本概念,掌握其內涵與外延關系及注意事項,才能準確解題。
糾錯鞏固1:如果向足量Ba(OH)2溶液中加入100mL0.4mol·L-1HCl溶液時,放出的熱量為2.292kJ。則Na2SO4溶液與BaCl2溶液反應的熱化學方程式及中和熱的有關敘述中正確的是 ( )。
A.中和熱ΔH=-57.3kJ·mol-1
B.稀的強酸與強堿反應的中和熱為ΔH=-128kJ·mol-1
D.在溶液中Ba2+與SO2-4生成1mol BaSO4時會放出13.4kJ的能量
答案:D
易錯點二:熱化學方程式的書寫
例2(1)真空碳熱還原—氯化法可實現由鋁土礦制備金屬鋁,其相關反應的熱化學方程式如下:
Al2O3(s)+AlC13(g)+3C(s)==3AlCl(g)+3CO(g) ΔH=akJ·mol-1
3AlCl(g)==2Al(l)+AlC13(g) ΔH=bkJ·mol-1
試寫出反應Al2O3(s)與C(s)反應生成Al(l)和CO(g)的熱化學方程式:____。
(2)0.3mol氣態高能燃料乙硼烷(B2H6)在O2中燃燒,生成固態的B2O3和液態水,放出649.5kJ熱量,其熱化學方程式為____。又已知:H2O(l)==H2O(g) ΔH=+44kJ·mol–1,則11.2L(標準狀況)乙硼烷完全燃燒生成氣態水時放出的熱量是____kJ。
錯因分析:對于這類問題,常見的錯誤形式有:不標明或標錯物質的狀態(特別是水)、ΔH的單位或正負號出錯,不注意量的關系等。
解析:(1)根據蓋斯定律,將所給熱化學方程式相加即可。
(2)先寫出乙硼烷燃燒的化學方程式,找出乙硼烷的物質的量與ΔH之間的關系,并算出ΔH,再按照熱化學方程式書寫要求寫出其結果。先寫出乙硼烷完全燃燒生成氣態水時的熱化學方程式B2H6(g)+3O2(g)==B2O3(s)+3H2O(g) ΔH=-2033kJ·mol-1,再計算0.5mol乙硼烷燃燒放出的熱量。
答案:(1)Al2O3(s)+3C(s)==2Al(l)+3CO(g) ΔH=(a+b)kJ·mol-1(2)B2H6(g)+3O2(g)==B2O3(s)+3H2O(l)ΔH=-2165kJ·mol-11016.5kJ
誤區警示:書寫熱化學方程式的依據形式很多,如依據化學計算、圖像圖表、蓋斯定律、限定信息等,因此,書寫熱化學方程式時,一要注意解題依據,二要遵循熱化學方程式書寫的基本要求,合理書寫。
糾錯鞏固2:(1)天旱時,可用單級小火箭發射碘化銀進行人工降雨,小火箭使用的主要燃料是偏二甲肼(C2H8N2)。現取6.0gC2H8N2(l)在O2中充分燃燒后生成8.8gCO2、7.2g H2O(g)和2.8gN2,同時放出熱量QkJ,寫出C2H8N2燃燒的熱化學方程式:___。
(2)25℃、101kPa條件下充分燃燒一定量的丁烷氣體放出熱量為QkJ,經測定,將生成的CO2通入足量澄清石灰水中產生25g白色沉淀,寫出表示丁烷燃燒熱的熱化學方程式:___。
答案:(1)C2H8N2(l)+4O2(g)==2CO2(g)+4H2O(g)+N2(g) ΔH===4CO2(g)+5H2O(l) ΔH=-16QkJ·mol-1
易錯點三:忽略物質的聚集狀態
例3已知H2(g)+Br2(l)==2HBr(g) ΔH=-72kJ·mol-1,蒸發1molBr2(l)需要吸收的能量為30kJ,其他的相關數據如表1。

表1
則表中a為( )。
A.404 B.260 C.230 D.200
錯因分析:根據反應熱概念,可列式:ΔH=436kJ·mol-1+akJ·mol-1-2×369kJ·mol-1=-72kJ·mol-1,計算得a=230,故選C項。該計算未考慮到題給熱化學方程式中Br2呈液態,而表格中Br2呈氣態,其間是存在能量差異的。
解析:根據題意可以寫出Br2(l)轉化為溴蒸氣時的熱化學方程式:Br2(l)==Br2(g) ΔH=+30kJ·mol-1,這樣可得:H2(g)+Br2(g)==2HBr(g) ΔH=-102kJ·mol-1;再根據ΔH=436kJ · mol-1+akJ·mol-1-2 ×369kJ·mol-1=-102kJ·mol-1,計算得a=200。
答案:D
誤區警示:物質狀態不同時,化學反應的熱效應是不同的,因此,反應熱計算或依據計算書寫熱化學方程式時,都要注意物質的聚集狀態,尤其是寫熱化學方程式時,一定不能忽略物質的聚集狀態。如CH4燃燒生成氣態水和生成液態水,其ΔH是不同的。
糾錯鞏固3:已知乙烯和乙炔燃燒的熱化學方程式分別為:
2C2H2(g)+5O2(g)==4CO2(g)+2H2O(l) ΔH=-2600kJ·mol-1
C2H4(g)+3O2(g)==2CO2(g)+2H2O(l) ΔH=-1411kJ·mol-1
又知燃燒時乙炔比乙烯的火焰溫度高。據此,下列說法錯誤的是( )。
A.物質的燃燒熱越大,火焰溫度越高
B.烴完全燃燒時,火焰溫度的高低不僅僅取決于其燃燒熱的高低
C.相同條件下等體積乙烯和乙炔完全燃燒時,乙炔放熱較少
D.1mol乙烯完全燃燒生成氣態產物時,放出的熱量小于1411kJ
答案:A
易錯點四:不清楚物質結構
例4已知H—H鍵能為436kJ·mol-1,H—N鍵能為391kJ·mol-1,根據熱化學方程式-92.4kJ·mol-1,則N≡N鍵的鍵能為( )。
A.431kJ·mol-1B.945.6kJ·mol-1
C.618.4kJ·mol-1D.649kJ·mol-1
錯因分析:根據ΔH=反應物的鍵能之和-生成物的鍵能之和,可求得:ΔH=E(N≡N)+3 × 436kJ· mol-1-2 ×391kJ·mol-1=-92.4kJ·mol-1,則E(N≡N)=-618.4kJ·mol-1,選C項。上述計算結果錯誤,主要是對NH3的結構未理解清楚,這樣導致其共價鍵數目未確定準。
解析:依據鍵能計算化學反應熱時,一要弄清楚物質的結構情況,知道每摩爾物質中所含共價鍵的數目;二要理解ΔH計算式的列式依據,即化學反應中斷鍵是吸熱過程,成鍵是放熱過程,因此,-92.4kJ·mol-1=E(N≡N)+3×436kJ·mol-1-2×3×391kJ·mol-1,解得:E(N≡N)=945.6kJ·mol-1。
答案:B
誤區警示:依據鍵能計算反應熱時,除把握準計算公式外,還要弄清有關物質中的共價鍵數目,如本題中,一個分子中含3個H—N鍵。其他如CH4、P4、PCl5、S8、晶體Si、SiO2晶體等物質中的共價鍵情況也要弄清楚。
糾錯鞏固4.已知圖1中E1=134kJ·mol-1,E2=368kJ·mol-1,根據要求回答問題:

圖1
(1)圖1是1molNO2(g)和1molCO(g)反應生成CO2和NO過程中的能量變化示意圖,若在反應體系中加入催化劑,反應速率增大,E1的變化是____(填“增大”“減小”或“不變”,下同),ΔH的變化是____。請寫出NO2和CO反應的熱化學方程式:___。
(2)甲醇質子交換膜燃料電池中將甲醇蒸氣轉化為氫氣的兩種反應的熱化學方程式如下:
①CH3OH(g)+H2O(g)==CO2(g)+3H2(g) ΔH=+49.0kJ·mol-1
又知③H2O(g)==H2O(l) ΔH=-44kJ·mol-1,則甲醇蒸氣燃燒為液態水的熱化學方程式為____。
(3)表2所示為部分化學鍵的鍵能參數。
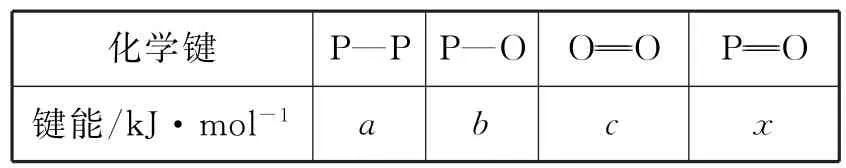
表2
已知白磷的燃燒熱為dkJ·mol-1,白磷及其完全燃燒的產物的結構如圖2所示,則表中x=____kJ·mol-1(用含a、b、c、d的代數式表示)。

圖2
答案:(1)減小 不變 NO2(g)+CO(g)==CO2(g)+NO(g) ΔH=-234kJ·mol-1
易錯點五:對圖示觀察不力
例5圖3是乙烷、二甲醚燃燒過程的能量變化圖,請回答下列問題:

圖3
(1)乙烷的燃燒熱ΔH=____kJ·mol-1。
(2)根據圖3寫出二甲醚燃燒熱的熱化學方程式:____。
錯因分析:常見錯誤答案為(1)
(2)aCH3OCH3(g)+cO2(g)==dCO2(g)+H2O(l) ΔH=-485kJ·mol-1。主要問題是對圖示觀察不仔細,其實,根據圖示信息是可以知道a、c、d的值的。
解析:根據圖示,生成物H2O前的計量數為1,根據元素守恒可知,則圖示中兩種物質燃燒的熱化學方程式分別為:
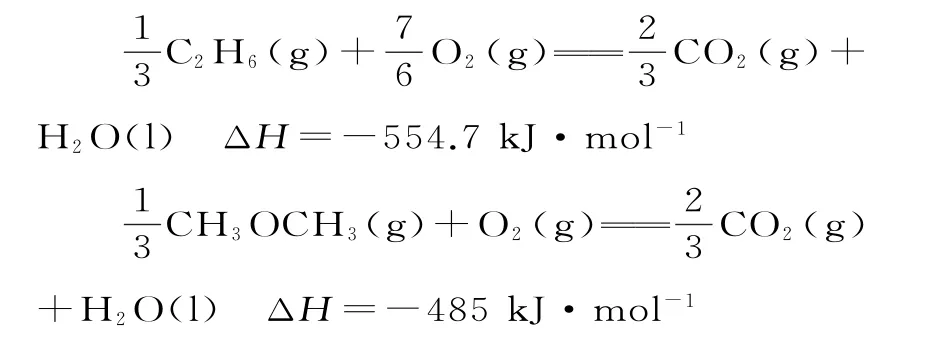
再根據燃燒熱定義,可知乙烷的燃燒熱ΔH=-1664.1kJ·mol-1;二甲醚燃燒熱的熱化學方程式為CH3OCH3(g)+3O2(g)==2CO2(g)+3H2O(l) ΔH=-1455kJ·mol-1。
答案:(1)1664.1
(2)CH3OCH3(g)+3O2(g)==2CO2(g)+3H2O(l) ΔH=-1455kJ·mol-1。
誤區警示:處理圖像問題時,除要弄懂點、線、面的意義外,還要注意圖示中其他的一些信息,如數據、符號、字母等提示內容,從中找到對解題有幫助的東西;另外還要注意反應物和生成物的能量高低,以確定反應是吸熱還是放熱。
糾錯鞏固5:(1)20世紀30年代,Eyring和Pelzer在碰撞理論的基礎上提出化學反應的過渡態理論:化學反應并不是通過簡單的碰撞就能完成的,而是在反應物到生成物的過程中經過一個高能量過渡態。圖4是NO2和CO反應生成CO2和NO過程中能量變化示意圖,請寫出NO2和CO反應的熱化學方程式:___。
(2)紅磷P(s)和Cl2(g)發生反應生成PCl3(g)和PCl5(g)。反應過程和能量關系如圖5所示(圖中的ΔH表示生成1mol產物的數據)。回答下列問題:
①P和Cl2反應生成PCl3的熱化學方程式為____。
②PCl5分解成PCl3和Cl2的熱化學方程式是____。

圖4

圖5
(3)科學家利用太陽能分解水生成氫氣,再用氫氣與二氧化碳在催化劑作用下反應生成甲醇,并開發出直接以甲醇(CH3OH)為燃料的燃料電池。已知:
請回答下列問題:
液態甲醇不完全燃燒生成一氧化碳氣體和液態水的熱化學方程式為____。
答案:(1)NO2(g)+CO(g)==CO2(g)+NO(g) ΔH=-234kJ·mol-1
(3)CH3OH(l)+O2(g)==CO(g)+2H2O(l) ΔH=-443.5kJ·mol-1

