運(yùn)用二力平衡原理 解析滲透裝置的相關(guān)問(wèn)題
徐宏偉 (浙江省海亮高級(jí)中學(xué) 浙江紹興 311800)
1 滲透裝置
1.1 滲透
擴(kuò)散是分子或離子從高濃度處向低濃度處運(yùn)動(dòng)的現(xiàn)象。水分子通過(guò)膜的擴(kuò)散稱為滲透。通過(guò)兩者的概念分析,可知滲透要發(fā)生需要符合兩個(gè)條件:①具有一層半透膜;②這層半透膜兩側(cè)的溶液具有濃度差。
1.2 滲透裝置
演示滲透現(xiàn)象的實(shí)驗(yàn)裝置簡(jiǎn)稱為滲透裝置(圖1),一般由球形漏斗、燒杯、半透膜和球形漏斗內(nèi)外不同的溶液組成。為了使實(shí)驗(yàn)現(xiàn)象比較明顯,一般情況下溶液a溶質(zhì)物質(zhì)的量濃度大于溶液A溶質(zhì)物質(zhì)的量濃度(溶劑分子都為水),且溶質(zhì)分子不能穿過(guò)半透膜。故一段時(shí)間之后即如圖1右側(cè)圖像所示,漏斗內(nèi)液面上升。
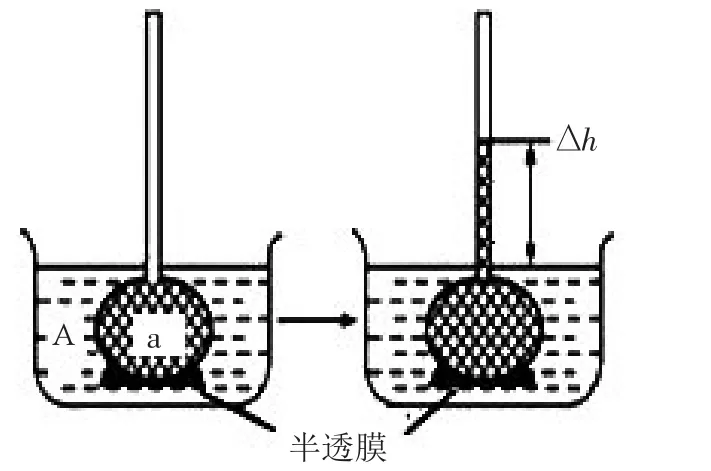
圖1 滲透作用示意圖
2 滲透裝置的力學(xué)分析
若從微觀上來(lái)分析半透膜兩側(cè)水分子的進(jìn)出,學(xué)生可以判斷出漏斗內(nèi)液面上升的趨勢(shì)。但當(dāng)液面不再發(fā)生變化,即達(dá)到滲透平衡時(shí),如何來(lái)判斷內(nèi)外溶液的溶質(zhì)物質(zhì)的量濃度大小,學(xué)生就比較難以理解。教師可以以半透膜兩側(cè)的液面為對(duì)象,進(jìn)行宏觀上的力學(xué)分析。在垂直方向上半透膜兩側(cè)的液面除了受到相等重力和支持力之外,還受到半透膜兩側(cè)溶質(zhì)的物質(zhì)的量濃度差產(chǎn)生的滲透壓力和由液面高度差產(chǎn)生的靜壓力。滲透壓力促使水分子從溶質(zhì)物質(zhì)的量濃度低的一側(cè)跨膜擴(kuò)散至溶質(zhì)物質(zhì)的量濃度高的一側(cè),靜壓力則促使水分子從液面高的一側(cè)跨膜擴(kuò)散至液面低的一側(cè)。
2.1 滲透壓力
溶液滲透壓,簡(jiǎn)單的說(shuō),是指溶液中溶質(zhì)微粒對(duì)水的吸引力,其本質(zhì)是一種壓強(qiáng)。1886年,荷蘭理論化學(xué)家范托夫從理論上推導(dǎo)出溶液的滲透壓力與溶液濃度和熱力學(xué)溫度的關(guān)系為:π=cRT(其中π是滲透壓,c為溶質(zhì)的物質(zhì)的量濃度,R為氣體常數(shù),T為熱力學(xué)溫度)。溶液滲透壓力F=πs(s為半透膜面積),將π=cRT代入即得到滲透壓力F=cRTs。半透膜兩側(cè)滲透壓力F的差值與溶質(zhì)物質(zhì)的量濃度差相關(guān),簡(jiǎn)單地表示為FΔc,方向是由溶質(zhì)物質(zhì)的量濃度較低一側(cè)指向溶質(zhì)物質(zhì)的量濃度較高一側(cè)。
2.2 靜壓力
靜壓力F,是由于液面高度差所導(dǎo)致的,其可表示為靜壓力F=ρghs(ρ為溶液密度,g重力加速度,h液面高度,s為半透膜面積)。半透膜兩側(cè)靜壓力F的差值與液面高度差相關(guān),簡(jiǎn)單得表示為FΔh,其方向是由液柱高度較高的一側(cè)指向液面較低的一側(cè)。
2.3 液面變化及平衡后濃度差分析
由于溶質(zhì)分子不能穿過(guò)半透膜,開(kāi)始時(shí)溶液a溶質(zhì)物質(zhì)的量濃度大于溶液A溶質(zhì)物質(zhì)的量濃度,即滲透壓力Fa大于FA,即存在FΔc,其方向從溶液A向溶液a,而此時(shí)兩液面高度差為0,即靜壓力FΔh=0,所以半透膜兩側(cè)水分子只受到了方向向上的滲透壓力F的作用。因此水分子總體上表現(xiàn)為從溶質(zhì)物質(zhì)的量濃度較低溶液A跨膜擴(kuò)散至溶質(zhì)物質(zhì)的量濃度較高溶液a,從而引起漏斗液面上升。
隨著水分子由溶液A不斷地跨膜擴(kuò)散至溶液a,即由燒杯向漏斗擴(kuò)散,引起燒杯內(nèi)溶液A溶質(zhì)物質(zhì)的量濃度逐漸上升,而漏斗內(nèi)溶液a溶質(zhì)物質(zhì)的量濃度逐漸下降,因而方向向上的滲透壓力FΔc逐漸變小。而漏斗內(nèi)液面的逐漸升高,使得漏斗和燒杯液面高度差逐漸變大,引起方向向下的靜壓力FΔh逐漸變大,當(dāng)二力平衡即FΔc=FΔh時(shí),出現(xiàn)理論上的液面靜止的滲透平衡現(xiàn)象,即圖1右側(cè)圖像所示。由FΔc=FΔh很容易分析得到當(dāng)滲透平衡時(shí),溶液a的溶質(zhì)物質(zhì)的量濃度依然大于溶液A的溶質(zhì)物質(zhì)的量濃度。
3 例析
圖2表示滲透作用裝置圖,其中半透膜為膀朧膜(蔗糖分子不能通過(guò),水分子可以自由通過(guò))。圖中溶液A、B、a、b均為蔗糖溶液,其物質(zhì)的量濃度分別用MA、MB、Ma、Mb表示,且MA>MB,Ma=Mb>MA。一段時(shí)間達(dá)到平衡后,甲裝置、乙裝置液面上升的高度分別為h1、h2,溶液a、b的物質(zhì)的量濃度分別為M1、M2,則( )
A.hl>h2,M1<M2B.hl<h2,M1=M2
C.hl>h2,Ml>M2D.hl<h2,Ml>M2
解析:由題可知Ma=Mb>MA>MB,即漏斗內(nèi)蔗糖溶液溶質(zhì)的物質(zhì)的量溶度大于燒杯內(nèi),且甲裝置的溶質(zhì)物質(zhì)的量濃度差小于乙裝置的溶質(zhì)物質(zhì)的量濃度差,即甲裝置的FΔc小于乙裝置FΔc,所以乙裝置漏斗內(nèi)水分子進(jìn)入的多,液面上升的高,即hl<h2。達(dá)到滲透平衡后,根據(jù)FΔc=FΔh,由于甲裝置高度差Δh較小,其Δc也較小,即Ma改變較小,同理Mb改變較大,所以Ml>M2。

圖2 滲透作用裝置圖
4 小結(jié)
通過(guò)力學(xué)分析,應(yīng)用學(xué)生較熟悉的二力平衡原理,將原本一個(gè)比較抽象的問(wèn)題具體化,用定量分析的方法,能夠讓學(xué)生很好地理解滲透裝置液面變化的原因,并且進(jìn)行滲透平衡后半透膜兩側(cè)溶液溶質(zhì)的物質(zhì)的量大小的比較。
- 中學(xué)生物學(xué)的其它文章
- 基于知識(shí)自主構(gòu)建的生物教學(xué)嘗試
——以“減數(shù)分裂基本概念分析”為例 - 落實(shí)生物學(xué)科核心素養(yǎng)應(yīng)處理好三種關(guān)系
- 優(yōu)化課外作業(yè)設(shè)計(jì) 引導(dǎo)學(xué)生學(xué)會(huì)學(xué)習(xí)
——珠海市高中生物課外作業(yè)現(xiàn)狀調(diào)查 - 透過(guò)2018高考理綜全國(guó)卷Ⅰ談2019復(fù)習(xí)啟示
- 變量分析法在高中生物實(shí)驗(yàn)試題求解中的應(yīng)用
- 基于學(xué)科核心素養(yǎng)培養(yǎng)下的“酶專題”復(fù)習(xí)例析

