連續中毒劑量維生素D3對大鼠腎組織結構的影響※
維生素D3(Vitamin D3, VD3)的經典生物學作用是調節鈣磷平衡,維持骨骼健康[1]。VD3中毒常因使用不當,或在治療佝僂病過程中反復大量使用VD3所致[2]。腎臟是 VD3代謝的重要器官,有學者指出VD3是預測多種慢性腎臟疾病進展的獨立危險因素[3]。腎損傷是不可逆轉的,組織病理切片和超微結構變化是揭示機體病理變化機制的重要手段之一,長期使用小劑量VD3時對腎小球組織結構的影響以增生為主[4]。中毒劑量 VD3造成腎損傷的研究報道較少。本研究通過觀察腎組織病理切片和超微結構變化,探討VD3對腎臟產生毒性的劑量,及不同劑量VD3對大鼠腎組織結構的影響程度,為研究VD3造成腎毒性的作用機制提供理論依據。
1 材料與方法
1.1 材料
1.1.1 實驗動物 健康 SD大鼠,雄雌各半,體重150~170 g,SPF級,購自河北醫科大學實驗動物中心,實驗動物生產許可證號:SCXK(冀)2008-1-003。飼養于山西省醫藥與生命科學研究院藥理研究室屏障動物房,實驗動物使用許可證號:SCXK(晉)2010-0005,適應性飼養1周后使用。
1.1.2 藥品與試劑 VD3注射液(上海通用藥業股份有限公司,批號:20170106,規格:7.5 mg:1 ml/支);甲醛(上海滬試實驗室器材股份有限公司,批號:20160523);無水乙醇(優級純GR);0.9%氯化鈉注射液(山東華魯制藥有限公司,批號:20170815)。另使用電子天平(北京賽多利斯儀器系統有限公司,型號:BT2202S)、病理切片機(德國徠卡,批號:TS6016+CV6030型)、光學顯微鏡Olympas HB-2。
1.2 方法
1.2.1 實驗分組 將40只健康SD大鼠隨機分為空白對照組(0 IU/kg)、VD3小劑量組(1875 IU/kg)、VD3中劑量組(3750 IU/kg)、VD3大劑量組(7500 IU/kg)、VD3超大劑量組(15 000 IU/kg),每組8只。
1.2.2 VD3配制 采用玉米油對維生素D3注射液進行等量遞增稀釋,分別配成所需濃度應用,每天在實驗前新鮮配制。
1.2.3 給藥方式、劑量和療程 采用常規灌胃方式給藥,給藥體積為0.5 ml/100 g,每天1次,連續3周。
1.3 觀察腎組織變化
1.3.1 大鼠腎組織病理學變化 采血后放血處死大鼠,剪開腹腔并取腎組織塊于10%甲醛內固定,24 h后換液,48 h后取材做石蠟包埋,做成4 μm厚切片,HE染色行光鏡檢查,觀察腎小球、腎小管上皮細胞形態結構并拍照記錄。
1.3.2 大鼠腎組織超微結構變化 取出單側腎置于培養皿中,滴入4%戊二醛磷酸緩沖液(pH7.2~7.4)充分浸潤,用雙面刀片將腎皮質部位組織修成小塊(1 mm3大小);吸取樣本放入加有4%戊二醛磷酸緩沖液(pH 7.3)小瓶內固定,標記后放入4℃冰箱中保存。標本固定24 h后采用0.1 mol/L磷酸緩沖液漂洗后,于4℃冰箱內梯度乙醇脫水,50%乙醇、70%乙醇、90%乙醇各15 min,再至90%乙醇和90%丙酮混合液脫水15 min,90%丙酮脫水15 min,再在100%丙酮室溫下脫水15 min,重復3次。采用環氧樹脂618包埋,做1 μm厚半薄切片,行甲苯胺藍染色,光學顯微鏡下定位,LKB-l型超薄切片機(瑞典Leica)切片,切片厚度為50 am,采用枸櫞酸鉛和醋酸雙氧鈾染色。日本日立H-7500 透射電子顯微鏡下觀察腎小球基底膜及足細胞足突形態學變化并拍照記錄。
2 結果
2.1 VD3對各組大鼠腎組織病理學的影響 HE染色結果顯示:與空白對照組相比,VD3各劑量組腎小管上皮組織細胞均發生了不同程度變化,主要表現為近曲腎小管上皮細胞腫脹、變性,以大劑量組最明顯。見圖1。
2.2 VD3對大鼠腎組織超微結構的影響 組織學電鏡超微結構檢測觀察顯示:空白對照組足突、基膜和毛細血管內皮細胞、窗孔結構無明顯異常,毛細血管管腔內透明;小劑量組基膜厚薄不均,毛細血管管腔內不透明,布滿顆粒狀物;中劑量組基膜增厚,毛細血管管腔內出現吞飲小泡;大劑量組足突部分融合,基膜增厚改變典型,內皮細胞分界不清;超大劑量組足細胞的足突和基膜、內皮細胞分界不清,融合在一起,兩側完整,出現內皮吞飲小泡,毛細血管管腔內有兩個大小不等的圓形均質體,細胞器結構清晰。見圖2。

圖1 腎組織病理學改變(HE 400X)
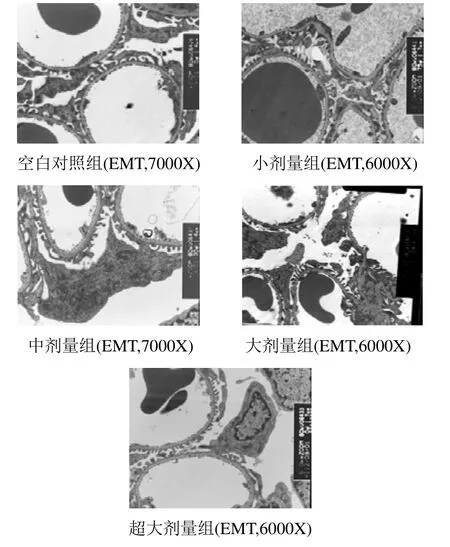
圖2 VD3對大鼠腎組織超微結構的影響
3 討論
隨著對 VD3研究的不斷深入,其臨床應用范圍不斷擴大,而 VD3的合理攝入量和安全性等問題需引起臨床高度重視。VD3攝入劑量過大、應用時間過長均可導致中毒。VD3在體內需經過兩次羥化后才能發揮其生物活性,第一次羥化在肝臟內,生成25-OH-D3,然后通過氧化反應,最終生成水溶性VD3-23羧酸,隨尿液排出[5];當機體攝入并蓄積過量VD3時,體內VD3自反饋調節作用失調,可導致血鈣升高[6],進而出現一系列繼發癥狀,臨床上嚴重的高鈣血癥可能影響腎臟、胃腸道、肌肉骨骼系統、眼睛和皮膚[7]。
目前,我國兒童(0~14歲)血清25-OH-D3水平正常參考值范圍為37.5~250.0 nmoL/L[8];有研究[9-10]報道,11例患者,每人平均誤食VD3為1308 IU,均出現臨床中毒癥狀,血鈣均增高至3.57~4.43 mmol/L,9例出現急性腎損傷,8例為急性腎功能衰竭。本研究中 VD3小劑量組(1875 IU/kg)、VD3中劑量組(3750 IU/kg)、VD3大劑量組(7500 IU/kg)、VD3超大劑量組(15 000 IU/kg),4組給藥劑量經換算均高于臨床正常使用劑量,并大于引起腎損傷的劑量,故給藥后大鼠均可能會出現高鈣血癥。
本研究組織病理學檢測顯示:VD3各劑量組大鼠腎小管與空白對照組比較均發生了明顯變化,主要表現為近曲小管上皮細胞腫脹、變性,管腔變小,出現管型等變化,偶見間質增生,中性粒細胞、巨噬細胞等炎癥細胞浸潤等,以大劑量組最明顯。提示使用VD3后造成的腎損傷主要以近曲腎小管上皮細胞損傷為主,以 7500 IU/kg劑量時最明顯。此現象是否與VD3主要是在腎小管上皮細胞轉化為1,25-(OH)2D3有關,有待進一步深入研究確證。
組織學電鏡超微結構檢測示:空白對照組大鼠腎小球組織結構清晰、完整。VD3各劑量組大鼠用藥3周后腎小球超微結構均發生了明顯變化,小劑量組基膜厚薄不均,毛細血管管腔內不透明,布滿顆粒狀物;中劑量組基膜增厚,毛細血管管腔內出現吞飲小泡;大劑量組足突部分融合,基膜增厚改變典型,內皮細胞分界不清;超大劑量組足細胞的足突和基膜、內皮細胞分界不清,融合在一起,兩側完整,出現內皮吞飲小泡,毛細血管管腔內有兩個大小不等的圓形均質體,細胞器結構清晰。表明中毒劑量VD3可造成腎小球毛細細胞內皮細胞、基膜、足細胞這三個主要過濾屏障系統超微結構發生明顯變化,破壞腎小球濾過功能,濾過功能發生異常,可能是其造成腎臟毒性的另一主要原因。雖然,電鏡顯示各劑量組超微結構特征有一定區別,但這種區別不能說明對腎臟的毒性改變呈劑量相關性,再增大劑量會不會導致更顯著變化,需進一步研究。因為藥物效應的強弱與其劑量大小并非簡單的線性相關關系,劑量-反應關系可表現為S形曲線,直線、雙曲線等。結合組織病理學檢查結果推斷,VD3對腎臟的毒性可以引起腎小管和腎小球功能損傷。
綜上所述,7500 IU/kg中毒劑量VD3可造成實驗大鼠明顯毒性反應,是建立實驗大鼠中毒模型的推薦劑量。

