氧化還原反應(yīng)規(guī)律及應(yīng)用
郭致明
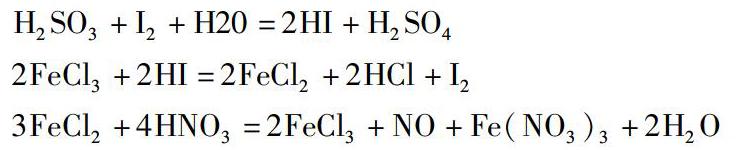
摘 要:化學(xué)作為高中階段的必修學(xué)科,在高考中占據(jù)著較大的考察比例。同時作為一名高中學(xué)生也必須要學(xué)習(xí)好化學(xué)這門學(xué)科。學(xué)習(xí)好化學(xué)學(xué)科必須掌握好氧化還原反應(yīng),可以說整個化學(xué)學(xué)科始終貫穿氧化還原反應(yīng)學(xué)習(xí),學(xué)習(xí)好氧化還原反應(yīng)是學(xué)習(xí)好其他知識的前提和基礎(chǔ)。氧化還原反應(yīng)有很多規(guī)律性可言,同時這些規(guī)律又是解答相關(guān)題目的依據(jù)。鑒于此,文章結(jié)合筆者自身的學(xué)習(xí)實際,總結(jié)了幾點氧化還原反應(yīng)的基本規(guī)律以及具體應(yīng)用。首先,明確了氧化還原的基本概念,然后分析了氧化還原反應(yīng)的基本規(guī)律及具體的應(yīng)用,希望對大家的化學(xué)學(xué)科學(xué)習(xí)有借鑒和幫助作用。
關(guān)鍵詞:高中化學(xué);氧化還原;規(guī)律;應(yīng)用
1.前言
氧化還原反應(yīng)屬于中學(xué)化學(xué)課堂的重要理論概念,貫穿中學(xué)化學(xué)學(xué)習(xí)的各個環(huán)節(jié),當(dāng)然也是化學(xué)學(xué)習(xí)的重難點。掌握好氧化還原的基本規(guī)律,同時在相關(guān)題目的解答中能夠高效應(yīng)用是關(guān)鍵。下面圍繞這一話題展開詳細(xì)的探討。
2.氧化還原反應(yīng)的基本概念
明確氧化還原反應(yīng)的基本規(guī)律以及具體規(guī)律的實際應(yīng)用。首先要了解的氧化還原反應(yīng)的基本概念。氧化還原反應(yīng)是化學(xué)反應(yīng)的基本反應(yīng)之一,氧化還原反應(yīng)的關(guān)鍵點在于氧化和還原。所謂氧化指的是物質(zhì)和氧化合的反應(yīng),而還原則指的是物質(zhì)失去氧的反應(yīng)。分析氧化還原反應(yīng)的本質(zhì)其實就是電子的得失或轉(zhuǎn)移。元素氧化數(shù)的變化正是由于電子得或者失去的結(jié)果,元素由于失去了電子,其氧化數(shù)升高了,就是氧化過程;而元素由于獲得了電子導(dǎo)致氧化數(shù)降低則是還原的過程。失去電子的物質(zhì)屬于還原劑,反之屬于氧化劑。
3.氧化還原反應(yīng)的基本規(guī)律和應(yīng)用
明確氧化還原反應(yīng)基本概念的前提下,我們再來總結(jié)幾點氧化還原反應(yīng)的基本規(guī)律。重點從守恒律,價態(tài)律,強弱率等幾點分析。
3.1守恒律及應(yīng)用
氧化還原中的守恒律指的是原子個數(shù)不能減少,得失電子剛剛好,也就是說氧化還原反應(yīng)發(fā)生后,反應(yīng)之前及反應(yīng)之后的原子,無論是數(shù)量還是類別都是相同的。同時電子數(shù)量的得與失也都是相同的。應(yīng)用守恒律解答相關(guān)問題的時候,同學(xué)們需要仔細(xì)閱讀題目,結(jié)合題目所給出的條件信息,分析氧化還原反應(yīng)前后原子的類別,原子的數(shù)量,電子數(shù)以及電子得失情況,結(jié)合氧化還原反應(yīng)的守恒律,明確氧化劑電子的總數(shù)和還原劑的電子的總數(shù)是相同的,同時氧化劑化合價失去的數(shù)量其實和還原劑化合價升高的數(shù)量也是相同的,也就是化學(xué)反應(yīng)前后電荷的具體數(shù)量相同,借助守恒律可以完成氧化還原反應(yīng)方程式的正確書寫,在檢驗化學(xué)反應(yīng)方程式配平的時候也可以利用守恒律,明確反應(yīng)式是否書寫正確,將具體的物質(zhì)的質(zhì)量求解出來。例如解答氧化還原反應(yīng)中反應(yīng)物的用量題目的時候。在特定條件下,PbO2與Cr3+件反應(yīng),產(chǎn)物是Cr2+和Pb,則與lmol Cr3+反應(yīng)所需PbO2的物質(zhì)的量是多少?分析題目大意,
PbO2和Cr3+反應(yīng),前者作為氧化劑,而后者則作為還原劑,PbO2得到兩個電子生成Pb2+,而Cr3+失去三個電子生成Cr2O72-,運用氧化還原反應(yīng)的守恒律能夠輕松得出問題的答案1mol×3e-=n(PbO2)×2e-,得出n(PbO2)=1.5mol,因此,題目的答案是1.5mol。再例如解答氧化還原反應(yīng)配平題目的時候,例如已知AgF+Cl2+H2O→AgCl+AgClO3+HF+O2,方程式配平之后Cl2的系數(shù)是a,那么求AgF的系數(shù)。已知AgCLO3的系數(shù)是b,O2的系數(shù)是c,那么AgCl的系數(shù)是?詳細(xì)分析題目發(fā)現(xiàn)在化學(xué)反應(yīng)方程式的右邊,是反應(yīng)的產(chǎn)物AgCl和AgClO3看出,銀元素的物質(zhì)的量和氯元素的物質(zhì)的量相同,已知Cl2的系數(shù)是a,那么可以輕松得出AgF的系數(shù)是2a。分析整合化學(xué)反應(yīng)的化合價的變化情況,發(fā)生化合價變化的是Cl和O。產(chǎn)生1molAgCl,AgClO3以及O2的時候,得失電子的數(shù)量是1mol,5mol,4mol已知AgCLO3系數(shù)是b,O2的系數(shù)是c,得出失去電子的總數(shù)是5b+4c,則AgCl的系數(shù)就是5b+4c。
3.2價態(tài)律及應(yīng)用
價態(tài)律也是氧化還原泛音的基本規(guī)律之一。價態(tài)律可以直接總結(jié)為高價氧,低價還,中間價態(tài)兩頭轉(zhuǎn)。意思就是在化學(xué)反應(yīng)中元素的原子處于最高價態(tài)的只能作為氧化劑存在,而位于最低價態(tài)的則只能作為還原劑所存在,中間價態(tài)的不僅可以做為氧化劑,同時還可以作為還原劑。例如:以下反應(yīng)中,必須將氧化劑加入到其中才可以完成的是()
A、 F2→F-B、 Fe→Fe2+C 、Cl2→ClO-D 、Na2O2→O2
在解答題目之前我們掌握了價態(tài)律,明白只有加入氧化劑才可以發(fā)生的反應(yīng)才可以成為氧化還原反應(yīng),基本特征就是元素的化合價相應(yīng)提升,因此A可以排除,而選項B中反應(yīng)物含有元素的化合價屬于最低價態(tài),只能做為還原劑,反應(yīng)中加入氧化劑,為此C、D中反應(yīng)物質(zhì)含有的元素都處于中間價態(tài),因此化合價不僅可以降低還可以升高,氧化還原反應(yīng)中可以同時作為氧化劑和還原劑,因此有可能不加入氧化劑也可以成立,所以選擇B。
3.3強弱率及應(yīng)用
強弱率簡單的歸納為一氧還對多還氧,強者占據(jù)先機(jī),就是如果在一個化學(xué)反應(yīng)中,一個氧化劑同時與多個還原劑發(fā)生反應(yīng),氧化劑計量不足的情況下,氧化劑與強還原劑發(fā)生反應(yīng),反之,多個氧化劑和一個還原劑發(fā)生反應(yīng)的時候,還原劑量不足,則與氧化性強的物質(zhì)發(fā)生反應(yīng),借助強弱率可以判斷物質(zhì)氧化性以及還原性的強弱。例如結(jié)合以下反應(yīng)判斷物質(zhì)還原性的強弱。
判斷相關(guān)物質(zhì)的還原性強弱,結(jié)合強弱率,還原劑的還原性始終比還原物的強,只需要識別反應(yīng)式中的還原劑和還原物就可以得出答案,即H2SO3>I->Fe2+>NO。
4.結(jié)語
綜上所述,氧化還原反應(yīng)作為中學(xué)化學(xué)學(xué)習(xí)的重點和難點,同學(xué)們一定要學(xué)習(xí)好這部分的內(nèi)容,深入掌握氧化還原的各種規(guī)律,并且學(xué)會用相關(guān)規(guī)律解決相關(guān)化學(xué)問題。
[參考文獻(xiàn)]
[1]錢三珍.氧化還原反應(yīng)規(guī)律[J].魅力中國,2014(21):254-254.
[2]王智友.氧化還原反應(yīng)規(guī)律剖析[J].教師,2009(6):92-93.
[3]張洪全.自制氧化還原反應(yīng)規(guī)律演示板[J].中學(xué)化學(xué)教學(xué)參考,2017(14):71-71.
[4]朱榮暉,張新中.氧化還原反應(yīng)的規(guī)律及其應(yīng)用[J].化學(xué)教學(xué),2010(10):72-75.
(作者單位:長沙市長郡濱江中學(xué),湖南 長沙 410000)

