Aurora-B介導NPM1蛋白磷酸化促進骨肉瘤細胞惡性表型的體外研究
皮聞森,劉家明,黃山虎,劉志禮
骨肉瘤(OS)是最常見的原發性惡性骨腫瘤,多發于兒童和青少年。雖然新輔助化療的出現使得原發患者的生存率有所提高(55%~80%),但發生肺部轉移的患者5年生存率仍低于20%,其中肺轉移是OS患者的主要死亡原因[1]。因此,闡明OS轉移的分子機制,可為OS轉移的防治提供有效的策略甚至靶點,對提高患者生存率非常必要。激光激酶-B(Aurora-B,又稱AURKB),是一種在多種惡性腫瘤中高表達的癌基因,與腫瘤發生、發展及轉移密切相關[2]。本研究采用骨肉瘤143B、U2-OS細胞株,結合生物信息學探討沉默Aurora-B介導NPM1蛋白磷酸化水平改變對骨肉瘤細胞遷移、侵襲和增殖能力的影響。
1 資料與方法
1.1 一般資料 人骨肉瘤細胞143B購自中國科學院上海細胞庫,Aurora-B沉默慢病毒(LV/ShAurora-B)、NPM1過表達慢病毒(LV/NPM1)和陰性對照慢病毒(LV/negative)購自上海吉凱基因。DMEM培養液和胎牛血清購自美國Gibco公司。總蛋白提取試劑盒(BB-3101)購自BestBio公司。凝膠制備試劑盒(AR018)購自于BOSTER公司。Aurora-B、NPM1(nucleophosmin1)和磷酸化NPM1ser125單克隆抗體(兔抗人)購自美國Abcam公司。β-actin單克隆抗體(鼠抗人)、辣根過氧化物酶(HRP)標記山羊抗兔多克隆抗體和HRP標記山羊抗鼠多克隆抗體購自北京中杉金橋公司。
1.2 方法
1.2.1 生物信息學預測 通過癌癥基因組圖譜(TCGA)數據庫(https://cancergenome.nih.gov/)查找NPM1在肉瘤中的表達水平以及預后情況;通過KinasePhos數據庫(http://kinasephos.mbc.nctu.edu.tw/)預測NPM1的磷酸化情況,預測AURKB與NPM1之間的關系。
1.2.2 細胞培養和慢病毒轉染 人骨肉瘤U2-OS細胞和143B細胞株用含15%胎牛血清的DMEM完全培養液培養,置于37℃、5%CO2的培養箱中培養。細胞分為LV/ShAurora-B組、NC(LV/negative)組、LV/ShAurora-B與LV/NPM1共轉染組。依據吉凱公司提供的轉染指南,分別轉染143B與U2-OS細胞,繼續培養72 h以后,用于后續實驗。
1.2.3 Western blot檢測Aurora-B、NPM1和pNPM1ser125蛋白表達 轉染后消化、收集Lv/ShAurora-B組和NC組的細胞,提取細胞蛋白后應用BCA蛋白定量法測定蛋白含量。SDSPAGE分離蛋白,于冰上濕轉,轉膜后置于含5%BSA的TBST中封閉2 h,加入Aurora-B(1∶5 000),NPM1(1∶2 000),磷酸化NPM1ser125(1∶2 000)和β-actin(1∶2 000)一抗,4℃孵育過夜,TBST振蕩洗膜10 min×3次,以封閉液稀釋的HRP標記的山羊抗小鼠及山羊抗兔IgG二抗(1∶5 000)室溫孵育1 h,TBST洗膜10 min×3次。于暗室中加入ECL顯色液曝光,采用Image J進行灰度分析。
1.2.4 Wound healing法檢測細胞遷移能力 取對數生長期的各組細胞,胰蛋白酶消化,以5×105個/mL細胞密度接種于6孔培養板,500μL/孔,常規孵育,直至細胞鋪滿,形成細胞單層。用200μL/移液器槍頭沿培養板底部呈“一”字型劃痕單層培養細胞,顯微鏡下(×200)觀察初始劃痕區并照相。吸取原有培養液,PBS清洗2次,去除被刮除的懸浮細胞,更換無血清的DMEM培養液,繼續培養24 h并拍照(×200)。Image J 1.47 H軟件計算細胞遷徙率[遷移率=(0 h的平均寬度-24 h的平均寬度)/0 h的平均寬度]。實驗平行做3次。
1.2.5 CCK-8法檢測細胞增殖能力 將轉染后的U2-OS和143B細胞(3 000個/孔)分別接種在96孔培養板中培養。48 h后每孔加入10μL的CCK-8溶液,并在37℃下再溫育2 h。用酶標儀測量在450 nm處光密度(OD)值。實驗平行做3次。
1.2.6 Transwell invasion法檢測細胞侵襲能力 將轉染48 h的各組U2-OS、143B細胞消化,用無血清培養基重懸,調整細胞密度為1×105個/mL,分別取150μL細胞懸液接種于小室內,將小室放入含10%FBS的培養液(600μL/孔)中繼續培養24 h。取出小室,吸棄上室液體,PBS漂洗2次,95%乙醇固定10 min,用棉簽擦凈小室膜上側未遷移的細胞。4 g/L結晶紫染色20 min,PBS漂洗2次。倒置顯微鏡下(×200)隨機讀取10個視野,觀察細胞穿膜情況并拍照。Image J 1.47 H軟件計算穿膜細胞數。
1.3 統計學方法 采用SPSS 17.0統計軟件對數據進行分析。符合正態分布的計量數據以均數±標準差(±s)表示,2組間比較采用t檢驗,多組間比較采用單因素方差分析,組間多重比較用LSD-t檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 生物信息學結果 通過TCGA數據庫發現,NPM1在肉瘤中高表達(圖1A),NPM1高表達的骨肉瘤患者預后較差(圖1B);通過KinasePhos數據庫庫發現,NPM1存在絲氨酸和蘇氨酸磷酸化位點(圖1C),而Aurora-B是絲氨酸和蘇氨酸激酶,因此Aurora-B與NPM1之間可能存在相互作用。
2.2 下調Aurora-B后檢測Aurora-B、NPM1和pNPM1ser125蛋白的表達情況 2種細胞中,與NC組相比,LV/ShAurora-B組Aurora-B和pNPM1ser125蛋白水平降低(P<0.05),而NPM1蛋白的變化差異無統計學意義,見表1、圖2。
Tab.1 Expressions of Aurora-B,NPM1 and pNPM1ser125 detected by Western blot assay表1 Western blot檢測Aurora-B、NPM1和pNPM1ser125蛋白的表達 (n=3,±s)
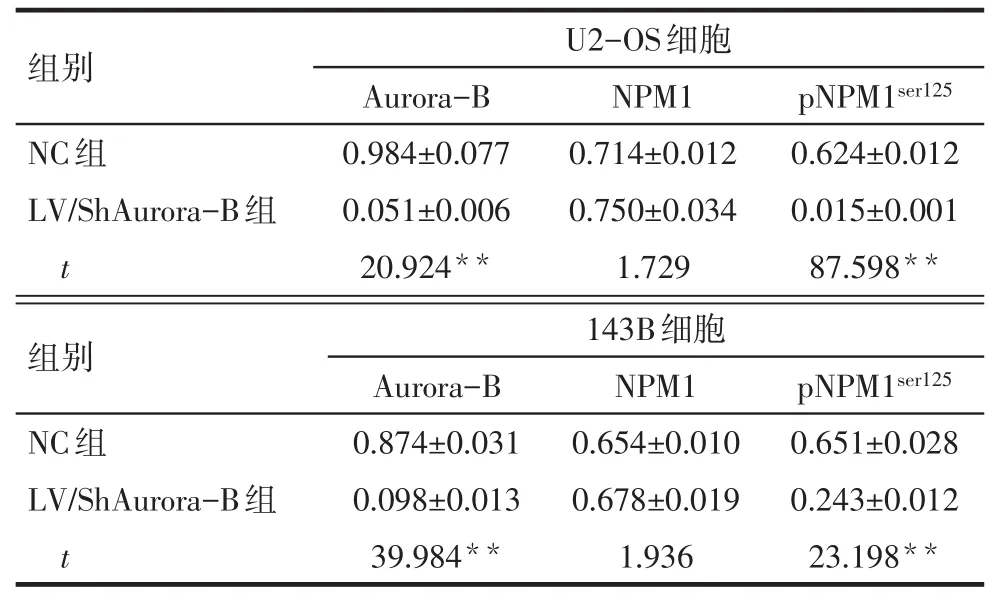
Tab.1 Expressions of Aurora-B,NPM1 and pNPM1ser125 detected by Western blot assay表1 Western blot檢測Aurora-B、NPM1和pNPM1ser125蛋白的表達 (n=3,±s)
**P<0.01
組別U2-OS細胞Aurora-B NPM1pNPM1ser125 NC組LV/ShAurora-B組t 0.984±0.077 0.051±0.006 20.924**0.714±0.012 0.750±0.034 1.729 0.624±0.012 0.015±0.001 87.598**組別NC組LV/ShAurora-B組t 143B細胞Aurora-B 0.874±0.031 0.098±0.013 39.984**NPM1 0.654±0.010 0.678±0.019 1.936 pNPM1ser125 0.651±0.028 0.243±0.012 23.198**
2.3 各組骨肉瘤細胞的遷移情況比較 LV/ShAurora-B組遷移率均低于NC組(P<0.05),且共轉染組中下調Aurora-B的遷移抑制被部分恢復(P<0.05),見表2。

Fig.1 The results of bioinformatics analysis圖1 生物信息學分析結果
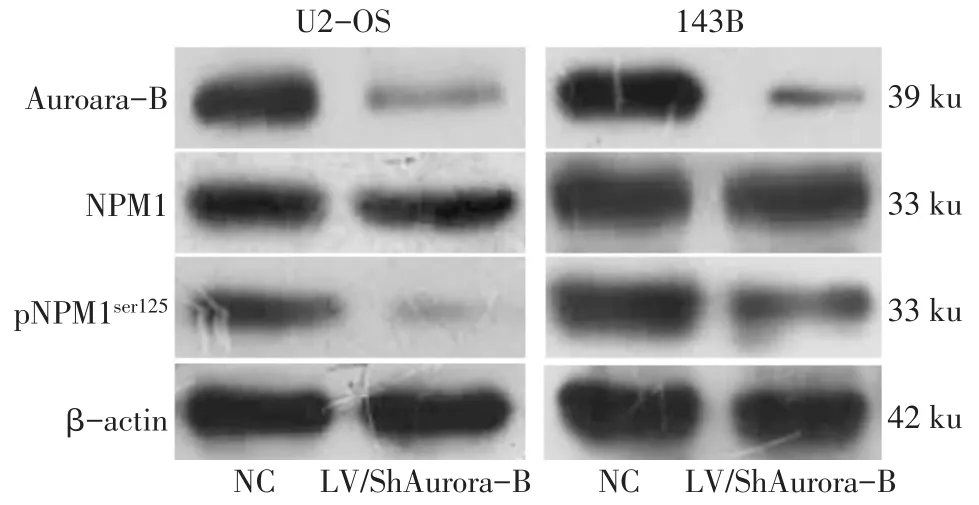
Fig.2 Expressions of Aurora-B,NPM1 and pNPM1ser125 detected by Western blot assay圖2 Western blot檢測Aurora-B、NPM1和pNPM1ser125蛋白的表達
Tab.2 The cell migration ability detected by Wound healing assay in OS cells表2 Wound healing實驗檢測骨肉瘤細胞的遷徙能力(n=3,%,±s)

Tab.2 The cell migration ability detected by Wound healing assay in OS cells表2 Wound healing實驗檢測骨肉瘤細胞的遷徙能力(n=3,%,±s)
*P<0.05,**P<0.01;a與NC組比較,b與LV/ShAurora-B組比較,P<0.05;表3、4同
組別NC組LV/ShAurora-B組共轉染組F U2-OS細胞50.7±10.4 20.2±5.6a 35.1±4.7ab 12.983**143B細胞61.5±12.8 23.0±9.8a 42.5±2.6ab 12.448*
2.4 各組骨肉瘤細胞的增殖情況比較 143B和U2-OS細胞中,LV/ShAurora-B組增殖能力均低于NC組(P<0.05),且LV/ShAurora-B+LV/NPM1共轉染組能部分恢復下調Aurora-B的增殖抑制(P<0.05),見表3。
Tab.3 The proliferation ability detected by CCK-8 assay in OS cells表3 CCK-8實驗檢測骨肉瘤細胞增殖能力(n=3,OD值,±s)
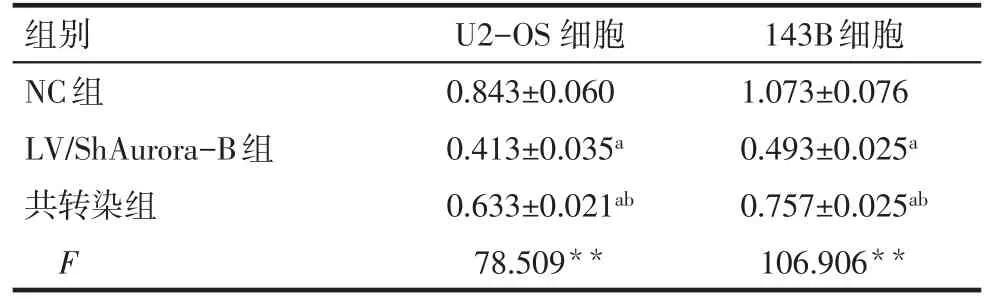
Tab.3 The proliferation ability detected by CCK-8 assay in OS cells表3 CCK-8實驗檢測骨肉瘤細胞增殖能力(n=3,OD值,±s)
組別NC組LV/ShAurora-B組共轉染組F U2-OS細胞0.843±0.060 0.413±0.035a 0.633±0.021ab 78.509**143B細胞1.073±0.076 0.493±0.025a 0.757±0.025ab 106.906**
2.5 各組骨肉瘤細胞的侵襲能力比較 在2種細胞中,LV/ShAurora-B組侵襲細胞數均低于NC組(P<0.05),且LV/ShAurora-B+LV/NPM1共轉染組能部分恢復下調Aurora-B的侵襲能力抑制(P<0.05),見表4、圖4。
Tab.4 The invasion ability detected by Tanswell invasion assay in OS cells表4 Transwell invasion實驗檢測骨肉瘤細胞的侵襲能力(n=3,個/視野,±s)

Tab.4 The invasion ability detected by Tanswell invasion assay in OS cells表4 Transwell invasion實驗檢測骨肉瘤細胞的侵襲能力(n=3,個/視野,±s)
組別NC組LV/ShAurora-B組共轉染組F U2-OS細胞155.000±14.526 82.333±22.745a 134.000±11.523a 14.613*143B細胞189.330±15.011 57.667±16.010a 120.667±13.051ab 63.997**

Fig.3 The cell migration ability detected by Wound healing assay in OS cells(×200)圖3 Wound healing實驗檢測骨肉瘤細胞的遷徙能力(×200)

Fig.4 The cell invasion ability detected by Tanswell invasion assay in OS cells(crystal violet staining,× 200)圖4 Transwell invasion實驗檢測骨肉瘤細胞的侵襲能力(結晶紫染色,×200)
3 討論
Aurora-B是Aurora家族3個成員之一,其功能是參與調節中心體和微管的功能、保證染色體的精確分離和胞漿的有效分離、著絲粒的復制、雙極紡錘體的形成以及監測紡錘體檢測點的忠實性等[3]。它們通常在G2/M期達到高峰,是調節細胞周期由G2期向M期進展的關鍵因子。Aurora-B基因定位在17p13,處在易位、缺失或擴增活躍的染色體區段,意味著它們具有天然的不穩定性。有研究顯示,Aurora-B通過激活蛋白激酶B(protein kinase B,AKt)/哺乳動物雷帕霉素靶點(mammalian target of rapamycin,mTOR)信號傳導途徑來促進淋巴瘤細胞存活和增殖[4]。本課題組前期研究表明,Aurora-B通過激活磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K)/AKt/核轉錄因子kappa β(nuclear factor kappa beta,NF-κβ)信號通路促進骨肉瘤惡性表型[5]。本次研究發現,PI3K/AKt抑制并不能完全逆轉Aurora-B介導的骨肉瘤侵襲轉移,提示Aurora-B所介導的骨肉瘤侵襲轉移可能還涉及其他分子機制。因此,進一步探討Aurora-B介導骨肉瘤侵襲轉移的分子機制顯得十分必要和重要。
NPM1是一種具有高活性的核仁蛋白,在核糖體蛋白組裝、染色質重塑以及DNA修復、復制和轉錄中發揮積極作用[6-8]。磷酸化、乙酰化和泛素化等翻譯后修飾可使生成的NPM1定位于不同的亞細胞區域,從而行使不同的功能。越來越多的證據表明,NPM1是一種直接參與癌癥發病機制的核仁蛋白。在包括前列腺癌、血液腫瘤和高級漿液性卵巢腺癌等多種惡性腫瘤中發現,NPM1的高表達且與腫瘤進展和抗藥性有關[9]。本研究通過生物信息數據庫查找,顯示NPM1在肉瘤中高表達以及NPM1高表達的患者預后較差,并且Aurora-B與NPM1之間可能存在磷酸化作用。以此為基礎,通過體外實驗,進一步證實了下調Aurora-B后磷酸化NPM1ser125蛋白的表達降低,而非磷酸化NPM1蛋白的表達不變。以上結果表明Aurora-B能夠介導NPM1的磷酸化。然而,Aurora-B介導的NPM1蛋白磷酸化并不一定對骨肉瘤細胞惡性表型產生效應,為此,進一步行體外惡性表型的驗證顯示,沉默Aurora-B后骨肉瘤的侵襲、增殖和遷移能力均受到抑制,且沉默Aurora-B后同時過表達NPM1發現,下調Aurora-B對骨肉瘤侵襲、轉移和增殖的抑制作用被部分緩解,這證實了Aurora-B能夠通過介導NPM1蛋白磷酸化促進骨肉瘤細胞惡性表型,但是NPM1介導骨肉瘤惡性表型改變的具體分子機制仍未可知。
Chen等[10]研究顯示,NPM1通過影響Akt活性,從而在乳腺癌中發揮抗凋亡作用。另外,研究證實RNA干擾(RNAi)沉默NPM1基因能顯著降低前列腺癌細胞中細胞外調節蛋白激酶1/2(extracellular regulated protein kinases 1/2,ERK1/2)的磷酸化水平[11]。ERK1/2的磷酸化可促使與NF-κβ相結合的Iκβα發生降解,使定位于胞漿的NF-κβ轉移至核內[12-13];NF-κβ的核內移位可促使基質金屬蛋白酶-2(matrix metalloprotein-2,MMP-2)、MMP-9等與腫瘤轉移相關的基因表達上調,促進包括骨肉瘤在內的多種腫瘤的細胞侵襲和轉移[14-15]。因此,在骨肉瘤細胞中,Aurora-B是否通過NPM1/ERK/NF-κβ信號軸促進骨肉瘤惡性表型亦是后續有意義的研究方向。
綜上所述,Aurora-B通過介導NPM1蛋白磷酸化促進骨肉瘤細胞惡性表型。但本研究僅做了Aurora-B沉默,且缺乏體內實驗證實這一結論。另外,NPM1介導骨肉瘤惡性表型改變的具體分子機制亦有待后續進一步研究。

