一氧化氮吸入聯合高頻震蕩通氣治療新生兒嚴重呼吸衰竭的療效分析
李玲,薛梅
新生兒嚴重呼吸衰竭(severe respiratory failure,SRF)是新生兒重癥監護室(neonatal intensive care unit,NICU)的危急重癥,是早期新生兒死亡的首位原因[1]。SRF發生時,由于肺血管持續痙攣,導致通氣-灌流失調,一般機械通氣和擴張肺血管藥物不能有效改善,而高頻振蕩通氣(high-frequency oscillatory ventilation,HFOV)、一氧化氮吸入(inhaled nitric oxide, iNO)等急救新技術的應用具有迅速改善低氧血癥的作用,同時還具有調節和抑制肺組織細胞炎癥的作用[2]。但臨床實踐中,單一技術往往效果欠佳,需要多種技術聯合應用。本研究觀察HFOV聯合iNO對新生兒SRF的治療效果,報告如下。
1 資料與方法
1.1一般資料2013年3月至2016年3月入住泰州市人民醫院南院新生兒科SRF患兒60例,日齡(5.93±3.35)h,男/女為34/26,體質量(3.48±0.39)kg,其中新生兒胎糞吸入綜合征(MAS)22例,新生兒呼吸窘迫綜合征(RDS)38例,入組標準:呼吸機正壓通氣下,吸入氧濃度(FIO2)>60%,經皮血氧飽和度(TcSO2)<80%;患兒近親屬簽署了知情同意書,排除標準:復雜先天性心臟病或嚴重左心衰、先天性呼吸道及消化道畸形、有出血性疾病及出血傾向、嚴重貧血、早產兒等。入組病例采取隨機數字法分為對照組28例和觀察組32例,兩組日齡、胎齡、出生體質量、性別、原發病因組成等差異無統計學意義。見表1。本研究通過泰州市人民醫院醫學倫理委員會批準。
1.2研究方法入住患兒均予STEPHANIE呼吸機,高頻震蕩通氣模式,采取肺保護性通氣策略,根據病情設置初調參數,依據臨床表現及結合血氣分析指導逐步調整參數,初調參數范圍:震蕩壓力15~20 cmH2O,震蕩幅度30~40 cmH2O,震蕩頻率7~12 Hz,吸氧濃度60%~100%。兩組均給予常規基礎治療如抗感染、改善循環、保護臟器功能、糾正酸堿失衡及電解質紊亂等。新生兒呼吸窘迫綜合征予肺泡表面活性物質應用,氣胸予胸腔閉式引流。對照組予單純HFOV治療,觀察組予iNO聯合HFOV治療。吸入的一氧化氮(NO)氣體經專用的質量流量控制儀接入呼吸機供氣管道,有專用的濃度監測儀檢測管道中的NO、NO2濃度。iNO治療起始濃度10~15 ppm,吸入1 h如TcSO2上升>10%,氧分壓(PaO2)上升>10 mmHg為有效,在氧合改善,TcSO2維持在90%以上時,逐步下調FiO2至60%,調節震蕩壓力至15 cmH2O,病情好轉,TcSO2穩定后,逐步下調iNO濃度1~2 ppm,至iNO濃度5~3 ppm時,撤離iNO。
1.3觀察指標動態監測入科即刻、治療后2 h和24 h后兩組的血氣分析(pH、PaO2、PaCO2)和呼吸功能指標[動脈氧分壓與吸入氧濃度比(PaO2/FiO2)、氧合指數(OI)],并記錄機械通氣時間、iNO吸入時間、救治成功率及并發癥發生率。
1.4統計學方法采用SPSS 22.0軟件對所采集數據進行統計學分析;計數資料使用χ2檢驗,計量資料使用成組t檢驗,部分指標雖為多時點觀測,但因關注重點為組間差異,故未行重復測量分析。P<0.05表示差異有統計學意義。
2 結果
2.1兩組動脈血氣指標比較開始治療前兩組患兒的動脈血氣指標組間比較差異無統計學意義(均P>0.05);治療2 h后,均出現pH 、PaO2的上升及PaCO2的下降,但僅pH值差異有統計學意義(P=0.040)。24 h后,觀察組的血氣指標均優于對照組,差異有統計學意義(P<0.05)。見表2。
2.2兩組呼吸功能指標比較開始治療前兩組患兒的呼吸指標組間比較差異無統計學意義(P>0.05);治療2 h后和24 h, 均出現PaO2/ FiO2的上升及OI值的降低,觀察組均優于對照組,差異有統計學意義(P<0.05)。見表3。
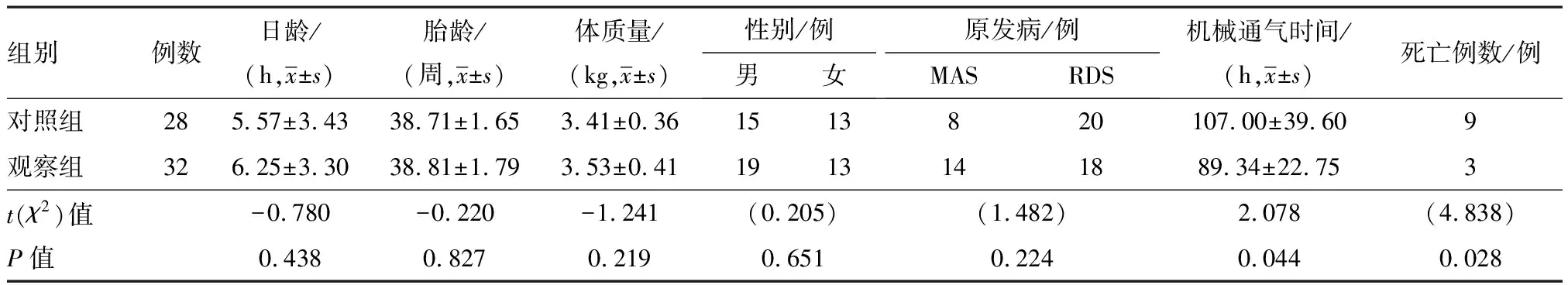
表1 兩組一般情況及治療后臨床轉歸情況比較

表2 治療前后患兒動脈血氣指標比較

表3 治療前后患兒呼吸功能指標比較
2.3兩組臨床轉歸及并發癥情況比較對照組機械通氣時間長于觀察組,差異有統計學意義(P=0.044);對照組有9例患兒出現死亡,觀察組3例患兒死亡,組間比較差異有統計學意義(P=0.028)。見表1。觀察組患兒均未見出血征象,出凝血時間檢測值均在正常范圍,監測NO2在安全范圍(<1×106)。監測高鐵血紅蛋白在安全范圍(<3%)。
3 討論
近年來,隨著機械通氣尤其是HFOV在NICU的廣泛應用,呼吸衰竭患兒的搶救成功率得到極大的提高,但仍有部分SFR患兒,需較高的呼吸機參數如高壓力或高吸氧濃度方能維持或勉強維持血氧飽和度在正常范圍,影響了新生兒的存活率及預后。分析其原因有:原發病嚴重,內源性NO分泌減少、肺動脈痙攣致肺動脈高壓等[3],因此,部分嚴重呼吸衰竭患兒采用單純機械通氣治療效果不佳[4]。謝桂芬等[5]發現新生兒呼吸衰竭和機械通氣時其內源性NO代謝物有下降的趨勢,證實NO在低氧狀態下產生減少,再加上危重患兒常合并酸中毒,使肺小動脈痙攣,并發持續肺動脈高壓(PPHN),加重低氧血癥,形成惡性循環[6]。
20世紀90年代初iNO作為一種新的呼吸支持技術應用于新生兒[7]。經過20多年來的多中心研究發現,一氧化氮治療嚴重呼吸衰竭效果較明顯[8]。大量臨床報告顯示, NO可以選擇性擴張肺血管,降低肺動脈壓,改善通氣/灌流比例失調,改善換氣和氧合,而不影響體循環血壓、血流。NO的選擇作用源自它與血紅蛋白內鐵離子有很強的親和力,一旦被吸入,能迅速彌散至肺泡壁周圍血管的內皮細胞,穿過細胞膜而到達血管平滑肌,激活鳥苷環化酶產生環磷酸鳥苷,從而抑制鈣離子內流,使肺血管舒張;NO一旦進入血液循環,即與血紅蛋白結合,活性被滅活,故不影響體循環系統。
NO是血管內皮細胞(VEC) 釋放、血管內皮衍生的舒張因子(EDRF)[9]。近年研究表明,NO是EDRF其中最具代表性的活性成分[10]。內源性NO具有調節血管張力、參與炎癥反應、提高宿主防御功能、舒張支氣管平滑肌、抑制血栓形成、參與神經傳遞。
本研究中應用iNO聯合HFOV,應用于SFR患兒,結果顯示iNO早期應用能顯著改善患兒氧合指數,使呼吸機參數逐漸下調至安全范圍,且合理調整參數后患兒無明顯不適,縮短患兒機械通氣時間,減少相關并發癥,提高呼吸衰竭病人的搶救成功率。同時iNO治療期間監測NO2濃度及高鐵血紅蛋白在安全范圍,凝血功能無明顯異常變化。
對于肺實質疾病引起的嚴重呼吸衰竭,iNO與高頻通氣聯合應用具有協同作用,其機制是NO到達有通氣的肺泡,可使相應的肺血管擴張,緩解肺動脈高壓,改善氧合,HFV可募集更多的肺泡,使肺通氣達最佳狀態,便于NO進入和發揮作用[2]。故iNO聯合高頻震蕩通氣治療模式具有良好的理論基礎。兩者聯合治療可改善氧合,使較高呼吸機參數盡快下調,減少機械通氣時間,減少并發癥發生率,提高存活率,且操作相對體外膜肺技術(ECMO)簡單、方便,易于大多數NICU病房開展,安全性高,值得推廣。

