HMGB1和HIF1a在乳頭狀甲狀腺癌中的表達(dá)及意義
龔龍,易春華,周明,鄭建偉
(1.華中科技大學(xué)同濟(jì)醫(yī)學(xué)院附屬荊州醫(yī)院,湖北 荊州 434020;2.華中科技大學(xué)同濟(jì)醫(yī)學(xué)院附屬同濟(jì)醫(yī)院,湖北 武漢 430030)
乳頭狀甲狀腺癌(papillary thyroid carcinoma,PTC)是最常見(jiàn)的甲狀腺癌,腫瘤細(xì)胞分化程度和有無(wú)淋巴結(jié)轉(zhuǎn)移是PTC預(yù)后的重要因素[1-2]。腫瘤微環(huán)境是腫瘤生長(zhǎng)和轉(zhuǎn)移的重要影響因素,而缺氧是眾多實(shí)體腫瘤微環(huán)境的顯著特點(diǎn)[3]。本研究采用免疫組織化學(xué)法檢測(cè)PTC組織及其癌旁組織中缺氧誘導(dǎo)因 子 1a(hypoxia-inducible factor 1-alpha, HIF1a) 和高遷移率族蛋白 1(high mobility group box-1 protein,HMGB1)表達(dá)情況,分析HIF-1α和HMGB1與PTC臨床病理特征的關(guān)系,旨在為進(jìn)一步研究HMGB1和缺氧在PTC細(xì)胞發(fā)生、發(fā)展過(guò)程中的作用和機(jī)制提供臨床證據(jù)。
1 資料與方法
1.1 一般資料
選取2008年1月—2017年10月經(jīng)華中科技大學(xué)同濟(jì)醫(yī)學(xué)院附屬荊州醫(yī)院甲狀腺外科術(shù)后確診的120例患者的癌組織及相應(yīng)癌旁組織石蠟標(biāo)本,所有標(biāo)本經(jīng)HE染色證實(shí)為PTC。其中,男性36例,女性84例;年齡31~76歲,平均46.9歲。患者術(shù)前均未行放化療,統(tǒng)計(jì)淋巴結(jié)轉(zhuǎn)移及甲狀腺癌臨床分期情況。其中,有淋巴結(jié)轉(zhuǎn)移38例,無(wú)淋巴結(jié)轉(zhuǎn)移82例。按照國(guó)際抗癌協(xié)會(huì)聯(lián)盟的TNM分期:Ⅰ、Ⅱ期77例,Ⅲ、Ⅳ期43例。
1.2 試劑
兔抗人HMGB1及HIF-1α多克隆抗體購(gòu)自英國(guó)ABCAM公司,兔SP免疫組織化學(xué)試劑盒[北京中杉金橋生物技術(shù)有限公司(SP-9001)],DAB顯示劑(武漢博士德生物工程有限公司)。
1.3 免疫組織化學(xué)
切取石蠟切片,每張切片厚約5μm,采用SP法檢測(cè)PTC組織及相應(yīng)癌旁組織中HIF-1α、HMGB1蛋白的表達(dá)(HIF1a一抗工作濃度為1∶100;HMGB1一抗工作濃度為1∶100)。所有操作步驟嚴(yán)格按照試劑盒說(shuō)明書(shū)進(jìn)行,以PBS替代一抗作為陰性對(duì)照,試劑公司提供的陽(yáng)性著色圖片作為陽(yáng)性對(duì)照。
1.4 結(jié)果判定
根據(jù)REMMELE等[4]提出的免疫反應(yīng)評(píng)分(immunoreactive score, IRS)進(jìn)行染色反應(yīng)的評(píng)價(jià):IRS=染色強(qiáng)度×陽(yáng)性細(xì)胞百分率。染色強(qiáng)度0為陰性,1為弱,2為中度,3為強(qiáng)。陽(yáng)性細(xì)胞百分率0%為陰性,>0%~10%為1;>10%~50%為2;>50%~80%為3;>80%為4。IRS評(píng)分0~12分,評(píng)分>4分定義為蛋白陽(yáng)性表達(dá)。
1.5 統(tǒng)計(jì)學(xué)方法
數(shù)據(jù)分析采用SPSS 16.0統(tǒng)計(jì)軟件。計(jì)數(shù)資料以率(%)表示,比較用χ2檢驗(yàn);變量之間的相互關(guān)系采用Spearman相關(guān)分析,P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié)果
2.1 HIF-1α和HMGB1蛋白在PTC及其癌旁組織中的表達(dá)
免疫組織化學(xué)染色顯示,PTC組織中,HMGB1陽(yáng)性呈棕色或褐色,主要定位于細(xì)胞核和細(xì)胞質(zhì)(見(jiàn)附圖A)。而癌旁組織中,HMGB1主要表達(dá)于細(xì)胞核中,表達(dá)較PTC組織減少,且染色減弱(見(jiàn)附圖B)。同樣地,PTC組織中HIF1a陽(yáng)性呈棕色或褐色顆粒,主要定位于細(xì)胞核和細(xì)胞質(zhì)(見(jiàn)附圖C)。而癌旁組織中,HIF1a主要表達(dá)于細(xì)胞核中,表達(dá)較PTC組織減少,且染色減弱(見(jiàn)附圖D)。

附圖 HMGB1、HIF1a在PTC及其癌旁組織中的表達(dá) (SP法×200)
2.2 PTC組織中HMGB1與HIF1a表達(dá)的相關(guān)性
HMGB1在PTC組織及癌旁組織中的陽(yáng)性表達(dá)率分別為65.0%和35.0%,經(jīng)χ2檢驗(yàn),差異有統(tǒng)計(jì)學(xué)意義(χ2=8.067,P=0.005),PTC組織陽(yáng)性表達(dá)率高于癌旁組織;HIF1a在PTC組織及癌旁組織中的陽(yáng)性表達(dá)率分別為59.2%和40.8%,經(jīng)χ2檢驗(yàn),差異有統(tǒng)計(jì)學(xué)意義(χ2=9.630,P=0.002),PTC組織陽(yáng)性表達(dá)率高于癌旁組織。相關(guān)性分析顯示,PTC組織標(biāo)本中HMGB1與HIF1a的表達(dá)呈正相關(guān)(P<0.05)。見(jiàn)表1。
2.3 PTC組織中HMGB1、HIF1a表達(dá)水平與臨床病理特征的關(guān)系
HIF1a和HMGB1在不同腫瘤直徑、腫瘤數(shù)量、淋巴結(jié)轉(zhuǎn)移情況及臨床分期方面比較,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見(jiàn)表 2。

表1 PTC組織中HMGB1與HIF1a表達(dá)的相關(guān)性 例
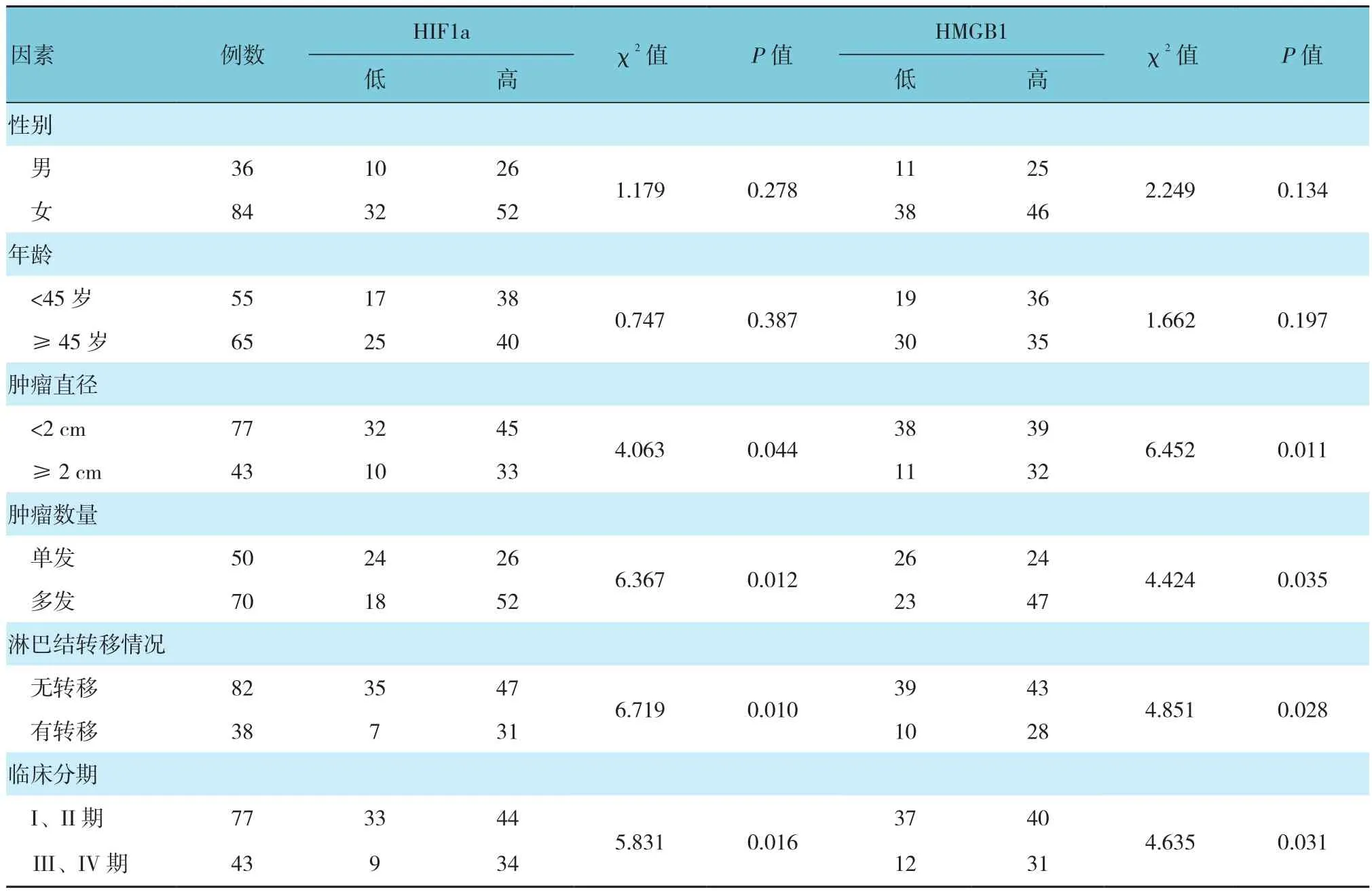
表2 PTC組織中HMGB1、HIF1a表達(dá)水平與臨床病理特征的關(guān)系 例
3 討論
組織缺氧是多數(shù)實(shí)體腫瘤常見(jiàn)的病理生理特征,越來(lái)越多人認(rèn)識(shí)到其在腫瘤進(jìn)展的不同階段中起關(guān)鍵作用[5]。腫瘤對(duì)缺氧的適應(yīng)主要受缺氧誘導(dǎo)因子(HIF-1α和HIF-2α)的調(diào)節(jié),HIF-1α與腫瘤啟動(dòng)子有關(guān),被認(rèn)為是一個(gè)促腫瘤因子,而HIF-2α則被證實(shí)是腫瘤抑制基因[6]。迄今為止,已有多項(xiàng)研究發(fā)現(xiàn)HIF-1α在卵巢、食管、頭頸部、乳腺癌、前列腺癌、膀胱癌及口腔上皮等腫瘤中過(guò)表達(dá)[7-11]。此外,最近一些研究檢測(cè)了甲狀腺癌組織中HIF-1α的表達(dá)[12-13]。然而,HIF-1α與炎癥效應(yīng)因子在PTC的發(fā)生、發(fā)展中的關(guān)系研究甚少,其相關(guān)機(jī)制有待進(jìn)一步研究。
HMGB1蛋白是一種豐富的非組蛋白染色體結(jié)合蛋白。其能穩(wěn)定核小體結(jié)構(gòu)并參與DNA的復(fù)制、轉(zhuǎn)錄及修飾[11]。在非惡性細(xì)胞中,HMGB1主要存在于細(xì)胞核內(nèi)。在腫瘤細(xì)胞中,HMGB1表達(dá)增多,且可轉(zhuǎn)位至細(xì)胞質(zhì)和細(xì)胞外空間中[14]。HMGB1參與炎癥因子的表達(dá)和釋放,以及腫瘤的發(fā)生、發(fā)展,而HIF-1α可能是HMGB1表達(dá)及細(xì)胞亞定位的重要調(diào)節(jié)因子[15]。QIU等[16]發(fā)現(xiàn)缺氧誘導(dǎo)HMGB1表達(dá),進(jìn)而通過(guò)ERK/JNK信號(hào)通路調(diào)控成骨細(xì)胞上皮間質(zhì)轉(zhuǎn)化。CHENG等[17]還發(fā)現(xiàn)缺氧誘導(dǎo)HMGB1轉(zhuǎn)為的釋放,進(jìn)而通過(guò)TLRs促進(jìn)促炎細(xì)胞因子產(chǎn)生。而PTC中缺氧與HMGB1的相互表達(dá)及作用方式還未見(jiàn)報(bào)道。
在本研究中,筆者通過(guò)免疫組織化學(xué)法檢測(cè)HIF-1α、HMGB1在PTC及癌旁組織中的表達(dá),發(fā)現(xiàn)這兩者在PTC中表達(dá)升高,主要定位于細(xì)胞核和細(xì)胞質(zhì)。進(jìn)一步分析發(fā)現(xiàn),HMGB1和HIF1a在PTC組織中的表達(dá)與腫瘤直徑、腫瘤個(gè)數(shù)、淋巴轉(zhuǎn)移及臨床分期有關(guān)。提示兩者可能參與PTC發(fā)生、發(fā)展過(guò)程。通過(guò)相關(guān)性分析顯示,PTC組織標(biāo)本中HMGB1與HIF1a的表達(dá)呈正相關(guān),提示HIF1a可能調(diào)控PTC細(xì)胞中HMGB1的表達(dá),進(jìn)而參與PTC的惡性過(guò)程。
盡管筆者在PTC臨床樣本中研究了HIF-1α與HMGB1的表達(dá)及其相關(guān)性,但還需要更多的細(xì)胞學(xué)實(shí)驗(yàn)來(lái)深入研究?jī)烧叩恼{(diào)節(jié)機(jī)制及可能的信號(hào)通路。同時(shí)進(jìn)一步研究?jī)烧呷绾螀⑴cPTC的發(fā)生、發(fā)展,如腫瘤的增殖、血管生成、遷移及轉(zhuǎn)移等,以期為以HMGB1為PTC診斷及治療的分子靶點(diǎn)提供更進(jìn)一步的理論基礎(chǔ)。

